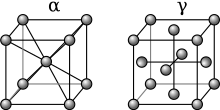
철분할당
Allotropes of iron
대기압에서는 온도에 따라 알파철(α-Fe), 감마철(α-Fe), 델타철(Δ-Fe)의 세 가지 균등성 형태의 철이 존재한다. 매우 높은 압력에서는 엡실론 철(epsilon-Fe)이라고 하는 네 번째 형태가 존재한다. 논란의 여지가 있는 일부 실험 증거는 매우 높은 압력과 온도에서 안정적인 제5의 고압 형태가 존재함을 시사한다.[1]
기압에서 철의 단계는 탄소 용해성의 차이 때문에 중요하며, 다른 종류의 강철을 형성한다. 철의 고압 단계는 행성 중심부의 고체 부분 모델로서 중요하다. 지구의 내핵은 일반적으로 ε 구조를 가진 결정체 철 니켈 합금으로 구성된다고 가정한다.[2][3][4] 고체 내핵을 둘러싼 외핵은 니켈과 미량의 가벼운 원소를 혼합한 액체 철로 구성된 것으로 생각된다.
표준 압력 할당체
알파 철(α-Fe)
912 °C(1,674 °F) 이하에서는 철이 체질 중심의 입방체(bcc) 결정구조를 가지고 있으며, α-철 또는 페라이트(perite) 그것은 열역학적으로 안정적이고 꽤 부드러운 금속이다. α-Fe는 ca. 15 GPA까지의 압력에 노출될 수 있다. 그 전에 아래에서 설명하는 ε-Fe라고 하는 고압 형태로 변모한다.
자석학적으로 α-철은 고온에서 파라마그네틱이다. 그러나 771 °C(1044K 또는 1420 °F)의 퀴리 온도(TC2 또는 A) 이하에서는 강자성이 된다.[5] 과거에 α-철의 파라마그네틱 형태는 베타 철(β-Fe)으로 알려져 있었다.[6][7] 강자성 상태의 약간 사방형 왜곡이 진정한 위상 전환을 구성하지만, 이러한 전환의 지속적인 특성은 강철 열 처리에서 아주 작은 중요성으로 귀결된다. A는2 그림 1의 위상 다이어그램에서 베타 철과 알파 장 사이의 경계를 형성한다.
마찬가지로 A는2 A1(Eutectoid), A3 및 A 임계cm 온도에 비해 아주 작은 중요도에 불과하다. 오스테나이트가 시멘타이트 + γ-Fe와 평형을 이루고 있는 A는cm 그림 1의 오른쪽 가장자리를 벗어난다. α + α 위상장은 기술적으로 A 위의2 β + γ이다. 베타 명칭은 철 및 강철 위상의 그리스 문자 진행의 연속성을 유지한다: α-Fe, β-Fe, 오스테나이트 (γ-Fe), 고온 Δ-Fe, 고압 헥사페럼 (ε-Fe).
상온에서 저탄소 또는 연강과 대부분의 주철은 강자성 α-Fe이다.[8][9] 그것의 경도는 대략 80 브리넬이다.[10][11] 탄소의 최대 용해도는 727°C(1,341°F)에서 약 0.02 wt%이고 0°C(32°F)에서는 0.001%이다.[12] 그것이 철에 용해될 때 탄소 원자는 중간 "구멍"을 차지한다. 4면 구멍의 직경의 약 2배에 달하는 탄소는 강한 국부 변형장을 도입한다.
연강(최대 약 0.2 wt% C의 탄소강)은 대부분 α-Fe와 증가하는 시멘타이트 양(FeC3, 철 카바이드)으로 구성된다. 이 혼합물은 펄라이트라고 불리는 층 구조물을 채택한다. 베이나이트와 펄라이트는 각각 α-Fe를 성분으로 함유하고 있기 때문에, 어떤 철탄소 합금도 실온에서 평형에 도달할 수 있게 된다면 어느 정도의 α-Fe를 함유할 것이다. α-Fe의 양은 냉각 과정에 따라 달라진다.
임계2 온도 및 유도 가열

β-Fe 및 A 임계2 온도는 표면 경화 열 처리와 같은 강철의 유도 난방에 중요하다. 강철은 일반적으로 급랭 및 담금질 전에 900–1000 °C로 유지된다. 유도 가열의 고주파 교번 자기장은 저항 또는 줄(IR2) 가열 및 강자성 이력 손실이라는 두 가지 메커니즘으로 강철을 가열한다. A2 위에서는 이력 메커니즘이 사라지고 온도 상승도 당 필요한 에너지의 양이 A 아래보다2 상당히 크다. 변화를 보상하기 위해 유도 전원의 임피던스를 변화시키기 위해 부하 매칭 회로가 필요할 수 있다.[13]
감마철(γ-Fe)
철을 912 °C(1,674 °F) 이상으로 가열하면 결정 구조가 얼굴 중심의 입방체(fcc) 결정 구조로 바뀐다. 이 형태에서 감마철(γ-Fe) 또는 오스트레나이트라고 불린다. γ-철은 상당히 많은 탄소를 용해시킬 수 있다(1,146 °C에서 질량으로 2.04%까지). 이 γ 형태의 탄소 포화도는 스테인리스강으로 전시되어 있다.
델타 철(Δ-Fe)
특히, 1,394 °C(2,541 °F) 이상의 철은 BCc 구조로 다시 변화하는데, Δ-Fe. [14]Δ-철은 1,475 °C에서 질량에 의해 0.08%의 탄소를 용해시킬 수 있다. 1,538 °C(2,800 °F)의 용해점까지 안정적이다.
고압분할증
엡실론 철 / 헥사페럼(ε-Fe)
약 10 GPA 이상의 압력과 수백 켈빈 이하의 온도에서 α-철은 육각형의 근접 포장(hcp) 구조로 변화하는데, α-철은 or-철 또는 헥사페럼이라고도 하며,[15] 고온 γ 위상도 ε-철로 변화하지만, 높은 압력에서 변화한다. Mn, Os, Ru와 함께 엡실론-Fe 합금에서의 반소자성이 관찰되었다.[16]
실험 고온 및 압력
대체 안정형 형태는 존재하는 경우 적어도 50 GPA의 압력과 1,500 K의 온도에서 나타날 수 있다. 즉, 직교합체 또는 이중 hcp 구조를 가진 것으로 생각되어 왔다.[1] 2011년[update] 12월 현재 고압 및 초밀도 탄소배당제에 대한 최근 및 지속적인 실험이 이루어지고 있다.
위상 전환
용융점 및 비등점
철의 용해점은 50 GPA 미만의 압력에 대해 실험적으로 잘 정의되어 있다.
더 큰 압력을 위해, 발표된 데이터(2007년 기준)는 γ-ε-액체 3중점을 수십 기가파스칼과 용해 지점에서 1000K가 다른 압력에 두었다. 일반적으로 분자역학 컴퓨터 시뮬레이션에서 철 용해 및 충격파 실험은 다이아몬드 앤빌 셀에서 수행되는 정적 실험보다 용해점이 높고 용해 곡선의 경사가 훨씬 더 가파르다는 것을 시사한다.[17]
철 발생의 엔탈피의 녹는점과 끓는점이, 그 이전의 그룹 스칸듐 크롬에서 3D요소보다 3일부 귀 서한에 따라서 전자의 금속 결합은 줄어든 공헌을 하는 것으로 그들은 움직임이 없는 그 핵심과 점점 더 핵에 의해서 매력을 느낍니다 보여 주고;[18] 하지만, 그들은 값보다 더 높다 낮다.sfor 이전의 원소 망간은 반만 채워진 3d 하위껍질을 가지고 있고 결과적으로 그것의 d-messages는 쉽게 소산되지 않기 때문이다. 이런 경향은 루테늄에도 나타나지만 오스뮴은 나타나지 않는다.[19]
구조 위상 전환
철이 한 결정 구조에서 다른 결정 구조로 이행되는 정확한 온도는 철에 용해되는 다른 원소의 양과 종류에 따라 달라진다. 상이한 고체상 사이의 위상 경계가 이항 위상 다이어그램에 그려지며, 일반적으로 온도 대 백분율 철로 표시된다. 크롬과 같은 원소를 첨가하면 감마 단계의 온도 범위가 좁아지는 반면, 다른 원소는 감마 단계의 온도 범위를 증가시킨다. 감마 위상 범위를 줄이는 요소에서 알파 감마 위상 경계는 감마-델타 위상 경계와 연결되며, 일반적으로 감마 루프라고 불리는 것을 형성한다. 감마루프 첨가제를 첨가하면 철이 체중 중심의 입방체 구조로 유지되고 강철은 다른 고체 상태로 단계적 전환을 겪지 않게 된다.[20]
참고 항목
참조
- ^ a b Boehler, Reinhard (2000). "High-pressure experiments and the phase diagram of lower mantle and core materials". Reviews of Geophysics. American Geophysical Union. 38 (2): 221–245. Bibcode:2000RvGeo..38..221B. doi:10.1029/1998RG000053. S2CID 33458168.
- ^ Cohen, Ronald; Stixrude, Lars. "Crystal at the Center of the Earth". Archived from the original on 5 February 2007. Retrieved 2007-02-05.
- ^ Stixrude, Lars; Cohen, R.E. (March 1995). "High-Pressure Elasticity of Iron and Anisotropy of Earth's Inner Core". Science. 267 (5206): 1972–5. Bibcode:1995Sci...267.1972S. doi:10.1126/science.267.5206.1972. PMID 17770110. S2CID 39711239.
- ^ "What is at the centre of the Earth?". BBC News. 31 August 2011.
- ^ a b Alloy Phase Diagrams. ASM Handbook. 3. ASM International. 1992. pp. 2.210, 4.9. ISBN 978-0-87170-381-1.
- ^ D. K. Bullens 외, 강철 및 열처리, Vol. I, Fourth Ed, J. Wiley & Sons Inc., 1938, 페이지 86.
- ^ Avner, S.H. (1974). Introduction to physical metallurgy (2nd ed.). McGraw-Hill. p. 225. ISBN 978-0-07-002499-1.
- ^ Maranian, Peter (2009), Reducing Brittle and Fatigue Failures in Steel Structures, New York: American Society of Civil Engineers, ISBN 978-0-7844-1067-7.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ Structure of plain steel, retrieved 2008-10-21.
- ^ Alvarenga HD, Van de Putte T, Van Steenberge N, Sietsma J, Terryn H (January 2015). "Influence of Carbide Morphology and Microstructure on the Kinetics of Superficial Decarburization of C-Mn Steels". Metall Mater Trans A. 46 (1): 123–133. Bibcode:2015MMTA...46..123A. doi:10.1007/s11661-014-2600-y. S2CID 136871961.
- ^ Smith, William F.; Hashemi, Javad (2006). Foundations of Materials Science and Engineering (4th ed.). McGraw-Hill. p. 363. ISBN 0-07-295358-6.
- ^ Semiatin, S.L.; Stutz, D.E. (1986). Induction Heat Treatment of Steel. ASM International. pp. 95–98. ISBN 978-0-87170-211-1.
- ^ Lyman, Taylor, ed. (1973). Metallography, Structures and Phase Diagrams. Metals Handbook. 8 (8th ed.). Metals Park, Ohio: ASM International. OCLC 490375371.
- ^ Mathon O; Baudelet F; Itié JP; Polian A; d'Astuto M; Chervin JC; Pascarelli S (14 December 2004). "Dynamics of the magnetic and structural alpha-epsilon phase transition in iron". Physical Review Letters. 93 (25): 255503. arXiv:cond-mat/0405439. Bibcode:2004PhRvL..93y5503M. doi:10.1103/PhysRevLett.93.255503. PMID 15697906. S2CID 19228886.
- ^ G. C. Fletcher; R. P. Addis (November 1974). "The magnetic state of the phase of iron" (PDF). Journal of Physics F: Metal Physics. 4 (11). p. 1954. Bibcode:1974JPhF....4.1951F. doi:10.1088/0305-4608/4/11/020. Retrieved December 30, 2011.
- ^ Boehler, Reinhard; Ross, M. (2007). "Properties of Rocks and Minerals_High-Pressure Melting". Mineral Physics. Treatise on Geophysics. 2. Elsevier. pp. 527–41. doi:10.1016/B978-044452748-6.00047-X. ISBN 9780444527486.
- ^ 그린우드와 어니쇼, 페이지 1116
- ^ 그린우드와 어니쇼, 1074-75페이지
- ^ Myer Kurz, ed. (2002-07-22). Handbook of Materials Selection. p. 44. ISBN 9780471359241. Retrieved December 19, 2013.