동위원소 라벨
Isotopic labeling동위원소 라벨링(또는 동위원소 라벨링)은 반응, 대사 경로 또는 세포를 통해 동위원소(중성자 수에서 검출 가능한 변동이 있는 원자)의 통과를 추적하는 데 사용되는 기법이다.반응물은 특정 원자를 동위원소로 대체함으로써 '라벨링'된다.그런 다음 반응물이 반응을 겪도록 허용된다.제품 내 동위원소 위치는 반응에서 동위원소 원자가 따르는 순서 또는 세포의 대사 경로를 결정하기 위해 측정된다.동위원소 표기에 사용되는 핵종은 안정적인 핵종 또는 방사성핵종일 수 있다.후자의 경우 라벨링은 라디오라벨링이라고 불립니다.
동위원소 라벨링에는 질량, 진동 모드 또는 방사성 붕괴를 통해 라벨링 동위원소의 존재를 검출하는 다양한 방법이 있다.질량분석법은 동위원소 질량의 차이를, 적외선 분광법은 동위원소 진동 모드의 차이를 검출한다.핵자기 공명은 다른 자이로마그네틱 비율을 가진 원자를 검출한다.방사성 붕괴는 겔의 이온화 챔버 또는 자동 방사선 촬영을 통해 검출할 수 있다.
동위원소 라벨링의 사용 예는 일반적인 수소(프로튬)를 중수소(중수소 라벨링)로 대체하여 물 속의 페놀(CHOH65)을 연구하는 것이다.중수소화수(통상적인2 HO 외에 DO를 포함한2 물)에 페놀을 첨가하면 페놀의 수산기(CHOD65)에서 수소 중수소가 치환되는 것이 관찰되어 페놀은 쉽게 물과 수소 교환 반응을 일으킨다.하이드록실기만 영향을 받아 나머지 5개의 수소 원자가 교환 [citation needed]반응에 참여하지 않음을 나타냅니다.
동위원소 트레이서
동위원소 추적기('동위원소 마커' 또는 '동위원소 라벨')는 화학 및 생화학에서 화학 반응과 상호작용을 이해하는 데 도움을 주기 위해 사용됩니다.이 기술에서는 관심 분자의 원자 중 하나 이상이 동일한 화학 원소의 원자 대신 다른 동위원소(방사능 추적에 사용되는 방사성 동위원소)를 사용한다.라벨이 붙은 원자는 같은 수의 양성자를 가지고 있기 때문에 라벨이 붙어 있지 않은 원자와 거의 같은 방식으로 행동하며, 몇 가지 예외를 제외하고는 조사 중인 반응을 방해하지 않는다.그러나 중성자 수의 차이는 같은 원소의 다른 원자와 분리하여 검출할 수 있음을 의미한다.
화학반응의 메커니즘을 조사하기 위해 핵자기공명(NMR)과 질량분석(MS)을 사용한다.NMR과 MS는 동위원소 차이를 검출하여 제품 구조에서 라벨이 부착된 원자의 위치에 대한 정보를 결정할 수 있다.생성물 중의 동위원소 원자의 위치정보에 의해 초기 대사물이 생성물로 변환하기 위해 이용하는 반응경로를 결정할 수 있다.방사성 동위원소는 겔 전기영동에 있는 겔의 자동 방사선 사진을 사용하여 테스트할 수 있다.방사성 동위원소를 포함한 화합물에 의해 방출되는 방사선은 사진 필름 조각을 어둡게 하고, 라벨이 부착된 화합물의 위치를 겔에 기록합니다.
동위원소 추적기는 일반적으로 동위원소 비율의 형태로 사용된다.동일한 원소의 두 동위원소 간의 비율을 연구함으로써, 우리는 원소의 전체적인 풍부성과 관련된 영향을 피하며, 이는 보통 훨씬 작은 동위원소 풍부성 변화를 흡수한다.동위원소 추적기는 지구 시스템의 복잡한 혼합 과정을 이해하는 데 사용될 수 있기 때문에 지질학에서 가장 중요한 도구 중 하나입니다.지질학에서의 동위원소 추적기 적용에 대한 추가 논의는 동위원소 지구화학의 제목으로 다루어진다.
동위원소 추적기는 일반적으로 안정 동위원소 추적기와 방사선 발생 동위원소 추적기의 두 가지 범주로 세분된다.안정 동위원소 추적기는 비방사성 동위원소만 포함하며 일반적으로 질량에 따라 달라진다.이론적으로, 두 개의 안정적인 동위원소를 가진 모든 원소를 동위원소 추적기로 사용할 수 있다.그러나 가장 일반적으로 사용되는 안정 동위원소 추적기는 자연 시스템에서 쉽게 분류되는 비교적 가벼운 동위원소를 포함한다.동위원소 시그니처도 참조해 주세요.방사성 동위원소 추적기는 방사성 붕괴에 의해 생성된 동위원소를 포함하며, 이는 일반적으로 비방사성 동위원소와 같은 비율이다(방사성 붕괴로 인해 지구 내 존재감이 변화하지 않는다).
안정적인 동위원소 라벨링
이 섹션은 확인을 위해 추가 인용문이 필요합니다.: 라벨링 · · · JSTOR (2011년 11월 (이 및 ) |
안정적인 동위원소 라벨링에는 여러 화학 및 생화학 시스템을 모델링하는 데 사용되는 추적기 역할을 할 수 있는 비방사성 동위원소의 사용이 포함된다.선택된 동위원소는 핵자기공명(NMR)과 질량분석(MS)을 통해 식별될 수 있는 화합물의 라벨 역할을 할 수 있다. 가장 일반적인 안정 동위원소 중 일부는 NMR 용제, 아미노산, 핵산, 지질, 일반 대사물 및 세포 성장 매체로 [4]추가로 생성될 수 있다.그 화합물 안정 동위 원소를 사용하여 생산은 표시된 동위 원소(30%균일하게 개개 포도당 표시 예 30%13탄소 동위 원소와 70%이 쓰여져 있는 혼합물 자연스럽게 탄소 라벨이 포함되어 있)의 비율 또는 화합물에 구체적으로 표시된 탄소 위치로(i.e. 1-13C에 의해 지정된고 있는 하이 파이에 분류되어 있는 글루코스.crst포도당의 아르본 위치).
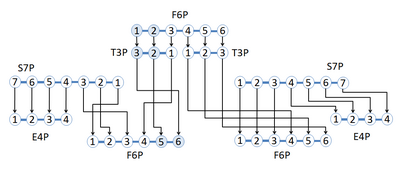
해당과정 경로 및 펜토오스 인산 경로에서 채택된 반응 네트워크는 라벨 부착 탄소 동위원소가 반응 네트워크 전체에서 다른 탄소 위치로 재배치되는 것을 나타낸다.네트워크는 과당 6-인산(F6P)에서 시작됩니다.이것에는 탄소 위치 1과 2,2-C F6P는 6개의 탄소 원자가 있으며, 1,2-C13 F6P는 2개의 글리세린알데히드 3-인산(G3P), 1개는 2,3-C13 T3P 및 1개는 라벨이 없는 T3P가 됩니다.2,3-C13 T3P는 이제 세도헵툴로오스 7-인산(S7P)과 반응하여 라벨이 없는 에리트로스 4-인산(E4P)과 5,6-C13 F6P를 형성할 수 있습니다.라벨이 부착되지 않은 T3P는 S7P와 반응하여 라벨이 부착되지 않은 [3]제품을 합성합니다.이 그림은 위치 고유 라벨 부착 화합물을 이용한 반응을 통해 탄소 원자 재배열을 발견하기 위해 안정적인 동위원소 라벨 부착을 사용하는 것을 보여준다.
안정적인 동위원소 표기를 이용한 대사 플럭스 분석
안정적인 동위원소 표기를 이용한 대사유속분석(MFA)은 세포 내 대사경로와 반응을 통해 특정 원소의 유속을 설명하는 중요한 도구이다.셀에 동위원소 라벨을 공급하고, 그 후 라벨이 부착된 피드를 이용해 셀을 성장시킨다.정상 대사 플럭스 분석의 경우 세포는 정상 상태(세포에 들어오고 나가는 동위원소가 시간에 따라 일정하게 유지됨) 또는 준 정상 상태(특정 [5]시간 동안 정상 상태에 도달함)에 도달해야 한다.출력 대사물의 동위원소 패턴이 결정된다.출력 동위원소 패턴은 각 [6]반응을 통해 플럭스의 크기, 반응 물질에서 생성물로의 전환 속도를 알아내는 데 사용할 수 있는 귀중한 정보를 제공합니다.
이 그림은 여러 라벨을 사용하여 특정 반응을 통해 플럭스를 결정하는 기능을 보여줍니다.3개의 탄소 화합물인 원래 대사물은 하나의 반응으로 2개의 탄소 대사물과 1개의 탄소 대사물로 분할된 후 재결합하거나 3개의 탄소 대사물로 남는 능력을 가지고 있다고 가정합니다.반응이 동일한 비율로 두 개의 대사물 동위원소로 제공될 경우, 하나는 완전히 라벨이 부착된(파란색 원), 다른 하나는 완전히 라벨이 없는(흰색 원) 것이다.그림의 왼쪽 아래 경로는 대사물의 변화를 나타내지 않는 반면 오른쪽은 분할 및 재조합을 나타냅니다.그림과 같이 대사물이 왼쪽 아래쪽으로만 경로를 취할 경우, 라벨이 부착되지 않은 대사물과 균일하게 라벨이 부착된 대사물의 비율이 50 대 50으로 유지된다.대사물이 우측만 취하면 새로운 라벨링 패턴이 발생할 수 있으며, 모든 것이 동일한 비율로 발생할 수 있습니다.다른 비율은 원래 대사물의 얼마나 많은 양이 경로의 왼쪽을 따르느냐 대 경로의 오른쪽을 따르느냐에 따라 발생할 수 있다.여기서는 대사물의 절반은 왼쪽, 절반은 오른쪽이지만 다른 비율이 [7]발생할 수 있는 상황에 대한 비율을 보여 줍니다.하나의 화합물에 있는 라벨이 부착된 원자와 라벨이 부착되지 않은 원자의 이러한 패턴은 동위원소체를 나타냅니다.서로 다른 표기의 대사물의 등방체 분포를 측정함으로써 각 반응을 통한 플럭스를 [8]결정할 수 있다.
MFA는 동위원소 라벨링에서 얻은 데이터를 각 반응, 제약조건 및 최적화 절차에 따라 플럭스 맵을 해결한다.돌이킬 수 없는 반응은 플럭스를 찾는 데 필요한 열역학적 제약을 제공합니다.반응의 화학량법을 포함한 매트릭스를 구성한다.세포 내 플럭스는 시뮬레이션 플럭스가 화학량학 모델에 삽입되는 반복 방법을 사용하여 추정됩니다.시뮬레이션된 플럭스는 플럭스 맵에 표시되며, 플럭스 맵은 각 [6]반응에 대해 반응물이 생성물로 변환되는 비율을 보여 줍니다.대부분의 플럭스 맵에서 화살표가 굵을수록 반응 [9]플럭스 값이 커집니다.
동위원소 라벨 측정 기법
동위원소체 간의 차이를 측정하는 모든 기술을 사용할 수 있다.두 가지 주요 방법인 핵자기공명(NMR)과 질량분석(MS)은 안정적인 동위원소 라벨링의 질량 동위원소체 측정을 위해 개발되었다.
양성자 NMR은 C-라벨링 실험에 사용된 첫 번째 기술이었다.이 방법을 사용하면 특정 대사물 풀 내의 단일 양성자화 탄소 위치를 다른 위치와 [10]분리하여 관찰할 수 있다.이를 통해 특정 위치에 라벨이 부착된 등방체 비율을 알 수 있습니다.양성자 NMR의 한계는 대사물에 탄소 원자가 n개일 경우, 최대 n개의 다른 위치 농축 값만 있을 수 있으며, 이는 전체 동위원소체 정보의 극히 일부에 불과하다.양성자 NMR 라벨링의 사용은 제한적이지만, 순수한 양성자 NMR 실험은 더 많은 동위원소체 정보를 가진 실험보다 평가하기가 훨씬 쉽다.
프로톤 NMR과 더불어 C NMR 기술을 사용하면 동위원소체 분포를 보다 자세히 볼 수 있습니다.라벨이 부착된 탄소 원자는 분자 [10]내 직접 이웃의 라벨 상태에 따라 다른 초미세 분할 신호를 생성합니다.인접한 탄소 원자에 라벨을 붙이지 않으면 싱글트 피크가 나타난다.인접한 탄소 원자 하나만 라벨이 붙어 있으면 더블렛 피크가 나타납니다.더블렛 분할의 크기는 인접한 탄소 원자의 작용기에 따라 달라집니다.인접한 2개의 탄소 원자가 라벨로 표시되어 있는 경우, 2개의 2개의 2개의 2개의 2개의 2개의 2개의 2개의 2개의 2개의 2개의 2개의 2개의 분할이 동일할 경우 3개의 3개의 3개의 2개의 2개의 2개의 2개의 2개의 2개의 2개의
대사 플럭스 분석 목적으로 NMR 기술을 사용하는 것의 단점은 NMR이 다소 전문화된 분야이기 때문에 다른 NMR 애플리케이션과 다르다는 것이다.일부 연구팀에서는 NMR 분광계를 직접 사용할 수 없습니다.NMR 측정 매개변수의 최적화와 피크 구조의 적절한 분석에는 숙련된 NMR 전문가가 필요합니다.또한 특정 대사물은 추가적인 동위원소체 데이터를 얻기 위해 특별한 측정 절차를 필요로 할 수 있다.또한 피크 영역의 정확한 양을 결정하고 얽힌 싱글릿, 더블렛 및 트리플렛 피크의 분해를 식별하기 위해 특별히 개조된 소프트웨어 도구가 필요합니다.
핵자기공명과 달리 질량분석법(MS)은 대사속 분석 실험에 더 적합하고 민감한 또 다른 방법이다.MS 계측기는 다양한 변종으로 제공됩니다.2차원 핵자기공명(2D-NMR)과는 달리 MS 계측기는 [10]가수분해물과 직접 작동합니다.
가스 크로마토그래피-질량분석(GC-MS)에서 MS는 가스 크로마토그래프에 결합되어 가수분해물의 화합물을 분리한다.그런 다음 GC 컬럼에서 유출되는 화합물은 이온화되고 동시에 단편화된다.GC-MS를 사용하면 분자 이온의 질량 동위원소체뿐만 아니라 여러 조각의 질량 동위원소체 스펙트럼도 측정되므로 측정 정보가 크게 증가한다는 장점이 있다.
액체 크로마토그래피-질량분석(LC-MS)에서는 GC를 액체 [11]크로마토그래프로 치환한다.가장 큰 차이점은 화학적 유도체가 필요하지 않다는 것이다.단, LC-MS를 MFA에 적용하는 경우는 거의 없습니다.
각각의 경우 MS 기기는 특정 아이소토포머 분포를 분자량으로 나눈다.동일한 수의 표식 탄소 원자를 포함하는 특정 대사물의 모든 동위원소체가 하나의 피크 신호로 수집된다.모든 아이소토포머는 MS 스펙트럼에서 정확히 하나의 피크에 기여하기 때문에 각 피크에 대해 백분율 값을 계산하여 질량 아이소토포머 [10]비율을 산출할 수 있습니다.n개의 탄소 원자를 가진 대사물의 경우 n+1 측정치를 생성한다.정규화 후에도 정확히 n개의 유익한 질량 등방체 양이 [10]남는다.
MS 기술을 사용하는 것의 단점은 가스 크로마토그래피의 경우 전하를 띤 분자를 얻기 위해 화학 유도체를 통해 샘플을 준비해야 한다는 것이다.시료를 추출하는 데 사용되는 화합물은 많습니다.N, N-디메틸포름아미드디메틸아세탈(DMFDMA)[12] 및 N-(tert-butydetimethylsilyl)-N-메틸트리플루오로아세트아미드(MTBSTFA)는 아미노산 유도체에 사용된 화합물의 2가지 예이다.
또한 관찰된 강력한 동위원소 효과는 GC 컬럼에 서로 다른 라벨로 표시된 동위원소체의 유지 시간에 영향을 미친다.GC 컬럼의 오버로드도 [13]방지해야 합니다.
마지막으로 탄소 이외의 다른 원자의 자연적 풍부함도 질량 등방체 스펙트럼의 교란을 일으킨다.예를 들어, 분자의 각 산소 원자는 O 동위원소 및 O 동위원소로 존재할 수 있다.동위원소의 자연적 풍부함의 더 큰 영향은 동위원소 Si와 Si의 자연적 풍부함과 함께 실리콘의 영향이다.Si는 MS [10]기술용 유도제에 사용된다.
인간 미네랄 영양 연구에 대한 응용
인간의 미네랄 영양과 신진대사를 연구하기 위해 안정적인 동위원소 추적기를 사용하는 것은 1960년대에 [14]처음 보고되었다.방사성 동위원소는 이전 수십 년 동안 인간의 영양 연구에 사용되었지만, 안정적인 동위원소는 특히 임신 및 수유 여성과 어린이와 같이 방사선 피폭에 대한 우려가 높은 주제에서 더 안전한 선택지를 제시하였다.안정 동위원소에 의해 제공되는 다른 이점으로는 적절한 방사성 동위원소가 없는 원소를 연구하고 장기 추적자 거동을 연구하는 기능이 [15][16]있다.따라서 안정 동위원소의 사용은 동위원소 농축 물질과 무기 질량 분석기의 가용성이 증가함에 따라 보편화되었다.방사성 동위원소 대신 안정적인 동위원소 사용에는 몇 가지 단점이 있다. 즉, 자연적으로 존재하는 광물을 교란시킬 가능성이 있는 대량의 추적기가 필요하다. 분석 샘플 준비는 더 복잡하고 질량 분석기기는 더 비싸다. 전신 또는 특정 조직에 추적기가 있어야 한다.주석을 [17]외부에서 측정합니다.그럼에도 불구하고, 인간 연구에서 안정적인 동위원소를 표준으로 만드는 장점이 우세하다.
인간의 건강에 필수적이고 영양학자들이 특히 관심을 갖는 대부분의 미네랄은 안정적인 동위원소를 가지고 있으며, 일부는 낮은 자연 [15][17]함량 때문에 생물 추적기로 적합하다.철, 아연, 칼슘, 구리, 마그네슘, 셀레늄 및 몰리브덴은 동위원소 추적법이 적용된 안정적인 동위원소를 가진 필수 광물 중 하나이다.특히 철분, 아연, 칼슘은 광범위하게 연구되어 왔다.
연구되는 미네랄 영양/대사의 측면에는 흡수(위장에서 체내로), 분포, 저장, 배설 및 이러한 과정의 동태가 포함된다.동위원소 추적기는 피험자에게 경구 투여(식품 유무 또는 미네랄 보충제와 함께) 및/또는 정맥 내 투여된다.그런 다음 혈장, 적혈구, 소변 및/또는 [18][19]대변에서 동위원소 농도를 측정한다.모유와[20] 장 내용물에서도 농축도가 측정되었다.추적기 실험 설계는 때때로 신진대사의 차이로 인해 미네랄 간에 차이가 있습니다.예를 들어 철분 흡수는 일반적으로 적혈구에 트레이서를 삽입하여 결정되며, 아연 또는 칼슘 흡수는 혈장, 소변 또는 [21][22]대변의 트레이서 외관으로부터 측정됩니다.단일 연구에서 여러 동위원소 추적기를 투여하는 것이 일반적이며, 보다 신뢰할 수 있는 측정 방법을 사용하고 신진대사의 여러 측면을 동시에 조사할 수 있다.
흔히 생물학적 가용성으로 간주되는 식단에서 미네랄 흡수 측정은 영양 연구에 동위원소 추적기 방법을 가장 일반적으로 적용하는 것이다.이러한 연구의 목적은 음식 유형(예: 식물 대 동물 소스, 모유 대 조제식), 식단의 다른 구성 요소(예: 피테이트), 질병 및 대사 장애(예: 환경 장기능 장애), 생식 주기, 식단 내 미네랄의 양, 만성 미네랄의 섭취에 대한 조사이다.결핍, 대상 연령 및 항상성 메커니즘.이러한 연구 결과가 광물에 대해 이용 가능한 경우, 이러한 [23][24]연구 결과는 광물의 인간 생리학적 및 식이학적 요구 사항을 추정하기 위한 기초가 될 수 있다.
추적자가 미네랄 흡수 및 대사를 관찰하기 위해 식품과 함께 투여될 때, 추적자는 내인성 또는 외인성 [25][26]라벨의 형태일 수 있다.고유 라벨은 식품의 생산 과정에서 식품에 도입된 동위원소이며, 따라서 식품의 천연 미네랄 함량을 풍부하게 하는 반면, 외인성 라벨은 연구 중에 식품에 추적자 동위원소를 추가하는 것을 의미한다.이것은 매우 시간이 많이 걸리고 비용이 많이 드는 접근법이기 때문에 본질적인 라벨링은 일상적으로 사용되지 않는다.다양한 식품의 내인성 및 외인성 라벨을 사용한 흡수 측정을 비교한 연구는 일반적으로 두 가지 라벨링 방법 간에 잘 일치하는 것으로 나타났으며, 외인성 및 천연 미네랄이 인간의 위장관에서 비슷하게 취급된다는 가설을 뒷받침한다.
농축은 질량분석에 의해 기준 동위원소에 대한 추적 동위원소 비율인 동위원소 비율 측정에서 정량화된다.농축의 다중 정의와 계산은 서로 다른 [27]연구자들에 의해 채택되었다.여러 트레이서를 동시에 사용할 경우 농축 계산은 더욱 복잡해집니다.농축 동위원소 제제는 결코 동위원소 순수하지 않기 때문에, 즉 모든 원소의 동위원소를 부자연스러운 풍부함으로 포함하므로, 다중 동위원소 추적기의 농축 계산은 다른 [27]추적기의 존재에 의한 각 동위원소 비율의 섭동을 고려해야 한다.
광물결핍의 만연과 자원빈국에서의 인간의 건강과 웰빙에 대한 중대한 영향 때문에 국제원자력기구는 최근 이 지식을 서양의 학회 이상의 연구자들에게 전파하기 위해 안정적인 동위원소 방법에 대한 상세하고 포괄적인 설명을 발표했다.nters([21][28]nters)
방사성 동위원소 라벨
방사성 동위원소 라벨링은 샘플이 시스템을 통과하는 과정을 추적하는 기술이다.이 물질은 화학 조성에 방사성핵종을 포함시켜 "라벨링"된다.이러한 붕괴가 발생하면 방출되는 방사선을 감지하여 이들의 존재를 확인할 수 있습니다.방사성 동위원소 라벨링은 동위원소 라벨링의 특별한 경우이다.
이러한 목적을 위해 특히 유용한 방사성 붕괴 유형은 양전자 방출이다.양전자가 전자와 충돌할 때, 그것은 정반대의 방향으로 이동하는 두 개의 고에너지 광자를 방출한다.만약 양전자가 고체 물체 안에서 생성된다면, 그것은 1밀리미터 [citation needed]이상 이동하기 전에 이것을 할 것이다.이 두 광자를 모두 검출할 수 있다면 붕괴 현상의 위치를 매우 정밀하게 결정할 수 있다.
엄격히 말하면, 방사성 동위원소 라벨링은 실험자가 인공적으로 방사능을 도입한 경우만 포함되지만, 일부 자연현상에서는 유사한 분석을 수행할 수 있다.특히 방사선 측정 연대는 밀접하게 관련된 원리를 사용한다.
프로테오믹스 응용 프로그램
게놈에 의해 발현되는 단백질의 전체 세트에 대한 연구인 프로테오믹스에서 질병을 식별하는 바이오마커는 단백질 [29]수준을 추정하기 위해 사용되는 동위원소 표지 형태의 아미노산을 제공하는 세포 배양(SILAC)에서 아미노산에 의한 안정적인 동위원소 표기의 사용을 포함할 수 있다.단백질 재조합에서, 조작된 단백질은 다량으로 생성되며, 동위원소 라벨링은 관련 단백질을 테스트하는 도구이다.이 방법은 C 또는 N으로 선택적으로 핵을 농축하거나 핵에서 H를 고갈시키는 것이었다.재조합체는 [30]질소의 공급원으로 염화 N-아모늄을 포함하는 배지와 함께 E.coli로 발현될 것이다.그 결과 N개의 라벨이 붙은 단백질은 고정화된 금속 친화력과 그 백분율로 정제된다.라벨 부착 단백질의 수율을 높이고 동위원소 라벨 부착 배지의 비용을 절감하기 위해 대체 절차는 라벨 부착 [31]배지의 최소 양에 도입하기 전에 라벨 부착되지 않은 배지를 사용하여 세포량을 증가시킨다.동위원소 라벨링의 또 다른 적용은 DNA 합성 측정, 즉 시험관 내 세포 증식이다.H-티미딘3 라벨을 사용하여 세포 [32]내 합성 패턴(또는 배열)을 비교합니다.
생태계 프로세스 분석을 위한 응용 프로그램
동위원소 추적기는 자연계, 특히 지상 및 수중 환경에서의 과정을 조사하기 위해 사용된다.토양과학에서는 질소순환을 연구하기 위해 N 트레이서를 광범위하게 사용하는 반면 탄소의 안정적이고 방사성 동위원소인 C와 C는 유기화합물의 회전 및 자가영양에 의한 CO의 고정화를2 연구하는데 사용된다.예를 들어, Marsh 등입니다.(2005)는 암모니아 산화제에 의한 에너지원(암모니아 산화)과 탄소원(화학적 영양성 탄소 고정)[33]의 이용을 입증하기 위해 이중 라벨(15N- 및 C) 요소를 사용했다.중수소수는 또한 나무나[34] [35]생태계에서 물의 운명과 나이를 추적하는데 사용된다.
해양학 응용 프로그램
추적기는 또한 해양학에서 광범위한 과정을 연구하기 위해 광범위하게 사용된다.사용된 동위원소는 일반적으로 잘 확립된 선원과 형성 및 붕괴 속도에서 자연적으로 발생한다.단, 인공 동위원소는 매우 성공적으로 사용될 수 있다.연구원들은 바다의 물리적 과정에 대한 정보를 추론하기 위해 다양한 장소와 시간에서 동위원소 비율을 측정한다.
입자 수송
바다는 광범위한 입자 수송망이다.토륨 동위원소는 연구자들이 물질의 수직과 수평의 움직임을 해독하는 데 도움을 줄 수 있다.234바다에서의 생산율은 일정하고 명확하게 정의되어 있으며 반감기는 24일입니다.이 자연발생 동위원소는 깊이에 따라 선형적으로 변화하는 것으로 나타났다.따라서 이 선형 패턴의 변화는 입자의 Th 수송에 기인할 수 있다.예를 들어 지표수의 동위원소 비율이 낮으면 값이 몇 미터 아래쪽에 매우 높으면 수직 플럭스를 나타낸다.또한 토륨 동위원소를 특정 깊이 내에서 추적하여 입자의 [36]횡방향 수송을 해독할 수 있다.
순환
베이, 하구 및 지하수와 같은 국소 시스템 내 순환은 라듐 동위원소로 조사할 수 있다.223Ra의 반감기는 11일이며 강이나 지하수원의 특정 위치에서 자연적으로 발생할 수 있다.원류 강에서 물이 만이나 하구로 유입되면 라듐의 동위원소 비율이 감소합니다.여러 위치에서 Ra의 양을 측정함으로써 순환 패턴을 [37]해독할 수 있다.이 정확한 과정은 지하수의 [38]이동과 방류를 연구하는 데도 사용될 수 있다.
납의 다양한 동위원소를 사용하여 전 지구적 규모의 순환을 연구할 수 있습니다.다른 해양(대서양, 태평양, 인도 등)은 다른 동위원소 신호를 가진다.이것은 다른 [39]해양에 있는 퇴적물과 암석의 동위원소 비율의 차이에서 비롯된다.납의 다른 동위원소들은 50-200년의 반감기를 가지고 있기 때문에, 동위원소 비율이 해양 전체에 걸쳐 균질화되기에는 충분한 시간이 없다.따라서 Pb 동위원소 비율의 정밀한 분석을 이용하여 다양한 [40]해양의 순환을 연구할 수 있다.
구조 과정과 기후변화
반감기가 매우 긴 동위원소와 그 붕괴 생성물은 구조론이나 극단적인 기후 변화와 같은 수백만 년 과정을 연구하는 데 사용될 수 있다.예를 들어 루비듐-스트론튬 연대 측정에서 얼음 코어 내에서 스트론튬(87Sr/86Sr)의 동위원소 비율을 분석하여 지구의 수명 동안의 변화를 조사할 수 있다.얼음핵 내의 이 비율의 차이는 지구 화학에 [40]큰 변화가 있음을 나타낼 것이다.
상기 공정은 자연발생 동위원소를 이용하여 측정할 수 있다.그럼에도 불구하고 인공 동위원소는 해양학적 측정에 매우 유용하다.핵무기 실험은 많은 양의 희귀한 동위원소를 세계 바다에 방출했다.3H, I, Cs는 바닷물에 용해되어 있고 Am, Pu는 입자에 부착되어 있다.물에 용해된 동위원소는 지구 순환 연구에 특히 유용하다.예를 들어, 바다 내 측방향 동위원소 비율의 차이는 강한 물 앞면 또는 회전을 나타낼 수 있다.[41]반대로 입자에 부착된 동위원소는 물기둥 내의 질량 수송을 연구하는 데 사용될 수 있다.예를 들어 Am 또는 Pu의 수치가 높으면 깊은 곳에서 관찰될 때 하강하거나 [42]표면에서 관찰될 때 상승할 수 있습니다.
동위원소 라벨링 방법
「 」를 참조해 주세요.
- 방사성핵종 사용
- 생물학에서의 방사능
- 방사성 트레이서
- 아이소토포머
- 아이소토폴로그
- 이소바릭
- 동위원소 희석
- 금속 카르보닐의 적외선 분광법
- 동위원소 방법 태깅에 의한 오가넬 단백질의 국재성
레퍼런스
- ^ Blake, Michael E.; Bartlett, Kevin L.; Jones, Maitland (2003). "Am-Benzyne too-Benzyne Conversion through a 1,2-Shift of a Phenyl Group". Journal of the American Chemical Society. 125 (21): 6485–6490. doi:10.1021/ja0213672. ISSN 0002-7863. PMID 12785789.
- ^ Dickin, A.P., 2005.방사성 동위원소 지질학, 캠브리지 대학 출판부.
- ^ a b Kruger, Nicholas; Antje von Schaewen (2003). "The oxidative pentose phosphate pathway: structure and organisation" (PDF). Current Opinion in Plant Biology. 6 (3): 236–246. doi:10.1016/s1369-5266(03)00039-6. PMID 12753973. Archived from the original (PDF) on April 15, 2012.
- ^ [1] 2012년 4월 4일 Wayback Machine에서 아카이브 완료
- ^ Wiechert, Wolfgang (2001). "13C Metabolic Flux Analysis". Metabolic Engineering. 3 (3): 195–206. doi:10.1006/mben.2001.0187. PMID 11461141.
- ^ a b Lee, Sang Yup; Park, Jong Myoung, and Kim, Tae Yong (2011). Chapter Four: Application of Metabolic Flux Analysis in Metabolic Engineering. Methods in Enzymology. Vol. 498. pp. 67–93. doi:10.1016/B978-0-12-385120-8.00004-8. ISBN 9780123851208. PMID 21601674.
{{cite book}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Stephanopoulos, Gregory; Aristos A. Aristidou (1998). "Chapter 9: Methods for the Experimental Determination of Metabolic Fluxes by Isotope Labeling". Metabolic engineering: principles and methodologies. San Diego: Academic Press. pp. 356–404. ISBN 978-0-12-666260-3.
- ^ Stephanopoulos, Gregory (1999). "Metabolic Fluxes and Metabolic Engineering". Metabolic Engineering. 1 (1): 1–11. doi:10.1006/mben.1998.0101. PMID 10935750.
- ^ Klamt, Steffen; Jorg Stelling, Martin Ginkel, and Ernst Dieter Gilles (2003). "FluxAnalyzer: exploring structure, pathways, and flux distributions in metabolic networks on interactive flux maps". Bioinformatics. 19 (2): 261–269. doi:10.1093/bioinformatics/19.2.261. PMID 12538248.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ a b c d e f Wiechert, Wolfgang (2001). "13C Metabolic Flux Analysis". Metabolic Engineering. 3 (3): 195–206. doi:10.1006/mben.2001.0187. PMID 11461141.
- ^ 드 그라프, A. A. (2000c).대사 플럭스 분석에 13C 라벨링 및 NMR 분광법 사용.바이오 테크놀로지의 NMR: 이론과 응용(J.-N. Barbotin 및 J.-C.Portais, Eds), Horizon Scientific Press.
- ^ Christensen, B. 및 Nielsen, J.(2000).13C 표식 포도당을 이용한 Penicillium chrysogenum의 대사망 분석.바이오테크놀.바이오엥. 68, 652/659
- ^ a b 다우너, M. 및 사우어, U.(2000).아미노산의 GC-MS 분석은 동위원소체 균형에 대한 풍부한 정보를 빠르게 제공합니다.바이오테크놀.프로그 16, 642-649
- ^ Turnlund, Judith (1989). "The use of stable isotopes in mineral nutrition research". Journal of Nutrition. 119 (1): 7–14. doi:10.1093/jn/119.1.7. PMID 2643698.
- ^ a b Woodhouse, Leslie; Abrams, Steven (2001). "Advances in Stable-isotope Methodology". In Lowe, Nicola; Jackson, Malcolm (eds.). Advances in Isotope Methods for the Analysis of Trace Elements in Man. Boca Raton, FL: CRC Press. pp. 1–22. ISBN 0-8493-8730-2. OCLC 44579072.
- ^ Patterson, Kristine; Veillon, Claude (2001). "Stable isotopes of minerals as metabolic tracers in human nutrition research". Experimental Biology and Medicine. 226 (4): 271–282. doi:10.1177/153537020122600403. PMID 11368418. S2CID 41966154.
- ^ a b Sandstrom, Brittmarie (1996). "Overview of isotope methods and inorganic nutrient metabolism". In Mellon, Fred; Sandstrom, Brittmarie (eds.). Stable isotopes in human nutrition : inorganic nutrient metabolism. London: Harcourt Brace. pp. 3–9. ISBN 0-12-490540-4. OCLC 35224694.
- ^ van Dokkum, Wim; Fairweather-Tait, Susan; Hurrell, Richard; Sandstrom, Brittmarie (1996). "Study Techniques". In Mellon, Fred; Sandstrom, Brittmarie (eds.). Stable Isotopes in Human Nutrition: Inorganic Nutrient Metabolism. London: Academic Press. pp. 23–42. ISBN 0-12-490540-4.
- ^ Fairweather-Tait, Susan; Fox, Tom; Harvey, L; Dainty, Jack (2001). "Methods for Analysis of Trace-element Absorption". In Lowe, Nicola; Jackson, Malcolm (eds.). Advances in Isotope Methods for the Analysis of Trace Elements in Man. Boca Raton, FL: CRC Press. pp. 59–80. ISBN 0-8493-8730-2.
- ^ Davidsson, Lena (2001). "Trace-element Studies in Infants and Pregnant or Lactating Women". In Lowe, Nicola; Jackson, Malcolm (eds.). Advances in Isotope Methods for the Analysis of Trace Elements in Man. Boca Raton, FL: CRC Press. pp. 167–186. ISBN 0-8493-8730-2.
- ^ a b Davidsson, L. (Lena), 1957- (2012). Assessment of iron bioavailability in humans using stable iron isotope techniques. International Atomic Energy Agency. Vienna: International Atomic Energy Agency. ISBN 978-92-0-126510-4. OCLC 819377220.
{{cite book}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Krebs, Nancy; Miller, Leland; Naake, Vernon; Lei, Sian; Westcott, Jamie; Fennessey, Paul; Hambidge, Michael (1995). "The use of stable isotope techniques to assess zinc metabolism". Journal of Nutritional Biochemistry. 6 (6): 292–301. doi:10.1016/0955-2863(95)00043-Y.
- ^ DRI : dietary reference intakes for vitamin A, vitamin K, arsenic, boron, chromium, copper, iodine, iron, manganese, molybdenum, nickel, silicon, vanadium, and zinc : a report of the Panel on Micronutrients ... and the Standing Committee on the Scientific Evaluation of Dietary Reference Intakes, Food and Nutrition Board, Institute of Medicine. Institute of Medicine (U.S.). Panel on Micronutrients. Washington, D.C.: National Academy Press. 2001. ISBN 0-309-51199-2. OCLC 52777031.
{{cite book}}: CS1 유지보수: 기타 (링크) - ^ European Food Safety Authority (2014). "Scientific Opinion on Dietary Reference Values for zinc". EFSA Journal. 12 (10): 3844. doi:10.2903/j.efsa.2014.3844. ISSN 1831-4732.
- ^ Fairweather-Tait, Susan; Fox, Tom (1996). "Intrinsic and Extrinsic Labelling of Inorganic Nutrients in Food Studies". In Mellon, Fred; Sandstrom, Brittmarie (eds.). Stable Isotopes in Human Nutrition: Inorganic Nutrient Metabolism. London: Academic Press. pp. 15–21. ISBN 0-12-490540-4.
- ^ IAEA. (2018). Assessment of Zinc Metabolism in Humans Using Stable Zinc Isotope Techniques. Vienna: IAEA. pp. 34–36. ISBN 978-92-0-108418-7. OCLC 1108521498.
- ^ a b IAEA. (2018). Assessment of Zinc Metabolism in Humans Using Stable Zinc Isotope Techniques. Vienna: IAEA. pp. 50–58. ISBN 978-92-0-108418-7. OCLC 1108521498.
- ^ IAEA. (2018). Assessment of Zinc Metabolism in Humans Using Stable Zinc Isotope Techniques. Vienna: IAEA. ISBN 978-92-0-108418-7. OCLC 1108521498.
- ^ "세포 배양 시 아미노산으로 안정적인 동위원소 표시"SILAC. Paydey Lab, Web, 2011년 11월 23일
- ^ Bunk, David.M. "임상 단백질 바이오마커의 질량 분석 정량화를 위한 내부 표준으로 사용하기 위한 안정적인 동위원소 라벨 단백질의 발현." NIST, 재료 측정 실험실.NIST(National Institute of Standards and Technology, National Institute of Standards and Technology)는 2009년 3월 30일 미국 상무부의 기관입니다.Web. 2011년 11월 19일
- ^ Marley, Jonathan; Lu, Min; Bracken, Clay (2001). "A methode for efficient isotopic labeling and recombinent protein". Journal of Biomolecular Labeling. 20 (1): 71–75. doi:10.1023/a:1011254402785. PMID 11430757. S2CID 7811948.
- ^ 독일인, 제임스"인간 혈액 세포의 염색체에서의 DNA 합성 패턴." 록펠러 대학은 20.1 37-65를 출판했다.인쇄.
- ^ 마쉬, K.L., G.K. 심스, R.L. 멀베이니.2005. 토양에 첨가된 14C 및 15N 라벨 요소의 운명과 관련하여 요소에서 자가영양 암모니아 산화세균에 대한 가용성.바이올 퍼트흙. 42:137-145.
- ^ James, Shelley A.; Meinzer, Frederick C.; Goldstein, Guillermo; Woodruff, David; Jones, Timothy; Restom, Teresa; Mejia, Monica; Clearwater, Michael; Campanello, Paula (2003-01-01). "Axial and radial water transport and internal water storage in tropical forest canopy trees". Oecologia. 134 (1): 37–45. doi:10.1007/s00442-002-1080-8. ISSN 1432-1939.
- ^ Evaristo, Jaivime; Kim, Minseok; Haren, Joost van; Pangle, Luke A.; Harman, Ciaran J.; Troch, Peter A.; McDonnell, Jeffrey J. (2019). "Characterizing the Fluxes and Age Distribution of Soil Water, Plant Water, and Deep Percolation in a Model Tropical Ecosystem". Water Resources Research. 55 (4): 3307–3327. doi:10.1029/2018WR023265. hdl:10150/634013. ISSN 1944-7973.
- ^ Coppola, L.; Roy-Barman, M.; et al. (2006). "Thorium isotopes as tracers of particles dynamics and deep water circulation in the Indian sector of the Southern Ocean (ANTARES IV)". Marine Chemistry. 100 (3–4): 299–313. doi:10.1016/j.marchem.2005.10.019.
- ^ Hougham, A. L.; Moran, S. B.; et al. (2008). "Seasonal changes in submarine groundwater discharge to coastal salt ponds estimated using 226Ra and 228Ra as tracers". Marine Chemistry. 109 (3–4): 268–278. doi:10.1016/j.marchem.2007.08.001.
- ^ Swarzenski, P. W.; Reich, C.; et al. (2007). "Ra and Rn isotopes as natural tracers of submarine groundwater discharge in Tampa Bay, Florida". Marine Chemistry. 104 (1–2): 69–84. doi:10.1016/j.marchem.2006.08.001.
- ^ Hickey-Vargas, R.; Bizimis, M.; Deschamps, A. (2008). "Onset of the Indian Ocean isotopic signature in the Philippine Sea Plate: Hf and Pb isotope evidence from Early Cretaceous terranes". Earth and Planetary Science Letters. 268 (3–4): 255–267. Bibcode:2008E&PSL.268..255H. doi:10.1016/j.epsl.2008.01.003.
- ^ a b Haley, B. A.; Frank, M.; et al. (2008). "Radiogenic isotope record of Arctic Ocean circulation and weathering inputs of the past 15 million years". Paleoceanography. 23 (1): PA1S13. Bibcode:2008PalOc..23.1S13H. doi:10.1029/2007PA001486.
- ^ Povinec, P. P.; Breier, R.; et al. (2011). "Tracing of water masses using a multi isotope approach in the southern Indian Ocean". Earth and Planetary Science Letters. 302 (1–2): 14–26. Bibcode:2011E&PSL.302...14P. doi:10.1016/j.epsl.2010.11.026.
- ^ Lee, S.-H.; Povinec, P. P.; et al. (2009). "Radionuclides as tracers of water fronts in the South Indian Ocean – ANTARES IV Results". Journal of Oceanography. 65 (3): 397–406. doi:10.1007/s10872-009-0035-7. S2CID 131348352.
외부 링크
| 라이브러리 리소스 정보 동위원소 라벨 |




