삼투압
Osmotic pressure삼투압은 용액의 순수 용매가 [1]반투과성 막을 통해 내부로 흐르지 않도록 하기 위해 가해야 하는 최소 압력이다.또한 용액이 순수 용매를 삼투압에 의해 흡수되는 경향의 측정값으로도 정의된다.잠재적 삼투압은 용액이 반투과성 막에 의해 순수한 용매로부터 분리되었을 때 발생할 수 있는 최대 삼투압이다.
삼투압은 다른 농도의 용질을 포함하는 두 용액이 선택적으로 투과되는 막에 의해 분리될 때 발생합니다.용제 분자는 저농도 용액에서 고농도 용액으로 우선적으로 막 속을 통과한다.용매 분자의 이동은 평형을 [1][2]이룰 때까지 계속될 것이다.
이론과 측정

Jacobus van't Hoff는 삼투압과 용질 농도 사이의 정량적 관계를 다음 방정식으로 나타내었다.
여기서 \Pi는 삼투압, i는 무차원 van't Hoff 지수, c는 용질의 몰 농도, R은 이상적인 가스 상수, T는 절대 온도(통상 켈빈 단위)이다.이 공식은 용질 농도가 충분히 낮아서 이상적인 용액으로 취급할 수 있을 때 적용된다.농도에 대한 비례성은 삼투압이 결합 특성이라는 것을 의미한다.이 공식은 P V T {\ P 의 이상 가스 법칙과 유사합니다. 여기서 n은 부피 V에 포함된 가스 분자의 총 몰 수이고 n/V는 가스 분자의 몰 농도입니다.Harmon Northrop Morse와 Frazer는 농도 단위가 [3]몰이 아닌 몰일 경우 이 방정식이 더 농축된 용액에 적용된다는 것을 보여주었습니다. 그래서 몰리티를 사용할 때 이 방정식은 모스 방정식이라고 불립니다.
보다 농축된 용액의 경우, van't Hoff 방정식은 용질 농도 c에서 멱급수로 확장될 수 있다.첫 번째 근사치까지,
여기서 0 _은 이상적인 압력이고 A는 경험적 파라미터입니다.매개변수 A의 값(및 고차 근사치의 매개변수 값)을 사용하여 피처 매개변수를 계산할 수 있습니다.경험적 매개변수는 열역학적인 의미에서 이상적인 솔루션이 아닌 이온 및 비이온성 용액의 거동을 정량화하기 위해 사용된다.
Pfeffer 세포는 삼투압 측정을 위해 개발되었습니다.
적용들
삼투압 측정은 분자량의 결정에 사용될 수 있다.
삼투압은 생물학적 [4]세포에 영향을 미치는 중요한 요인이다.삼투압 조절은 삼투압 균형에 도달하는 유기체의 항상성 메커니즘이다.
생물학적 세포가 저혈압 환경에 있을 때, 세포 내부에 물이 축적되고, 물이 세포막을 가로질러 세포로 흘러 들어가 세포 팽창을 일으킨다.식물 세포에서, 세포벽은 팽창을 제한하고, 그로 인해 세포벽이 팽압이라고 불리는 내부로부터 압력을 받게 됩니다.팽윤압은 초본식물을 똑바로 세울 수 있게 해준다.그것은 또한 식물이 기공의 구멍을 어떻게 조절하는지에 대한 결정적 요소이다.동물 세포에서 과도한 삼투압은 세포분해를 초래할 수 있다.
삼투압은 정수 과정에서 일반적으로 사용되는 여과("역삼투")의 기초이다.챔버에 정제수를 넣어 물과 그 안에 용해된 용질보다 더 큰 압력을 가한다.챔버의 일부는 물 분자를 통과시키는 차등 투과성 막으로 열려 있지만 용질 입자는 통과시키지 않습니다.바닷물의 삼투압은 약 27atm입니다.역삼투는 바닷물의 담수를 담수화한다.
반트 호프 공식의 도출
시스템이 균형에 도달한 시점에서 시스템을 고려하십시오.이에 대한 조건은 막의 양쪽에 있는 용제의 화학적 잠재력이 동일하다는 것입니다(평형 방향으로 자유롭게 흐를 수 있기 때문입니다).순수 용제를 포함하는 컴파트먼트의 전위는 0 () { 입니다. 서p {\ p는 압력입니다.다른 세계는 칸은 용질이 포함된에서 용제의 화학적 잠재력은 용제의 몰비, 0<>)v<1{0<, x_{v\displaystyle}< 1}에. 게다가, 이 칸′{\displaystyle p'}동업- 다른 압력 추정할 수 있다. 그러므로 우리는톤의 화학적 잠재력을 쓸 수가 달려 있그는 solventv ( v , _로 표기합니다. p + { p' = 라고 표기하면 화학적 전위의 균형은 다음과 같습니다.
여기서 두 구획 p - \ \ p의 압력차는 용질이 가하는 삼투압으로 정의한다.압력을 유지하면 용질을 추가하면 화학적 잠재력이 감소합니다(엔트로피 효과).따라서 화학적 잠재력의 손실을 보상하기 위해 용액의 압력을 증가시켜야 한다.
삼투압인(\를 구하기 위해 용질을 포함한 용액과 순수와의 평형을 고려하였다.
왼쪽은 다음과 같이 쓸 수 있습니다.
- v ( v , + ) 0 ( + ) + v v \ style \ _ { } ( x { ; p + ) = \ { ( + \ ) +\ ln ( { } , {
여기서 v _는 용제의 활성 계수입니다. v \ style \ _ { } _ { }} 제품은 용제의 활성이라고도 하며, 물은 w \_ { 의 물 입니다.압력 추가는 팽창 에너지에 대한 식을 통해 표현됩니다.
서 V m{ _ { } where 、 mol ) 。위에 제시된 식을 전체 시스템의 화학 전위 방정식에 삽입하고 정렬하면 다음과 같은 결과가 됩니다.
액체가 압축할 수 없는 경우 몰 부피는 일정합니다.m ( V \ V _ { } \ V _ { } 。적분은 V \ style \ _ { }가 됩니다.이렇게 해서
활성 계수는 농도와 온도의 함수이지만 희석 혼합물의 경우 1.0에 매우 가깝기 때문에
용질의 몰 분율 는 1- v이므로 ln v은 lndisplaystyle \로 대체할 수 있습니다. style \lns})은 xdisplaystyle x_가 작을 사용할 수 있습니다.
몰 s는 n/ ( s + v){입니다.s(\s})가 작을 x / displaystyle 로 근사할 수도 있습니다.는 V = / { _ { m }/ _ { v} 。이것들을 조합하면 다음과 같은 결과를 얻을 수 있다.
소금 수용액의 경우 이온화를 고려해야 한다.예를 들어, NaCl 1몰은 이온 2몰로 이온화된다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b Voet, Donald; Judith Aadil; Charlotte W. Pratt (2001). Fundamentals of Biochemistry (Rev. ed.). New York: Wiley. p. 30. ISBN 978-0-471-41759-0.
- ^ Atkins, Peter W.; de Paula, Julio (2010). "Section 5.5 (e)". Physical Chemistry (9th ed.). Oxford University Press. ISBN 978-0-19-954337-3.
- ^ Lewis, Gilbert Newton (1908-05-01). "The Osmotic Pressure of Concentrated Solutions and the Laws of the Perfect Solution". Journal of the American Chemical Society. 30 (5): 668–683. doi:10.1021/ja01947a002. ISSN 0002-7863.
- ^ 살아있는 세포 부피의 기탄성 삼투압 조절, Iscience, 24(12), 103482 (120) doi=10.1016/j.isci.201.1982


 삼투압, i는
삼투압, i는  n은 부피 V에 포함된 가스 분자의 총 몰 수이고 n/V는 가스 분자의 몰 농도입니다.
n은 부피 V에 포함된 가스 분자의 총 몰 수이고 n/V는 가스 분자의 몰 농도입니다.
 이상적인 압력이고 A는 경험적 파라미터입니다.매개변수 A의 값(및 고차 근사치의 매개변수 값)을
이상적인 압력이고 A는 경험적 파라미터입니다.매개변수 A의 값(및 고차 근사치의 매개변수 값)을 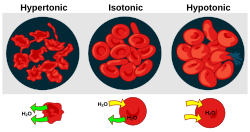

 압력입니다.다른 세계는 칸은 용질이 포함된에서 용제의 화학적 잠재력은 용제의 몰비, 0<>)v<1{0<, x_{v\displaystyle}< 1}에. 게다가, 이 칸′{\displaystyle p'}동업- 다른 압력 추정할 수 있다. 그러므로 우리는톤의 화학적 잠재력을 쓸 수가 달려 있그는 solvent
압력입니다.다른 세계는 칸은 용질이 포함된에서 용제의 화학적 잠재력은 용제의 몰비, 0<>)v<1{0<, x_{v\displaystyle}< 1}에. 게다가, 이 칸′{\displaystyle p'}동업- 다른 압력 추정할 수 있다. 그러므로 우리는톤의 화학적 잠재력을 쓸 수가 달려 있그는 solvent


 압력차는 용질이 가하는 삼투압으로 정의한다.압력을 유지하면 용질을 추가하면 화학적 잠재력이 감소합니다(
압력차는 용질이 가하는 삼투압으로 정의한다.압력을 유지하면 용질을 추가하면 화학적 잠재력이 감소합니다(

 용제의
용제의 




















