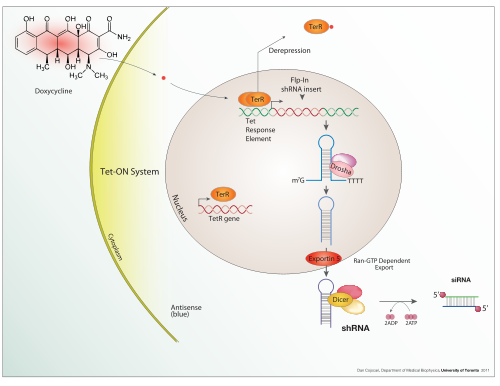
테트라사이클린 제어 전사 활성화
Tetracycline-controlled transcriptional activation테트라사이클린 제어 전사인 활성화는 항생제 테트라사이클린 또는 그 파생상품들 중 하나(예: 복시사이클린)가 있는 곳에서 전사가 역전적으로 켜지거나 꺼지는 유도성 유전자 발현 방법이다.[1]
테트라사이클린 제어 유전자 발현은 그램 음성 박테리아에서 발견되는 테트라사이클린 항생제 치료에 대한 저항성 메커니즘에 기초한다.자연적으로 Ptet 프로모터는 억제제인 테트R과 세포에서 테트라사이클린 항생제를 뿜어내는 단백질인 테타를 표현한다.[2]
Tet-On과 Tet-Off의 차이는 이름에서 알 수 있듯이, 불활성화기가 유전자를 켜거나 끄느냐가 아니라, 두 단백질 모두 발현을 활성화시킨다.차이는 테트라사이클린 또는 독시사이클린(Dox, 보다 안정적인 테트라사이클린 아날로그)에 대한 각각의 반응과 관련이 있다.Tet-Off는 Dox가 없을 때 식을 활성화하는 반면, Tet-On은 Dox가 있을 때 활성화된다.
테트오프 및 테트온
eukaryote 세포생물학 연구에 가장 일반적으로 사용되는 두 가지 유도성 표현 시스템은 Tet-Off와 Tet-On으로 명명된다.[3]포유류 세포에 관심 있는 유전자의 발현을 조절하기 위한 테트오프 시스템은 하이델베르크 대학의 헤르만 부야드와 만프레드 고센 교수가 개발하여 1992년에 처음 출판되었다.[4]
테트오프 시스템은 대장균 박테리아에서 발견된 테트라사이클린 억제제(Tetracycline repressor) 1개 단백질을 헤르페스 심플렉스 바이러스에서 발견된 또 다른 단백질인 VP16의 활성화 영역과 융합해 만든 테트라사이클린(tTA) 단백질을 활용한다.[5]
그 결과 tTA 단백질은 특정 TetO 연산자 시퀀스에서 DNA에 결합할 수 있다.대부분의 Tet-Off 시스템에서는 그러한 TetO 시퀀스의 여러 반복이 CMV 프로모터와 같은 최소 프로모터의 업스트림 위에 배치된다.최소촉진자가 있는 몇 개의 TetO 시퀀스 전체를 테트라사이클린 반응요소(TRE)라고 하는데, 그 촉진자의 유전자나 유전자의 다운스트림 발현이 증가하여 테트라사이클린 트랜스액티브 단백질 tTA의 결합에 반응하기 때문이다.
TET-Off 시스템에서는 TRE 제어 유전자의 발현이 테트라사이클린과 그 유도체에 의해 억제될 수 있다.그들은 tTA를 결합하고 TRE 시퀀스에 결합할 수 없게 만들어 TRE 제어 유전자의 불활성화를 방지한다.
테트온 시스템은 비슷한 방식으로 작동하지만 반대로 작동한다.Tet-Off 시스템에서 tTA는 Tet-On 시스템에서 Tetracycline이나 Doxyclin과 같은 그 파생상품들 중 하나에 구속되지 않는 경우에만 조작자를 구속할 수 있는 반면, rtTA 단백질은 Tetracycline에 구속되는 경우에만 조작자를 구속할 수 있다.따라서 시스템에 독시사이클린을 도입하면 유전적 산물의 전사가 시작된다.테트온 시스템은 더 빠른 응답성으로 인해 때때로 테트오프보다 선호된다.
Tet-Off 표현 시스템은 관심 유전자를 조건부로 표현하는 유전자 변형 생쥐를 생성하는 데도 사용된다.
Tet-On Advanced 및 Tet-On 3G
테트온 어드밴스드 트랜스액티베이터(rtTA2-M2S)는 기본 표현이 줄어든 것을 보여주는 테트온의 대체 버전이며, 테트오프보다 10배 낮은 도스 농도로 기능한다.또한 인간의 코돈에 최적화되어 3개의 최소 전사 활성화 영역을 활용하기 때문에 진핵 세포에서 표현이 더 안정적이라는 평가를 받고 있다.그것은 2000년에 H. Bujard와 그의 동료들에 의해 불규칙한 Tet repressor 유전자의 무작위 돌연변이 유발 후 개선된 두 개의 돌연변이 중 하나로 발견되었다.[6]Tet-On 3G(rtTA-V10이라고도 함)는 Tet-On Advanced와 유사하지만 rtTA2-M2가S 아닌 rtTA2-S2에서S 파생된 것이다. 또한 최소 세 개의 VP16 활성화 도메인으로 구성된 인간 코돈이다.다만 테트온 3G 단백질은 테트온어드밴드에 비해 아미노산 차이가 5가지나 나 Dox에 대한 민감도가 더욱 높아진 것으로 보인다.테트온 3G는 기존 테트온보다 100배 적은 도크스에 민감하고 7배 더 활동적이다.[8]
기타 시스템
Life Technologies에 의한 T-REX 시스템과 같은 다른 시스템들은 다른 방식으로 작동한다.[9]관심 유전자는 업스트림 CMV 프로모터와 두 개의 TetO2 사이트 옆에 있다.관심 유전자의 표현은 테트라사이클린이 없는 경우 각 테토2 시퀀스에 대한 테트R 호모디머의 높은 친화력 결합에 의해 억제된다.테트라사이클린을 도입하면 각 테트R 호모디머에 테트라사이클린이 1개씩 결합되고, 이후 테트R 호모디머에 의해 테토2가 방출된다.TetR 호모디머와 TetO2의 결합을 풀면 관심 유전자가 감압된다.
T-REX의 수정된 버전은 선형자 합성 생물학회로, 진핵 세포에서 유전자 발현 튜닝에 최적화되어 있다.TetO2 사이트를 TetR표현 추진자에 통합함으로써 음성 피드백을 만들어 균일한 표현(저소음)과 테트라사이클린 아날로그에 대한 선형 선량-반응을 보장한다.[10]
테트라사이클린 반응 요소(TRE)
가장 일반적으로 사용되는 플라스미드에서 테트라사이클린 반응 요소는 스페이서 시퀀스로 구분된 19bp 박테리아 테토 시퀀스(TCCCTATCAGTAGTAGTAGA)의 7회 반복으로 구성된다(예: ACCATGTCGAGTTAC).Tet-On 또는 Tet-Off의 TetR 부분에 의해 인식되고 구속되는 것이 TetO이다.TRE는 일반적으로 바운드된 테트 오프(또는 테트 온)가 없을 때 기초 표현이 매우 낮은 최소 프로모터의 업스트림에 배치된다.
장단점
테트 시스템은 크레, FRT, ER(에스트로겐 수용체) 조건부 유전자 발현 시스템에 비해 장점이 있다.Cre와 FRT 시스템에서는 일단 재조합이 이루어지면 유전자의 활성화나 녹아웃은 되돌릴 수 없는 반면 Tet와 ER 시스템에서는 되돌릴 수 있다.Tet 시스템은 표현에 대한 매우 엄격한 제어를 가지고 있는 반면에 ER 시스템은 다소 누출이 있다.[11]그러나 대상 유전자의 전사 및 후속번역에 의존하는 테트 체계는 이미 발현된 대상 단백질을 호르몬 투여에 따라 안정시키는 ER 체계만큼 빠르게 작용하지 않는다.또한 19bp tet-o 염기서열은 포유류 세포에서 자연적으로 존재하지 않기 때문에 호르몬 조절 방법에 비해 늑막염은 최소화되는 것으로 생각된다.세포 배양에서 테트 시스템을 사용할 때, 각 태아 소 혈청을 검사하여 테트라시클린을 오염시키는 것이 없거나 너무 낮아서 유도를 방해하지 않는지 확인하는 것이 중요하다.
테트라시클린의 항균 효과를 위한 작용 메커니즘은 박테리아의 단백질 번역을 방해하여 미생물의 성장과 회복 능력을 손상시키지만 진핵 미토콘드리아에서도 단백질 번식이 방해되어 실험 결과를 혼동할 수 있는 효과로 이어진다.[12]
참고 항목
참조
- ^ Gossen M, Freundlieb S, Bender G, Müller G, Hillen W, Bujard H (June 1995). "Transcriptional activation by tetracyclines in mammalian cells". Science. 268 (5218): 1766–9. Bibcode:1995Sci...268.1766G. doi:10.1126/science.7792603. PMID 7792603.
- ^ Orth P, Schnappinger D, Hillen W, Saenger W, Hinrichs W (2000). "Structural basis of gene regulation by the tetracycline inducible Tet repressor-operator system" (PDF). Nature Structural & Molecular Biology. 7 (3): 215–219. doi:10.1038/73324. PMID 10700280. S2CID 19973826.
- ^ Tet-On과 Tet-Off는 미국 Clontech Laboratories, Inc.의 등록 상표다.
- ^ Gossen M, Bujard H (June 1992). "Tight control of gene expression in mammalian cells by tetracycline-responsive promoters". Proc. Natl. Acad. Sci. U.S.A. 89 (12): 5547–51. Bibcode:1992PNAS...89.5547G. doi:10.1073/pnas.89.12.5547. PMC 49329. PMID 1319065.
- ^ Allen ND, Plagge A, Kelsey G (2000). "Directed Mutagenesis in Embryonic Stem Cells". In Jackson IJ, Abbott CM (eds.). Mouse Genetics and Transgenics: A Practical Approach. Oxford University Press. pp. 259–263. ISBN 978-0-19-963708-9.
- ^ Urlinger S, Baron U, Thellmann M, Hasan MT, Bujard H, Hillen W (July 2000). "Exploring the sequence space for tetracycline-dependent transcriptional activators: novel mutations yield expanded range and sensitivity". Proc. Natl. Acad. Sci. U.S.A. 97 (14): 7963–8. Bibcode:2000PNAS...97.7963U. doi:10.1073/pnas.130192197. PMC 16653. PMID 10859354.
- ^ Das AT, Tenenbaum L, Berkhout B (June 2016). "Tet-On Systems For Doxycycline-inducible Gene Expression". Current Gene Therapy. 16 (3): 156–67. doi:10.2174/1566523216666160524144041. PMC 5070417. PMID 27216914.
- ^ Zhou X, Vink M, Klaver B, Berkhout B, Das AT (October 2006). "Optimization of the Tet-On system for regulated gene expression through viral evolution". Gene Ther. 13 (19): 1382–90. doi:10.1038/sj.gt.3302780. PMID 16724096.
- ^ "T-REx System". ThermoFisher Scientific.
- ^ Nevozhay D, Adams RM, Murphy KF, Josic K, Balázsi G (March 31, 2009). "Negative autoregulation linearizes the dose-response and suppresses the heterogeneity of gene expression". Proc. Natl. Acad. Sci. U.S.A. 106 (13): 5123–8. Bibcode:2009PNAS..106.5123N. doi:10.1073/pnas.0809901106. PMC 2654390. PMID 19279212.
- ^ Sohal DS, Nghiem M, Crackower MA, Witt SA, Kimball TR, Tymitz KM, Penninger JM, Molkentin JD (July 2001). "Temporally regulated and tissue-specific gene manipulations in the adult and embryonic heart using a tamoxifen-inducible Cre protein". Circ. Res. 89 (1): 20–25. doi:10.1161/hh1301.092687. PMID 11440973.
- ^ Moullan N, Mouchiroud L, Wang X, Ryu D, Williams EG, Mottis A, Jovaisaite V, Frochaux MV, Quiros PM, Deplancke B, Houtkooper RH, Auwerx J (March 2015). "Tetracyclines Disturb Mitochondrial Function across Eukaryotic Models: A Call for Caution in Biomedical Research". Cell Rep. 10 (10): 1681–1691. doi:10.1016/j.celrep.2015.02.034. PMC 4565776. PMID 25772356.
- Chatzispyrou IA, Held NM, Mouchiroud L, Auwerx J, Houtkooper RH (November 2015). "Tetracycline antibiotics impair mitochondrial function and its experimental use confounds research". Cancer Res. 75 (21): 4446–9. doi:10.1158/0008-5472.CAN-15-1626. PMC 4631686. PMID 26475870.
외부 링크
- 독일 테트시스템스
- YouTube의 Tet-On Advanced 애니메이션
- 기능성 암 연구와 유전체학에서 테트시스템에 대한 자세한 개요