응축 반응
Condensation reaction유기 화학에서, 응축 반응은 두 분자가 결합되어 단일 분자를 형성하고, 보통 물과 같은 작은 분자의 [1]손실을 동반하는 화학 반응의 한 종류이다.만약 물이 손실되면, 그 반응은 탈수 합성으로도 알려져 있다.그러나 암모니아, 에탄올, 아세트산, [2]황화수소와 같은 다른 분자들도 손실될 수 있다.
두 분자의 첨가는 보통 평형 상태에서 물 분자의 손실(따라서 [3]응축이라는 이름)과 함께 첨가 생성물에 대한 단계적인 방식으로 진행된다.그렇지 않으면 분자의 작용기를 포함할 수 있으며, 산성 또는 염기성 조건 또는 촉매 존재 하에서 발생할 수 있는 다용도 반응입니다.이러한 종류의 반응은 아미노산 사이의 펩타이드 결합의 [4]형성과 지방산의 생합성에 필수적이기 때문에 삶의 필수적인 부분이다.
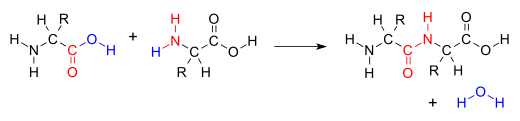
펩타이드 결합을 제공하기 위해 2개의 아미노산이 응축된 것을 나타내는 이상적인 스킴.
응축 반응에는 다양한 종류가 있습니다.대표적인 예로는 부산물로 물을 형성하는 알돌 응축과 크노에베나겔 응축, 부산물로 [5]알코올을 형성하는 클라이젠 응축과 디크만 응축(분자 내 클라이젠 응축) 등이 있습니다.
「 」를 참조해 주세요.
레퍼런스
- ^ "25.18 Condensation Reactions". Book: Introductory Chemistry (CK-12). Chemistry Libre Texts. 12 August 2020. Retrieved 9 January 2021.
- ^ "Condensation Reaction". IUPAC Compendium of Chemical Terminology (Gold Book). IUPAC. 2014. doi:10.1351/goldbook.C01238. Retrieved 7 December 2017.
- ^ Fakirov, S. (2019-02-01). "Condensation Polymers: Their Chemical Peculiarities Offer Great Opportunities". Progress in Polymer Science. 89: 1–18. doi:10.1016/j.progpolymsci.2018.09.003. ISSN 0079-6700. S2CID 105101288.
- ^ Voet, Donald; Voet, Judith; Pratt, Chriss (2008). Fundamentals of Biochemistry. Hoboken, NJ: John Wiley & Sons, Inc. pp. 88. ISBN 978-0470-12930-2.
- ^ Bruckner, Reinhard (2002). Advanced Organic Chemistry (First ed.). San Diego, California: Harcourt Academic Press. pp. 414–427. ISBN 0-12-138110-2.


