쿠싱증후군
Cushing's syndrome| 쿠싱증후군 | |
|---|---|
| 기타이름 | 고코르티솔리즘, 이센코-쿠싱 증후군, 고아드레노코르티즘 |
 | |
| 흡입 플루티카손으로[1] 치료 후 3개월이 지난 사람의 얼굴 모습 | |
| 전문 | 내분비학 |
| 증상 | 고혈압, 팔다리가 얇은 복부비만, 불그스름한 튼살, 동그란 얼굴, 안면홍반, 어깨사이 지방덩어리, 약한 근육, 여드름, 연약한[2] 피부 |
| 합병증 | 고혈압(고혈압), 제2형 당뇨병, 빈번하거나 특이한 감염, 근육량 및 힘의 손실, 뼈의 손실(골다공증).[3] |
| 보통발병 | 20-50년[4] |
| 원인들 | 코티솔에[4] 장기간 노출됨 |
| 진단방법 | 여러 단계가[5] 필요합니다. |
| 치료 | 근본적인[6] 원인을 기준으로 함 |
| 예후 | 일반적으로[7] 치료에 좋습니다. |
| 빈도수. | 연간[8] 백만 명당 2-3명(1/333,333명에서 1/500,000명) |
쿠싱증후군은 코르티솔과 같은 글루코코르티코이드에 장기간 노출되어 나타나는 징후와 증상의 집합체입니다.[4][9][10] 고혈압, 복부비만, 팔과 다리가 가늘고 붉은 색의 스트레치 마크, 얼굴 주름으로 인한 동그란 붉은 얼굴,[11] 어깨 사이의 지방 덩어리, 약한 근육, 약한 뼈, 여드름, 치료가 잘 되지 않는 연약한 피부 등의 증상과 증상이 나타날 수 있습니다.[12][2] 여성들은 더 많은 머리카락과 불규칙한 월경을 할 수 있습니다.[2] 때때로 기분의 변화, 두통, 만성적인 피로감이 있을 수 있습니다.[2]
쿠싱증후군은 프레드니손과 같은 과도한 코르티솔 유사 약물이나 부신에 의해 과도한 코르티솔이 생성되거나 생성되는 종양에 의해 발생합니다.[13] 뇌하수체 선종으로 인한 경우는 쿠싱병으로 알려져 있는데, 쿠싱증후군의 원인은 약물치료 다음으로 많습니다.[4] 뇌하수체 밖에 위치하기 때문에 종종 이소성이라고 불리는 많은 다른 종양도 쿠싱의 원인이 될 수 있습니다.[4][14] 이 중 일부는 다발성 내분비신생물 1형, 카니 콤플렉스 등 유전성 질환과 연관이 있습니다.[8] 진단에는 여러 단계가 필요합니다.[5] 첫 번째 단계는 사람이 먹는 약을 확인하는 것입니다.[5] 두 번째 단계는 덱사메타손 복용 후 소변, 침 또는 혈액 내 코르티솔 수치를 측정하는 것입니다.[5] 이 검사에 이상이 있을 경우 밤늦게 코르티솔이 측정될 수 있습니다.[5] 코르티솔이 높게 유지되면 ACTH에 대한 혈액 검사가 수행될 수 있습니다.[5]
대부분의 경우 치료 및 치료가 가능합니다.[7] 약물로 인해 필요하거나 천천히 중단하는 경우 이러한 것들은 종종 천천히 감소될 수 있습니다.[6][15] 종양으로 인한 경우 수술, 화학요법 및/또는 방사선의 병용요법으로 치료할 수 있습니다.[6] 뇌하수체가 영향을 받은 경우 다른 약물이 손실된 기능을 대체해야 할 수 있습니다.[6] 치료를 받으면 일반적으로 기대 수명이 정상입니다.[7] 수술로 종양 전체를 제거할 수 없는 일부는 사망 위험이 증가합니다.[16]
백만 명당 2~3명 정도는 명백하게 종양에 의해 발생합니다.[8] 가장 일반적으로 20세에서 50세 사이의 사람들에게 영향을 미칩니다.[4] 여성은 남성보다 3배 더 자주 영향을 받습니다.[8] 그러나 뚜렷한 증상 없이 가벼운 정도의 코르티솔 과잉 생산이 더 일반적입니다.[17] 쿠싱 증후군은 1932년 미국의 신경 외과 의사 하비 쿠싱에 의해 처음 기술되었습니다.[18] 쿠싱증후군은 고양이, 개, 말을 포함한 다른 동물들에게도 발생할 수 있습니다.[19][20]
징후 및 증상
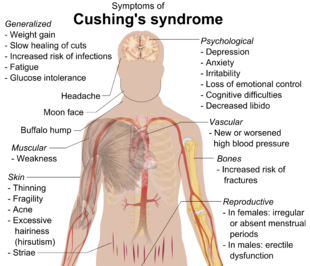

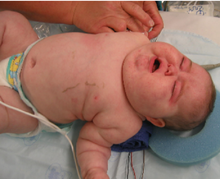
증상은 급격한 체중 증가, 특히 팔다리를 제외한 몸통과 얼굴의 급격한 체중 증가를 포함합니다(중앙 비만). 일반적인 징후로는 쇄골을 따라, 목 뒤쪽에, 그리고 얼굴에 지방질 패드가 자라는 것이 있습니다. 다른 증상으로는 과도한 땀, 모세혈관 확장, 피부의 얇아짐(특히 손을 포함하여 멍이 들고 건조해지기 쉬운 원인), 점막, 보라색 또는 빨간색 줄무늬(쿠싱증후군의 체중 증가로 피부가 가늘고 약해져 출혈이 발생함) 등이 있습니다. 또는 유방, 근위 근육 약화(엉덩이, 어깨) 및 다모증(facial 남성-pattern의 모발 성장), 대머리 및/또는 극도로 건조하고 부서지기 쉬운 모발. 드물게 쿠싱스는 저칼슘혈증을 일으킬 수 있습니다. 과잉 코르티솔은 또한 다른 내분비계에 영향을 미칠 수 있으며, 예를 들어, 불면증, 아로마타제 억제, 성욕 감소, 남성의 발기부전, 안드로겐의 증가로 인한 무월경, 성욕 저하 및 여성의 불임을 유발할 수 있습니다. 또한 연구에 따르면 무월경은 시상하부로 되돌아가 GnRH 방출 수준이 감소하는 과코르티솔리즘 때문인 것으로 나타났습니다.[23]
인슐린 저항성, 고혈압, 비만, 중성지방의 혈중 농도 상승 등 쿠싱의 많은 특징들은 대사증후군에서 볼 수 있는 것들입니다.[24]
우울증뿐만 아니라 기억력과 주의력 기능 장애를 포함한 인지 상태는 일반적으로 코르티솔 상승과 관련이 있으며 [25]외인성 또는 내인성 쿠싱의 초기 지표일 수 있습니다. 우울증과 불안장애도 흔합니다.[26]
쿠싱 증후군에서 나타날 수 있는 다른 현저하고 고통스러운 피부 변화로는 얼굴 여드름, 표재성 진균(피부사상균 및 말라세지아) 감염에 대한 민감성, 복부의 특징적인 보라색, 위축성 줄무늬가 있습니다.[27]: 500
다른 징후로는 소변량 증가(그리고 그에 수반되는 갈증 증가), 지속적인 고혈압(코티솔의 에피네프린의 혈관 수축 효과의 향상으로 인한), 인슐린 저항성(특히 뇌하수체 외부의 ACTH 생산에서 일반적), 당뇨병을 유발할 수 있는 고혈당 및 인슐린 저항성으로 이어집니다. 인슐린 저항성은 겨드랑이와 목 주변의 흑색변과 같은 피부 변화와 함께 겨드랑이의 피부 태그를 동반합니다. 치료되지 않은 쿠싱 증후군은 심장병과 사망률 증가로 이어질 수 있습니다. 코르티솔은 또한 고농도에서 미네랄 코르티코이드 활성을 나타내어 고혈압을 악화시키고 저칼륨혈증(이방성 ACTH 분비에서 흔히 발생)과 고나트륨혈증(혈장 내 Na+ 이온 농도 증가)을 유발할 수 있습니다. 또한, 과도한 코르티솔은 면역 및 염증 반응에 대한 코르티솔의 억제와 관련하여 위장 장애, 기회 감염 및 손상된 상처 치유를 유발할 수 있습니다. 골아세포 활동이 억제되기 때문에 쿠싱증후군에서도 골다공증이 문제가 되고 있습니다. 또한 쿠싱증후군은 특히 엉덩이, 어깨, 허리의 관절이 아프고 아플 수 있습니다.[citation needed]
뇌위축과 같은 뇌의 변화가 발생할 수 있습니다.[28] 이 위축은 해마와 같은 글루코코르티코이드 수용체 농도가 높은 영역과 관련이 있으며 정신병리학적 성격 변화와 높은 상관관계가 있습니다.[29][30][31][32]
- 급격한 체중증가
- 기분, 과민성 또는 우울증
- 근육과 뼈의 약함
- 기억력 및 주의력 기능 장애
- 골다공증
- 당뇨병
- 고혈압
- 면역억제
- 수면장애
- 여성의 무월경과 같은 월경장애
- 여성의 불임
- 남성의 발기부전
- 히르수티즘
- 대머리
- 고콜레스테롤혈증
과색소침착
과잉 ACTH로 인한 쿠싱증후군도 과색소침착을 유발할 수 있습니다. 이것은 프로-오피오멜라노코르틴(POMC)으로부터 ACTH 합성의 부산물로서 멜라닌 세포 자극 호르몬 생성 때문입니다. 대안적으로, 약한 MSH 기능을 포함하는 높은 수준의 ACTH, β-리포트로핀 및 γ-리포트로핀이 멜라노코르틴 1 수용체에 작용할 수 있다고 제안됩니다. 쿠싱병의 변종은 이소성, 예를 들어 소세포 폐암으로부터 뇌하수체외, ACTH 생산에 의해 발생할 수 있습니다.[33]
쿠싱증후군이 부신의 수준에서 (선종이나 증식을 통해) 코르티솔의 증가로 인해 발생하면, 부정적인 피드백은 궁극적으로 뇌하수체에서 ACTH 생산을 감소시킵니다. 이런 경우 ACTH 수치가 낮게 유지되고 과색소침착이 발생하지 않습니다.[33]
원인들
쿠싱 증후군은 약물이나 내부 과정으로 인해 글루코코르티코이드 수치가 증가하는 모든 원인으로 인해 발생할 수 있습니다.[10][34] 그러나 일부 출처에서는 글루코코르티코이드 약물 유발 상태를 "쿠싱증후군"으로 간주하지 않고 대신 "쿠싱로이드"라는 용어를 사용하여 내인성 상태를 모방한 약물 부작용을 설명합니다.[35][34][36]
쿠싱병은 뇌하수체 종양으로 인해 ACTH(부신피질자극호르몬)가 과도하게 생성되어 발생하는 쿠싱증후군의 특정 유형입니다. 과도한 ACTH는 부신 피질을 자극하여 높은 수준의 코르티솔을 생성하여 질병 상태를 만듭니다. 모든 쿠싱병이 쿠싱증후군을 일으키는 반면, 모든 쿠싱증후군이 쿠싱병 때문인 것은 아닙니다.[37] 쿠싱증후군의 몇 가지 가능한 원인은 글루토코티코이드 성분을 기재하지 않은 일반의약품 보충제를 복용하는 것을 포함하여 알려져 있습니다.[38][39]
외생적
쿠싱증후군의 가장 흔한 원인은 처방된 글루코코르티코이드를 다른 질병(의인성 쿠싱증후군) 치료에 사용하는 것입니다. 글루코코르티코이드는 천식, 류마티스 관절염을 비롯한 다양한 질환의 치료에 사용되며, 장기 이식 후 면역 억제에도 사용됩니다. 합성 ACTH의 투여도 가능하지만 ACTH는 비용과 효용이 적기 때문에 처방되는 경우가 적습니다. 드물게 쿠싱증후군도 메드록시프로게스테론 아세테이트 사용 때문일 수 있습니다.[40][41] 외인성 Cushing's에서 부신은 종종 ACTH에 의한 자극 부족으로 인해 점진적으로 위축될 수 있으며, 이는 글루코코르티코이드 약물에 의해 생성이 억제됩니다. 따라서 약물을 갑자기 중단하면 급성 및 잠재적으로 생명을 위협할 수 있는 부신 기능부전이 발생할 수 있으므로 내부 코르티솔 생산이 회복될 수 있도록 용량을 천천히 조심스럽게 줄여야 합니다. 환자는 충분한 수준의 내부 생산을 회복하지 못하고 평생 생리학적 용량으로 글루코코르티코이드를 계속 복용해야 하는 경우도 있습니다.[35][42]
어린 시절 쿠싱증후군은 특히 드물고 일반적으로 글루코코르티코이드 약물의 사용으로 인해 발생합니다.[43]
내생적
내인성 쿠싱증후군은 신체 자체의 코르티솔 분비 시스템의 일부 이상에서 비롯됩니다. 일반적으로 ACTH는 부신에서 코르티솔의 방출을 자극하기 위해 필요할 때 뇌하수체에서 방출됩니다.[citation needed]
- 뇌하수체 쿠싱스에서 양성 뇌하수체 선종이 ACTH를 분비합니다. 이는 쿠싱병이라고도 하며 내인성 쿠싱증후군의 70%를 담당합니다.[44]
- 부신 쿠싱에서 과잉 코르티솔은 부신 종양, 과형성 부신 또는 결절성 부신 증식이 있는 부신에 의해 생성됩니다.
- 정상 뇌하수체-부신계 밖의 종양은 부신에 영향을 미치는 ACTH(가끔 CRH와 함께)를 생성할 수 있습니다. 이 병인은 이소성 또는 부신성 쿠싱병으로 불리며 소세포폐암과 같은 질병에서 나타납니다.[45]
- 마지막으로 뇌하수체 ACTH 생성을 자극하는 CRH 분비 종양(ACTH 분비가 없는)의 드문 사례가 보고되었습니다.[46]
슈도쿠싱증후군
총 코르티솔 수치가 상승하는 것은 경구 피임약에서 발견되는 에스트로겐과 프로게스테론이 혼합되어 의사 쿠싱 증후군으로 이어지는 에스트로겐 때문일 수도 있습니다. 에스트로겐은 코르티솔 결합 글로불린의 증가를 유발하여 전체 코르티솔 수치를 상승시킬 수 있습니다. 하지만 24시간 소변 채취로 측정한 소변 유리 코르티솔은 체내 활성 호르몬인 총 유리 코르티솔은 정상입니다.[47]
병태생리학
시상하부는 뇌에 있고 뇌하수체는 그 바로 아래에 위치합니다. 시상하부의 부심실핵(PVN)은 뇌하수체를 자극하여 부신피질자극호르몬(ACTH)을 방출합니다. ACTH는 혈액을 통해 부신으로 이동하여 코르티솔의 분비를 자극합니다. 코르티솔은 부신의 피질에서 ACTH에 반응하여 근막대라고 불리는 부위에서 분비됩니다. 코르티솔 수치가 높아지면 시상하부의 CRH에 부정적인 피드백을 주어 뇌하수체 전엽에서 방출되는 ACTH의 양이 줄어듭니다.[citation needed]
엄밀히 말하면, 쿠싱증후군은 어떤 병이든 (증후군은 증상의 집단을 의미함에 따라) 과잉 코르티솔을 말합니다. 쿠싱증후군의 원인 중 하나는 부신의 피질에 있는 코르티솔 분비 선종입니다. 선종은 혈액 속의 코티솔 수치를 매우 높게 만들고, 높은 코티솔 수치에서 나오는 뇌하수체에 대한 부정적인 피드백은 ACTH 수치를 매우 낮게 만듭니다.[citation needed]
쿠싱병은 피질영양성 뇌하수체 선종으로부터 ACTH의 과잉 생산(2차성 고코르티솔리즘/고코르티솔리즘) 또는 시상하부 CRH(코르티코트로핀 방출 호르몬)의 과잉 생산(3차성 고코르티솔리즘/고코르티솔리즘)에 따른 고코르티솔리즘만을 의미합니다. 이것은 부신에서 나오는 코르티솔과 함께 혈중 ACTH 수치를 상승시킵니다. ACTH 수치는 종양이 높은 코르티솔 수치에서 나오는 부정적인 피드백에 반응하지 않기 때문에 높게 유지됩니다.[citation needed]
쿠싱증후군이 여분의 ACTH 때문인 경우는 이소성 쿠싱증후군으로 알려져 있습니다.[48] 이것은 부신생물 증후군에서 볼 수 있습니다.
쿠싱 증후군이 의심되는 경우, 덱사메타손 억제 테스트(덱사메타손 투여 및 코티솔 및 ACTH 수치의 빈번한 측정) 또는 코티솔에 대한 24시간 소변 측정이 동일한 검출률을 제공합니다.[49] 덱사메타손은 글루코코르티코이드이며 뇌하수체에 대한 부정적인 피드백을 포함하여 코르티솔의 효과를 시뮬레이션합니다. 덱사메타손을 투여하고 혈액 샘플을 검사하면 50nmol/L 이상의 코르티솔 수치(1.81μg/dL)는 덱사메타손에 의해 억제되지 않는 코르티솔 또는 ACTH의 이소성 공급원이 존재하기 때문에 쿠싱 증후군을 나타냅니다. 최근 미국 FDA에 의해 승인된 새로운 접근법은 24시간 동안 타액에서 코르티솔을 샘플링하는 것인데, 이는 쿠싱로이드 환자의 심야 타액 코르티솔 수치가 높기 때문에 마찬가지로 민감할 수 있습니다. 다른 뇌하수체 호르몬 수치를 확인해야 할 수도 있습니다. 뇌하수체 병변이 의심되면 신체 검사를 통해 시야 결함을 확인할 수 있으며, 이는 시신경을 압박하여 전형적인 반시반시를 유발할 수 있습니다.[citation needed]
이러한 검사 중 하나라도 양성이면 부신 CT 스캔 및 뇌하수체 MRI를 수행하여 부신 또는 뇌하수체 선종 또는 부수적인 종괴(무해 병변의 부수적 발견)를 감지합니다. 요오드콜레스테롤 스캔으로 부신의 신티그래피가 필요할 때가 있습니다. 때때로 정맥 카테터 삽입을 통해 체내 다양한 정맥의 ACTH 수치를 결정하고 뇌하수체를 향해 작업해야 합니다. 쿠싱병을 일으키는 종양은 크기가 2mm 미만으로 MRI나 CT 촬영으로 발견하기 어려운 경우가 많습니다. 뇌하수체 쿠싱병이 확인된 환자 261명을 대상으로 한 한 연구에서 수술 전 MRI를 이용해 뇌하수체 병변을 확인한 경우는 48%에 불과했습니다.[50]
혈장 CRH 수치는 말초 희석 및 CRHBP와의 결합으로 인해 진단 시 부적절합니다([51]CRH를 분비하는 종양의 가능성 제외).
진단.

ACTH= adren피질자극호르몬.
CBG= cort코스테로이드 결합 글로불린.
CRH= corticotropin 방출 호르몬.
DST= dexamet에 한 가지 억제 테스트가 있습니다.
IPSS= inferior 대퇴동 샘플링.
UFC= urinary 프리 코티솔.
*직경 6 mm 미만의 병변이 있는 모든 환자는 IPSS를 가져야 하며 ≥10 mm의 병변이 있는 환자는 IPSS가 필요하지 않다는 데에는 의견이 일치하지만 전문가 의견은 직경 6-9 mm의 병변에 대해 달랐다.
†이 대안 옵션은 명확한 합의점이 없으며 추가 연구가 필요하며 이는 더 어두운 상자로 표시됩니다.
초록색 상자는 고려해야 할 점을 나타냅니다.
어두운 색상은 검증이 덜 된 테스트 경로를 나타냅니다.
쿠싱증후군은 다음과 같은 다양한 검사를 통해 확인할 수 있습니다.[53]
- 24시간 소변이 없는 코르티솔
- 덱사메타손 억제 테스트
- 타액 코르티솔 수치
치료
쿠싱로이드 증상의 대부분은 천식, 관절염, 습진 및 기타 염증 상태에 사용되는 코르티코스테로이드 약물에 의해 발생합니다. 따라서 대부분의 환자는 증상을 유발하는 약물을 조심스럽게 줄이면서(그리고 결국에는 중단) 효과적으로 치료를 받습니다.[citation needed]
부신선종이 확인되면 수술로 제거할 수도 있습니다. ACTH 분비 피질영양성 뇌하수체 선종은 진단 후 제거해야 합니다. 선종의 위치에 관계없이 뇌하수체 ACTH와 정상 부신 조직의 장기간 억제가 즉시 회복되지 않기 때문에 대부분의 환자들은 적어도 수술 후 스테로이드 교체가 필요합니다. 분명히 두 부신이 모두 제거되면 하이드로코르티손이나 프레드니솔론으로 대체하는 것이 필수적입니다.[citation needed]
수술을 받기에 적합하지 않거나 원치 않는 환자의 경우, 여러 약물이 코티솔 합성을 억제하는 것으로 밝혀졌지만 효과는 제한적입니다.[citation needed] Mifepristone은 강력한 글루코코르티코이드 타입 II 수용체 길항제이며, 정상적인 코르티솔 항상성 타입 I 수용체 전달을 방해하지 않기 때문에 쿠싱 증후군의 인지 효과를 치료하는 데 특히 유용할 수 있습니다.[54] 그러나 이 약은 낙태 환자로 사용되어 상당한 논란에 직면해 있습니다. 2012년 2월 FDA는 수술 대상자가 아니거나 이전 수술에 반응하지 않은 성인 환자의 고혈당 수치(고혈당)를 조절하기 위해 미페프리스톤을 승인했습니다. 2020년 3월 쿠싱증후군[55][56][57] 과정에서 임신은 극히 드물지만, 임신한 여성은 마이페프리스톤을 절대 사용해서는 안 된다는 경고와 함께, 이스투리사(osilodrostat) 경구용 정제 11-베타-하이드록실라제 효소 억제제는 뇌하수체 수술을 받을 수 없는 환자나 수술을 받았지만 계속 병을 앓고 있는 환자를 치료하기 위해 FDA의 승인을 받았습니다.[59]

DST= dexamet에 한 가지 억제 테스트가 있습니다.
IPSS= inferior 대퇴동 샘플링.
ACTH= adren피질자극호르몬.
*뇌하수체 수술은 숙련된 외과의사가 시행해야 합니다.
†ACTH 염색 선종의 부재.
‡의학적 치료 선택에 관한 고려 사항은 표 2 및 패널 3을 참조하십시오.
§방사선 분야에서 뇌하수체 저하증 및 이차성 신생물에 대한 평생 모니터링이 필요합니다.
최대 허용 용량의 약물입니다.
알려진 종양이 없는 상태에서 부신을 제거하는 것은 과도한 코르티솔의 생성을 제거하기 위해 때때로 수행됩니다.[60] 어떤 경우에는, 이것은 빠르게 성장하기 시작하고 극단적인 수준의 ACTH를 생성하여 과색소침착을 유발하는 이전에 잠근 뇌하수체 선종으로부터 부정적인 피드백을 제거합니다. 이 임상 상황은 넬슨 증후군으로 알려져 있습니다.[61]
역학
코르티코스테로이드 치료로 인한 쿠싱증후군이 가장 흔한 형태입니다. 쿠싱병은 희귀합니다. 덴마크의 한 연구는 1년에 백만 명당 1명 미만의 발병률을 발견했습니다.[62] 그러나 뇌하수체의 무증상 미세선종(크기 10 mm 미만)은 약 6명 중 1명꼴로 발견됩니다.[63]
쿠싱증후군 환자는 일반인에 비해 이환율과 사망률이 증가했습니다. 쿠싱증후군의 가장 흔한 사망원인은 심혈관계 사건입니다. 쿠싱증후군 환자는 일반인에 비해 심혈관계 사망률이 4배 가까이 높아졌습니다.[citation needed]
쿠싱증후군 환자의 약 0.9~1%는 정맥혈전증이 발생하는 경향이 있습니다. 수술과 비만과 같은 다른 요인들도 혈전증에 걸릴 확률을 증가시킵니다.[64]
다른 동물들
말의 형태에 대한 자세한 내용은 뇌하수체 간 기능 장애를 참조하십시오.[citation needed]
참고 항목
- 애디슨병
- 부신기능부전(저코르티솔리즘)
- 코르티코스테로이드 유발 지방이영양증
참고문헌
- ^ a b Celik O, Niyazoglu M, Soylu H, Kadioglu P (August 2012). "Iatrogenic Cushing's syndrome with inhaled steroid plus antidepressant drugs". Multidisciplinary Respiratory Medicine. 7 (1): 26. doi:10.1186/2049-6958-7-26. PMC 3436715. PMID 22958272.
- ^ a b c d "What are the symptoms of Cushing's syndrome?". 2012-11-30. Archived from the original on 2 April 2015. Retrieved 16 March 2015.
- ^ "Cushing syndrome". mayoclinic.org. Mayo Clinic. Retrieved June 5, 2022.
- ^ a b c d e f "Cushing's Syndrome". National Endocrine and Metabolic Diseases Information Service (NEMDIS). July 2008. Archived from the original on 10 February 2015. Retrieved 16 March 2015.
- ^ a b c d e f "How do health care providers diagnose Cushing's syndrome?". 2012-11-30. Archived from the original on 2 April 2015. Retrieved 16 March 2015.
- ^ a b c d "What are the treatments for Cushing's syndrome?". 2012-11-30. Archived from the original on 2 April 2015. Retrieved 16 March 2015.
- ^ a b c "Is there a cure for Cushing's syndrome?". 2012-11-30. Archived from the original on 27 March 2015. Retrieved 16 March 2015.
- ^ a b c d "How many people are affected by or at risk for Cushing's syndrome?". 2012-11-30. Archived from the original on 2 April 2015. Retrieved 16 March 2015.
- ^ Forbis P (2005). Stedman's medical eponyms (2nd ed.). Baltimore, Md.: Lippincott Williams & Wilkins. p. 167. ISBN 9780781754439. Archived from the original on 2017-09-08.
- ^ a b Sharma ST, Nieman LK (June 2011). "Cushing's syndrome: all variants, detection, and treatment". Endocrinology and Metabolism Clinics of North America. 40 (2): 379–91, viii–ix. doi:10.1016/j.ecl.2011.01.006. PMC 3095520. PMID 21565673.
- ^ Afshari, A; Ardeshirpour, Y; Lodish, MB (October 2015). "Facial Plethora: Modern Technology for Quantifying an Ancient Clinical Sign and Its Use in Cushing Syndrome". The Journal of Clinical Endocrinology and Metabolism. 100 (10): 3928–33. doi:10.1210/jc.2015-2497. PMC 4596033. PMID 26301943.
- ^ Patel, Reema; Sherf, Sahar; Lai, Ngan Betty; Yu, Run (2022-11-01). "Exogenous Cushing Syndrome Caused by a "Herbal" Supplement". AACE Clinical Case Reports. 8 (6): 239–242. doi:10.1016/j.aace.2022.08.001. ISSN 2376-0605. PMC 9701910. PMID 36447831.
- ^ "What causes Cushing's syndrome?". 2012-11-30. Archived from the original on 2 April 2015. Retrieved 16 March 2015.
- ^ Nieman LK, Ilias I (December 2005). "Evaluation and treatment of Cushing's syndrome". The American Journal of Medicine. 118 (12): 1340–1346. doi:10.1016/j.amjmed.2005.01.059. PMID 16378774.
- ^ "Cushing syndrome - Diagnosis and treatment - Mayo Clinic". www.mayoclinic.org. Retrieved 2019-04-21.
- ^ Graversen D, Vestergaard P, Stochholm K, Gravholt CH, Jørgensen JO (April 2012). "Mortality in Cushing's syndrome: a systematic review and meta-analysis". European Journal of Internal Medicine. 23 (3): 278–282. doi:10.1016/j.ejim.2011.10.013. PMID 22385888.
- ^ Steffensen C, Bak AM, Rubeck KZ, Jørgensen JO (2010). "Epidemiology of Cushing's syndrome". Neuroendocrinology. 92 (Suppl 1): 1–5. doi:10.1159/000314297. PMID 20829610.
- ^ "Cushing Syndrome: Condition Information". 2012-11-30. Archived from the original on 2 April 2015. Retrieved 16 March 2015.
- ^ Etienne Cote (2014). Clinical Veterinary Advisor: Dogs and Cats (3 ed.). Elsevier Health Sciences. p. 502. ISBN 9780323240741. Archived from the original on 2017-09-08.
- ^ McCue PM (December 2002). "Equine Cushing's disease". The Veterinary Clinics of North America. Equine Practice. 18 (3): 533–43, viii. doi:10.1016/s0749-0739(02)00038-x. PMID 12516933.
- ^ "Cushing syndrome". Mayo Clinic. March 28, 2013. Archived from the original on May 25, 2015. Retrieved 2015-05-25.
- ^ Fudge EB, von Allmen D, Volmar KE, Calikoglu AS (2009). "Cushing Syndrome in a 6-Month-Old Infant due to Adrenocortical Tumor". International Journal of Pediatric Endocrinology. 2009: 168749. doi:10.1155/2009/168749. PMC 2798106. PMID 20049152.
- ^ Lado-Abeal J, Rodriguez-Arnao J, Newell-Price JD, Perry LA, Grossman AB, Besser GM, Trainer PJ (September 1998). "Menstrual abnormalities in women with Cushing's disease are correlated with hypercortisolemia rather than raised circulating androgen levels". The Journal of Clinical Endocrinology and Metabolism. 83 (9): 3083–3088. doi:10.1210/jcem.83.9.5084. PMID 9745407.
- ^ Arnaldi G, Scandali VM, Trementino L, Cardinaletti M, Appolloni G, Boscaro M (2010). "Pathophysiology of dyslipidemia in Cushing's syndrome". Neuroendocrinology. 92 (Suppl 1): 86–90. doi:10.1159/000314213. PMID 20829625.
- ^ Belanoff JK, Gross K, Yager A, Schatzberg AF (2001). "Corticosteroids and cognition". Journal of Psychiatric Research. 35 (3): 127–145. doi:10.1016/s0022-3956(01)00018-8. PMID 11461709.
- ^ Yudofsky SC, Hales RE (2007). The American Psychiatric Publishing Textbook of Neuropsychiatry and Behavioral Neurosciences (5th ed.). American Psychiatric Pub, Inc. ISBN 978-1-58562-239-9.
- ^ James W, Berger T, Elston D (2005). Andrews' Diseases of the Skin: Clinical Dermatology (10th ed.). Saunders. ISBN 0-7216-2921-0.
- ^ Andela CD, van Haalen FM, Ragnarsson O, Papakokkinou E, Johannsson G, Santos A, et al. (July 2015). "MECHANISMS IN ENDOCRINOLOGY: Cushing's syndrome causes irreversible effects on the human brain: a systematic review of structural and functional magnetic resonance imaging studies". European Journal of Endocrinology. 173 (1): R1-14. doi:10.1530/EJE-14-1101. PMID 25650405.
- ^ Dorn LD, Burgess ES, Friedman TC, Dubbert B, Gold PW, Chrousos GP (March 1997). "The longitudinal course of psychopathology in Cushing's syndrome after correction of hypercortisolism". The Journal of Clinical Endocrinology and Metabolism. 82 (3): 912–919. doi:10.1210/jcem.82.3.3834. PMID 9062506.
- ^ Cope LM, Shane MS, Segall JM, Nyalakanti PK, Stevens MC, Pearlson GD, et al. (November 2012). "Examining the effect of psychopathic traits on gray matter volume in a community substance abuse sample". Psychiatry Research. 204 (2–3): 91–100. doi:10.1016/j.pscychresns.2012.10.004. PMC 3536442. PMID 23217577.
- ^ Wolkowitz OM, Lupien SJ, Bigler ED (June 2007). "The "steroid dementia syndrome": a possible model of human glucocorticoid neurotoxicity". Neurocase. 13 (3): 189–200. doi:10.1080/13554790701475468. PMID 17786779. S2CID 39340010.
- ^ Weber S, Habel U, Amunts K, Schneider F (2008). "Structural brain abnormalities in psychopaths-a review". Behavioral Sciences & the Law. 26 (1): 7–28. doi:10.1002/bsl.802. PMID 18327824.
- ^ a b "Cushing's Syndrome". The Lecturio Medical Concept Library. Retrieved 11 July 2021.
- ^ a b Chaudhry HS, Singh G (2019). "Cushing Syndrome". StatPearls. StatPearls Publishing. PMID 29261900. Retrieved 2019-04-20.
- ^ a b Baek JH, Kim SK, Jung JH, Hahm JR, Jung J (March 2016). "Recovery of Adrenal Function in Patients with Glucocorticoids Induced Secondary Adrenal Insufficiency". Endocrinology and Metabolism. 31 (1): 153–160. doi:10.3803/EnM.2016.31.1.153. PMC 4803552. PMID 26676337.
- ^ Nieman LK (October 2015). "Cushing's syndrome: update on signs, symptoms and biochemical screening". European Journal of Endocrinology. 173 (4): M33–M38. doi:10.1530/EJE-15-0464. PMC 4553096. PMID 26156970.
- ^ Lynnette K. 니먼, 비벌리 M.K. 빌러, 제임스 W. 핀들링, 존 뉴웰 프라이스, 마틴 O. 세비지, 폴 M. 스튜어트, 빅터 M. 몬토리, 쿠싱증후군 진단: 내분비학회 임상 실무 지침서, 임상 내분비학 및 대사 저널, 93권, 2008년 5월 5일 1호, 1526-1540페이지,
- ^ Research, Center for Drug Evaluation and (2022-10-31). "Public Notification: Artri King contains hidden drug ingredients". FDA.
- ^ Patel, Reema; Sherf, Sahar; Lai, Ngan Betty; Yu, Run (2022-11-01). "Exogenous Cushing Syndrome Caused by a "Herbal" Supplement". AACE Clinical Case Reports. 8 (6): 239–242. doi:10.1016/j.aace.2022.08.001. ISSN 2376-0605. PMC 9701910. PMID 36447831.
- ^ Siminoski K, Goss P, Drucker DJ (November 1989). "The Cushing syndrome induced by medroxyprogesterone acetate". Annals of Internal Medicine. 111 (9): 758–760. doi:10.7326/0003-4819-111-9-758. PMID 2552887.
- ^ Merrin PK, Alexander WD (August 1990). "Cushing's syndrome induced by medroxyprogesterone". BMJ. 301 (6747): 345. doi:10.1136/bmj.301.6747.345-a. PMC 1663616. PMID 2144198.
- ^ Broersen LH, Pereira AM, Jørgensen JO, Dekkers OM (June 2015). "Adrenal Insufficiency in Corticosteroids Use: Systematic Review and Meta-Analysis". The Journal of Clinical Endocrinology and Metabolism. 100 (6): 2171–2180. doi:10.1210/jc.2015-1218. PMID 25844620.
- ^ Stratakis CA (December 2012). "Cushing syndrome in pediatrics". Endocrinology and Metabolism Clinics of North America. 41 (4): 793–803. doi:10.1016/j.ecl.2012.08.002. PMC 3594781. PMID 23099271.
- ^ 쿠싱증후군 2011-04-10 미국 국립내분비대사질환정보원 웨이백 기계에 보관되어 있습니다. 2008년 7월. 인용: *
- ^ Schteingart DE, Lloyd RV, Akil H, Chandler WF, Ibarra-Perez G, Rosen SG, Ogletree R (September 1986). "Cushing's syndrome secondary to ectopic corticotropin-releasing hormone-adrenocorticotropin secretion". The Journal of Clinical Endocrinology and Metabolism. 63 (3): 770–775. doi:10.1210/jcem-63-3-770. PMID 3525603.
- ^ Voyadzis JM, Guttman-Bauman I, Santi M, Cogen P (February 2004). "Hypothalamic hamartoma secreting corticotropin-releasing hormone. Case report". Journal of Neurosurgery. 100 (2 Suppl Pediatrics): 212–216. doi:10.3171/ped.2004.100.2.0212. PMID 14758953.
- ^ Katz J (October 1992). "Motive to sin". Nature. 359 (6398): 769. Bibcode:1992Natur.359..769K. doi:10.1136/jcp.s1-3.1.11. PMC 1436049. PMID 1436049.
- ^ A.D.M. 의학 백과사전, PubMedHealth, National Institute of Health의 Wayback Machine에서 보관된 이소성 쿠싱 증후군 2013-10-02
- ^ Raff H, Findling JW (June 2003). "A physiologic approach to diagnosis of the Cushing syndrome". Annals of Internal Medicine. 138 (12): 980–991. doi:10.7326/0003-4819-138-12-200306170-00010. PMID 12809455. S2CID 14930007.
- ^ Jagannathan J, Smith R, DeVroom HL, Vortmeyer AO, Stratakis CA, Nieman LK, Oldfield EH (September 2009). "Outcome of using the histological pseudocapsule as a surgical capsule in Cushing disease". Journal of Neurosurgery. 111 (3): 531–539. doi:10.3171/2008.8.JNS08339. PMC 2945523. PMID 19267526.
- ^ Blevins LS, ed. (2002). Cushing's syndrome. Boston: Kluwer Academic. p. 115. ISBN 978-1-4020-7131-7.
- ^ a b Fleseriu M, Auchus R, Bancos I, Ben-Shlomo A, Bertherat J, Biermasz NR; et al. (2021). "Consensus on diagnosis and management of Cushing's disease: a guideline update". Lancet Diabetes Endocrinol. 9 (12): 847–875. doi:10.1016/S2213-8587(21)00235-7. PMC 8743006. PMID 34687601.
{{cite journal}}: CS1 maint: 다중 이름: 저자 목록 (링크) - ^ "Cushing syndrome: MedlinePlus Medical Encyclopedia". medlineplus.gov. Retrieved 16 March 2018.
- ^ Belanoff JK, Flores BH, Kalezhan M, Sund B, Schatzberg AF (October 2001). "Rapid reversal of psychotic depression using mifepristone". Journal of Clinical Psychopharmacology. 21 (5): 516–521. doi:10.1097/00004714-200110000-00009. PMID 11593077. S2CID 3067889.
- ^ Parksook WW, Porntharukchareon T, Sunthornyothin S (2022-05-30). "Desmopressin Stimulation Test in a Pregnant Patient with Cushing's Disease". AACE Clinical Case Reports. 8 (3): 105–108. doi:10.1016/j.aace.2021.11.005. PMC 9123553. PMID 35602876.
- ^ Caimari F, Valassi E, Garbayo P, Steffensen C, Santos A, Corcoy R, Webb SM (February 2017). "Cushing's syndrome and pregnancy outcomes: a systematic review of published cases". Endocrine. 55 (2): 555–563. doi:10.1007/s12020-016-1117-0. PMID 27704478. S2CID 19349163.
- ^ Lindsay JR, Jonklaas J, Oldfield EH, Nieman LK (May 2005). "Cushing's syndrome during pregnancy: personal experience and review of the literature". The Journal of Clinical Endocrinology and Metabolism. 90 (5): 3077–3083. doi:10.1210/jc.2004-2361. PMID 15705919. S2CID 37344210.
- ^ "FDA approves mifepristone (Korlym*) for patients with endogenous Cushing' s syndrome". February 18, 2012. Archived from the original on September 9, 2012.
- ^ Office of the Commissioner (2020-03-24). "FDA Approves New Treatment for Adults with Cushing's Disease". FDA. Retrieved 2020-06-21.
- ^ Aggarwal S, Yadav K, Sharma AP, Sethi V (June 2013). "Laparoscopic bilateral transperitoneal adrenalectomy for Cushing syndrome: surgical challenges and lessons learnt". Surgical Laparoscopy, Endoscopy & Percutaneous Techniques. 23 (3): 324–328. doi:10.1097/SLE.0b013e318290126d. PMID 23752002. S2CID 34513590.
- ^ Nelson DH, Meakin JW, Thorn GW (March 1960). "ACTH-producing pituitary tumors following adrenalectomy for Cushing's syndrome". Annals of Internal Medicine. 52 (3): 560–569. doi:10.7326/0003-4819-52-3-560. PMID 14426442.
- ^ Lindholm J, Juul S, Jørgensen JO, Astrup J, Bjerre P, Feldt-Rasmussen U, et al. (January 2001). "Incidence and late prognosis of cushing's syndrome: a population-based study". The Journal of Clinical Endocrinology and Metabolism. 86 (1): 117–123. doi:10.1210/jcem.86.1.7093. PMID 11231987.
- ^ Ezzat S, Asa SL, Couldwell WT, Barr CE, Dodge WE, Vance ML, McCutcheon IE (August 2004). "The prevalence of pituitary adenomas: a systematic review". Cancer. 101 (3): 613–619. doi:10.1002/cncr.20412. PMID 15274075. S2CID 16595581.
- ^ Van Zaane B, Nur E, Squizzato A, Dekkers OM, Twickler MT, Fliers E, et al. (August 2009). "Hypercoagulable state in Cushing's syndrome: a systematic review". The Journal of Clinical Endocrinology and Metabolism. 94 (8): 2743–2750. doi:10.1210/jc.2009-0290. PMID 19454584.
외부 링크
- "Cushing's Syndrome". MedlinePlus. U.S. National Library of Medicine.


