니트로소늄 테트라플루오로보토스
Nitrosonium tetrafluoroborate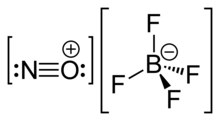 | |
| 이름 | |
|---|---|
| IUPAC 이름 니트로소늄 테트라플로보토스 | |
| 기타 이름 니트로실 테트라플루오로보토스 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.035.148 |
펍켐 CID | |
| 유니 | |
| |
| |
| 특성. | |
| BF4NO | |
| 어금질량 | 116.81 g·116−1 |
| 외관 | 무색의 결정체 고체 |
| 밀도 | 2.192g cm−3 |
| 녹는점 | 250°C(482°F, 523K) (하위) |
| 부패하다 | |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
니트로소늄 테트라플루오로보토(Nitrosonium tetrafluorobot)는 니트로실 테트라플루오로보토(Nitrosyl tetrafluorobotot)라고도 불리며, 화학식 NOBF를4 함유한 화학 화합물이다.이 무색 고체는 유기합성에 니트로싱제로 사용된다.[1]
NOBF는4 불소산의 니트로소늄염으로, 니트로소늄 양이온, [NO]+와 사불화탄 음이온 [BF4]−로 구성되어 있다.
반응
NOBF의4 지배적인 특성은 니트로소늄 양이온의 산화력과 전기영양적 특성이다.헥사메틸벤젠과 18크라운-6으로 컬러 전하 전달 콤플렉스를 형성한다.짙은 황색종인 후자는 디클로로메탄에서 NOBF를4 녹이는 수단을 제공한다.[2]
니트로소늄 테트라플루오보테를 사용하여 [MII(CHCN3)][xBF4]2 유형의 금속 염을 준비할 수 있다(M = Cr, Mn, Fe, Co, Ni, Cu).니트로소늄 양이온은 산화제 역할을 하며,[3] 그 자체가 산화질소로 감소된다.
- M + 2NOBF4 + xCH3CN → [M(CH3CN)x](BF4)2 + 2NO
페로센과 함께 페로세늄 테트라플루오보졸이 형성된다.[4]
참조
- ^ "A15806 Nitrosonium tetrafluoroborate, 98%". Alfa Aesar website. Retrieved 2010-09-04.
- ^ Lee, K. Y.; Kuchynka, D. J.; Kochi, Jay K. (1990). "Redox equilibria of the nitrosonium cation and of its nonbonded complexes". Inorganic Chemistry. 29 (21): 4196–4204. doi:10.1021/ic00346a008.
- ^ Heintz, Robert A.; Smith, Jennifer A.; Szalay, Paul S.; Weisgerber, Amy; Dunbar, Kim R. (August 2004). "11. Homoleptic Transition Metal Acetonitrile Cations with Tetrafluoroborate or Trifluoromethanesulfonate Anions". Inorg. Synth. 33: 75–83. doi:10.1002/0471224502.ch2. ISBN 978-0-471-46075-6.
- ^ Roger M. Nielson; George E. McManis; Lance K. Safford; Michael J. Weaver (1989). "Solvent and electrolyte effects on the kinetics of ferrocenium-ferrocene self-exchange. A reevaluation". J. Phys. Chem. 93 (5): 2152. doi:10.1021/j100342a086.


