피라미드식 탄수화물
Pyramidal carbocation이 글은 대부분의 독자들이 이해하기에는 너무 기술적인 것일 수도 있다. 정보를 할 수 하십시오.(2017년 2월)(이를 및 |
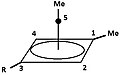
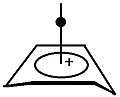
피라미드형 탄수화물은 특정한 구성을 가진 탄수화물의 일종이다.이 이온은 고전 이온과 비고전 이온 외에 제3종으로서 존재한다.이온들에서는 하나의 탄소 원자가 4면 또는 5면 다각형 위로 맴돌며, 사실상 피라미드를 형성한다.4면 피라미드 이온에는 1+의 전하가, 5면 피라미드에는 2+의 전하가 들어간다.영상(오른쪽 위)에서 수직선의 검은 점은 맴도는 탄소 원자를 나타낸다.
피라미드 상단의 탄소 원자와 관련된 겉보기 조정 번호 5 또는 심지어 6은 통상적인 최대치인 4와 비교했을 때 드물다.
역사
이러한 양이온을 연구하는 것은 그 당시 계산 화학에서 놀라운 결과를 얻음으로써 촉발되었다.3-클로로트리시클로[2.1.0.02,5]펜탄에서 염화물을 추출하여 발생하는 모노 정화의 최적 기하학적 형상을 계산하는 동안, 3개의 교량은 약 120°의 각도로 우주에서 방향을 잡을 것으로 기대되었다.그러나 그 계산은 4면 피라미드가 가장 안정적인 구성임을 보여주었다.이 피라미드의 꼭대기에는 탄소 원자가 살고 있는데, 여전히 수소와 연결되어 있다.당초 예상한 구조는 에너지 최소치에 근접하지도 않은 것으로 밝혀졌다. 즉, 최대치를 나타낸다.[1]
- 그림 1: (CH)5 양이온에 대한 몇 가지 가능성

- 1a 계산에서 출발 상황: 염화물이온이 방금 떠났다.
- 1b 예상 구조세 개의 탄소 원자에 대해 전하가 소산되었다.
- 1c 피라미드 이온의 표현.
사용 방법에 따라 그림 1의 이온 1c는 절대적이거나 상대적 최소치일 뿐이다.
이론적 배경
완전한 이론적 논의는 모든 기여 원자의 모든 궤도를 사용할 것이다.첫 번째 근사치에서는 피라미드의 밑부분을 형성하는 폴리곤의 분자 궤도 LCAO와 비정형 원자의 궤도를 피라미드의 맨 위에 있는 탄소 원자로 사용할 수 있다.이 근사치는 구조물의 본질적인 안정성에 대한 통찰력을 제공할 것이다.
아피컬 탄소 원자
비정형 탄소 원자는 다른 대체 물질 한 가지에만 연결되어 있으므로 sp-하이브리드화가 예상된다.대체자는 위로 향하게 될 것이다.기본 다각형을 향해 세 개의 궤도를 사용할 수 있다.
- 두 번째 삽관.이 궤도선은 s-오르비탈의 기여로 인해 에너지가 상대적으로 낮다.나머지 p-orbitals에 있는 결절 평면에 관해서 이 궤도상의 대칭은 양쪽 평면에 대칭인 [2]SS로xy 쓸 수 있다.궤도에는 다소 낮은 에너지가 있는데, 후켈 방법의 관점에서 보면 궤도에는 상당한 s자격이 있을 것이기 때문에 α 이하가 되겠지만 그 값은 추정하기가 쉽지 않다.
- p-orbital 두 개.이 궤도들은 sp-Orbital보다 더 높은 에너지 함량을 가지고 있다.허클법으로 환산하면 에너지는 α가 될 것이다.대칭 항에서 이러한 궤도들은 직교하며, AS와xy SA로xy[2] 설명된다.
피라미드의 기초
| 그림 2: 비정형 탄소 원자의 궤도(위) 및 베이스의 MO(아래)[2] |
| 그림 3: 유인 궤도 및 기저 궤도 사이의 상호작용.위에 있는 "A"는 무정탄소, "P"는 피라미드 구조를 나타내고, "B"는 피라미드의 기초 부분을 위한 것이다. |
피라미드 밑부분의 근사치는 탄소 원자의 닫힌 고리인데, 그들 모두가 혼합되었다2.정확한 결과는 링 크기에 따라 달라진다. 전체적인 결론은 다음과 같이 공식화될 수 있다.
- 가장 낮은 분자궤도는 피라미드의 정점에서 관찰된 것으로, 결절면이 없다.대칭은 SS가xy 될 것이다.[2]후켈법에서 그 에너지는 (α - 2β)이다.
- 다음 단계의 에너지는 퇴화된 두 개의 궤도에 의해 점유된다.대칭어로는 SAxy, AS로xy 표기한다.[2]에너지는 링의 크기에 따라 달라진다.
| 반지 사이즈 | 에너지 수준 |
|---|---|
| 3 | (α + β) |
| 4 | α |
| 5 | (α - 0.618β) |
| 6 | (α - β) |
- 기지 규모에 따라 다른 MO도 있겠지만 현재의 논의와는 무관하다.
꼭지점과 기준점 사이의 상호작용
원자 또는 분자 부분 간의 결합 상호작용을 얻으려면 다음 두 조건을 충족해야 한다.
- 결합할 궤도는 동일한 대칭을 가져야 한다.
- 결합 궤도 사이의 에너지 차이가 작으면 안정화 효과가 더 커진다.
비정형 탄소와 기본 다각형의 궤도들은 그들의 대칭에 관해서 결합할 수 있다.그 결과는 피라미드를 위한 더 안정적인 구성이 될 것이다.그림 2에는 대칭 측면이 묘사되어 있다.
- 아피컬 스피어 오비탈은 기본 링의 최저 MO와 결합하여 낮은 본딩과 높은 안티 본딩 오비탈을 이룬다.
- 두 개의 비정형 p 궤도들은 기본 링에서 두 번째로 낮은 에너지 레벨과 결합한다.두 개의 본딩과 두 개의 반본딩 궤도 결과가 나온다.그림 3은 결과를 그래픽으로 나타낸 것이다.
염기 크기가 다른 피라미드 구조물에 원자 및 분자 궤도를 채우면 다음 표로 이어진다.단지 본딩 궤도만이 설명된다.
| n=3 (트리거) | n=4 (제곱) | n=5 (주문) | n=6 (사각형) | |||||
|---|---|---|---|---|---|---|---|---|
| 궤도 | 요금을 받다 | 궤도 | 요금을 받다 | 궤도 | 요금을 받다 | 궤도 | 요금을 받다 | |
| 1s 탄소의 궤도 | 4 | −8 | 5 | −10 | 6 | −12 | 7 | −14 |
| σ 수소와 아피칼탄소의 결합 | 1 | −2 | 1 | −2 | 1 | −2 | 1 | −2 |
| σ 수소와 기본탄소의 결합 | 3 | –6 | 4 | –8 | 5 | 10 | 6 | –12 |
| σ 기본 탄화수소 사이의 결합 | 3 | –6 | 4 | –8 | 5 | –10 | 6 | –12 |
| 비정형과 최저 기본 궤도 사이의 결합 MO | 1 | –2 | 1 | –2 | 1 | –2 | 1 | –2 |
| 비정형 및 두 번째로 낮은 기본 궤도 사이의 결합 MO | 2 | –4 | 2 | –4 | 2 | –4 | 2 | –4 |
| 전자의 총수 | –28 | –34 | –40 | –46 | ||||
| 총 핵 전하: (n+1)*(C+H)=(n+1)*(6+1) | +28 | +35 | +42 | +49 | ||||
| 구조물의 순충전 | 0 | 1+ | 2+ | 3+ | ||||
3면 피라미드의 경우, 분명히 이온 결과는 없다; 알려진 중립 종인 사면체(Tetrahedrane)가 발생한다.이 분자에 대한 이러한 서술방식은 대체 양자역학적 서술이다.
다른 피라미드 구조물은 그것의 기저 크기와 관련하여 충전될 것이다.
예
모노케이션
- 그림 4: 동일한 피라미드 계정으로 이어지는 트리클로2,4[3,1,0,0]펜탄(TCP)의 여러 파생 모델떠나는 집단을 운반하는 탄소 원자는 기본이 되는 반면, 반대 위치에 있는 탄소는 무정체가 된다.
그룹 "R"은 H 또는 H(D):
1972년 마사무네는 -70°C에서 다수의 전구체를 4d(그림 4)로 용해한 결과를 설명한다.superacid2 (SOClF와 FSOH의3 혼합물)로.C와 H-NMR-spectrum에 기초하여 증거는 명확하다: 각 경우에 동일한 중개자가 형성된다.또한 메탄올이나 벤조산으로 초산성 매질이 파괴되면 같은 제품이 형성된다.(참조: 반응...아래에[3]
| 집단/ ! 원자 | 13C | 1H | |
|---|---|---|---|
| 1 | 93.56 | - |  |
| 2 / 4 | 73.00 | 4.62 | |
| 3 (R=H일 경우) | 60.97 | 4.68 | |
| 5 | -23.04 | - | |
| 1시 메틸 | 7.45 | 2.15 | |
| 메틸로5번길 | -1.03 | 1.84 | |
| () ! 이 표에서는 탄소 원자가 불리고, H-NMR에서는 불린 탄소가 운반하는 수소의 신호가 묘사된다. | |||
- 수소 스펙트럼의 할당은 부분적으로 강도(기본 링에서의 수소)에 관한 것이며, 원형 결합 시스템의 바깥쪽에 있는 공통 경험 수소의 경우 TMS에 비해 높은 ppm의 신호를 갖는 반면, 링 위에 위치한 신호는 TMS에 비해 낮거나 심지어 부정적인 신호를 갖는다.
- C-NMR의 과제는 H와 동일한 고려사항을 따른다.탄소 NMR 강도는 원자의 수에 대한 나쁜 지침이지만, 기본 링에서 미분화 탄소는 그 숫자에 대한 표시로 강도를 사용할 만큼 충분히 유사하다.강력한 도구 역시 와의 결합으로 인한 탄소 신호의 다중성이다.
- 마사무네 자신은 중간이온의 성질에 대해 아무것도 진술하지 않는다.[5]그럼에도 불구하고 올라가 공식화한 규칙을 바탕으로 현지화된 양이온(예: 1-부틸)이나 델로컬화된 양이온(예: 아일)은 배제할 수 있다.[6]이온 신호의 경우 약 200ppm이 예상된다.
메탄올과 벤조산과의 반응
- 그림 5: 메탄올과 벤조산을 사용한 디메틸 피라미드 큐레이션의 디액션 제품.
"R" 그룹은 H 또는1 H(D):
위에서 설명한 바와 같이, 피라미드 이온 5a는 합성 경로와 무관하게 메탄올이나 벤조산염과 반응하여 시약과 대체 패턴에 의해 분명한 반응 매체에 의해 관리되는 제품을 발생시킨다.1972년 마사무네는 중간의 다른 행동을 설명할 수 없다.HSAB 이론의 관점에서 설명이 제공될 수 있다.
1975년에 마사무네는 수소 원자에서 대부분의 전하량을 비대체 이온으로 계산했다[7].메틸 그룹의 중심 원자인 탄소를 위해 수소를 대체하면 보다 전기적인 대체물(2.5 대 폴링 척도 2.1)이 골격 탄소에 집중된다.이 전하 농도는 다음과 같은 여러 가지 효과를 가진다.
- 벤조이트와의 반응은 π - π 상호작용에 의해 지배된다.대체 메틸 집단이 존재하기 때문에 기본 MO 시스템의 변질성은 상실될 것이다.유인원은 접근하기 어렵기 때문에 피라미드 바닥에서 벤조이트가 접근할 것이다.두 π 시스템 사이의 상호작용은 둘 다 한 지점에서 교란되어 특정한 방향을 강요할 것이다.피라미드의 메틸 그룹에 의해 발생하는 양전하와 카복실 그룹에 인접한 전하 사이의 상호작용이 시스템을 피라미드 베이스의 탄소 2 또는 4를 가진 카복실 그룹의 반응으로 유도하는 방향.탄소 2 교량에서 벤조산염과의 반응이 일어나면 원자 1과 3 사이에 형성된다.또한 반탄소 4와 정점 사이에 유대감이 형성될 것이다.탄소 4에서의 반응은 동일한 효과를 낼 것이다. 비록 결과 분자가 위치 2에서 반응으로 인해 발생하는 분자와 관련하여 거울 관계를 가지고 있지만 말이다.
- 메탄올에 대한 반응은 전하로 구동된다.기본 시스템에서는 메틸 그룹을 운반하는 탄소에는 식별할 수 있는 양의 전하의 중심이 존재한다.산소에 단단한 기반을 둔 메탄올은 긍정의 중심에서 반응할 것이다.메톡시 그룹은 탄소 1에 나타나서, 탄소 2와 4 사이에 다리를 형성하여, 현재 항탄소 3 사이에, 정점에 이르도록 강요한다.
비쇼모노카르바위션
화학에서 접두사 "homo-"는 호몰로그를 의미하며, 이와 마찬가지로 1개 또는 2개의 추가 CH 그룹을2 포함한다.비쇼모 이온의 공통적인 면은 사이클로부타디엔이 아닌 1,4 사이클로헥사디엔이온의 보유다.
일반적으로 고리가 확대되면 피라미드 구조물의 중심에 있는 궤도 사이의 결합이 감소하기 때문에 처음에는 이 이온의 안정성이 이상하게 보일 수 있다.여기서 sp2 혼합, 그리고 결과적으로 의 원자와 sp2 중심부에 직접 결합된 원자의 평면성은 기저 탄소의 p-orbital의 상단을 서로 향해 강제하며, 따라서 유인 탄소가 앉을 수 있는 견고한 기초를 만든다.호모-atoms 사이의 다리로 구성을 굳히고, 피라미드의 밑부분을 노르보르나디엔으로 변환시키면, 훨씬 더 안정적인 구조가 만들어진다.
도킹
표 1에 제시된 결과에 따라, 5면 피라미드 탄수화물은 분리될 것이다.이것은 호게베엔의 이론적[8]·실용적 작업으로 확인된다.[9][10]여러 가지 대체 패턴으로 설명되는 단위치와 대조적으로, 도취는 주로 그것의 헥사메틸 유도체에 의해 연구된다.합성은 헥사메틸 데와르 벤젠(표 4의 콤팩트 I)에서 시작하여2, 클과 반응하여 5,6-디클로로-1,2,3,4,5,6-헥사메틸비시클로[2.1]헥스-2-엔(표 4의 콤팩트 II)으로 한다.플루오르설폰산에서 이 화합물이 용해되면 도화가 발생한다(표 4의 구조 III).
 |  |  |
| 나: 미데와르6 벤젠 | II6: 메 드와르 벤젠의 염소 반응 제품 | III: 피라미드 도킹 |
플루오르설폰산 용액에 피라미드 이온의 존재는 H-와 C-NMR-spectrum(표 5)으로 입증된다.
| 강도 | 1H | 13CSingulet | 13CQuartet |
|---|---|---|---|
| 1 | 1.96개 | 22,5 | - 2.0 |
| 5 | 2,65개 | 126,3 | 10,6 |
신호의 배정은 그 강도와 승수에 기초한다.피라미드 구조물의 배정은 스펙트럼의 관찰된 단순성에 기초한다. 즉, 하나의 뛰어난 C-CH3 그룹과 결합된 5개의 동일한 C-CH3 그룹이다.이 데이터로 분자체를 구성하는 유일한 방법은 5면 피라미드다.신호의 위치가 그러한 종류의 구조물에 대한 예상값과 일치하지 않기 때문에 퇴화된 고전적 또는 비고전적 탄화물 사이의 급속 평형은 폐기된다.[8]
[C6(CH3)]62+ (SbF6−)2 • HSOF의3 결정구조는 2017년에 확보되었다.비록 비정형 탄소 원자가 육각화 되었지만, 탄소의 4차 유효성의 규칙은 여전히 충족된다.C-CH3 본드 길이 1.479(3) å은 C-C 단일 본드에 대해 일반적인 반면, 나머지 5개의 매우 긴 C-C 거리는 1.694(2)-1.715(3) å은 채권 순서 <1>을 나타낸다.[11]
도킹의 반응
| 그림 6: 피라미드 카르보디케이션의 반응 |
|---|
|
도취의 반응은 다음과 같이 세 그룹으로 나뉜다.[9][10]
- 열반응 헥사메틸 대체디케이션은 최대 40 °C(104 °F)의 안정적 구조다.이 온도 반응 이상: 하이드라이드를 취한 후, 불소황산 매질에서 안정된 마이젠하이머 콤플렉스로 되돌릴 수 없는 재배치가 일어난다(그림 6, 상부 반응 참조).
- Charged nucleophiles (hydride, methoxide, hydroxide) react reversible, leading to, independent of the nucleofile at hand, identical 2,4-substituted tricyclo[3.1.0.03,6]hexane derivatis, e.g.: with methoxide: 2,4-dimethoxy-tricyclo[3.1.0.03,6]hexane is formed (see: Figure 6, middle reaction path).
- 무충전 뉴클레오파일(트리에틸아민과 같은 아민)은 이온에서 두 개의 수력체를 추출하는 가역성 역할을 하며, 실제로 벤츠발렌의 디메틸렌 파생물을 생성한다(그림 6, 저반응 참조).
Doccommunications의 기타 대체 패턴
트리에틸아민에 대한 도취 반응의 산물은 헥사메틸 다음으로 다른 대체 패턴에 대한 경로를 제공한다.[12]한 개 또는 두 개의 이중 결합이 케톤으로 산화된다.케톤은 알킬화 수산화물을 생성하는 유기농 화합물과 반응한다.이렇게 형성된 화합물은 산화 이중 결합의 수에 따라 한두 개의 다른 알킬 그룹을 가지고 있다.알콜이 플루오르설폰산에 용해되었을 때, 그것들은 다시 새로운 피라미드 디커뮤니케이션들을 낳는다.두 비메틸 집단은 모두 기저 자리를 차지하고 있다.피라미드 골격에서 서로 다른 위치는 여전히 메틸 그룹을 지니고 있다.표 6은 이러한 결과를 요약한다.
 |  |  |  |  |
| I: EtN과의3 반응 제품 | II: 모노키톤 | III: 알킬화 단알코올 | IV: FSOH에서3 처음으로 용해되었을 때의 피라미드 이온 | V: FSOH에서3 두 번째로 용해되었을 때의 피라미드 큐레이션 |
 |  |  |  | |
| II: 디케톤 | III: 알킬레이트 디올 | IV: FSOH에서3 처음으로 용해되었을 때의 피라미드 이온 | V: FSOH에서3 두 번째로 용해되었을 때의 피라미드 큐레이션 |
이때까지 분피라미드 이온의 치환 패턴은 그 거동에는 미미한 중요성이 있다.V형(표6)의 이온을 연구할 경우 열안정성이 확보된다. -40°C(-40°F)에서 아피알 에틸 대체이온은 48시간 동안 안정적이지만, 아피알 이온의 흔적은 더 이상 검출할 수 없다.
Tervalent 및 상위 이온
문헌 조사(1978년 말) 당시, 3차원 이상의 피라미드 계수에 대한 보고는 없었다.
참고 사항 및 참조
- ^ Stohrer, W.D.; Hoffmann, R. (1972). "Bond-stretch isomerism and polytopal rearrangements in (CH)5+, (CH)5-, and (CH)4CO". J. Am. Chem. Soc. 94 (5): 1661–1668. doi:10.1021/ja00760a039.
- ^ a b c d e 궤도경사가 첨자로 표시된 평면에 대칭임을 나타내는 S.A는 첨자 표시 평면에 의한 에 대한 반대칭성을 설명한다.
- ^ a b Masamune, S.; Sakai, M.; Ona, H. (1972). "Nature of the (CH)5+ species. I. Solvolysis of 1,5-dimethyltricyclo[2.1.0.02,5]pent-3-yl benzoate". J. Am. Chem. Soc. 94 (25): 8955–8956. doi:10.1021/ja00780a078.
- ^ a b S. Masamune, S.; Sakai, M.; Ona, H.; Jones, A.J. (1972). "Nature of the (CH)5+ species. II. Direct observation of the carbonium ion of 3-hydroxyhomotetrahedrane derivatives". J. Am. Chem. Soc. 94 (25): 8956. doi:10.1021/ja00780a079.
- ^ 마사무네는 같은 해 후반에 스토레르, 호프만과 같은 이론적인 결과를 내놓지만, 이론적 작업의 함의가 명확해진 순간 마사무네가 논문을 편집할 수 있었던 것 같지는 않다.
- ^ Olah, G.A.; Donovan, D.J.; Prakash, G. (1978). "The α, 1-dimethylcyclopropylcarbinyl cation". Tetrahedron Letters. 19 (48): 4779–4782. doi:10.1016/s0040-4039(01)85729-4.
- ^ Masamune, S. (1975). "Some aspects of strained systems. [4]Annulene and its CH+ adduct". Pure and Applied Chemistry. 44 (4): 861–884. doi:10.1351/pac197544040861.
- ^ a b Hogeveen, H.; Kwant, P. W.; Postma, J.; van Duynen, P. Th. (1974). "Electronic spectra of pyramidal dications, (CCH3)62+ and (CCH)62+". Tetrahedron Letters. 15 (49–50): 4351–4354. doi:10.1016/S0040-4039(01)92161-6.
- ^ a b Hogeveen, H.; Kwant, P. W. (1974). "Chemistry and spectroscopy in strongly acidic solutions. XL. (CCH3)62+, an unusual dication". Journal of the American Chemical Society. 96 (7): 2208–2214. doi:10.1021/ja00814a034.
- ^ a b Hogeveen, H.; Kwant, P. W. (1973). "Direct observation of a remarkably stable dication of unusual structure: (CCH3)62⊕". Tetrahedron Letters. 14 (19): 1665–1670. doi:10.1016/S0040-4039(01)96023-X.
- ^ Malischewski, Moritz; Seppelt, K. (2016-11-25). "Crystal Structure Determination of the Pentagonal-Pyramidal Hexamethylbenzene Dication C6(CH3)6 2+". Angewandte Chemie International Edition. 56 (1): 368–370. doi:10.1002/anie.201608795. ISSN 1433-7851. PMID 27885766.
- ^ G. Giordano, G.; Heldeweg, R.; Hogeveen, H. (1977). "Pyramidal dications. Introduction of basal and apical substituents". J. Am. Chem. Soc. 99 (15): 5181–5183. doi:10.1021/ja00457a050.