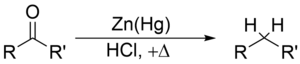클레멘센 감소
Clemmensen reduction| 클레멘센 감소 | |
|---|---|
| 이름을 따서 명명됨 | 에릭 크리스천 클레멘슨 |
| 반응형 | 유기 리독스 반응 |
| 식별자 | |
| 유기화학포털 | 명료감소 |
| RSC 온톨로지 ID | RXNO:0000038 |
클렘멘슨 감소는 아연 아말감과 농축 염산을 이용하여 알칸에 케톤(또는 알데히드)을 감소시키는 화학반응이다.[1][2][3] 이 반응은 덴마크의 화학자인 에릭 크리스티안 클레멘센의 이름을 따서 지어졌다.[4]
원래의 Clemmensen 감소 조건은 Friedel-Crafts acylation에서 형성된 것과 [5][6]같은 아릴-알킬 케톤을 줄이는 데 특히 효과적이다. Clemmensen 감소가 뒤따르는 Friedel-Crafts acylation의 2단계 순서는 아레네스의 1차 알킬화를 위한 고전적인 전략을 구성한다. 알리페틱 케톤이나 순환 케톤은 디에틸에테르나 아세트산 무수화물에서 염화수소의 무수 용액에서 활성 아연 먼지를 이용한 변형 클렘멘센 조건이 훨씬 효과적이다.[7]
기판은 Clemmensen 감소(37% HCl)의 강한 산성 조건에 내성이 있어야 한다. 몇 가지 대안이 있다. 산성에 민감한 기판은 울프-키슈너 감소를 통해 감소할 수 있으며, 라네이 니켈이 존재하는 상태에서 수소 분해에 안정된 기판을 위한 보다 가벼운 방법은 2단계 모징고 감소를 의미한다.
이러한 반응의 고색창연한 사실에도 불구하고, 클레멘센 감소의 메커니즘은 여전히 불명확하다. 반응의 이질적인 성질 때문에 기계론적 연구는 어렵고, 소수의 연구만 공개되었다.[8][9] 기계론적 제안은 일반적으로 유기농 중간체를 호출하는데, 때로는 아연 카브노이드(아연 금속 표면에 묶인 유기 조각)를 포함하기도 한다. 그러나 클렘멘센 조건에 알코올을 투하할 경우 일반적으로 알칸 제품을 공급할 수 없기 때문에 해당 알코올은 중간 알코올이 아닌 것으로 간주된다.[10]
참고 항목
참조
- ^ Clemmensen, E. (1913). "Reduktion von Ketonen und Aldehyden zu den entsprechenden Kohlenwasserstoffen unter Anwendung von amalgamiertem Zink und Salzsäure". Chemische Berichte. 46 (2): 1837–1843. doi:10.1002/cber.19130460292.
- ^ Clemmensen, E. (1914). "Über eine allgemeine Methode zur Reduktion der Carbonylgruppe in Aldehyden und Ketonen zur Methylengruppe". Chemische Berichte. 47: 51–63. doi:10.1002/cber.19140470108.
- ^ Clemmensen, E. (1914). "Über eine allgemeine Methode zur Reduktion der Carbonylgruppe in Aldehyden und Ketonen zur Methylengruppe. (III. Mitteilung.)". Chemische Berichte. 47: 681–687. doi:10.1002/cber.191404701107.
- ^ 화학자의 전기, 2007년 2월 6일 접속
- ^ "γ-Phenylbutyric acid". Organic Syntheses. 2: 499. 1943.; 15권, 페이지 64 (1935)
- ^ "Creosol". Organic Syntheses. 4: 203. 1963.; 33권, 페이지 17 (1953)
- ^ "Modified Clemmensen Reduction: Cholestane". Organic Syntheses. 6: 289. 1988.; 제53권, 페이지86 (1973)
- ^ Brewster, James H. (2002-05-01). "Reductions at Metal Surfaces. II. A Mechanism for the Clemmensen Reduction 1". Journal of the American Chemical Society. 76 (24): 6364–6368. doi:10.1021/ja01653a035.
- ^ Nakabayashi, Tadaaki (2002-05-01). "Studies on the Mechanism of Clemmensen Reduction. I. The Kinetics of Clemmensen Reduction of p-Hydroxyacetophenone". Journal of the American Chemical Society. 82 (15): 3900–3906. doi:10.1021/ja01500a029.
- ^ Martin, Elmore L. (2004-01-01). "The Clemmensen Reduction". Organic Reactions. John Wiley & Sons,Inc. pp. 155–209. doi:10.1002/0471264180.or001.07. ISBN 9780471264187.
리뷰
- Martin, E. L. (1942). "The Clemmensen reduction". Org. React. 1: 155.
- Buchanan, J. G. St. C.; Woodgate, P. D. (1969). "The Clemmensen reduction of difunctional ketones". Quarterly Reviews, Chemical Society. 23 (4): 522. doi:10.1039/QR9692300522.
- Vedejs, E. (1975). "Clemmensen reduction of ketones in anhydrous organic solvents". Org. React. 22: 401–422.
- Yamamura, S.; Nishiyama, S. (1991). "1.13.2.2 Clemmensen reduction". Comprehensive Organic Synthesis. 8: 309–313.