한계영역
Marginal zone| 한계영역 | |
|---|---|
 | |
| 식별자 | |
| FMA | 15852 |
| 해부학적 용어 | |
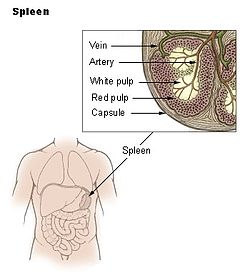
한계 구역은 비림프성 적색 펄프와 비장의 림프성 백색 펄프 사이의 접점에 있는 지역이다. (일부 소스는 이 부분을 흰 펄프와 경계를 이루는 붉은 펄프의 일부로 간주하는 반면, 다른 소스는 붉은 펄프도 흰 펄프도 아닌 것으로 간주한다.)
구조
골수 분화의 골수 부위에서 주로 파생된 세포로 구성되어 있다.더 최근에, 중성미자 킬러의 개체수가 한계 구역의 주변 영역을 채우기 위해 설명되었다.[2]최소 3개의 구별되는 세포 표지를 사용하여 MOMA-1, ERTR-9 및 MARCO의 세포를 식별할 수 있다.
혈류
한계영역(MZ)은 일반 혈액순환으로부터 다량의 혈액을 받는 전이가 심한 지역이다.놀랍게도, 비장 미세조직은 쥐와 인간의 두드러진 차이를 보여준다.인간에서 비장은 비장동맥으로부터 혈액을 받고, 비장동맥은 중앙과 음경동맥으로 갈라진다.[3]역사적으로 정의된 한계부정맥동의 부재로 인해, 음경동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥동맥류는과립구(perifollicular zone)는 MZ와 붉은 펄프를 분리하는 저항 감소의 잘 정의된 영역이다.경혈성 구역과 적혈구 모두 비장성 코드로 알려진 혈이 채워진 공간의 개방된 순환계로 구성되는데, 이 공간은 내피성 구분이 정의되지 않고 적혈구의 정맥 정맥동맥 혈관과 밀접하게 접촉하고 있다.[4]
함수
한계지대의 주요 역할은 순환에서 미립자 항원을 가두어 비장의 림프구에 항원을 제시하는 것이다.
실험 결과 불활성 라텍스 구슬은 물론 대장균, 리스테리아 모노키토제네스와 같은 살아있는 박테리아가 한계지대에 갇혀 있는 것으로 나타났다.그러나 면역 유발 물질, 즉 박테리아만이 백색펄프의 T세포와 B세포 영역으로 밀거래되어 면역 반응을 이끌어내기 위해 효율적으로 제시된다.
림프구
한계영역 림프구는 그곳에서 생성된 B세포(Marginal-Zone B세포, 약칭 "MZ B세포")의 일종으로 IgM-항생 복합체를 결합할 수 있다.그들은 면역 체계에서 몇 가지 다른 역할을 하는 능력으로 유명하다.MZ B세포는 여러 미생물 분자 패턴에 결합하는 다발성 BCR을 표현한다.[5]
한계 영역 대식량
한계 영역 내에 이 영역에 고유한 두 가지 유형의 대식세포가 존재한다: 한계 영역 대식세포와 한계 야금성 대식세포.이 두 가지 대식세포 하위형은 한계 영역 대식세포에 SIGN-R1을, 한계 야금성 대식세포에 CD169(시글렉-1, 시알로아데신)를 표현한 것이 특징이다.
일반적으로 그곳에 존재하는 한계영역 B세포 외에도 혈액에 존재하는 많은 다른 세포형태가 한계영역(예: 림프구, 과립구)을 통과한다.또 덴드리트 세포의 다수는 자극과 항원 흡수에 따른 백색 펄프로 이주하기 전에 일시적으로 한계 영역에 상주하는 것으로 생각되며, 또한 백색 펄프로 이행하는 과정에서 상당수의 림프구가 일정 기간 동안 한계 영역에 남아 있다.이 두 세포가 한계 구역 대식세포와 상호작용한다고 가정할 수 있다.
최근 연구에 따르면 한계대 대식세포는 적응 면역 반응을 촉진할 수 있을 뿐만 아니라 중요한 선천적 기능을 모두 가지고 있기 때문에 이러한 대식세포가 선천적 면역과 적응적 면역력을 연결시킬 수 있다.
한계대 대식세포는 다양한 기능을 가지고 있는데, 그 중 하나가 혈액에 의한 병원균의 포교세포증이다.한계 구역의 해부학 때문에, 그 안에 있는 혈액이 느려지고 따라서 체계적 순환에 존재하는 병원균들은 양쪽 한계 구역 대식세포에 의해 피구균이 된다.병원균의 섭취와 퇴치에서 이 두 대식세포 하위세트의 특정 역할에 관한 자료는 한정되어 있다.그러나 특정 병원균, 특히 캡슐화된 박테리아를 인지하고 제거하는 데 한계 구역 대식세포에 다양한 병원체 수용체가 특정한 관여가 있음을 보여주는 증거와 보고서가 있다.예를 들어 C형 렉틴 SIGN-R1 수용체(소외대 대식세포에 있음)는 폐렴구균 당류의 인식을 매개하며, 폐렴구균의 정리에 필요하다.
더욱이, 두 가지 유형의 한계 구역 대식세포는 바이러스의 간극과 분해에서 나타난다. 예를 들어, 소두 바이러스와 아데노바이러스 세로형 5.한계대 대식세포에 의한 림프구 교감염 바이러스의 간극이 바이러스 감염이 주변 장기로 확산되는 것을 막는 데 결정적이라는 증거가 나왔다.[6]
참고 항목
참조
- ^ "Lymph nodes & spleen, nonlymphoma".
- ^ Puga, Irene; Cols, Montserrat; Barra, Carolina M; He, Bing; Cassis, Linda; Gentile, Maurizio; Chen, Kang; Cerutti, Andrea (December 2011). "B cell–helper neutrophils stimulate the diversification and production of immunoglobulin in the marginal zone of the spleen". Nature Immunology. 13 (2): 170–80. doi:10.1038/ni.2194. PMC 3262910. PMID 22197976.
- ^ Mebius, Reina E.; Kraal, Georg (August 2005). "Structure and function of the spleen". Nature Reviews Immunology. 5 (1): 606–616. doi:10.1038/nri1669. PMID 16056254. S2CID 3258595.
- ^ Steiniger, Birte; Timphus, Eva Maria; Barth, Peter J. (December 2006). "The splenic marginal zone in humans and rodents: an enigmatic compartment and its inhabitants". Histochemistry and Cell Biology. 126 (6): 641–648. doi:10.1007/s00418-006-0210-5. PMID 16816939. S2CID 31943597.
- ^ Martin, Flavius; Kearney, John F. (May 2002). "Marginal-zone B cells". Nature Reviews Immunology. 2 (5): 323–35. doi:10.1038/nri799. PMID 12033738. S2CID 22573840.
- ^ den Haan, Joke M.M.; Kraal, Georg (2012). "Innate Immune Functions of Macrophage Subpopulations in the Spleen". Journal of Innate Immunity. 4 (5–6): 437–445. doi:10.1159/000335216. ISSN 1662-8128. PMC 6741446. PMID 22327291.
외부 링크
- Pillai S, Cariappa A, Moran ST (2005). "Marginal zone B cells". Annual Review of Immunology. 23: 161–96. doi:10.1146/annurev.immunol.23.021704.115728. PMID 15771569.
- Ferguson AR, Corley RB (2005). "Accumulation of marginal zone B cells and accelerated loss of follicular dendritic cells in NF-κB p50-deficient mice". BMC Immunology. 6: 8. doi:10.1186/1471-2172-6-8. PMC 1087843. PMID 15836790.
- 한계영역 림프종
- Song H, Cerny J (December 2003). "Functional heterogeneity of marginal zone B cells revealed by their ability to generate both early antibody-forming cells and germinal centers with hypermutation and memory in response to a T-dependent antigen". The Journal of Experimental Medicine. 198 (12): 1923–35. doi:10.1084/jem.20031498. PMC 2194154. PMID 14662910.
- Kraal G (1992). Cells in the marginal zone of the spleen. International Review of Cytology. Vol. 132. pp. 31–74. doi:10.1016/S0074-7696(08)62453-5. ISBN 9780123645326. PMID 1555921.
- Kumararatne DS, MacLennan IC (November 1981). "Cells of the marginal zone of the spleen are lymphocytes derived from recirculating precursors". European Journal of Immunology. 11 (11): 865–9. doi:10.1002/eji.1830111104. PMID 6976895. S2CID 22799132.


