페로브스카이트(구조물)
Perovskite (structure)페로브스카이트는 산화칼슘(CaTiO3)으로 구성된 페로브스카이트(perovskite)라는3 광물로 처음 발견된 공식 ABX에 따른 결정 구조를 가진 모든 물질이다.[2] 이 광물은 1839년 구스타프 로즈에 의해 러시아의 우랄 산맥에서 처음 발견되었고 러시아의 광물학자 L. A. 페로브스키(1792–1856)의 이름을 따서 명명되었다. 여기서 'A'와 'B'는 두 개의 이온으로, 종종 크기가 매우 다르고, X는 두 이온에 결합하는 이온(흔히 산화)이다. 'A' 원자는 일반적으로 'B' 원자보다 크다. 이상적인 입방 구조는 음이온의 팔면체로 둘러싸인 6배 조정에 B 양이온을, 12배 입체음향 조정에 A 양이온을 가지고 있다. A 사이트와 B 사이트 중 하나 또는 둘 다 A1A2x-1x 및/또는 B1B2의y-1y 구성을 가지며, A 사이트와 B 사이트 내의 이온이 산화 상태의 변화를 겪을 때 X가 이상적인 조정 구성에서 벗어날 수 있는 추가적인 페로브스카이트 형태가 존재할 수 있다.[3]
가장 풍부한 구조적 가족 중 하나인 페로브스카이트는 광범위한 성질, 응용성, 중요성을 지닌 수많은 화합물에서 발견된다.[4] 이 구조를 가진 천연 화합물은 페로브스카이트, 로파라이트, 규산페로브스카이트 브리지그마나이트 등이다.[2][5] 2009년 메틸람모늄 납 할리드 페로브스카이트가 함유된 페로브스카이트 태양전지가 발견된 이후 페로브스카이트 소재에 대한 연구적 관심이 상당했다.[6]
구조
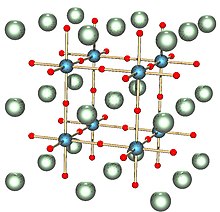
페로브스카이트 구조물은 화학식 ABO를3 가진 많은 산화물에 의해 채택된다. 이상화된 형태는 입방 구조(우주군 Pm3m, 221호)로 거의 접하지 못한다. 직교범위상(예: 우주군 Pnma, no. 62 또는 Amm2, no. 68)과 4각형(예: 우주군 I4/mcm, no. 140 또는 P4mm, no. 99)은 가장 일반적인 비큐빅 변형이다. 페로브스카이트 구조는 CaTiO의3 이름을 따서 명명되었지만, 이 광물은 이상화되지 않은 형태를 형성한다. SrTiO와3 CaRbF는3 큐빅 페로브스카이트의 예다. 티탄산바륨은 온도에 따라 림보헤드랄(우주군 R3m, 제160호), 직교, 사방형, 입방형 형태를 취할 수 있는 페로브스카이트의 예다.[7]
In the idealized cubic unit cell of such a compound, the type 'A' atom sits at cube corner position (0, 0, 0), the type 'B' atom sits at the body-center position (1/2, 1/2, 1/2) and oxygen atoms sit at face centered positions (1/2, 1/2, 0), (1/2, 0, 1/2) and (0, 1/2, 1/2). 오른쪽의 도표는 큐브 코너 위치에 A가 있는 등가 단위 셀에 대한 가장자리, 신체 중심에 B가 있고 얼굴 중심 위치에 O가 있는 것을 나타낸다.
계양 쌍방은 ABX+2+−3, [8]1:2 perovskites, ABX2+4+2−3 또는 2:4 perovskites, ABX3+3+2−3 또는 3:3 perovskites, ABX+5+2−3 또는 1:5 perovskites 등 4가지 범주로 가능하다.
입방 구조물의 안정성을 위한 상대 이온 크기 요건은 상당히 엄격하기 때문에 약간의 좌굴과 왜곡은 A 양이온, B 양이온 또는 둘 모두의 조정 번호가 감소되는 몇 개의 저대칭 왜곡 버전을 생성할 수 있다. BO6 옥타헤드라를 기울이면 과소평가된 A cation의 조정이 12에서 8까지 감소한다. 반대로, 그것의 팔면체 내에서 저체중 B cation의 오프센터링은 그것이 안정적인 결합 패턴을 얻을 수 있게 한다. 그 결과 발생하는 전기 쌍극은 강전 성질을 책임지고 이러한 방식으로 왜곡되는 BaTiO와3 같은 페로브스키트에 의해 보여진다.
복잡한 페로브스카이트 구조물은 두 개의 다른 B-사이트 계수를 포함한다. 이것은 순서와 질서 정연한 변형의 가능성을 초래한다.
레이어드 페로브스카이트
페로브스카이트는 ABO
3 구조물을 얇은 침입 물질 시트로 분리하여 층으로 구조할 수 있다. 침입의 화학적 구조에 근거한 다른 형태의 침입은 다음과 같이 정의된다.[9]
- Aurivillius phase: 침입층은
2
2 2+[BiO] 이온으로 구성되어 있으며, 모든 n개의 ABO
3 층이 발생하여 [BiO
2
2]-ABO의
(n−1)
2
7 전반적인 화학 공식으로 이어진다. 이들의 산화 이온 전도 성질은 다카하시 외 연구진에 의해 1970년대에 처음 발견되었으며, 그 이후로도 이러한 목적으로 사용되어 왔다.[10] - Dion-Jacobson 단계: 침입층은 모든 n ABO
3 층마다 알칼리 금속(M)으로 구성되어 있어 전체 공식을 MABO로+
(n−1)
n
(3n+1) 한다. - 루들즈덴-포퍼 위상: 가장 간단한 페이즈로 침입 계층은 ABO
3 격자의 모든 레이어(n = 1) 또는 여러 레이어(n > 1) 사이에서 발생한다. 루들즈덴-포퍼 단계는 일반적으로 A가 크고(La[11] 또는 Sr[12] 등) B 이온이 훨씬 작은 일반적으로 전이 금속(Mn,[11] Co[13] 또는 Ni[14] 등)인 원소의 원자 반지름 측면에서 페로브스카이트와 유사한 관계를 갖는다. 최근에는 하이브리드 유기농 유기층 적층 페로브스카이트가 개발되었는데,[15] 여기서 구조가 하나 이상의 MX옥타헤드라64- 층으로 구성되어 M은 +2 금속(Pb2+ 또는 Sn2+ 등), X와 할라이드 이온(예: F−, Cl−, Br−, I−, 유기 양이온 층(예: 부틸람모늄 또는 페닐틸람모늄)으로 분리된다.[16][17]
박막
페로브스카이트는 펄스 레이저 증착, 분자 빔 상피 등의 기술을 사용하여 다른 페로브스카이트 위에 상피 박막으로 침전할 수 있다.[18] 이 필름들은 두 나노미터 두께일 수도 있고 단일 단위 세포만큼 작을 수도 있다.[19] 필름과 기질 사이의 인터페이스에서 잘 정의되고 고유한 구조물은 새로운 유형의 특성이 발생할 수 있는 인터페이스 엔지니어링에 사용될 수 있다.[20] 이것은 기질과 필름 사이의 불일치 변형, 산소 팔면 회전 변화, 구성 변화, 양자 구속 등 여러 메커니즘을 통해 발생할 수 있다.[21] 그 예로는 SrTiO에서3 성장한 LaAlO가3 있다. 여기서 LaAlO와3 SrTiO3 모두 비전도성이지만 인터페이스는 전도성을 나타낼 수 있다.[22]
예
광물
페로브스카이트 구조는 지구 맨틀에서 가장 흔한 광물인 화학식(Mg,Fe)SiO를3 가진 규산염인 브리지그마나이트에 의해 고압으로 채택된다. 압력이 증가함에 따라, 지배적인 실리카를 함유하는 광물의 SiO44− 4면체 단위는 SiO68− 8면체 단위에 비해 불안정해진다. 하부 맨틀의 압력 및 온도 조건에서 두 번째로 풍부한 물질은 암석 구조(Mg,Fe)O산화물, 과리클라아제일 가능성이 높다.[2]
지구의 하단 맨틀의 고압 조건에서, 피록신 enstatite, MgSiO는3 보다 밀도가 높은 페로브스카이트 구조 다형체로 변한다. 이 위상은 지구에서 가장 흔한 광물일 수 있다.[23] 이 단계에는 ~24 GPA ~ 110 GPA의 압력에서 안정성이 있는 직교 왜곡 페로브스카이트 구조(GdFeO형3 구조)가 있다. 그러나, 그것은 수백 km 깊이의 깊이에서 지구 표면으로 다시 밀도가 낮은 물질로 변형되지 않고는 운반될 수 없다. 일반적으로 규산염 페로브스카이트로 알려진 MgSiO3 페로브스카이트는 높은 압력에서 포스트 페로브스카이트로 변한다.
다른이들
가장 흔한 페로브스카이트 화합물은 산소를 함유하고 있지만, 산소가 없이 형성되는 페로브스카이트 화합물이 몇 가지 있다. NaMgF와3 같은 플루오르화 페로브스키트는 잘 알려져 있다. 많은 종류의 금속 페로브스카이트 화합물은 RTM3(R: 희토류 또는 기타 상대적으로 큰 이온, T: 전이 금속 이온 및 M: 경금속)으로 나타낼 수 있다. 야금류는 이들 화합물에서 8각으로 조정된 "B" 부지를 차지하고 있다. RPdB3, RRhB3, CeRuC3 등이 그 예다. mgCni는 금속성 페로브스카이트 화합물로 초전도 특성 때문에 많은 관심을 받아왔다. 훨씬 더 이국적인 형태의 페로브스카이트가 Cs와 Rb의 산화-아우라이드 혼합물로 대표되는데, CsAuO는3 전통적인 "음이온" 부지에 큰 알칼리 양이 들어 있고, O와2− Au− 음이온에 결합되어 있다.[citation needed]
재료 특성
페로브스카이트 소재는 이론적 측면과 응용적 측면 모두에서 흥미롭고 흥미로운 특성을 많이 보인다. 이 제품군에서는 대규모 자기저항, 강전, 초전도성, 전하 순서, 스핀 종속 운송, 높은 열전원 및 구조, 자기 및 운송 특성의 상호작용이 일반적으로 관찰된다. 이들 화합물은 특정 유형의 연료전지에서[24] 센서와 촉매 전극으로 사용되며 메모리 소자와 스핀트로닉스 응용의 후보물질이다.[25]
많은 초전도 세라믹 재료(고온 초전도체)는 페로브스카이트와 같은 구조를 가지고 있는데, 구리를 포함한 금속이 3개 이상이고, 일부 산소 위치는 비어 있는 경우가 많다. 대표적인 예가 산소 함량에 따라 절연 또는 초전도성을 할 수 있는 이트리움 바륨 구리 산화물이다.
화학 기술자들은 디젤 차량용 촉매변환기의 백금 대체 물질로 코발트 기반 페로브스카이트 물질을 고려하고 있다.[26]
적용들
페로브스카이트 중 재료과학에 관심 있는 물리적 특성은 초전도성, 자기저항성, 이온전도성, 다수의 유전체 특성 등이 있는데, 이는 마이크로 전자와 통신에서 매우 중요하다. 그들은 또한 방사선 변환을 위한 광 수율이 크기 때문에 섬광기에 관심이 있다. 페로브스카이트 구조에 내재된 결합 각도의 유연성 때문에 이상적인 구조에서 발생할 수 있는 많은 다른 유형의 왜곡이 있다. 여기에는 옥타헤드라의 기울기, 조정 다면체의 중심에서 양이온의 변위, 전자적 요인에 의한 옥타헤드라의 왜곡(Jahn-Teller 왜곡) 등이 포함된다.[27]
광전학

합성[30][31][32] 페로브스카이트는 NREL이 2020년에[29][30] 보고한 최대 25.5%의 변환 효율을 보이며 박막 실리콘 태양전지에 사용한 것과 동일한 박막 제조 기술을 사용하여 제조할 수 있는 고효율 상업용 광전지의 저렴한 기본 재료로 확인되었다.[33] 메틸람모늄 주석 할로겐화물과 메틸람모늄 납 할로겐화물은 염료감응형 태양전지에 사용하기 위해 관심이 높다.[34][35] 2016년 7월, 박사팀이 이끄는 연구팀. 알렉산더 베버-바르기오니는 페로브스카이트 PV 전지가 이론적으로 최대 효율 31%[36]에 도달할 수 있다는 것을 증명했다.
지금까지 연구된 메틸람모늄 할로겐화물 중 가장 흔한 것은 메틸람모늄 납삼다이오드(CHNHPbI
3
3
3)이다. 충전 캐리어 이동성과 충전 캐리어 수명이 높아 세포 내 열로서의 에너지를 잃지 않고 전류가 될 수 있을 만큼 광 발생 전자와 구멍이 멀리 이동할 수 있다. CHNHPbI
3
3
3 유효 확산 길이는 전자와 구멍 모두에 대해 약 100 nm이다.[37]
메틸람모늄 할로겐화물은 저온 용액법(일반적으로 스핀코팅)에 의해 침전된다. 다른 저온(100°C 미만) 용액 처리 필름은 확산 길이가 상당히 작은 경향이 있다. 스트랜크스 등은 혼합메틸람모늄 납 할라이드(CHNHPBICl333−xx)를 이용한 나노구조화 전지를 설명, 변환 효율이 11.4%인 아모르퍼스 박막 태양전지 1개와 진공 증발을 이용해 15.4%에 도달한 다른 전지를 시연했다. 약 500~600nm의 필름 두께는 전자와 홀 확산 길이가 적어도 이 순서의 길이였음을 의미한다. 혼합 페로브스카이트의 경우 1μm를 초과하는 확산 길이의 값을 측정했는데, 이는 순수한 요오드화물의 경우 100nm보다 큰 크기 순서였다. 그들은 또한 혼합된 페로브스카이트의 운반자 수명이 순수한 요오드화합물보다 길다는 것을 보여주었다.[37] 류 외 연구진은 스캐닝 포토 전류 현미경을 적용해 (110) 평면을 따라 혼합할라이드 페로브스카이트의 전자 확산 길이가 10μm임을 보여주었다.[38]
CHNHPbI의
3
3
3 경우 일반적으로 개방 회로 전압(VOC)이 1V에 근접하며, Cl 함량이 낮은 CHNHPbI
3
3(I,Cl)
3의 경우 VOC > 1.1V가 보고되었다. 양쪽의 대역 격차(Eg)가 1.55 eV이기 때문에 V-EOCg 대 V 비율은 유사한 제3세대 셀에서 보통 관측되는 것보다 높다. 보다 넓은 밴드갭 페로브스카이트로 V 최대OC 1.3V의 V가 시연되었다.[37]
이 기술은 저온 용해법과 희귀 원소의 부재 때문에 저비용의 가능성을 제공한다. 현재 셀 내구성이 상업적으로 사용하기에 불충분하다.[37]
평면 이질결합 과롭스카이트 태양전지는 증기 증착만을 사용하여 (복잡한 나노구조 없이) 단순화된 장치 구조로 제조될 수 있다. 이 기법은 시뮬레이션된 전체 햇빛 아래에서 측정했을 때 15%의 태양-전기 전력 변환을 생성한다.[39]
레이저스
2008년에 연구원들은 페로브스카이트가 레이저 광선을 생성할 수 있다는 것을 증명했다. 라알로는3 네오디뮴 도핑으로 레이저를 1080nm로 방출했다.[40] 2014년에 광학적으로 펌프된 수직-케이블 표면 방출 레이저(VCSEL)로 성형된 혼합 메틸람모늄 납 할리드(CHNHPBICl333−xx) 셀이 가시 펌프 빛을 70% 효율로 IR에 근접한 레이저 광으로 변환하는 것으로 나타났다.[41][42]
발광다이오드
높은 광 발광 양자 효율성으로 인해 페로브스카이트는 발광 다이오드(LED)에 사용할 수 있는 좋은 후보일 수 있다.[43] 페로브스카이트 LED의 안정성은 아직 III-V나 유기발광다이오드(Organic LED)에 비해 좋지 않지만, 페로브스카이트 LED에 유기분자나[44] 칼륨 도펜트를[45] 통합하는 등 이 문제를 해결하기 위한 연구가 진행 중이다.
광전자분해
2014년 9월 스위스 로잔의 EPFL 연구진은 페로브스카이트 광전지를 이용한 고효율 저비용 물분해 셀에서 12.3%의 효율로 수전분해를 달성했다고 보고했다.[46][47]
섬광기
1997년 세륨 도핑 루테튬 알루미늄 페로브스카이트의 섬광 특성(LuAP:ce) 단일 결정이 보고되었다.[48] 이러한 결정의 주요 성질은 8.4 g/cm의3 큰 질량 밀도로 X선 및 감마선 흡수 길이가 짧다. 섬광 수율과 Cs137 방사선 선원의 붕괴 시간은 각각 11,400개의 광자/MeV와 17ns이다.[49] 그러한 특성들은 LUAP:Ce 섬광기를 광고에 매력적으로 만들었고 그것들은 고에너지 물리학 실험에서 꽤 자주 사용되었다. 그로부터 11년이 지나도록 일본의 한 단체는 루들즈덴-포퍼 솔루션 기반의 하이브리드 유기농 페로브스카이트 결정을 저비용 섬광기로 제안했다.[50] 그러나 루AP에 비해 그 속성은 그다지 인상적이지 않았다.Ce. 이후 9년까지 솔루션 기반의 하이브리드 유기농 페로브스카이트 크리스탈은 극저온에서 10만 광자/MeV 이상의 높은 광수율에 대한 보고서를 통해 다시 인기를 끌었다.[51] X선 영상화면을 위한 페로브스카이트 나노결정 섬광기의 최근 시연이 보고되었으며 페로브스카이트 섬광기에 대한 더 많은 연구 노력을 촉발시키고 있다.[52] 레이어드 루들즈덴-포퍼 페로브스카이트는 실온 조명이 최대 40,000개의 광자/MeV, 5ns 미만의 빠른 붕괴 시간 및 무시할 수 있는 잔광기를 가진 빠른 소설 섬광기로서 잠재력을 보여 왔다.[16][17] 또한 이 등급의 물질은 알파 입자와 열 중성자를 포함한 광범위한 입자 검출 능력을 보여주었다.[53]
페로브스카이트의 예
단순:
- 티탄산 스트론튬
- 타이탄산칼슘
- 티탄산 납
- 비스무트 페라이트
- 란타넘 이테르비움 산화물
- 규산페로브스카이트
- 란타넘망가나이트
- 이트리움 알루미늄 페로브스카이트(YAP)
- 루테튬 알루미늄 페로브스카이트(LuAP)
- 란타넘 스트론튬망가나이트
- LSAT(란타넘 알루민산염 – 스트론튬 알루미늄 탄탈레이트)
- 탄탈산 납 스칸듐
- 지르콘산 티탄산 유도
- 메틸람모늄 납 할로겐화
- 메틸람모늄 주석 할로겐화
- 포마미디늄 주석 할로겐화
참고 항목
참조
- ^ A. Navrotsky (1998). "Energetics and Crystal Chemical Systematics among Ilmenite, Lithium Niobate, and Perovskite Structures". Chem. Mater. 10 (10): 2787. doi:10.1021/cm9801901.
- ^ a b c Wenk, Hans-Rudolf; Bulakh, Andrei (2004). Minerals: Their Constitution and Origin. New York, NY: Cambridge University Press. ISBN 978-0-521-52958-7.
- ^ N. Orlovskaya, N. Browning, ed. (2003). Mixed Ionic Electronic Conducting Perovskites for Advanced Energy Systems.
- ^ Artini, Cristina (2017-02-01). "Crystal chemistry, stability and properties of interlanthanide perovskites: A review". Journal of the European Ceramic Society. 37 (2): 427–440. doi:10.1016/j.jeurceramsoc.2016.08.041. ISSN 0955-2219.
- ^ Bridgemanite on Mindat.org
- ^ Fan, Zhen; Sun, Kuan; Wang, John (2015-09-15). "Perovskites for photovoltaics: a combined review of organic–inorganic halide perovskites and ferroelectric oxide perovskites". Journal of Materials Chemistry A. 3 (37): 18809–18828. doi:10.1039/C5TA04235F. ISSN 2050-7496.
- ^ Johnsson, Mats; Lemmens, Peter (2007). "Crystallography and Chemistry of Perovskites". Handbook of Magnetism and Advanced Magnetic Materials. arXiv:cond-mat/0506606. doi:10.1002/9780470022184.hmm411. ISBN 978-0470022177. S2CID 96807089.
- ^ Becker, Markus; Klüner, Thorsten; Wark, Michael (2017-03-14). "Formation of hybrid ABX3 perovskite compounds for solar cell application: first-principles calculations of effective ionic radii and determination of tolerance factors". Dalton Transactions. 46 (11): 3500–3509. doi:10.1039/C6DT04796C. ISSN 1477-9234. PMID 28239731.
- ^ Cava, Robert J. "Cava Lab: Perovskites". Princeton University. Retrieved 13 November 2013.
- ^ Kendall, K. R.; Navas, C.; Thomas, J. K.; Zur Loye, H. C. (1996). "Recent Developments in Oxide Ion Conductors: Aurivillius Phases". Chemistry of Materials. 8 (3): 642–649. doi:10.1021/cm9503083.
- ^ a b Munnings, C; Skinner, S; Amow, G; Whitfield, P; Davidson, I (15 October 2006). "Structure, stability and electrical properties of the La(2−x)SrxMnO4±δ solid solution series". Solid State Ionics. 177 (19–25): 1849–1853. doi:10.1016/j.ssi.2006.01.009.
- ^ Munnings, Christopher N.; Sayers, Ruth; Stuart, Paul A.; Skinner, Stephen J. (January 2012). "Structural transformation and oxidation of Sr2MnO3.5+x determined by in-situ neutron powder diffraction" (PDF). Solid State Sciences. 14 (1): 48–53. Bibcode:2012SSSci..14...48M. doi:10.1016/j.solidstatesciences.2011.10.015. hdl:10044/1/15437.
- ^ Amow, G.; Whitfield, P. S.; Davidson, I. J.; Hammond, R. P.; Munnings, C. N.; Skinner, S. J. (January 2004). "Structural and sintering characteristics of the La2Ni1−xCoxO4+δ series". Ceramics International. 30 (7): 1635–1639. doi:10.1016/j.ceramint.2003.12.164.
- ^ Amow, G.; Whitfield, P. S.; Davidson, J.; Hammond, R. P.; Munnings, C.; Skinner, S. (11 February 2011). "Structural and Physical Property Trends of the Hyperstoichiometric Series, La2Ni(1−x)CoxO4+δ". MRS Proceedings. 755. doi:10.1557/PROC-755-DD8.10.
- ^ Stoumpos, Constantinos C.; Cao, Duyen H.; Clark, Daniel J.; Young, Joshua; Rondinelli, James M.; Jang, Joon I.; Hupp, Joseph T.; Kanatzidis, Mercouri G. (2016-04-26). "Ruddlesden–Popper Hybrid Lead Iodide Perovskite 2D Homologous Semiconductors". Chemistry of Materials. 28 (8): 2852–2867. doi:10.1021/acs.chemmater.6b00847. ISSN 0897-4756.
- ^ a b Xie, Aozhen; Maddalena, Francesco; Witkowski, Marcin E.; Makowski, Michal; Mahler, Benoit; Drozdowski, Winicjusz; Springham, Stuart Victor; Coquet, Philippe; Dujardin, Christophe; Birowosuto, Muhammad Danang; Dang, Cuong (2020-10-13). "Library of Two-Dimensional Hybrid Lead Halide Perovskite Scintillator Crystals". Chemistry of Materials. 32 (19): 8530–8539. doi:10.1021/acs.chemmater.0c02789. ISSN 0897-4756. S2CID 224916409.
- ^ a b Maddalena, Francesco; Xie, Aozhen; Arramel; Witkowski, Marcin E.; Makowski, Michal; Mahler, Benoit; Drozdowski, Winicjusz; Mariyappan, Thambidurai; Springham, Stuart Victor; Coquet, Philippe; Dujardin, Christophe (2021-03-01). "Effect of commensurate lithium doping on the scintillation of two-dimensional perovskite crystals". Journal of Materials Chemistry C. 9 (7): 2504–2512. doi:10.1039/D0TC05647B. ISSN 2050-7534. S2CID 233789445.
- ^ Martin, L.W.; Chu, Y.-H.; Ramesh, R. (May 2010). "Advances in the growth and characterization of magnetic, ferroelectric, and multiferroic oxide thin films". Materials Science and Engineering: R: Reports. 68 (4–6): 89–133. doi:10.1016/j.mser.2010.03.001.
- ^ Yang, G.Z; Lu, H.B; Chen, F; Zhao, T; Chen, Z.H (July 2001). "Laser molecular beam epitaxy and characterization of perovskite oxide thin films". Journal of Crystal Growth. 227–228 (1–4): 929–935. Bibcode:2001JCrGr.227..929Y. doi:10.1016/S0022-0248(01)00930-7.
- ^ Mannhart, J.; Schlom, D. G. (25 March 2010). "Oxide Interfaces--An Opportunity for Electronics". Science. 327 (5973): 1607–1611. Bibcode:2010Sci...327.1607M. doi:10.1126/science.1181862. PMID 20339065. S2CID 206523419.
- ^ Chakhalian, J.; Millis, A. J.; Rondinelli, J. (24 January 2012). "Whither the oxide interface". Nature Materials. 11 (2): 92–94. Bibcode:2012NatMa..11...92C. doi:10.1038/nmat3225. PMID 22270815.
- ^ Ohtomo, A.; Hwang, H. Y. (January 2004). "A high-mobility electron gas at the LaAlO3/SrTiO3 heterointerface". Nature. 427 (6973): 423–426. Bibcode:2004Natur.427..423O. doi:10.1038/nature02308. PMID 14749825. S2CID 4419873.
- ^ John Lloyd; John Mitchinson (2006). "What's the commonest material in the world". QI: The Book of General Ignorance. Faber & Faber. ISBN 978-0-571-23368-7.
- ^ Kulkarni, A; FT Ciacchi; S Giddey; C Munnings; et al. (2012). "Mixed ionic electronic conducting perovskite anode for direct carbon fuel cells". International Journal of Hydrogen Energy. 37 (24): 19092–19102. doi:10.1016/j.ijhydene.2012.09.141.
- ^ J. M. D. Coey; M. Viret; S. von Molnar (1999). "Mixed-valence manganites". Advances in Physics. 48 (2): 167–293. Bibcode:1999AdPhy..48..167C. doi:10.1080/000187399243455.
- ^ Alexandra Witze (2010). "Building a cheaper catalyst". Science News Web Edition.
- ^ Lufaso, Michael W.; Woodward, Patrick M. (2004). "Jahn–Teller distortions, cation ordering and octahedral tilting in perovskites". Acta Crystallographica Section B. 60 (Pt 1): 10–20. doi:10.1107/S0108768103026661. PMID 14734840.
- ^ Eames, Christopher; Frost, Jarvist M.; Barnes, Piers R. F.; o'Regan, Brian C.; Walsh, Aron; Islam, M. Saiful (2015). "Ionic transport in hybrid lead iodide perovskite solar cells". Nature Communications. 6: 7497. Bibcode:2015NatCo...6.7497E. doi:10.1038/ncomms8497. PMC 4491179. PMID 26105623.
- ^ Bullis, Kevin (8 August 2013). "A Material That Could Make Solar Power "Dirt Cheap"". MIT Technology Review. Retrieved 8 August 2013.
- ^ a b Li, Hangqian. (2016). "A modified sequential deposition method for fabrication of perovskite solar cells". Solar Energy. 126: 243–251. Bibcode:2016SoEn..126..243L. doi:10.1016/j.solener.2015.12.045.
- ^ "Research Cell Efficiency Records" (PDF). Office of Energy Efficiency & Renewable Energy. 2020.
- ^ Zhu, Rui (2020-02-10). "Inverted devices are catching up". Nature Energy. 5 (2): 123–124. Bibcode:2020NatEn...5..123Z. doi:10.1038/s41560-020-0559-z. ISSN 2058-7546. S2CID 213535738.
- ^ Liu, Mingzhen; Johnston, Michael B.; Snaith, Henry J. (2013). "Efficient planar heterojunction perovskite solar cells by vapour deposition". Nature. 501 (7467): 395–398. Bibcode:2013Natur.501..395L. doi:10.1038/nature12509. PMID 24025775. S2CID 205235359.
- ^ Lotsch, B.V. (2014). "New Light on an Old Story: Perovskites Go Solar". Angew. Chem. Int. Ed. 53 (3): 635–637. doi:10.1002/anie.201309368. PMID 24353055.
- ^ Service, R. (2013). "Turning Up the Light". Science. 342 (6160): 794–797. Bibcode:2013Sci...342..794S. doi:10.1126/science.342.6160.794. PMID 24233703.
- ^ "Nanoscale discovery could push perovskite solar cells to 31% efficency (sic)". 2016-07-04.
- ^ a b c d Hodes, G. (2013). "Perovskite-Based Solar Cells". Science. 342 (6156): 317–318. Bibcode:2013Sci...342..317H. doi:10.1126/science.1245473. PMID 24136955. S2CID 41656229.
- ^ Liu, Shuhao; Wang, Lili; Lin, Wei-Chun; Sucharitakul, Sukrit; Burda, Clemens; Gao, Xuan P. A. (2016-12-14). "Imaging the Long Transport Lengths of Photo-generated Carriers in Oriented Perovskite Films". Nano Letters. 16 (12): 7925–7929. arXiv:1610.06165. Bibcode:2016NanoL..16.7925L. doi:10.1021/acs.nanolett.6b04235. ISSN 1530-6984. PMID 27960525. S2CID 1695198.
- ^ Liu, M.; Johnston, M. B.; Snaith, H. J. (2013). "Efficient planar heterojunction perovskite solar cells by vapour deposition". Nature. 501 (7467): 395–398. Bibcode:2013Natur.501..395L. doi:10.1038/nature12509. PMID 24025775. S2CID 205235359.
- ^ Dereń, P. J.; Bednarkiewicz, A.; Goldner, Ph.; Guillot-Noël, O. (2008). "Laser action in LaAlO3:Nd3+ single crystal". Journal of Applied Physics. 103 (4): 043102–043102–8. Bibcode:2008JAP...103d3102D. doi:10.1063/1.2842399.
- ^ 월리스, 존 (2014년 3월 28일) 고효율 페로브스카이트 광전지 소재도 레이스를 한다. 레이저포커스월드
- ^ "Study: Perovskite solar cells can double as lasers". Rdmag.com. 2014-03-28. Retrieved 2014-08-24.
- ^ Stranks, Samuel D.; Snaith, Henry J. (2015-05-01). "Metal-halide perovskites for photovoltaic and light-emitting devices". Nature Nanotechnology. 10 (5): 391–402. Bibcode:2015NatNa..10..391S. doi:10.1038/nnano.2015.90. ISSN 1748-3387. PMID 25947963.
- ^ Wang, Heyong; Kosasih, Felix Utama; Yu, Hongling; Zheng, Guanhaojie; Zhang, Jiangbin; Pozina, Galia; Liu, Yang; Bao, Chunxiong; Hu, Zhangjun; Liu, Xianjie; Kobera, Libor; Abbrent, Sabina; Brus, Jiri; Jin, Yizheng; Fahlman, Mats; Friend, Richard H.; Ducati, Caterina; Liu, Xiao-Ke; Gao, Feng (December 2020). "Perovskite-molecule composite thin films for efficient and stable light-emitting diodes". Nature Communications. 11 (1): 891. Bibcode:2020NatCo..11..891W. doi:10.1038/s41467-020-14747-6. PMC 7021679. PMID 32060279.
- ^ Andaji‐Garmaroudi, Zahra; Abdi‐Jalebi, Mojtaba; Kosasih, Felix U.; Doherty, Tiarnan; Macpherson, Stuart; Bowman, Alan R.; Man, Gabriel J.; Cappel, Ute B.; Rensmo, Håkan; Ducati, Caterina; Friend, Richard H.; Stranks, Samuel D. (December 2020). "Elucidating and Mitigating Degradation Processes in Perovskite Light‐Emitting Diodes". Advanced Energy Materials. 10 (48): 2002676. doi:10.1002/aenm.202002676. S2CID 228806435.
- ^ Jingshan Luo; et al. (26 September 2014). "Water photolysis at 12.3% efficiency via perovskite photovoltaics and Earth-abundant catalysts". Science. 345 (6204): 1593–1596. Bibcode:2014Sci...345.1593L. doi:10.1126/science.1258307. PMID 25258076. S2CID 24613846.
- ^ "Harvesting hydrogen fuel from the Sun using Earth-abundant materials". Phys.org. Sep 25, 2014. Retrieved 26 September 2014.
- ^ Moszynski, M (11 January 1997). "Properties of the new LuAP:Ce scintillator". Nuclear Instruments and Methods in Physics Research A. 385 (1): 123–131. Bibcode:1997NIMPA.385..123M. doi:10.1016/S0168-9002(96)00875-3.
- ^ Maddalena, Francesco; Tjahjana, Liliana; Xie, Aozhen; Arramel; Zeng, Shuwen; Wang, Hong; Coquet, Philippe; Drozdowski, Winicjusz; Dujardin, Christophe; Dang, Cuong; Birowosuto, Muhammad Danang (February 2019). "Inorganic, Organic, and Perovskite Halides with Nanotechnology for High–Light Yield X- and γ-ray Scintillators". Crystals. 9 (2): 88. doi:10.3390/cryst9020088.
- ^ Kishimoto, S (29 December 2008). "Subnanosecond time-resolved x-ray measurements using an organic-inorganic perovskite scintillator". Appl. Phys. Lett. 93 (26): 261901. Bibcode:2008ApPhL..93z1901K. doi:10.1063/1.3059562.
- ^ Birowosuto, Muhammad Danang (16 November 2016). "X-ray Scintillation in Lead Halide Perovskite Crystals". Sci. Rep. 6: 37254. arXiv:1611.05862. Bibcode:2016NatSR...637254B. doi:10.1038/srep37254. PMC 5111063. PMID 27849019.
- ^ Chen, Quishui (27 August 2018). "All-inorganic perovskite nanocrystal scintillators". Nature. 561 (7721): 88–93. Bibcode:2018Natur.561...88C. doi:10.1038/s41586-018-0451-1. PMID 30150772. S2CID 52096794.
- ^ Xie, Aozhen; Hettiarachchi, Chathuranga; Maddalena, Francesco; Witkowski, Marcin E.; Makowski, Michał; Drozdowski, Winicjusz; Arramel, Arramel; Wee, Andrew T. S.; Springham, Stuart Victor; Vuong, Phan Quoc; Kim, Hong Joo (2020-06-24). "Lithium-doped two-dimensional perovskite scintillator for wide-range radiation detection". Communications Materials. 1 (1): 37. Bibcode:2020CoMat...1...37X. doi:10.1038/s43246-020-0038-x. ISSN 2662-4443.
추가 읽기
- Tejuca, Luis G (1993). Properties and applications of perovskite-type oxides. New York: Dekker. p. 382. ISBN 978-0-8247-8786-8.
- Mitchell, Roger H (2002). Perovskites modern and ancient. Thunder Bay, Ontario: Almaz Press. p. 318. ISBN 978-0-9689411-0-2.
외부 링크
- "Cubic Perovskite Structure". Center for Computational Materials Science. U.S. Naval Research Laboratory. Archived from the original on 2008-10-08. (구조물을 대화식으로 회전시킬 수 있는 Java 애플릿 포함)