외상후 간질
Post-traumatic epilepsy| 외상후 간질 | |
|---|---|
| 전문 | 신경학 |
외상 후 간질(PTE)은 후천성 간질의 일종으로 뇌에 대한 신체적 외상으로 인한 뇌손상(외상성 뇌손상, 약칭 TBI)이다.[1]외상 후 발작(PTS, TBI로 인한 발작)[2]이 처음 부상당한 후 일주일 이상 경과한 경우.PTE는 전체 간질 환자의 5%와 후천 간질[3][4][1](발작이 식별 가능한 유기적 뇌 상태에 의해 발생하는 경우)의 20% 이상을 구성하는 것으로 추정된다.[5]
TBI 이후 누가 간질병에 걸릴지, 누가 발병하지 않을지를 어떻게 예측해야 할지는 알려지지 않았다.[6]그러나 사람이 PTE에 걸릴 확률은 부상의 심각도와 유형에 영향을 받는다. 예를 들어 관통상을 입거나 뇌내 출혈을 수반하는 부상 등은 더 높은 위험을 준다.PTE의 발병은 그것을 유발하는 신체적 외상의 짧은 시간 내에 또는 수개월 또는 수 년 후에 발생할 수 있다.[3]머리 외상을 입은 사람들은 부상 후 수십 년이 지난 후에도 일반 사람들보다 외상 후 발작의 위험이 더 높을 수 있다.[7]PTE는 뇌세포의 과다섭취, 활성산소에 의한 뇌조직 손상 등 외상 후 뇌에서 일어나는 몇 가지 생화학 작용에 의해 유발될 수 있다.[8]
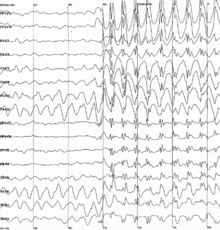
진단 방안으로는 뇌파검사(EEG)와 자기공명영상촬영 등 뇌영상기법 등이 있지만 완전히 신뢰할 수 있는 것은 아니다.방부제는 머리 부상 후 PTE의 발달을 막는 것이 아니라, 발생할 경우 치료하는 데 사용할 수 있다.발작을 억제하기 위해 약물치료가 효과가 없을 때, 수술이 필요할 수도 있다.[9]PTE를 위한 현대의 수술 기술은 19세기에 그 뿌리를 두고 있지만, 고대 문화권에서는 그 상태를 위해 트레패닝(두골에 구멍을 내는 것)이 사용되었을지도 모른다.[10]
분류
발작은 외상성 뇌손상 후에 일어날 수 있다; 이것들은 외상 후 발작이라고 알려져 있다.그러나 외상 후 발작이 있는 모든 사람이 외상 후 간질을 계속 앓는 것은 아니며, 이는 후자가 만성 질환이기 때문이다.그러나 의학 문헌에서 PTS와 PTE라는 용어는 서로 바꾸어 사용된다.[11][12]외상 후 간질로 인한 발작은 외상 후 원인과 시기에 따라 비외상 발작과 구별된다.PTE를 앓고 있는 사람은 초기 외상 후 일주일 이상 경과한 발작을 일으킨다.[13]늦은 발작은 이유 없는 것으로 간주되는 반면, 초기 발작(외상 1주일 이내에 발생한 발작)은 부상의 직접적인 영향에서 비롯되는 것으로 생각된다.자극받은 발작은 뇌의 결함보다는 외상의 즉각적인 영향과 같은 예외적이고 반복되지 않는 원인에 기인하는 것이다; 그것은 간질의 징후가 아니다.[14]따라서 PTE 진단을 위해서는 발작이 원인 없이 이루어져야 한다.
PTE를 하나 이상의 늦은, 이유 없는 발작의 발생으로 정의할지, 아니면 둘 이상의 사람에게만 그 상태를 진단해야 하는지에 대해서는 의견이 분분하다.[15]의료원에서는 보통 이유 없는 발작이 한 번이라도 발생하면 PTE가 존재하는 것으로 보고 있으나, 최근에는 하나 이상의 발작이 일어나는 조건만을 포함하도록 모든 종류의 간질의 정의를 제한하는 것이 받아들여지고 있다.[11]PTE 진단을 위해 두 번 이상의 발작을 요구하는 것은 간질의 현대적 정의에 더 부합하지만 첫 발작 후 약물치료를 통해 발작을 조절하는 사람들을 제거하는 것이다.[11]
다른 형태의 간질과 마찬가지로 PTE에서 발작형은 부분(뇌의 한 반구 일부만 영향을 미침)이거나 일반화(두 반구 모두에 영향을 미치고 의식 상실과 관련됨)될 수 있다.[16]약 3분의 1의 경우에, PTE를 가진 사람들은 부분적인 발작을 일으킨다; 이것들은 간단하거나 복잡할 수 있다.[17]단순한 부분 발작에서는 의식의 수준이 변하지 않는 반면 복잡한 부분 발작 의식은 손상된다.[14]일반화된 발작이 일어나면 부분적인 발작에서 시작하여 일반화되기까지 확산될 수 있다.[17]
원인들

매우 유사한 부상을 입은 다른 환자들은 그렇지 않은 반면, 일부 환자들은 왜 PTE를 발병시키는지 명확하지 않다.[11]그러나 부상 심각도와 유형, 초기 발작 유무, 유전적 요인 등 가능한 위험 요인이 확인되었다.
유전학
유전학은 한 사람이 PTE를 발전시킬 위험에서 역할을 할 수 있다; ApoE-234 알레르기를 가진 사람들은 PTE에 더 높은 위험에 처할 수 있다.[7]Haptoglobin Hp2-2 알레일은 헤모글로빈을 잘 결합하지 못해 더 많은 철분이 빠져나와 조직을 손상시키기 때문에 또 다른 유전적 위험인자가 될 수 있다.[7]그러나 대부분의 연구에서 간질을 가진 가족을 갖는 것이 PTS의 위험을 크게 증가시키지 않는다는 것을 밝혀내면서 유전학이 강한 위험요인은 아니라는 것을 시사했다.[11]
트라우마의 심각도
뇌 트라우마가 심할수록 늦은 PTE에 시달릴 가능성이 높다.[19]증거에 따르면 가벼운 머리 부상은 PTE 발병의 위험을 증가시키지 않는 반면, 더 심각한 유형은 발병 위험을 증가시키지 않는다.[20]단순 경미한 TBI에서 PTE에 대한 위험은 미주입 인구의 1.5배 정도 된다.[18]일부 추정치에 따르면, 중증 뇌 외상 환자의 절반 이상이 PTE를 경험하고 있으며,[19] 다른 추정치는 모든 TBI 환자의 경우 5%, 중증 TBI의 경우 15~20%의 위험이 있다고 한다.[21]한 연구에서는 오른쪽 도표에 나타난 바와 같이 30년 동안의 PTE 발병 위험이 경미한 TBI의 경우 2.1%, 중간 정도의 경우 4.2%, 중상해의 경우 16.7%로 나타났다.[18][22]
트라우마의 특성
머리 외상의 성격도 PTE의 위험성에 영향을 미친다.TBI로 인해 두개골 골절, 관통두상 외상, 초기 PTS, 추간 및 경막하혈모세포 등을 앓는 사람들은 특히 PTE에 걸리기 쉽다. PTE는 이러한 발견을 가진 사람의 30% 이상에서 발생한다.[19]머리 관통 외상을 입은 환자의 약 50%는 PTE가 발병하며,[8][20] 비산물 부상과 뇌 용적 상실은 특히 이 질환의 발생 가능성이 높은 것과 관련이 있다.[23]군사 환경에서 발생하는 부상은 PTE에 대한 위험성이 보통보다 높은데, 이는 아마도 더 일반적으로 뇌에 침투하는 부상과 더 광범위한 영역에 걸친 뇌 손상을 수반하기 때문일 것이다.[7]두개골 내부에 혈액이 축적되는 두개골 내 혈종은 PTE의 가장 중요한 위험인자 중 하나이다.[24]경막하 혈종은 경막외 혈종보다 PTE의 위험이 더 높은데, 아마도 뇌 조직에 더 많은 손상을 주기 때문일 것이다.[8]반복적인 뇌내 수술은 늦은 PTE에 높은 위험을 초래하는데, 아마도 수술이 더 필요한 사람들은 큰 혈종이나 뇌 붓기와 같은 더 나쁜 뇌 외상과 관련된 요소들을 더 많이 가지고 있기 때문일 것이다.[8]또한 PTE가 발생할 확률은 뇌병변 위치에 따라 다르다. 전두엽 중 하나 또는 다른 한쪽에서 발생하는 뇌 압전은 20%의 PTE 위험을 안고 있는 반면, 두정엽 중 하나의 압전은 19%의 위험을 안고 있고 측두엽 중 하나는 16%의 확률로 나타난다.[22]양쪽 반구에서 타박상이 발생할 때 위험은 전두엽 26%, 두정엽 66%, 측두 31%이다.[22]
외상 후 발작
사람이 PTE를 개발할 위험은 높아지지만 PTS가 발생할 경우 100%가 아니다.[20]PTE와 초기 PTS에 대한 위험요인의 상당수는 동일하기 때문에 PTS의 발생 자체가 위험요인인지 알 수 없다.[7]그러나 다른 일반적인 위험요인과 무관하게 초기 PTS는 대부분의 연구에서 PTE의 위험을 25% 이상으로 증가시키는 것으로 밝혀졌다.[4]발작이 늦은 사람은 초기 PTS를 가진 사람보다 더 큰 위험에 처해있다; 간질은 발작이 늦은 사람의 80%에서 발생한다.[25]계속적인 발작이나 급속한 연속적인 다중 발작인 상태 간질증은 특히 PTE의 발달과 밀접한 관련이 있다; 상태 발작은 전체 TBI의 6%에서 발생하지만 그 시간의 42%와 연관되어 있으며, 상태 발작을 빨리 중단하면 PTE가 발전할 가능성이 줄어든다.[22]
병리학
알 수 없는 이유로 트라우마는 뇌에 간질을 일으키는 변화를 일으킬 수 있다.[3][26]TBI가 PTE를 유발하는 많은 제안된 메커니즘이 있으며, 그 중 하나 이상이 주어진 사람에게 존재할 수 있다.[8]뇌손상과 간질 발현 사이에 뇌세포가 새로운 시냅스와 축대를 형성하고, 세포사멸이나 괴사를 겪으며 유전자 발현을 변화시킬 수 있다.[25]또한 해마와 같은 피질의 특히 취약한 부위의 손상은 PTE를 유발할 수 있다.[4]
부상 후 뇌에 모이는 혈액은 뇌 조직을 손상시켜 간질을 유발할 수 있다.[8]혈액에서 헤모글로빈이 분해되어 생기는 제품들은 뇌 조직에 독성이 있을 수 있다.[8]"철의 가설"은 PTE가 혈액에서 철로 촉매되는 산소 활성산소에 의한 손상 때문이라고 한다.[19]쥐를 이용한 동물실험을 통해 뇌에 철분을 주입하면 간질 발작이 발생할 수 있다는 사실이 밝혀졌다.[8]철은 Haber-Weiss 반응에 의해 히드록시산소의 형성을 촉진한다; 그러한 활성산소는 세포막의 지질들을 과산화하여 뇌세포를 손상시킨다.[8][27]혈액에서 나온 철은 또한 PTE에 기여한다고 생각되는 또 다른 요소인 질산화물 신타아제라고 불리는 효소의 활동을 감소시킨다.[19]
TBI 이후, 뇌세포가 서로 의사소통하기 위해 사용하는 화학물질인 신경전달물질의 방출에 이상이 존재한다; 이러한 이상은 PTE의 발달에 역할을 할 수 있다.[8]TBI는 글루탐산염과 다른 흥분성 신경전달물질(뇌세포를 자극하고 발화 가능성을 높이는 물질)의 과도한 방출로 이어질 수 있다.이러한 과도한 글루탐산염 방출은 흥분성 신경전달물질에 결합하고 반응하는 생화학 수용체의 과잉활성화를 통해 뇌세포에 손상을 줄 수 있다.글루탐산염 수용체의 과잉 활성화는 뉴런을 손상시킨다. 예를 들어 그것은 활성산소의 형성을 이끈다.[8]흥분독성은 PTE의 발달에 가능한 요인이다;[13] 그것은 만성 간질병 유발 주제의 형성을 초래할 수 있다.[8]간질적 집중은 간질적 방전이 발생하는 뇌의 부분이다.[28]
세포의 화학적 변화 외에도 뇌에서 간질을 유발하는 구조적 변화가 일어날 수 있다.[3]TBI 직후에 발생하는 발작은 신경망을 재편성할 수 있고 발작을 반복적으로 그리고 나중에 자연적으로 발생시킬 수 있다.[4]이 친절한 가설은 뇌에 새로운 신경 연결이 형성되어 흥분성의 증가를 일으킨다는 것을 암시한다.[19]kindling이라는 단어는 은유인데, 반복적인 노출에 의해 자극에 대한 뇌의 반응이 증가하는 방법은 타오르는 작은 나뭇가지들이 큰 불을 낼 수 있는 방법과 비슷하다.[29]이러한 신경망의 재구성은 그들을 더욱 흥분하게 만들지도 모른다.[4]트라우마로 인해 과대포화 상태에 있는 뉴런은 뇌에 간질 집중을 일으켜 발작을 일으킬 수 있다.[12]또한, 뉴런의 흥분성의 증가는 다른 뉴런들이 발화할 가능성을 감소시키는 역할을 하는 억제성 뉴런의 상실을 동반할 수 있다; 이러한 변화들은 또한 PTE를 발생시킬 수도 있다.[4]
진단
PTE 진단을 받으려면 머리 외상의 이력이 있어야 하며, 부상 전 발작 이력이 없어야 한다.[30]발작을 목격하는 것이 PTE를 진단하는 가장 효과적인 방법이다.[12]뇌파검사(EEG)는 발작장애를 진단하기 위해 사용되는 도구지만, PTE를 가진 사람들의 상당수는 간질을 나타내는 비정상적인 "증상형" EEG 발견을 가지고 있지 않을 수 있다.[12]한 연구에서, 부상 후 3개월 후에 정상 뇌파검사를 받은 사람의 약 5분의 1이 후에 PTE에 걸렸다.그러나 EEG는 누가 PTE를 개발할 것인가를 예측하는 데는 유용하지 않지만 간질 집중을 국소화하고, 중증도를 판단하며, 사람이 항균제 복용을 중단하면 더 많은 발작을 겪게 될 것인지를 예측하는 것은 유용할 수 있다.[8]
자기공명영상(MRI)은 PTE를 가진 사람을 대상으로 진행되며, CT 스캔을 통해 MRI를 사용할 수 없을 경우 뇌병변을 감지할 수 있다.[8]그러나 신경영상법을 사용하여 간질적 초점을 검출하지 못하는 경우가 많다.[31]
PTE 진단을 위해 발작은 또 다른 명백한 원인에 기인해서는 안 된다.[4]머리 부상 후에 일어나는 발작은 반드시 간질이나 심지어 머리 외상 때문도 아니다.[11]다른 사람들과 마찬가지로 TBI 생존자들은 액체나 전해질의 불균형, 다른 원인에 의한 간질, 저산소증, 허혈(뇌로 충분한 혈액이 흐르지 않음) 등의 요인으로 발작을 겪을 수 있다.[11]술에서 물러나는 것도 발작의 또 다른 잠재적 원인이다.[32]따라서 이러한 요인들은 PTE 진단을 내리기 전에 머리를 다친 사람의 발작의 원인으로 배제되어야 한다.
예방
PTE의 예방은 일반적으로 뇌 외상을 예방하는 것을 포함한다; 보호 조치들은 자전거 헬멧과 어린이 안전 좌석을 포함한다.[8]TBI 발생 후 간질 발병을 막기 위한 구체적인 치료법은 존재하지 않는다.[3]과거에는 PTE의 발달을 막기 위한 목적으로 항균제를 사용하였다.[3]그러나, 항균제는 초기 PTS를 예방할 수 있지만, 임상 연구는 항균제의 예방적 사용이 PTE의 발전을 방해한다는 것을 보여주지 못했다.[2][3][7][33]임상시험에서 방제제가 왜 PTE의 발달을 막지 못했는지는 명확하지 않지만, 여러 가지 설명이 제시되었다.[7]약물은 단순히 간질을 예방할 수 없거나, 약물의 효익이 발견되지 않는 방식으로 약물이 설치되었을 수 있다(예: 약물이 너무 늦게 또는 부적절한 용량으로 투여되었을 수 있음).[7]동물 연구는 비슷하게 페니토인이나 카바마제핀과 같은 PTE 실험에서 가장 흔히 사용되는 발작 약물의 보호 효과를 많이 보여주지 못했다.[7]방제약은 예방책이 아닌 이미 PTE 진단을 받은 사람에게만 늦은 발작을 예방하는 것이 좋다.[34]앞서 언급한 연구를 근거로 간질의 발달을 막기 위한 치료법은 널리 받아들여지지 않는다.[19]다만 항우울제 투여 시 간질유전증(간질병 발병)을 예방할 수 있는 TBI 후 약 1시간 정도의 좁은 창이 존재할 수 있다는 제안이 나왔다.[9]
코르티코스테로이드도 PTE 예방을 위해 조사되었으나, 임상 실험 결과 이 약물이 늦은 PTS를 감소시키지 않았고 실제로 초기 PTS 수의 증가와 관련이 있는 것으로 밝혀졌다.[3]
치료
더 이상의 발작을 예방하기 위해 항균제가 투여될 수 있다; 이 약들은 PTE를 가진 사람들의 약 35%에 대한 발작을 완전히 제거한다.[22]그러나 항우울제는 복용하는 동안에만 발작을 예방할 뿐, 환자가 일단 약을 끊으면 발병률을 줄이지 않는다.[2]발작이 2년 동안 억제된 후에 약물치료가 중단될 수 있다.[4]PTE는 일반적으로 약물요법으로 치료하기 어렵고,[3][35] 항소독제는 부작용과 관련이 있을 수 있다.[34]항우울제 카바마제핀과 발프로테이트는 PTE 치료에 사용되는 가장 일반적인 약이다. 페니토인 또한 사용될 수 있지만, 손상된 사고와 같은 인지적 부작용의 위험을 증가시킬 수 있다.[9]PTE 치료에 일반적으로 사용되는 다른 약으로는 클로나제팜, 페노바르비톨, 프리미돈, 가바펜틴, 에토스시미드 등이 있다.[12]TBI(페니토인, 발프로이트 나트륨, 카바마제핀, 페노바르비탈) 이후 발작 방지를 위해 시험한 항소독제 가운데 무작위 통제 실험에서 나온 어떤 증거도 다른 것에 비해 우월함을 보여주지 못했다.[8]
PTE가 약물치료에 반응하지 않는 사람들은 발작을 일으키는 뇌의 부분인 간질 유발 집중을 제거하기 위한 수술을 받을 수 있다.[9]그러나 PTE의 수술은 다른 원인에 의한 간질보다 더 어려울 수 있고,[9] 다른 형태의 간질보다 PTE에 도움이 될 가능성이 적다.[8]TBI가 뇌의 확산 부위에 영향을 미칠 수 있기 때문에 PTE에서 간질 집중을 국소화하는 것은 특히 어려울 수 있다.[31]발작의 초점을 찾기가 어려운 것은 수술에 대한 억제책으로 보인다.[4]그러나 난치성 PTE를 가진 사람의 약 3분의 1을 구성하고 있는 (측두엽 내측) 중측두엽에 경화증이 있는 사람에게는 수술이 좋은 결과를 낳을 가능성이 높다.[4]여러 가지 간질성 집중이 있거나 초점이 국부화 될 수 없고 약물치료가 효과적이지 않을 때는 부랑신경 자극도 PTE 치료의 또 다른 선택이다.[31]
PTE를 앓고 있는 사람들은 건강관리 제공자들이 신경학적, 신경정신학적 기능을 모니터하고 약물의 효능과 부작용을 평가하는 사후 방문도 한다.[8]다른 종류의 간질 환자와 마찬가지로, PTE 환자들은 암벽등반과 같이 발작이 특히 위험할 수 있는 활동을 할 때 주의를 기울여야 한다.[9]
예후
트라우마에 의한 간질 예후가 원인 미확인의 간질 예후보다 더 나쁘다.[20]PTE를 앓고 있는 사람들은 발작을 일으키지 않는 뇌손상을 입은 사람들보다 수명이 더 짧은 것으로 여겨진다.[12]유사한 구조적 뇌손상을 입었지만 PTE가 없는 사람들에 비해 PTE가 있는 사람들은 부상으로부터 회복하는 데 시간이 더 오래 걸리고, 더 많은 인지 및 운동 장애를 가지고 있으며, 일상 업무에서 더 나쁜 성과를 낸다.[12]이 발견은 PTE가 그 자체가 결과를 악화시키는 합병증이라기 보다는 더 심각한 뇌손상의 지표라는 것을 암시할 수 있다.[12]또한 PTE는 더 나쁜 사회적, 기능적 결과와 관련이 있지만 환자의 재활이나 복직 능력을 악화시키지 않는 것으로 밝혀졌다.[8]그러나 PTE를 가진 사람들은 발작을 인정하면, 특히 그들의 일이 중장비를 작동시키는 것을 수반한다면, 일자리를 찾는데 어려움을 겪을 수 있다.[36]
부상과 간질병 발병 사이의 기간은 다양하며, 부상이 재발하지 않고 잠복기가 뒤따르는 경우도 드물지 않다.[25]발작을 일으키지 않고 오래 갈수록 간질이 발병할 가능성은 낮아진다.[4]적어도 PTE를 가진 사람들의 80~90%가 TBI로부터 2년 이내에 첫 발작을 일으킨다.[8]부상 후 3년 이내에 발작이 없는 사람은 간질이 생길 확률은 5%에 불과하다.[37]그러나 한 연구에 따르면 머리 외상 생존자들은 보통 TBI 이후 10년, 심한 TBI 이후 20년 이상 PTE에 걸릴 위험이 증가하였다.[7]두부 외상이 상당히 흔하고 부상 후 늦게 간질이 발생할 수 있기 때문에 과거 두부 외상에 의한 간질인지, 외상이 부수적인 것인지 판단하기 어려울 수 있다.[31]
PTE를 앓고 있는 사람이 일반 인구보다 발작 위험이 얼마나 높은지 의문이다.[7]PTE 사례의 약 절반은 감원되지만, 나중에 발생하는 경우는 감원될 가능성이 더 작을 수 있다.[20]
역학
연구에 따르면, PTE의 발병률은 TBI 환자의 1.9에서 30% 이상이며, 부상의 심각도와 연구가 피험자를 추적한 TBI 이후의 시간에 따라 차이가 있다.[7]
뇌외상은 간질발달의 가장 강력한 소인중 하나이며, 특히 청소년들에게 중요한 요인이다.[22]머리 부상 위험이 가장 높은 청년층도 PTE 비율이 가장 높아 젊은 층의 신종 간질병의 가장 큰 원인이다.[8][38]아이들은 간질병에 걸릴 위험이 낮다; 심각한 TBI를 앓고 있는 어린이의 10%, 유사하게 다친 어른의 16~20%가 PTE에 걸린다.[22]65세 이상이 되는 것도 뇌 외상 후 간질 발병의 예측 요인이다.[25]한 연구는 PTE가 여성보다 남성 TBI 생존자들에게 더 흔하다는 것을 발견했다.[12]
역사
PTE에 대한 기록은 기원전 3000년부터 존재한다.[36]두개골에 구멍을 내는 트레패니언은 고대 문화에서 PTE를 치료하는데 사용되었을지도 모른다.[10]19세기 초, 외과의사 Larrey와 WC Wells는 각각 PTE를 위한 수술을 했다고 보고했다.[10]프랑스 교육을 받은 미국인 외과의사 벤자민 윈슬로우 더들리(1785–1870)는 켄터키에서 1819년에서 1832년 사이에 PTE를 위해 6번의 트레패닝을 수행했고, 항진증이 불가능함에도 불구하고 좋은 결과를 얻었다.[39]수술은 부상 부위의 두개골을 열고, 부상당한 조직을 괴사하며, 때로는 두라모자 밑에서 혈액이나 액체를 빼내는 것이었다.[39]더들리의 작품은 그 때까지 행해진 것 중 가장 큰 시리즈였고, 그것은 다른 외과의사들이 외상 후 발작을 위해 트레페네이션을 사용하도록 장려했다.[39]그의 수술에 대한 보고는 두개골 내의 과도한 압력을 완화시키는 수술이 간질을 치료하는 데 효과적이라는 것이 받아들여지기 전에 나왔지만, 그것은 PTE가 일반적인 관행이 될 수 있는 계기를 마련하는 데 도움이 되었다.[39]이 절차는 한 때 항분해가 가능하고 뇌 국산화라는 것이 익숙한 개념이었던 19세기 후반에 더욱 받아들여지게 되었다.[39]그러나 1890년 독일의 저명한 의사인 어네스트 폰 베르그만은 그 절차를 비판하였다. 그는 그 절차에 대해 의문을 제기했고, 장기적 이익을 줄 것인지 여부를 알기 위한 절차가 끝난 후 너무 빨리 수술이 성공적이라고 선언되었다고 제안했다.[10]19세기 후반에는 두개골과 뇌수막만을 포함하는 두개골 수술을 넘어 발작을 일으키는 것으로 여겨지는 뇌 병변을 수술하는 두개골 내 수술의 출현을 보았다.[10]1893년까지 미국에서 PTE를 위해 최소 42번의 두개내 수술이 수행되었고, 성공은 제한적이었다.[10]
수술은 제2차 세계 대전 이후 몇 년 동안 PTE의 표준 치료법이었다. 이때 두부 외상으로 살아남은 병사들이 그것을 개발하면서 그 상태가 더 주목을 받았다.[19]PTE를 치료하기 위한 약의 필요성 증가는 항우울제를 이용한 실험으로 이어졌다; 이러한 초기 실험들은 그 약이 간질유전증을 예방할 수 있다는 것을 시사했다.[19]항균제는 1970년대에도 간질유전증을 예방할 수 있다고 생각되었다;[27] 1973년 조사된 의사들 중 60%가 PTE를 예방하기 위해 그것을 사용했다.[33]그러나, 항피립틱스의 보호 효과를 뒷받침하던 임상 실험은 통제되지 않았다. 이후 통제된 실험은 항피립트 유발 효과를 보여주지 못했다.[40]연구는 항우울제가 부상 후 일주일 이내에 발작을 예방한다는 것을 보여주었고, 1995년 뇌외상 재단의 태스크 포스는 외상 후 조기 발작으로부터 보호하기 위해 그들의 사용을 제안하는 권고안을 발표했다.[33]그러나 1998년 미국 물리치료학회의 뇌손상 특수이익단체와 2000년 미국 신경외과 협회에 의해 부상 후 일주일 이상 경과한 항균제 사용에 대한 권고안이 발표되었다.[12]
리서치
뇌에 상처가 난 후 간질이 어떻게 발생하는지는 완전히 이해되지 않으며, 그러한 이해를 얻는 것은 연구자들이 간질을 예방하는 방법을 찾거나 덜 심각하거나 치료하기 쉽게 하는 데 도움을 줄 수 있다.[22]연구자들은 간질이 발병하는 경로를 타겟으로 할 수 있는 약물을 찾기 위한 수단으로 간질유전증이 발생하고 있다는 생물학적 지표인 바이오마커(biomarker)를 규명하기를 바라고 있다.[25]예를 들어 뇌조직에 대한 자유로운 과격파손상 등의 경로를 차단함으로써 2차 뇌손상(외상 순간에는 발생하지 않지만, 뇌조직에 의해 시작된 과정에서 발생하는 부상)을 방해하는 약물을 개발할 수 있다.[31]외상 후 간질 발육에서 나이 차이에 대한 이해도가 높아지면 간질유전증의 생체지표를 찾는 데도 도움이 될 수 있다.[25]간질유전증에 간섭할 가능성이 있는, 더 많은 방부제를 찾는 데도 관심이 있다.[41]토피라마이트, 가바펜틴, 라모트리진 등 일부 신종 항균제가 이미 개발돼 PTE 치료에 유망한 것으로 나타났다.[8]어떤 동물 모델도 인간에게 간질유전증의 모든 특징을 가지고 있지 않기 때문에, 연구 노력의 목표는 간질유전증의 한 가지 특징을 규명하는 것이다.[22][25]그러한 모델은 연구자들이 새로운 치료법을 찾고 간질유전증에 관련된 과정을 확인하는 데 도움을 줄 수 있다.[7]그러나, 유체 타악기 부상, 피질 충격 제어, 체중 감소 부상 모델과 같은 외상성 뇌 손상의 가장 일반적인 기계적 모델은 원격 뇌파 및 행동 발작 증세가 기록되어 있는 만성 시점에서 간질유전증을 보이고, 발작 민감성이 증가한다.[42]제브라피쉬에서도 PTE가 발생할 수 있어 인간의 TBI에 대해서도 유사한 병태생리학적 반응을 일으킬 수 있다고 보고되었다.[43]
참고 항목
참조
- ^ a b Brady, Rhys D.; Casillas-Espinosa, Pablo M.; Agoston, Denes V.; Bertram, Edward H.; Kamnaksh, Alaa; Semple, Bridgette D.; Shultz, Sandy R. (March 2019). "Modelling traumatic brain injury and posttraumatic epilepsy in rodents". Neurobiology of Disease. 123: 8–19. doi:10.1016/j.nbd.2018.08.007. PMC 6348144. PMID 30121231.
- ^ a b c Pagni CA, Zenga F (2005). "Posttraumatic epilepsy with special emphasis on prophylaxis and prevention". Acta Neurochirurgica. Acta Neurochirurgica Supplementum. 93: 27–34. doi:10.1007/3-211-27577-0_3. ISBN 978-3-211-24150-9. PMID 15986723.
- ^ a b c d e f g h i Garga N, Lowenstein DH (2006). "Posttraumatic Epilepsy: A Major Problem in Desperate Need of Major Advances". Epilepsy Currents. 6 (1): 1–5. doi:10.1111/j.1535-7511.2005.00083.x. PMC 1363374. PMID 16477313.
- ^ a b c d e f g h i j k Mani J, Barry E (2006). "Posttraumatic epilepsy". In Wyllie E, Gupta A, Lachhwani DK (eds.). The Treatment of Epilepsy: Principles and Practice. Hagerstown, MD: Lippincott Williams & Wilkins. pp. 521–524. ISBN 0-7817-4995-6.
- ^ Scheffer, Ingrid E.; Berkovic, Samuel; Capovilla, Giuseppe; Connolly, Mary B.; French, Jacqueline; Guilhoto, Laura; Hirsch, Edouard; Jain, Satish; Mathern, Gary W. (April 2017). "ILAE classification of the epilepsies: Position paper of the ILAE Commission for Classification and Terminology". Epilepsia. 58 (4): 512–521. doi:10.1111/epi.13709. PMC 5386840. PMID 28276062.
- ^ Pitkänen A, Kharatishvili I, Karhunen H, et al. (2007). "Epileptogenesis in experimental models". Epilepsia. 48 (Supplement 2): 13–20. doi:10.1111/j.1528-1167.2007.01063.x. PMID 17571349. S2CID 23523719.
- ^ a b c d e f g h i j k l m D'Ambrosio R, Perucca E (2004). "Epilepsy after head injury". Current Opinion in Neurology. 17 (6): 731–735. doi:10.1097/00019052-200412000-00014. PMC 2672045. PMID 15542983.
- ^ a b c d e f g h i j k l m n o p q r s t u v Agrawal A, Timothy J, Pandit L, Manju M (2006). "Post-traumatic epilepsy: An overview". Clinical Neurology and Neurosurgery. 108 (5): 433–439. doi:10.1016/j.clineuro.2005.09.001. PMID 16225987. S2CID 2650670.
- ^ a b c d e f Posner E, 로렌초 N (2006년 10월 11일)."외상후 간질"Emedicine.com.2008-07-30에 검색됨.
- ^ a b c d e f Eadie MJ, Bladin PF (2001). A Disease Once Sacred: A History of the Medical Understanding of Epilepsy. London: John Libbey. pp. 215–216. ISBN 0-86196-607-4.
- ^ a b c d e f g Frey LC (2003). "Epidemiology of posttraumatic epilepsy: A critical review". Epilepsia. 44 (Supplement 10): 11–17. doi:10.1046/j.1528-1157.44.s10.4.x. PMID 14511389. S2CID 34749005. Archived from the original on 2012-12-16.
- ^ a b c d e f g h i j Tucker GJ (2005). "Seizures". In Silver JM, McAllister TW, Yudofsky SC (eds.). Textbook Of Traumatic Brain Injury. American Psychiatric Pub., Inc. pp. 309–321. ISBN 1-58562-105-6.
- ^ a b Gupta YK, Gupta M (2006). "Post traumatic epilepsy: A review of scientific evidence" (PDF). Indian Journal of Physiology and Pharmacology. 50 (1): 7–16. PMID 16850898. Archived from the original (PDF) on 2011-07-13. Retrieved 2008-07-31.
- ^ a b Ayd FJ (2000). Lexicon of Psychiatry, Neurology, and the Neurosciences. Philadelphia, Pa: Lippincott-Williams & Wilkins. pp. 888–890. ISBN 0-7817-2468-6.
- ^ Statler KD (2006). "Pediatric posttraumatic seizures: Epidemiology, putative mechanisms of epileptogenesis and promising investigational progress". Dev. Neurosci. 28 (4–5): 354–363. doi:10.1159/000094162. PMID 16943659. S2CID 24833791.
- ^ Cuccurullo S (2004). Physical Medicine and Rehabilitation Board Review. Demos Medical Publishing. pp. 68–71. ISBN 1-888799-45-5.
- ^ a b Parent JM, Aminoff MJ (2004). "Treatment of epilepsy in general medical conditions". In Dodson WE, Avanzini G, Shorvon SD, Fish DR, Perucca E (eds.). The Treatment of Epilepsy. Oxford: Blackwell Science. p. 244. ISBN 0-632-06046-8.
- ^ a b c Annegers JF, Hauser WA, Coan SP, Rocca WA (January 1998). "A population-based study of seizures after traumatic brain injuries". New England Journal of Medicine. 338 (1): 20–4. doi:10.1056/NEJM199801013380104. PMID 9414327.
- ^ a b c d e f g h i Iudice A, Murri L (2000). "Pharmacological prophylaxis of post-traumatic epilepsy". Drugs. 59 (5): 1091–9. doi:10.2165/00003495-200059050-00005. PMID 10852641. S2CID 28616181.
- ^ a b c d e JW Sander, MC Walker and JE Smalls (editors) (2007). "Chapter 12: Adult onset epilepsies, DW Chadwick" (PDF). Epilepsy: From Cell to Community – A Practical Guide to Epilepsy (PDF). National Society for Epilepsy. pp. 127–132. ISBN 978-0-9519552-4-6. Retrieved 2008-07-26.
{{cite book}}:author=일반 이름 포함(도움말) - ^ Oliveros-Juste A, Bertol V, Oliveros-Cid A (2002). "Preventive prophylactic treatment in posttraumatic epilepsy". Revista de Neurología (in Spanish). 34 (5): 448–459. doi:10.33588/rn.3405.2001439. PMID 12040514.
- ^ a b c d e f g h i Pitkänen A, McIntosh TK (2006). "Animal models of post-traumatic epilepsy". Journal of Neurotrauma. 23 (2): 241–261. doi:10.1089/neu.2006.23.241. PMID 16503807.
- ^ Beghi E (2004). "Aetiology of epilepsy". In Dodson WE, Avanzini G, Shorvon SD, Fish DR, Perucca E (eds.). The Treatment of Epilepsy. Oxford: Blackwell Science. p. 61. ISBN 0-632-06046-8.
- ^ de la Peña P, Porta-Etessam J (1998). "Post-traumatic epilepsy". Revista de Neurología (in Spanish). 26 (150): 256–261. doi:10.33588/rn.26150.981066. PMID 9580443.
- ^ a b c d e f g Herman ST (2002). "Epilepsy after brain insult: Targeting epileptogenesis". Neurology. 59 (9 Suppl 5): S21–S26. doi:10.1212/wnl.59.9_suppl_5.s21. PMID 12428028. S2CID 6978609.
- ^ Mazarati A (2006). "Is Posttraumatic Epilepsy the Best Model of Posttraumatic Epilepsy?". Epilepsy Currents. 6 (6): 213–214. doi:10.1111/j.1535-7511.2006.00149.x. PMC 1783489. PMID 17260063.
- ^ a b Willmore LJ (1990). "Post-traumatic epilepsy: Cellular mechanisms and implications for treatment". Epilepsia. 31 (Supplement 3): S67–73. doi:10.1111/j.1528-1157.1990.tb05861.x. PMID 2226373. S2CID 34342615.
- ^ Morimoto K, Fahnestock M, Racine RJ (May 2004). "Kindling and status epilepticus models of epilepsy: Rewiring the brain". Prog. Neurobiol. 73 (1): 1–60. doi:10.1016/j.pneurobio.2004.03.009. PMID 15193778. S2CID 36849482.
- ^ Abel MS, McCandless DW (1992). "The kindling model of epilepsy". In Adams RN, Baker GB, Baker JM, Bateson AN, Boisvert DP, Boulton AA, et al. (eds.). Neuromethods: Animal Models of Neurological Disease. Totowa, NJ: Humana Press. pp. 153–155. ISBN 0-89603-211-6.
- ^ Menkes JH, Sarnat HB, Maria BL (2005). Child Neurology. Hagerstown, MD: Lippincott Williams & Wilkins. pp. 683–684. ISBN 0-7817-5104-7.
- ^ a b c d e Firlik KS, Spencer DD (2004). "Surgery of post-traumatic epilepsy". In Dodson WE, Avanzini G, Shorvon SD, Fish DR, Perucca E (eds.). The Treatment of Epilepsy. Oxford: Blackwell Science. pp. 775–778. ISBN 0-632-06046-8.
- ^ Barry E, Bergey GK, Krumholz A, et al. (1997). "Posttraumatic seizure types vary with the interval after head injury". Epilepsia. 38 (Supplement 8): 49S–50S. doi:10.1111/j.1528-1157.1997.tb01495.x. S2CID 221735326.
- ^ a b c Schierhout G, Roberts I (2001 (Unchanged in 2008)). Schierhout, Gillian (ed.). "Anti-epileptic drugs for preventing seizures following acute traumatic brain injury". Cochrane Database of Systematic Reviews (4): CD000173. doi:10.1002/14651858.CD000173. PMID 11687070.
{{cite journal}}:날짜 값 확인:date=(도움말) (회수됨, doi:10.1002/14651858.cd000173.pub2 참조 - ^ a b Beghi E (2003). "Overview of studies to prevent posttraumatic epilepsy". Epilepsia. 44 (Supplement 10): 21–26. doi:10.1046/j.1528-1157.44.s10.1.x. PMID 14511391. S2CID 25635858.
- ^ Aroniadou-Anderjaska V, Fritsch B, Qashu F, Braga MF (February 2008). "Pathology and Pathophysiology of the Amygdala in Epileptogenesis and Epilepsy". Epilepsy Res. 78 (2–3): 102–16. doi:10.1016/j.eplepsyres.2007.11.011. PMC 2272535. PMID 18226499.
- ^ a b Young B (1992). "Post-traumatic epilepsy". In Barrow DL (ed.). Complications and Sequelae of Head Injury. Park Ridge, Ill: American Association of Neurological Surgeons. pp. 127–132. ISBN 1-879284-00-6.
- ^ Swash M (1998). Outcomes in Neurological and Neurosurgical Disorders. Cambridge, UK: Cambridge University Press. pp. 172–173. ISBN 0-521-44327-X.
- ^ Diaz-Arrastia R, Agostini MA, Frol AB, et al. (November 2000). "Neurophysiologic and neuroradiologic features of intractable epilepsy after traumatic brain injury in adults". Archives of Neurology. 57 (11): 1611–1616. doi:10.1001/archneur.57.11.1611. PMID 11074793.
- ^ a b c d e Jensen RL, Stone JL (1997). "Benjamin Winslow Dudley and early American trephination for posttraumatic epilepsy". Neurosurgery. 41 (1): 263–268. doi:10.1097/00006123-199707000-00045. PMID 9218316.
- ^ Willmore LJ (December 2005). "Antiepileptic drugs and neuroprotection: Current status and future roles". Epilepsy & Behavior. 7 (Supplement 3): S25–S28. doi:10.1016/j.yebeh.2005.08.006. PMID 16239127. S2CID 40670766.
- ^ Chang BS, Lowenstein DH (2003). "Practice parameter: Antiepileptic drug prophylaxis in severe traumatic brain injury: Report of the Quality Standards Subcommittee of the American Academy of Neurology". Neurology. 60 (1): 10–16. doi:10.1212/01.wnl.0000031432.05543.14. PMID 12525711.
- ^ Glushakov, Alexander V.; Glushakova, Olena Y.; Doré, Sylvain; Carney, Paul R.; Hayes, Ronald L. (2016). "Animal Models of Posttraumatic Seizures and Epilepsy". Methods in Molecular Biology. 1462: 481–519. doi:10.1007/978-1-4939-3816-2_27. ISBN 978-1-4939-3814-8. ISSN 1940-6029. PMC 6036905. PMID 27604735.
- ^ Cho, Sung‐Joon; Park, Eugene; Telliyan, Tamar; Baker, Andrew; Reid, Aylin Y. (August 2020). "Zebrafish model of posttraumatic epilepsy". Epilepsia. 61 (8): 1774–1785. doi:10.1111/epi.16589. ISSN 0013-9580. PMID 32592416. S2CID 220120920.