표피
Epidermis| 표피 | |
|---|---|
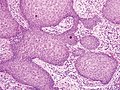
 흰색 막대로 표시된 피부 외층을 구성하는 표피의 현미경 이미지 | |
 표피의 층을 나타내는 현미경 이미지.검체 준비가 다르기 때문에 이 영상에서는 각질층이 위보다 더 콤팩트하게 나타납니다. | |
| 세부 사항 | |
| 일부 | 피부. |
| 시스템. | 피복계 |
| 식별자 | |
| 라틴어 | 표피 |
| 메쉬 | D004817 |
| TA98 | A16.0.00.009 |
| TA2 | 7046 |
| TH | H3.12.00.1.01001 |
| FMA | 70596 |
| 미세해부술의 해부학적 용어 | |
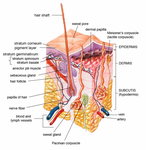
표피는 피부를 구성하는 세 층 중 가장 바깥쪽에 있으며, 안쪽 층은 진피와 [1]피하층이다.표피층은 환경[2] 병원균에 의한 감염을 차단하고 경피 수분 [3]손실을 통해 체내에서 대기 중으로 방출되는 물의 양을 조절한다.
표피는 수직으로 배열된 주상 세포로 구성된 기본층(지층 기저부)을 덮는 여러 층의 평평한[4] 세포로 구성되어 있습니다.세포층은 기초층의 줄기세포로부터 발달한다.인간의 표피는 상피, 특히 층상 편평상피의 친숙한 예이다.
표피라는 단어는 고대 그리스 표피에서 라틴어로 유래했으며, 그 자체는 고대 그리스 에피 'over, upon'과 고대 그리스 진피 'skin'에서 유래했다.표피와 관련된 것 또는 표피의 일부를 표피라고 한다.
구조.
셀룰러 컴포넌트
표피는 주로 세포의 90%를 구성하는 각질세포[4](증식성 기저세포 및 분화상피세포)로 구성되지만 멜라노사이트, 랑게르한스세포, 메르켈세포 [5]: 2–3 및 염증세포도 포함한다.Rete 융기라고 불리는 표피 비후는 피부 유두 [6]사이를 아래로 뻗는다.혈관은 표피 아래에 있으며 동맥과 정맥에 연결되어 있습니다.표피 자체에는 혈액 공급이 없고 주변 [7]공기로부터 확산된 산소에 의해 거의 독점적으로 영양이 공급된다.표피의 모든 [8]층에서 수분과 나트륨 수준(ENAC)을 조절하는 세포 메커니즘이 발견됩니다.
세포 접합부
표피 세포는 외부 환경에 대한 엄격한 장벽 역할을 하기 위해 서로 단단히 연결되어 있습니다.표피 세포 사이의 접합은 카드헤린이라고 불리는 막 통과 단백질에 의해 형성되는 아데렌스 접합 타입입니다.세포 안에서, 카드헤린은 액틴 필라멘트와 연결되어 있다.면역 형광 현미경법에서 액틴 필라멘트 네트워크는 [8]세포막을 둘러싸고 있는 두꺼운 경계로 나타나지만, 액틴 필라멘트는 실제로 세포 내부에 위치하고 세포막과 평행하게 움직인다.인접한 세포의 근접성과 접합부의 밀도로 인해 액틴 면역 형광은 [8]세포 사이의 경계로 나타난다.
레이어
표피는 [9]고려되는 피부 부위에 따라 4층 또는 5층으로 구성되어 있습니다.이러한 계층은 내림차순으로 다음과 같습니다.[2]
- 각질층(각질층)
- 10~30층의 다면체, 무핵 각막(각질세포 분화의 마지막 단계)으로 구성되어 있으며, 손바닥과 발바닥이 가장 많은 층을 가지고 있다.각막세포는 플라즈마막 아래에 단백질 외피(각질 외피단백질)를 포함하고, 수용성 케라틴 단백질로 채워져 각막모솜을 통해 결합되고,[10] 쌓인 지질층에 의해 세포외 공간에 둘러싸여 있다.표피의 대부분의 장벽 기능은 이 [11]층에 국한된다.
- 투명/반투명층(반투명층, 손바닥과 발바닥에만 해당)
- 이 좁은 층은 손바닥과 발바닥에만 있습니다.이 두 부위의 표피는 "두꺼운 피부"로 알려져 있는데, 왜냐하면 이 여분의 층으로 피부는 4개 대신 5개의 표피 층을 가지고 있기 때문입니다.
- 과립층(과립층)
- 각질세포는 핵을 잃고 세포질이 과립으로 보인다.층상체 내의 각질세포에 포함된 지질은 세포외공간에 세포외를 통해 방출되어 체내 수분손실 및 이물질 유입을 방지하는 지질장벽을 형성한다.그 극지방은 무극지질로 변환되어 세포표면과 평행하게 배열된다.예를 들어 글리코스핑고지질은 세라마이드가 되고 인지질은 유리지방산이 [10]된다.
- 가느다란 층(가느다란 층)
- 각질세포는 데스모솜을 통해 연결되고 골지 내에서 극지방, 글리코스핑고리피드, 유리스테롤, 인지질 및 이화효소로 [3]풍부한 층상체를 생성한다.면역학적으로 활성 세포인 랑게르한스 세포는 이 [10]층의 중앙에 위치합니다.
- 기저층/배엽층(배엽층/배엽층)
- 주로 증식 및 비증식 각질세포로 구성되며, 반쪽모솜에 의해 기저막에 부착된다.멜라노사이트가 존재하며, 수상돌기를 통해 이것과 다른 지층의 수많은 각질세포와 연결된다.메르켈 세포는 또한 손가락 끝과 입술과 같은 접촉에 민감한 부위에 많은 수가 있는 지층 기저부에서 발견됩니다.그것들은 피부 신경과 밀접하게 관련되어 있으며 가벼운 [10]촉각과 관련이 있는 것으로 보인다.
- 말피기층(말피기층)
- 이것은 기저층과 스피노섬 [4]지층이다.
표피와 진피, 그 밑부분의 조직은 지하의 막에 의해 분리된다.
세포역동학
세포분열
층상편평상피로서 표피는 층저부 내의 세포분열에 의해 유지된다.분화세포는 기저막에서 탈아미네이트되어 표피층을 통해 바깥쪽으로 이동하며, 여러 단계의 분화를 거쳐 각질층에서 핵을 잃고 편평상피 시트로 융합되어 표면에서 최종적으로 탈락한다(탈락).분화된 각질세포는 피부 장벽 기능의 필수적인 부분인 세포외 기질 형성에 기여하는 케라틴 단백질을 분비한다.정상적인 피부에서, 각질세포의 생성 속도는 [4]손실 속도와 같으며, 세포가 층 바닥에서 과립층 꼭대기까지 이동하는 데 약 2주가 걸리고,[2] 각질층을 가로지르는 데 추가로 4주가 걸린다.전체 표피는 약 48일 [12]동안 새로운 세포 증식으로 대체된다.
칼슘 농도
표피 전체의 각질세포 분화는 부분적으로 칼슘 구배에 의해 매개되며, 칼슘 구배에서 증가하여 최대치에 도달하는 외층 과립층까지 증가하여 각질층에서 감소한다.각질층의 칼슘 농도가 매우 낮은 것은 부분적으로 상대적으로 건조한 세포들이 이온을 녹일 수 없기 때문이다.이 칼슘 구배는 각질세포 분화와 평행하며 표피층 [3]형성의 핵심 조절제로 간주됩니다.
세포외 칼슘 농도의 상승은 세포내 유리 칼슘 [13]농도의 증가를 유도한다.세포 내 증가의 일부는 세포[14] 내 저장소에서 방출되는 칼슘에서 나오고, 다른 일부는 칼슘에 민감한 염화물[16] 채널과 [17]칼슘에 투과되는 전압의존성 양이온 채널을 통해 막 통과 칼슘 [15]유입에서 나온다.또한 세포외 칼슘 감지 수용체(CaSR)도 세포내 칼슘 [18]농도 상승에 기여하는 것으로 나타났다.
발전
표피의 형성인 표피의 형성은 중추신경계의 형성인 신경조절 후에 배아를 덮고 있는 세포에서 시작된다.대부분의 척추동물에서 이 원래의 1층 구조는 2층 조직으로 빠르게 변화한다; 내부 기저층 또는 생식층이 [19]형성되면 배치되는 임시 외부층인 주변엽.
이 내층은 모든 표피세포를 발생시키는 배아의 상피이다.그것은 분열하여 바깥쪽 가느다란 층을 형성한다.마르셀로 말피기(Marcello Malpighi)의 이름을 따서 말피기 층이라고 불리는 [19]이 두 층의 세포는 표피의 표피 입상 층(Stratum granulosum).
과립층에 있는 세포들은 분열하지 않고, 대신 각질 과립에서 각질세포라고 불리는 피부 세포를 형성합니다.이 피부 세포들은 마침내 가장 바깥쪽 표피층인 옥수수 층이 되고, 그곳에서 세포핵이 세포의 한 끝에 위치한 평평한 주머니가 된다.태어난 후 이 가장 바깥의 세포들은 과립층의 새로운 세포들로 대체되고 그들은 매 시간마다 0.001 - 0.003 온스의 피부 박리 또는 [20]매일 0.024 - 0.072 온스의 속도로 없어집니다.
표피 발육은 다음과 같은 여러 성장 인자의 산물이다.[19]
- 변환성장인자 알파(TGFα)는 기초세포가 자신의 분열을 자극하는 자가분비성장인자다.
- 케라티노사이트 성장인자(KGF 또는 FGF7)는 기초세포의 증식을 조절하는 기초 피부섬유아세포에 의해 생성되는 파라크린 성장인자이다.
기능.
장벽
표피는 미생물 병원균, 산화제 스트레스(UV광) 및 화합물로부터 신체를 보호하는 장벽 역할을 하며 경미한 부상에도 기계적 저항을 제공합니다.이 장벽의 역할은 대부분 [11]각질층에 의해 이루어진다.
- 특성.
- 물리적 장벽: 표피 각질세포는 세포골격 단백질과 관련된 세포-세포 접합에 의해 단단하게 연결되어 표피의 기계적 [3]강도를 부여한다.
- 화학적 장벽:고도로 조직화된 지질, 산, 가수 분해 효소 및 항균 펩타이드는[3] 외부 화학 물질과 병원체의 체내 전달을 억제합니다.
- 면역학적으로 활성 장벽:표피에서 발견되는 면역계의[3] 체액과 세포 구성 요소는 적극적으로 감염과 싸운다.
- 각질층의 수분 함량이 지표면을 향해 떨어져 병원성 미생물의 성장에 [11]적대적인 조건을 형성한다.
- 산성 pH(약 5.0)와 낮은 양의 물은 표피를 많은 미생물 [11]병원체에 적대적으로 만듭니다.
- 표피 표면에 있는 비병원성 미생물은 음식을 얻기 위해 경쟁하고, 그것의 가용성을 제한하며, 병원성 [11]미생물들의 성장을 억제하는 화학 분비를 만들어냄으로써 병원체로부터 병원체를 방어하는데 도움을 준다.
- 투과성
- 글루코콜티코이드의 증가를 통한 심리적 스트레스는 각질층을 손상시켜 장벽 [21]기능을 약화시킨다.
- 갑작스럽고 큰 습도의 변화는 병원성 미생물의 [22]침입을 허용하는 방식으로 각질 수화층을 변화시킨다.
피부 수분 공급
피부의 수분 보유 능력은 주로 각질층에 기인하며 건강한 [23]피부를 유지하는 데 매우 중요합니다.각막측정법을 [24]사용하여 피부 수화량을 정량한다.각질층의 세포 사이에 구배를 통해 조직적으로 배치된 지질은 경피 수분 손실을 [25][26]막는 장벽을 형성한다.
피부색
표피 속 멜라닌 색소의 양과 분포는 호모 사피엔스의 피부색 변화의 주요 원인이다.멜라닌은 멜라노사이트에서 형성되는 입자인 작은 멜라노솜에서 발견되며, 멜라닌은 주변 각질세포로 전달된다.멜라노솜의 크기, 수, 배열은 인종 집단마다 다르지만 멜라노사이트의 수는 신체 부위마다 다를 수 있지만, 모든 인간의 개별 신체 부위에서는 동일하다.흰색과 아시아계 피부에서는 멜라노솜이 "응집체"로 채워져 있지만, 검은색 피부에서는 더 크고 균등하게 분포되어 있습니다.각질세포의 멜라노솜 수는 자외선 피폭에 따라 증가하지만, 이들의 분포는 대체로 영향을 [27]받지 않는다.
임상적 의의
표피의 특성을 대부분 재현하는 3D 구조(인공 피부)를 형성하기 위한 각질세포의 실험실 배양은 약물 개발 및 테스트를 위한 도구로 일상적으로 사용된다.
과형성
표피과형성증(세포 증식으로 인해 두꺼워짐)은 다음과 같은 다양한 형태를 가집니다.
- 진드기는 확산성 표피과형성증(피부가 두꺼워지고 진드기와 [28]혼동되지 않음)이다.이는 말피기 층의 두께가 증가했음을 의미한다(층 기저층과 스피노섬 [29]층).아칸소시스 니그리칸스는 검은색, 제대로 정의되지 않은 벨벳성 초색소화 아칸소시스이며, 보통 목 뒷부분, 겨드랑이, 그리고 다른 접힌 피부 부위에서 관찰된다.
- 국소상피과형성증(Heck's disease)은 무증상 양성 종양 질환으로 [30][5]: 411 구강에서 확산적으로 발생하는 흰색에서 분홍색을 띠는 여러 개의 구진이 특징이다.
- Peudo epitheliomatous hyperplasia(PEH)는 피부 [31]부속물의 표피와 상피의 과형성이 특징이며, 불규칙한 편평상피 가닥이 [32]진피까지 뻗어 편평상피세포암(SCC)[31]을 밀접하게 시뮬레이션하는 양성 질환이다.
계약상 과각화증은 각질층의 비후화이며 반드시 과형성에 의한 것은 아니다.
기타 이미지
「 」를 참조해 주세요.
레퍼런스
- ^ Young, Barbara (2014). Wheater's functional histology a text and colour atlas. Elsevier. pp. 160 & 175. ISBN 9780702047473.
- ^ a b c Marks, James G; Miller, Jeffery (2006). Lookingbill and Marks' Principles of Dermatology (4th ed.). Elsevier. pp. 1–7. ISBN 978-1-4160-3185-7.
- ^ a b c d e f Proksch, E.; Brandner, J.; Jensen, J.M. (2008). "The skin: an indispensable barrier". Experimental Dermatology. 17 (12): 1063–1072. doi:10.1111/j.1600-0625.2008.00786.x. PMID 19043850. S2CID 31353914.
- ^ a b c d McGrath, J.A.; Eady, R.A.; Pope, F.M. (2004). Rook's Textbook of Dermatology (7th ed.). Blackwell Publishing. pp. 3.1–3.6. ISBN 978-0-632-06429-8.
- ^ a b James, William D.; Berger, Timothy G.; et al. (2006). Andrews' Diseases of the Skin: clinical Dermatology. Saunders Elsevier. ISBN 0-7216-2921-0.
- ^ The FreeDictionary > rete ridge 인용:미국유산 의학사전 저작권 2007, 2004
- ^ Stücker, M; Struk, A; Altmeyer, P; Herde, M; Baumgärtl, H; Lübbers, DW (2002). "The cutaneous uptake of atmospheric oxygen contributes significantly to the oxygen supply of human dermis and epidermis". The Journal of Physiology. 538 (3): 985–994. doi:10.1113/jphysiol.2001.013067. PMC 2290093. PMID 11826181.
- ^ a b c Hanukoglu I, Boggula VR, Vaknine H, Sharma S, Kleyman T, Hanukoglu A (January 2017). "Expression of epithelial sodium channel (ENaC) and CFTR in the human epidermis and epidermal appendages". Histochemistry and Cell Biology. 147 (6): 733–748. doi:10.1007/s00418-016-1535-3. PMID 28130590. S2CID 8504408.
- ^ 피부 노화 - 구조
- ^ a b c d "Skin structure and function" (PDF). Archived from the original (PDF) on 2010-12-14. Retrieved 2015-01-07.
- ^ a b c d e Elias, P.M. (2007). "The skin barrier as an innate immune element". Seminars in Immunopathology. 29 (1): 3–14. doi:10.1007/s00281-007-0060-9. PMID 17621950. S2CID 20311780.
- ^ Iizuka, Hajime (1994). "Epidermal turnover time". Journal of Dermatological Science. 8 (3): 215–217. doi:10.1016/0923-1811(94)90057-4. PMID 7865480.
- ^ Hennings, H; Kruszewski, FH; Yuspa, SH; Tucker, RW (1989). "Intracellular calcium alterations in response to increased external calcium in normal and neoplastic keratinocytes". Carcinogenesis. 10 (4): 777–80. doi:10.1093/carcin/10.4.777. PMID 2702726.
- ^ Pillai, S; Bikle, DD (1991). "Role of intracellular-free calcium in the cornified envelope formation of keratinocytes: Differences in the mode of action of extracellular calcium and 1,25 dihydroxyvitamin D3". Journal of Cellular Physiology. 146 (1): 94–100. doi:10.1002/jcp.1041460113. PMID 1990023. S2CID 21264605.
- ^ Reiss, M; Lipsey, LR; Zhou, ZL (1991). "Extracellular calcium-dependent regulation of transmembrane calcium fluxes in murine keratinocytes". Journal of Cellular Physiology. 147 (2): 281–91. doi:10.1002/jcp.1041470213. PMID 1645742. S2CID 25858560.
- ^ Mauro, TM; Pappone, PA; Isseroff, RR (1990). "Extracellular calcium affects the membrane currents of cultured human keratinocytes". Journal of Cellular Physiology. 143 (1): 13–20. doi:10.1002/jcp.1041430103. PMID 1690740. S2CID 8072916.
- ^ Mauro, TM; Isseroff, RR; Lasarow, R; Pappone, PA (1993). "Ion channels are linked to differentiation in keratinocytes". The Journal of Membrane Biology. 132 (3): 201–9. doi:10.1007/BF00235738. PMID 7684087. S2CID 13063458.
- ^ Tu, CL; Oda, Y; Bikle, DD (1999). "Effects of a calcium receptor activator on the cellular response to calcium in human keratinocytes". The Journal of Investigative Dermatology. 113 (3): 340–5. doi:10.1046/j.1523-1747.1999.00698.x. PMID 10469331.
- ^ a b c Gilbert, Scott F (2000). "The Epidermis and the Origin of Cutaneous Structures". Developmental Biology. Sinauer Associates. ISBN 978-0-87893-243-6.
- ^ Weschler, Charles J. (April 8, 2011). "Squalene and Cholesterol in Dust from Danish Homes and Daycare Centers" (PDF). Environ. Sci. Technol. 45 (9): 3872–3879. Bibcode:2011EnST...45.3872W. doi:10.1021/es103894r. PMID 21476540.
- ^ Denda, M.; Tsuchiya, T.; Elias, P.M.; Feingold, K.R. (2000). "Stress alters cutaneous permeability barrier homeostasis". Am J Physiol Regul Integr Comp Physiol. 278 (2): R367–372. doi:10.1152/ajpregu.2000.278.2.R367. PMID 10666137. S2CID 558526.
- ^ Tsai, Jui-Chen; Guy, Richard H.; Thornfeldt, Carl R.; Gao, Wen Ni; Feingold, Kenneth R.; Elias, Peter M. (1996). "Metabolic Approaches To Enhance Transdermal Drug Delivery. 1. Effect of Lipid Synthesis Inhibitors". Journal of Pharmaceutical Sciences. 85 (6): 643–648. doi:10.1021/js950219p. PMID 8773963.
- ^ Blank, IH (1952). "Factors which influence the water content of the stratum corneum". The Journal of Investigative Dermatology. 18 (6): 433–40. doi:10.1038/jid.1952.52. PMID 14938659.
- ^ C. W. Blichmann, J. Serup: 피부 수분 평가, Acta Derm.Venerol. (Stockli) 1988; 68: 284–290
- ^ Downing, DT; Stewart, ME; Wertz, PW; Colton, SW; Abraham, W; Strauss, JS (1987). "Skin lipids: An update". The Journal of Investigative Dermatology. 88 (3 Suppl): 2s–6s. doi:10.1111/1523-1747.ep12468850. PMID 2950180.
- ^ Bonté, F; Saunois, A; Pinguet, P; Meybeck, A (1997). "Existence of a lipid gradient in the upper stratum corneum and its possible biological significance". Archives of Dermatological Research. 289 (2): 78–82. doi:10.1007/s004030050158. PMID 9049040. S2CID 10787600.
- ^ Montagna, William; Prota, Giuseppe; Kenney, John A. (1993). Black skin: structure and function. Gulf Professional Publishing. p. 69. ISBN 978-0-12-505260-3.
- ^ Kumar, Vinay, Fausto, Nelso; Abbas, Abul(2004) Robins & Cotran Pathological Basis of Disease(7호).손더스.페이지 1230.ISBN 0-7216-0187-1.
- ^ M. S. Stone; T. L. Ray (September 1995). "Acanthosis". DermPathTutor. Department of Dermatology, University of Iowa. Archived from the original on 29 May 2012. Retrieved 17 May 2012.
- ^ Tenore, G.; Palaia, G.; Del Vecchio, A.; Galanakis, A.; Romeo, U. (2013-10-24). "Focal epithelial hyperplasia (Heck's disease)". Annali di Stomatologia. 4 (Suppl 2): 43. ISSN 1824-0852. PMC 3860189. PMID 24353818.
- ^ a b Chakrabarti, Suvadip; Chakrabarti, PreetiRihal; Agrawal, Deepak; Somanath, Shreyas (2014). "Pseudoepitheliomatous hyperplasia: A clinical entity mistaken for squamous cell carcinoma". Journal of Cutaneous and Aesthetic Surgery. 7 (4): 232–4. doi:10.4103/0974-2077.150787. ISSN 0974-2077. PMC 4338470. PMID 25722605.
- ^ Lynch, Jane M. (2004). "Understanding Pseudoepitheliomatous Hyperplasia". Pathology Case Reviews. 9 (2): 36–45. doi:10.1097/01.pcr.0000117275.18471.5f. ISSN 1082-9784. S2CID 71497554.