지방산
Fatty acid| 식품의 지방 종류 |
|---|
| 「 」를 참조해 주세요. |
화학, 특히 생화학에서 지방산은 포화 또는 불포화 지방족 사슬을 가진 카르본산이다.대부분의 자연적으로 발생하는 지방산은 4에서 [1]28까지의 짝수 탄소 원자의 가지 없는 사슬을 가지고 있습니다.지방산은 미세 조류와[2] 같은 일부 종에서 지질(최대 70 중량%)의 주요 성분이지만, 일부 다른 유기체에서는 독립적인 형태로 발견되지 않고, 대신 세 가지 종류의 에스테르로 존재한다: 트리글리세리드, 인지질, 그리고 콜레스테릴 에스테르.어떤 형태로든, 지방산은 동물들에게 중요한 연료 공급원이자 세포의 중요한 구조적 구성요소이다.
역사
지방산의 개념은 1813년 미셸 외젠 셰브룰에 [3][4][5]의해 도입되었지만, 그는 처음에 그라이스 아시드와 아시드 휴뢰 ("산성 지방"과 "올리산")[6]라는 다른 용어를 사용했다.
지방산의 종류
지방산은 길이에 따라, 포화 대 비포화, 짝수 대 홀수 탄소 함량에 의해, 그리고 선형 대 분지에 의해 여러 가지 방법으로 분류된다.
지방산의 길이
- 짧은 사슬 지방산(SCFA)은 지방족 꼬리가 5개 이하인 지방산(예: 낙산)[7]이다.
- 중간 사슬 지방산(MCFA)은 지방족 꼬리가 6~12개인[8] 지방산으로, 중간 사슬 트리글리세리드를 형성할 수 있습니다.
- 긴 사슬 지방산(LCFA)은 지방족 꼬리가 13~[9]21개 탄소인 지방산이다.
- 매우 긴 사슬 지방산(VLCFA)은 지방족 꼬리가 22개 이상인 지방산이다.
포화 지방산
포화지방산은 C=C 이중결합이 없다.이들은 같은 공식 CH3(CH2)nCOOH를 가지며, "n"의 변형도 있다.중요한 포화 지방산은 스테아린산(n = 16)으로, 양잿물로 중화되었을 때 가장 일반적인 비누 형태이다.
| 통칭 | 화학 구조 | C:D[10] |
|---|---|---|
| 카프릴산 | CH32(6COOH | 8:0 |
| 염소산 | CH32(8COOH | 10:0 |
| 라우르산 | CH32(10COOH | 12:0 |
| 미리스트산 | CH32(12COOH | 14:0 |
| 팔미트산 | CH32(14COOH | 16:0 |
| 스테아린산 | CH32(16COOH | 18:0 |
| 아라키드산 | CH32(18COOH | 20:0 |
| 베헨산 | CH32(20COOH | 22:0 |
| 리그노세르산 | CH32(22COOH | 24:0 |
| 세로토산 | CH32(24COOH | 26:0 |
불포화 지방산
불포화지방산은 1개 이상의 C=C 이중결합을 가진다.C=C 이중 결합은 시스 또는 트랜스 이성질체를 제공할 수 있습니다.
- 시스
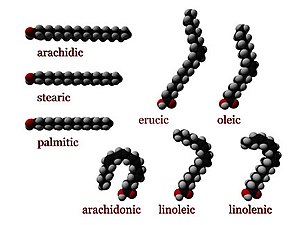
- cis 구성은 이중 결합에 인접한 두 수소 원자가 사슬의 같은 쪽에 돌출되어 있는 것을 의미한다.이중 결합의 강성은 그 배열을 동결시키고, 시스 이성질체의 경우 체인을 구부려 지방산의 배향 자유도를 제한한다.cis 구성에서 체인의 이중 결합이 많을수록 유연성이 떨어집니다.체인에 많은 cis 결합이 있을 경우, 가장 접근하기 쉬운 형태로 상당히 구부러집니다.예를 들어, 하나의 이중 결합을 가진 올레산은 그 안에 "꼬임"을 가지고 있는 반면, 두 개의 이중 결합을 가진 리놀산은 더 뚜렷한 굴곡을 가지고 있다.α-리놀렌산은 3개의 이중 결합을 가지며 갈고리 모양을 선호한다.그 효과는 지방산이 지질 이중층의 인지질이나 지질 방울의 트리글리세라이드의 일부인 경우와 같이 제한된 환경에서 시스 결합은 지방산의 밀착 포장 능력을 제한하므로 막이나 지방의 용해 온도에 영향을 미칠 수 있다.그러나 시스 불포화 지방산은 세포막 유동성을 증가시키는 반면 트랜스 불포화 지방산은 그렇지 않다.
- 트랜스
- 반면 트랜스 구성은 인접한 두 수소 원자가 사슬의 반대편에 있다는 것을 의미합니다.그 결과 사슬이 잘 구부러지지 않고 직선 포화지방산과 모양이 비슷하다.
대부분의 자연발생 불포화지방산에서 각각의 이중결합은 그 뒤에 3개의 (n-3), 6개의 (n-6) 또는 9개의 (n-9)개의 탄소원자를 가지며, 모든 이중결합은 시스구성을 가진다.트랜스 지방(트랜스 지방)의 대부분의 지방산은 자연에서 발견되지 않으며, 인간의 처리(예: 수소화)의 결과물이다.일부 트랜스 지방산은 또한 반추동물의 우유와 고기에서 자연적으로 발생합니다.그것들은 발효에 의해 이 동물들의 반추에서 생산된다.그것들은 반추동물의 우유에서 나온 유제품에서도 발견되며, 식단에서 그것들을 얻은 여성의 모유에서도 발견될 수 있다.
포화 지방산과 불포화 지방산 사이의 기하학적 차이는 생물학적 과정과 생물학적 구조(세포막 등)의 건설에 중요한 역할을 한다.
| 통칭 | 화학 구조 | Δx[11] | C:D[10] | IUPAC[12] | n−x[13] |
|---|---|---|---|---|---|
| 미리스톨레산 | CH3(CH2)3CH=CH(CH2)7COOH | 시스9 | 14:1 | 14:1(9) | n−5 |
| 팔미톨레산 | CH3(CH2)5CH=CH(CH2)7COOH | 시스9 | 16:1 | 16:1(9) | n−7 |
| 사피엔산 | CH3(CH2)8CH=CH(CH2)4COOH | 시스6 | 16:1 | 16:1(6) | n−10 |
| 올레인산 | CH3(CH2)7CH=CH(CH2)7COOH | 시스9 | 18:1 | 18:1(9) | n−9 |
| 엘라이드산 | CH3(CH2)7CH=CH(CH2)7COOH | 트랜스-IR9 | 18:1 | 18:1(9t) | n−9 |
| 박센산 | CH3(CH2)5CH=CH(CH2)9COOH | 트랜스-IR11 | 18:1 | 18:1 (11t) | n−7 |
| 리놀산 | CH3(CH2)4CH=CH2(CH2)7COOH | cis, cis-δ9, δ12 | 18:2 | 18:2(9,12) | n−6 |
| 리노엘라이드산 | CH3(CH2)4CH=CH2(CH2)7COOH | 트랜스, 트랜스9, δ12 | 18:2 | 18:2(9t,12t) | n−6 |
| α-리놀렌산 | CHCH32=CHCH2=CHCH2=CH(CH2)7COOH | cis, cis, cis-δ9, δ1215, δ | 18:3 | 18:3(9,12,15) | n−3 |
| 아라키돈산 | CH3(CH2)4CH2=CHCH2=CHCH=CH2(CH2)3COOHNIST | cis, cis, cis, cis-δ58, δ1114, δ | 20:4 | 20:4(5,8,11,14) | n−6 |
| 에이코사펜타엔산 | CHCH32=CHCH2=CHCH22=CHCH=CH2(CH2)3COOH | 시스, 시스, 시스, 시스, 시스-5,, ,, δ81114, δ, cis17 | 20:5 | 20:5(5,8,11,14,17) | n−3 |
| 에루크산 | CH3(CH2)7CH=CH(CH2)11COOH | 시스13 | 22:1 | 22:1(13) | n−9 |
| 도코사헥사엔산 | CHCH33=CHCH2=CHCH22=CHCH2=CHCH2=2CH(CH2)COOH | cis, cis, cis, cis, cis, cis-4,, ,, ,, δ71013, cis1619 | 22:6 | 22:6(4,7,10,13,16,19) | n−3 |
짝수 대 홀수 사슬 지방산
대부분의 지방산은 예를 들어 스테아린(C18)과 올레산(C18)과 같이 짝수 탄소 원자로 구성되어 있습니다.일부 지방산은 탄소 원자의 수가 홀수이다; 그것들은 홀수 사슬 지방산이라고 불린다.가장 일반적인 OCFA는 유제품에서 [14][15]발견되는 포화 C15 및 C17 유도체, 펜타데카노산 및 헵타데카노산이다.분자 수준에서 OCFA는 균일한 사슬의 친척과는 약간 다르게 생합성 및 대사된다.
명명법
탄소 원자 번호부여
대부분의 자연적으로 발생하는 지방산은 탄소 원자의 가지 없는 사슬을 가지고 있으며, 한쪽 끝에는 카르복실기(–COOH)가 있고 다른 한쪽 끝에는 메틸기(–CH3)가 있다.
지방산의 등뼈에서 각 탄소 원자의 위치는 보통 -COOH 끝에서 1부터 세어 표시된다.탄소 번호 x는 종종 C-x(또는 때때로 Cx)로 약칭되며 x = 1, 2, 3 등입니다.이것은 IUPAC가 권장하는 번호부여 방식입니다.
또 다른 관습은 카르복실기 뒤의 첫 번째 탄소부터 순서대로 그리스 알파벳 문자를 사용한다.따라서 탄소α(α)는 C-2, 탄소β(β)는 C-3이다.
지방산의 길이는 다양할 수 있지만, 이 두 번째 규칙에서는 사슬의 마지막 탄소는 항상 그리스 알파벳의 마지막 문자인 β(오메가)로 표시된다.세 번째 번호부여 규약은 " third", "--1", "--2"라는 라벨을 사용하여 그 끝에서 탄소를 계수한다.또는 라벨 "θ-x"는 "n-x"로 표기되며, 여기서 "n"은 [16]사슬 내의 탄소수를 나타낸다.
어느 쪽이든 카르복실기에 [16]가장 가까운 탄소의 라벨을 부여함으로써 지방산 사슬에서의 이중결합의 위치를 항상 특정한다.따라서 18개의 탄소지방산에서 C-12(또는 δ-6)와 C-13(또는 δ-5) 사이의 이중결합은 C-12 또는 δ-6 위치에 있다고 한다."옥타데크-12-에노산"(또는 보다 발음하기 쉬운 변형 "12-옥타데카노산")과 같은 산의 IUPAC 명명법은 항상 "C" 번호에 기초한다.
δx,y,... 표기법은 전통적으로 x,y,... 위치에 이중 결합을 가진 지방산을 지정하는데 사용된다. (그리스 대문자 "δ"(델타)는 이중 결합의 경우 로마자 "D"에 해당한다.)따라서 예를 들어 20-탄소 아라키돈산은 δ로5,8,11,14 탄소5와 6, 8과 9, 11과 12, 14와 15 사이에 이중결합을 가진다.
인간의 식생활 및 지방대사의 맥락에서 불포화지방산은 필수지방산과 같은 다중 이중결합의 경우에도 종종 γ탄소에 가장 가까운 이중결합의 위치에 따라 분류된다(단, 불포화지방산은 필수지방산과 같은 다중 이중결합의 경우에도 마찬가지이다.따라서 리놀레산(18탄소, δ9,12), 리놀렌산(18-탄소, δ6,9,12) 및 아라키돈산(20-탄소, δ5,8,11,14)은 모두 "γ-6" 지방산으로 분류되며, 공식은 -CH=CH-CH-CH-CH-CH-CH-CH-CH-CH로
2
2
2
2
3 끝난다.
탄소 원자가 홀수인 지방산은 홀수 사슬 지방산이고 나머지는 짝수 사슬 지방산이다.그 차이는 포도당신생성과 관련이 있다.
지방산 명명
다음 표는 지방산을 명명하는 가장 일반적인 시스템을 설명합니다.
| 명명법 | 예 | 설명. |
|---|---|---|
| 사소하다 | 팔미톨레산 | 일반 이름(또는 일반 이름)은 문헌에서 가장 자주 사용되는 이름 체계적이지 않은 과거 이름입니다.대부분의 일반적인 지방산은 체계적 이름 외에도 사소한 이름을 가지고 있다.이러한 이름은 어떤 패턴도 따르지 않는 경우가 많지만 간결하고 모호하지 않은 경우가 많습니다. |
| 체계적 | 시스-9-옥타데크-9-에노산 (9Z)-옥데크-9-에노산 | 계통명(또는 IUPAC명)은 [17]1979년에 발표된 표준 IUPAC 규칙과 1977년에 [18]지질에 대해 특별히 발표된 권고에서 파생되었다.탄소 원자 번호는 분자 골격의 카르복실기 끝에서 시작한다.이중 결합은 적절한 경우 cis/trans- 표기법 또는 E-/Z- 표기법으로 라벨링된다.이 표기법은 일반적으로 일반적인 명명법보다 더 상세하지만 기술적으로 더 명확하고 설명적이라는 장점이 있습니다. |
| Δx | cis-δ9, cis-δ12 옥타데카디엔산 | δx(또는 델타-x) 명명법에서, 각 이중 결합은 δ로x 표시되며, 여기서 이중 결합은 분자 골격의 카르본 말단에서 계산되어 x번째 탄소-탄소 결합에서 시작된다.각 이중 결합은 결합 주위의 분자의 구성을 나타내는 cis- 또는 trans-prefix 뒤에 온다.예를 들어 리놀산은 cis-δ9, cis-δ12 옥타데카디엔산이라고 한다.이 명명법은 체계적 명명법보다 장황하지 않다는 장점이 있지만 기술적으로 명확하거나 [citation needed]설명적이지 않습니다. |
| n−x (또는 µ-x) | n−3 (또는 --3) | n-x(n - x; 또한 γ-x 또는 오메가-x) 명명법은 모두 개별 화합물에 대한 이름을 제공하고 동물에서 가능한 생합성 특성에 따라 이들을 분류한다.이중th 결합은 x 탄소-탄소 결합에 위치하며, 분자 골격의 메틸 말단에서 계산된다.예를 들어 α-리놀렌산은 n-3 또는 오메가-3 지방산으로 분류되므로 이러한 유형의 다른 화합물과 생합성 경로를 공유할 가능성이 높다.γ-x, 오메가-x 또는 "오메가" 표기법은 일반적인 영양 문헌에서 사용되지만 IUPAC는 기술 [17]문서에서 n-x 표기법을 선호하여 이를 폐지했다.가장 일반적으로 연구되는 지방산 생합성 경로는 n-3과 n-6이다. |
| 지질수 | 18:3 18:3n3 18:3, cis, cis, cis-δ9, δ1215, δ 18:3(9,12,15) | 지질 수치는 C:[10]D의 형태를 취하며, 여기서 C는 지방산 중의 탄소 원자의 수이고 D는 지방산 중의 이중 결합의 수이다.D가 하나 이상일 경우 이중 결합은 CH 단위 2, 즉 사슬을 따라 3개의 탄소 원자의 간격으로 간섭된다고 가정한다.예를 들어 α-리놀렌산은 18:3 지방산이며, 그 3개의 이중결합은 위치9 δ, δ12, δ에15 위치한다.이 표기법은 일부 다른 지방산이 동일한 C:D 번호를 가질 수 있기 때문에 모호할 수 있습니다.따라서 모호성이 존재하는 경우, 이 표기법은 일반적으로x δ 또는 n-x [17]항 중 하나와 쌍을 이룬다.예를 들어 α-리놀렌산 및 γ-리놀렌산은 모두 18:3이지만, 각각 18:3n3 및 18:3n6 지방산으로 명확하게 기술할 수 있다.같은 목적으로 IUPAC는 C:D [12]표기법에 추가된 괄호 안의 이중 결합 위치 목록을 사용할 것을 권장합니다.예를 들어 α-리놀렌산과 γ-리놀렌산에 대한 IUPAC 권장 표기법은 각각 18:3(9,12,15)과 18:3(6,9,12)이다. |
유리 지방산
에스테르가 아닌 혈장(플라즈마 지방산)에서 순환할 때, 지방산은 비에스테르화 지방산(NEFAs) 또는 유리 지방산(FFAs)으로 알려져 있습니다.FFA는 항상 알부민과 [19]같은 운반 단백질과 결합됩니다.
FFA는 또한 가수 분해에 의해 트리글리세리드 식용유와 지방으로부터 형성되어 특징적인 악취의 [20]원인이 된다.유사한 과정이 바이오디젤에서도 발생하며 부분 부식의 위험이 있습니다.
생산.
산업의
지방산은 보통 글리세롤의 제거와 함께 트리글리세라이드의 가수 분해에 의해 산업적으로 생산된다.인지질은 또 다른 공급원을 나타냅니다.일부 지방산은 알케인의 [21]하이드로카복실화에 의해 합성된다.
고산소 지방산
과산소 지방산은 국소용 스킨크림을 위한 특정 공업 공정에 의해 생산된다.이 과정은 제어된 온도에서 자외선과 기포가 발생하는 산소의 존재를 통해 지방산에스테르에 과산화물이 도입 또는 포화되는 것을 기반으로 합니다.특히 리놀렌산은 피부의 수분 장벽 기능(수분 손실 및 피부 [22]탈수 방지)을 유지하는 데 중요한 역할을 하는 것으로 나타났습니다.스페인의 한 연구는 2005년 3월 Journal of Wind Care에 보고되었으며 상업용 제품과 기름진 위약을 비교한 결과 특정 제품이 더 효과적이고 비용 [23]효과도 높다고 한다.그러한 OTC 의약품은 현재 폭넓게 구할 수 있다.그러나 2015년 [24][25]스페인에서 실시된 "무작위 트리플 블라인드 제어 비우호성" 시험에서는 국부적으로 도포된 올리브유가 열등하지 않은 것으로 나타났다.상업용 제품은 올리브 오일이나 석유 젤리보다 취급하기에 덜 지저분하고 세탁이 더 쉬우며, 국소적으로 바르면 의류와 침구가 더러워질 수 있습니다.
동물별
동물에서 지방산은 주로 [26]간, 지방 조직 및 수유 중에 유선에서 탄수화물로 형성된다.
탄수화물이 지방산으로 [26]전환되는 첫 번째 중요한 단계로서 해당과정에 의해 탄수화물이 피루브산으로 전환된다.그런 다음 피루브산은 탈탄산되어 미토콘드리아에서 아세틸-CoA를 형성한다.그러나 이 아세틸 CoA는 지방산 합성이 일어나는 세포로 운반되어야 한다.이것은 직접 발생할 수 없습니다.세포질 아세틸-CoA를 얻기 위해 구연산 회로에서 구연산(아세틸-CoA와 옥살로아세테이트의 축합에 의해 생성됨)을 제거하고 미토콘드리아 내막을 통해 세포질로 [26]운반한다.여기서 그것은 ATP 구연산분해효소에 의해 아세틸-CoA와 옥살아세트산염으로 분해된다.옥살아세트산은 말산으로 미토콘드리아로 [27]돌아간다.세포질 아세틸-CoA는 아세틸 CoA 카르복실화효소에 의해 말로닐-CoA로 카르복실화되며, 이는 지방산 [27][28]합성의 첫 번째 커밋 단계이다.
다음으로 말로닐-CoA는 성장 중인 지방산 사슬을 한 번에 두 개의 탄소만큼 연장시키는 일련의 반복 반응에 관여한다.따라서 거의 모든 천연 지방산은 짝수 탄소 원자를 가지고 있다.합성이 완료되면 유리 지방산은 거의 항상 글리세롤과 결합되어 지방산의 주요 저장 형태인 트리글리세리드를 형성하고 이에 따라 동물에서 에너지의 형태를 형성합니다.하지만, 지방산은 또한 세포의 모든 막이 구성되는 인지질 이중층을 형성하는 인지질의 중요한 구성 요소이다.[26]
동물의 순환에서 발견되는 "비결합 지방산" 또는 "유리지방산"은 저장된 트리글리세라이드의 [26][29]분해(또는 지방분해)에서 유래한다.이러한 지방산은 물에 녹지 않기 때문에 혈장 알부민에 결합되어 운반된다.혈중 "유리지방산"의 수치는 알부민 결합 부위의 가용성에 의해 제한된다.그것들은 미토콘드리아를 가진 모든 세포에 의해 혈액에서 흡수될 수 있다.지방산은 미토콘드리아에서만 분해될 수 있으며, 이어서 구연산 순환에서 CO와 물로 가는2 추가 연소를 통해 분해될 수 있다.중앙 신경계의 세포는 비록 그들이 미토콘드리아를 가지고 있지만, 혈액-뇌 장벽은 짧은 사슬 지방산과 중간 사슬 [30][31]지방산을 제외한 대부분의 유리 지방산에 [citation needed]침투하지 않기 때문에 혈액에서 자유 지방산을 섭취할 수 없다.이 세포들은 세포막과 세포소기관지의 [26]인지질을 생산하고 유지하기 위해 위에서 설명한 것과 같이 탄수화물로부터 그들 자신의 지방산을 생산해야 한다.
동물 종간의 변화
포유류와 파충류의 세포막에 대한 연구는 포유류의 세포막이 [32]파충류보다 더 높은 비율의 다불포화 지방산으로 구성되어 있다는 것을 발견했다.조류 지방산 조성에 대한 연구는 포유동물과 유사한 비율을 보였지만 주어진 신체 [33]크기에서 오메가-6에 비해 오메가-3 지방산이 1/3 정도 적다는 것을 알아냈다.이 지방산 조성물은 보다 유동적인 세포막을 만들지만 다양한 이온에 투과할 수 있는 막을 만들기도 한다.H+&Na+)를 통해 세포막을 유지하는데 비용이 더 많이 든다.이러한 유지비용은 포유류와 [32]조류의 높은 대사율과 그에 수반되는 온혈성의 주요 원인 중 하나라고 주장되어 왔다.그러나 세포막의 다포화는 만성적인 한랭 온도에 반응하여 발생할 수도 있다.점점 추워지는 어류 환경에서는 [34][35]낮은 온도에서 막 유동성(및 기능성)을 높이기 위해 단불포화 지방산과 다불포화 지방산의 세포막 함량이 높아집니다.
식이성 지방의 지방산
다음 표는 몇 가지 일반적인 [36][37]식이 지방의 지방산, 비타민 E, 콜레스테롤 구성을 보여줍니다.
| 포화 상태 | 단일불포화 | 다불포화 | 콜레스테롤 | 비타민 E | |
|---|---|---|---|---|---|
| g/100g | g/100g | g/100g | mg/100g | mg/100g | |
| 동물성 지방 | |||||
| 오리 지방[38] | 33.2 | 49.3 | 12.9 | 100 | 2.70 |
| 라드[38] | 40.8 | 43.8 | 9.6 | 93 | 0.60 |
| 타로우[38] | 49.8 | 41.8 | 4.0 | 109 | 2.70 |
| 버터 | 54.0 | 19.8 | 2.6 | 230 | 2.00 |
| 식물성 지방 | |||||
| 코코넛 오일 | 85.2 | 6.6 | 1.7 | 0 | .66 |
| 코코아 버터 | 60.0 | 32.9 | 3.0 | 0 | 1.8 |
| 팜 커널 오일 | 81.5 | 11.4 | 1.6 | 0 | 3.80 |
| 팜유 | 45.3 | 41.6 | 8.3 | 0 | 33.12 |
| 면실유 | 25.5 | 21.3 | 48.1 | 0 | 42.77 |
| 밀배아유 | 18.8 | 15.9 | 60.7 | 0 | 136.65 |
| 콩기름 | 14.5 | 23.2 | 56.5 | 0 | 16.29 |
| 올리브유 | 14.0 | 69.7 | 11.2 | 0 | 5.10 |
| 옥수수 기름 | 12.7 | 24.7 | 57.8 | 0 | 17.24 |
| 해바라기 기름 | 11.9 | 20.2 | 63.0 | 0 | 49.00 |
| 홍화유 | 10.2 | 12.6 | 72.1 | 0 | 40.68 |
| 마유 | 10 | 15 | 75 | 0 | 12.34 |
| 카놀라/라피즈 오일 | 5.3 | 64.3 | 24.8 | 0 | 22.21 |
지방산의 반응
지방산은 다른 카르본산처럼 에스테르화 및 산염기 반응을 일으킨다.
산도
지방산은 각각의 pK{sub}a}에서 알 수 있듯이 산성도에 큰 변화를 보이지 않는다.예를 들어 노난산은 pK가a 4.96으로 아세트산(4.76)보다 약간 약하다.사슬 길이가 증가함에 따라 물 속 지방산의 용해도가 감소하므로 긴 사슬 지방산은 수용액의 pH에 미치는 영향을 최소화한다.중성 pH 부근에서 지방산은 그 켤레 염기, 즉 올레산염 등에 존재한다.
에탄올 중 지방산 용액은 페놀프탈레인을 지표로 수산화나트륨 용액으로 적정할 수 있다.이 분석은 지방의 유리 지방산 함량, 즉 가수 분해된 트리글리세리드 비율을 결정하는 데 사용됩니다.
비누화(비누 제조)의 한 형태인 지방산의 중화는 금속 [39]비누에 대한 널리 알려진 방법입니다.
수소화 및 경화
불포화지방산의 수소화는 널리 행해지고 있다.일반적인 조건에는 2.0~3.0 MPa의 H2 압력, 150°C의 니켈이 촉매로 실리카에 지지됩니다.이 치료법은 포화지방산을 공급한다.수소화 정도는 요오드 수치로 나타난다.수소화 지방산은 산화가 잘 되지 않는다.포화 지방산은 불포화 전구체보다 녹는 정도가 높기 때문에 경화라고 합니다.관련 기술은 식물성 기름을 마가린으로 바꾸는 데 사용된다.트리글리세리드(vs 지방산)의 수소화는 카르본산이 니켈 촉매를 분해하여 니켈 비누를 제공하기 때문에 유리하다.부분 수소화 중에 불포화지방산은 cis에서 [40]trans 구성으로 이성화될 수 있다.
수소화를 더 강하게 하면(즉, 높은 압력의 H와2 높은 온도의 사용), 지방산을 지방 알코올로 전환합니다.그러나 지방 알코올은 지방산에스테르에서 더 쉽게 생산됩니다.
Varrentrapp 반응에서는 특정 불포화지방산이 용해된 알칼리에서 분해되며, 이 반응은 한때 구조 설명과 관련이 있었다.
자가산화 및 악취
불포화 지방산은 자동 산화라고 알려진 화학적 변화를 겪습니다.이 공정은 산소(공기)를 필요로 하며 미량 금속이 존재하면 가속됩니다.식물성 기름은 토코페롤과 같은 항산화 물질을 함유하고 있기 때문에 이 과정에 약간 저항합니다.지방과 기름은 종종 금속 촉매를 제거하기 위해 구연산과 같은 킬레이트제로 처리된다.
오존 분해
불포화 지방산은 오존에 의해 분해되기 쉽다.이 반응은 올레산으로부터 아젤라산([40]CH2)(7COH2)2을 생산하는 데 실행된다.
순환
소화 및 섭취
짧은 사슬 지방산과 중간 사슬 지방산은 다른 흡수된 영양소와 마찬가지로 장 모세혈관을 통해 혈액으로 직접 흡수되고 간문맥을 통해 이동한다.그러나 긴 사슬 지방산은 장 모세혈관으로 직접 방출되지 않는다.대신에 그것들은 장융모의 지방벽으로 흡수되고 다시 트리글리세리드화물로 재결합된다.트리글리세라이드는 콜레스테롤과 단백질로 코팅되어 카이로미크론이라고 불리는 화합물로 만들어진다.
세포 내에서, 카이로미크론은 유즙이라고 불리는 림프관 모세관으로 방출되고, 이것은 더 큰 림프관으로 합쳐집니다.그것은 림프계와 흉관을 통해 심장 근처의 위치(동맥과 정맥이 더 큰 곳)까지 운반됩니다.흉관은 쇄골하 좌측 정맥을 통해 카이로미크론을 혈류로 비웁니다.이 시점에서 카이로미크론은 트리글리세라이드를 에너지를 위해 저장되거나 대사되는 조직으로 운반할 수 있습니다.
대사
지방산은 세포내 미토콘드리아에 의해 베타산화 및 구연산 사이클에 의해 CO와 물로2 분해된다.마지막 단계(산소 인산화)에서, 산소와 반응하는 것은 많은 양의 ATP의 형태로 많은 에너지를 방출한다.많은 세포들은 이러한 목적을 위해 포도당이나 지방산을 사용할 수 있지만, 지방산은 그램 당 더 많은 에너지를 방출합니다.지방산(섭취 또는 지방조직에 저장된 트리글리세리드 흡입에 의해 공급됨)은 근육 수축 및 일반 신진대사를 위한 연료로 기능하기 위해 세포에 분배된다.
필수 지방산
건강에 필요하지만 다른 기질로부터 충분한 양을 만들 수 없고, 따라서 음식에서 얻어야 하는 지방산을 필수 지방산이라고 한다.필수 지방산에는 두 가지 시리즈가 있습니다. 하나는 메틸 말단으로부터 3개의 탄소 원자가 떨어져 있고, 다른 하나는 메틸 말단으로부터 6개의 탄소 원자가 이중 결합되어 있습니다.인간은 카르본산 [41]쪽에서 계산했을 때 9번과 10번 이상의 지방산에 이중 결합을 도입하는 능력이 부족하다.두 가지 필수 지방산은 리놀산(LA)과 알파-리놀렌산(ALA)이다.이 지방산들은 식물성 기름에 널리 분포되어 있다.인체는 ALA를 더 긴 사슬의 오메가-3 지방산인 에이코사펜타엔산(EPA)과 도코사헥사엔산(DHA)으로 변환하는 능력이 제한적이며, 이는 어류에서도 얻을 수 있다.오메가-3 및 오메가-6 지방산은 항감염, 항불안제 및 신경유전자 특성을 [42]가진 엔도카나비노이드에 대한 생합성 전구체이다.
분배
혈중 지방산은 혈액순환의 여러 단계에서 뚜렷한 형태를 취한다.그것들은 카이로미크론에서 장을 통해 섭취되지만, 간에서 처리된 후 매우 낮은 밀도 리포단백질(VLDL)과 저밀도 리포단백질(LDL)에도 존재한다.또한 지방세포에서 방출되면 지방산은 혈중 유리지방산으로 존재한다.
포유류의 피부에서 배출되는 지방산의 배합은 젖산, 피루브산과 함께 특징적이며 후각이 예민한 동물이 개체 [43]분화를 가능하게 한다고 제안되었다.
분석.
지질에 있는 지방산의 화학적 분석은 일반적으로 원래 에스테르(트리글리세리드, 왁스, 인지질 등)를 분해하여 메틸에스테르로 변환하는 관심화 단계로 시작하여 가스 크로마토그래피에 [44]의해 분리됩니다.또는 가스 크로마토그래피와 중간 스펙트럼법에 의해 분석됩니다.
은이온보완 박층 크로마토그래피로 [45][46]불포화 이성질체의 분리가 가능하다.다른 분리 기술로는 고성능 액체 크로마토그래피(수소 원자가 은 이온과 교환된 결합 페닐술폰산 그룹과 실리카 겔로 채워진 짧은 기둥 포함)가 있습니다.은의 역할은 불포화합물과 복합체를 형성하는 능력에 있다.
산업용도
지방산은 주로 비누 생산에 사용되며, 미용 목적과 금속 비누의 경우 윤활제로 사용됩니다.지방산은 또한 메틸에스테르를 통해 계면활성제, 세제 [40]및 윤활제의 전구물질인 지방 알코올과 지방 아민으로 전환됩니다.기타 용도로는 유화제, 텍스처화제, 습윤제,[47] 항포말제 또는 안정제 사용이 있습니다.
간단한 알코올을 함유한 지방산에스테르(메틸, 에틸, n-프로필, 이소프로필, 부틸에스테르 등)는 화장품 및 기타 퍼스널 케어 제품의 에몰리먼트 및 합성 윤활제로 사용된다.소르비톨, 에틸렌글리콜, 디에틸렌글리콜 및 폴리에틸렌글리콜과 같은 보다 복잡한 알코올을 가진 지방산에스테르를 식품에 소비하거나 개인관리 및 수처리에 사용하거나 금속가공을 위한 합성윤활제 또는 액체로 사용한다.
「 」를 참조해 주세요.
레퍼런스
- ^ Moss, G. P.; Smith, P. A. S.; Tavernier, D. (1997). IUPAC Compendium of Chemical Terminology. Pure and Applied Chemistry. Vol. 67 (2nd ed.). International Union of Pure and Applied Chemistry. pp. 1307–1375. doi:10.1351/pac199567081307. ISBN 978-0-521-51150-6. S2CID 95004254. Retrieved 2007-10-31.
- ^ Chen, Lin (2012). "Biodiesel production from algae oil high in free fatty acids by two-step catalytic conversion". Bioresource Technology. 111: 208–214. doi:10.1016/j.biortech.2012.02.033. PMID 22401712.
- ^ 슈브렐, M.E. (1813년)Sur Plusiurs 군단 그라, et speculierment sur Leurs combiniasons avec les alcalis.Annales de Chimie, t. 88, 페이지 225-261. 링크(갤리카), 링크(구글)
- ^ 쉐브룰, M.E. Sur Les Corpgras d'original animale.1823년 파리, 레브라우트링크를 클릭합니다.
- ^ Leray, C.지질중심의 연대기적 역사.사이버 지질 센터.최종 갱신일은 2017년 11월 11일. 링크 2017-10-13 Wayback Machine에서 보관.
- ^ Menten, P. 사전지 드 치미: un accessche attymologique et historique.드 복크, 브룩셀스링크를 클릭합니다.
- ^ Cifuentes, Alejandro, ed. (2013-03-18). "Microbial Metabolites in the Human Gut". Foodomics: Advanced Mass Spectrometry in Modern Food Science and Nutrition. John Wiley & Sons, 2013. ISBN 9781118169452.
- ^ Roth, Karl S. (2013-12-19). "Medium-Chain Acyl-CoA Dehydrogenase Deficiency". Medscape.
- ^ Beermann, C.; Jelinek, J.; Reinecker, T.; Hauenschild, A.; Boehm, G.; Klör, H.-U. (2003). "Short term effects of dietary medium-chain fatty acids and n−3 long-chain polyunsaturated fatty acids on the fat metabolism of healthy volunteers". Lipids in Health and Disease. 2: 10. doi:10.1186/1476-511X-2-10. PMC 317357. PMID 14622442.
- ^ a b c "C:D"는 지방산의 탄소 원자의 총량과 그 중 (D)ouble(불포화) 결합의 수이며, D > 1이면 이중 결합이 하나 이상의 메틸렌 브릿지에 의해 분리된 것으로 가정한다.
- ^ 지방산의 각 이중 결합은 δx로 나타내며, 이중 결합은 카르본산 끝에서 계산하여 x번째 탄소-탄소 결합에 위치한다.
- ^ a b "IUPAC Lipid nomenclature: Appendix A: names of and symbols for higher fatty acids". www.sbcs.qmul.ac.uk.
- ^ n 빼기 x(γ-x 또는 오메가-x) 명명법에서 지방산의 이중 결합은 x번째 탄소-탄소 결합에 위치하며, 말단 메틸 탄소(n 또는 γ로 지정됨)에서 카르보닐 탄소 쪽으로 계수된다.
- ^ Pfeuffer, Maria; Jaudszus, Anke (2016). "Pentadecanoic and Heptadecanoic Acids: Multifaceted Odd-Chain Fatty Acids". Advances in Nutrition. 7 (4): 730–734. doi:10.3945/an.115.011387. PMC 4942867. PMID 27422507.
- ^ Smith, S. (1994). "The Animal Fatty Acid Synthase: One Gene, One Polypeptide, Seven Enzymes". The FASEB Journal. 8 (15): 1248–1259. doi:10.1096/fasebj.8.15.8001737. PMID 8001737. S2CID 22853095.
- ^ a b c 일반적인 실수는 마지막 탄소가 "θ-1"이라고 말하는 것이다.
또 다른 흔한 실수는 오메가 표기법에서 결합의 위치가 END에 가장 가까운 탄소 수라고 말하는 것입니다.
이중 결합의 경우, 이 두 가지 실수가 서로 보상하기 때문에, "γ-3" 지방산은 메틸기를 1로 계산하면서 끝에서 3번째와 4번째 탄소 사이의 이중 결합을 가집니다.
그러나 치환 및 기타 목적으로는 그렇지 않습니다. "θ-3"에 있는 하이드록실기는 16이 아닌 탄소 15(끝에서 4번째) 위에 있습니다.이 문서의 예를 참조해 주세요.도이: 10.1016/0005-2760(75)90089-2
또한 오메가 표기의 "-"는 마이너스 기호이며, "θ-3"은 원칙적으로 "Omega - 3"으로 읽어야 한다.그러나 (특히 비과학 문헌에서는) 이것을 "θ-3" (하이픈/대시 포함)로 쓰고 "Omega-3"로 읽는 것이 매우 일반적이다.예를 들어 Karen Dully(2008), Omega-3 지방산 및 당뇨병을 참조하십시오. - ^ a b c Rigaudy, J.; Klesney, S. P. (1979). Nomenclature of Organic Chemistry. Pergamon. ISBN 978-0-08-022369-8. OCLC 5008199.
- ^ "The Nomenclature of Lipids. Recommendations, 1976". European Journal of Biochemistry. 79 (1): 11–21. 1977. doi:10.1111/j.1432-1033.1977.tb11778.x.
- ^ Dorland's Illustrated Medical Dictionary. Elsevier.
- ^ Mariod, Abdalbasit; Omer, Nuha; Al, El Mugdad; Mokhtar, Mohammed (2014-09-09). "Chemical Reactions Taken Place During deep-fat Frying and Their Products: A review". Sudan University of Science & Technology SUST Journal of Natural and Medical Sciences. Supplementary issue: 1–17.
- ^ Anneken, David J.; Both, Sabine; Christoph, Ralf; Fieg, Georg; Steinberner, Udo; Westfechtel, Alfred (2006). "Fatty Acids". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a10_245.pub2.
- ^ "Essential fatty-acids lubricate skin prevent pressure sores (see "suggested reading at end)".
- ^ "The effectiveness of a hyper-oxygenated fatty acid compound in preventing pressure ulcers".
- ^ Lupiañez-Perez, I.; Uttumchandani, S. K.; Morilla-Herrera, J. C.; Martin-Santos, F. J.; Fernandez-Gallego, M. C.; Navarro-Moya, F. J.; Lupiañez-Perez, Y.; Contreras-Fernandez, E.; Morales-Asencio, J. M. (2015). "Topical Olive Oil is Not Inferior to Hyperoxygenated Fatty Aids to Prevent Pressure Ulcers in High-Risk Immobilised Patients in Home Care. Results of a Multicentre Randomised Triple-Blind Controlled Non-Inferiority Trial". PLOS ONE. 10 (4): e0122238. Bibcode:2015PLoSO..1022238L. doi:10.1371/journal.pone.0122238. PMC 4401455. PMID 25886152.
- ^ 임상시험번호 NCT01595347 - "1차 진료에서 고정화된 환자의 압력 궤양 예방에 있어 올리브 오일 크림 효과(PrevenUP)" (ClinicalTrials.gov
- ^ a b c d e f Stryer, Lubert (1995). "Fatty acid metabolism.". Biochemistry (4th ed.). New York: W. H. Freeman and Company. pp. 603–628. ISBN 978-0-7167-2009-6.
- ^ a b Ferre, P.; Foufelle, F. (2007). "SREBP-1c Transcription Factor and Lipid Homeostasis: Clinical Perspective". Hormone Research. 68 (2): 72–82. doi:10.1159/000100426. PMID 17344645.
this process is outlined graphically in page 73
- ^ Voet, Donald; Voet, Judith G.; Pratt, Charlotte W. (2006). Fundamentals of Biochemistry (2nd ed.). John Wiley and Sons. pp. 547, 556. ISBN 978-0-471-21495-3.
- ^ Zechner, R.; Strauss, J. G.; Haemmerle, G.; Lass, A.; Zimmermann, R. (2005). "Lipolysis: pathway under construction". Curr. Opin. Lipidol. 16 (3): 333–340. doi:10.1097/01.mol.0000169354.20395.1c. PMID 15891395. S2CID 35349649.
- ^ Tsuji A (2005). "Small molecular drug transfer across the blood-brain barrier via carrier-mediated transport systems". NeuroRx. 2 (1): 54–62. doi:10.1602/neurorx.2.1.54. PMC 539320. PMID 15717057.
Uptake of valproic acid was reduced in the presence of medium-chain fatty acids such as hexanoate, octanoate, and decanoate, but not propionate or butyrate, indicating that valproic acid is taken up into the brain via a transport system for medium-chain fatty acids, not short-chain fatty acids. ... Based on these reports, valproic acid is thought to be transported bidirectionally between blood and brain across the BBB via two distinct mechanisms, monocarboxylic acid-sensitive and medium-chain fatty acid-sensitive transporters, for efflux and uptake, respectively.
- ^ Vijay N, Morris ME (2014). "Role of monocarboxylate transporters in drug delivery to the brain". Curr. Pharm. Des. 20 (10): 1487–98. doi:10.2174/13816128113199990462. PMC 4084603. PMID 23789956.
Monocarboxylate transporters (MCTs) are known to mediate the transport of short chain monocarboxylates such as lactate, pyruvate and butyrate. ... MCT1 and MCT4 have also been associated with the transport of short chain fatty acids such as acetate and formate which are then metabolized in the astrocytes [78].
- ^ a b Hulbert AJ, Else PL (August 1999). "Membranes as possible pacemakers of metabolism". Journal of Theoretical Biology. 199 (3): 257–74. Bibcode:1999JThBi.199..257H. doi:10.1006/jtbi.1999.0955. PMID 10433891.
- ^ Hulbert AJ, Faulks S, Buttemer WA, Else PL (November 2002). "Acyl composition of muscle membranes varies with body size in birds". The Journal of Experimental Biology. 205 (Pt 22): 3561–9. doi:10.1242/jeb.205.22.3561. PMID 12364409.
- ^ Hulbert AJ (July 2003). "Life, death and membrane bilayers". The Journal of Experimental Biology. 206 (Pt 14): 2303–11. doi:10.1242/jeb.00399. PMID 12796449.
- ^ Raynard RS, Cossins AR (May 1991). "Homeoviscous adaptation and thermal compensation of sodium pump of trout erythrocytes". The American Journal of Physiology. 260 (5 Pt 2): R916–24. doi:10.1152/ajpregu.1991.260.5.R916. PMID 2035703.
- ^ McCann; Widdowson; Food Standards Agency (1991). "Fats and Oils". The Composition of Foods. Royal Society of Chemistry.
- ^ Altar, Ted. "More Than You Wanted To Know About Fats/Oils". Sundance Natural Foods. Retrieved 2006-08-31.
- ^ a b c "USDA National Nutrient Database for Standard Reference". U.S. Department of Agriculture. Archived from the original on 2015-03-03. Retrieved 2010-02-17.
- ^ Klaus Schumann, Kurt Siekmann (2005). Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a24_247.
{{cite encyclopedia}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ a b c Anneken, David J.; et al. "Fatty Acids". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH.
- ^ Bolsover, Stephen R.; et al. (15 February 2004). Cell Biology: A Short Course. John Wiley & Sons. pp. 42ff. ISBN 978-0-471-46159-3.
- ^ Ramsden, Christopher E.; Zamora, Daisy; Makriyannis, Alexandros; Wood, JodiAnne T.; Mann, J. Douglas; Faurot, Keturah R.; MacIntosh, Beth A.; Majchrzak-Hong, Sharon F.; Gross, Jacklyn R. (August 2015). "Diet-induced changes in n-3 and n-6 derived endocannabinoids and reductions in headache pain and psychological distress". The Journal of Pain. 16 (8): 707–716. doi:10.1016/j.jpain.2015.04.007. ISSN 1526-5900. PMC 4522350. PMID 25958314.
- ^ "Electronic Nose Created To Detect Skin Vapors". Science Daily. July 21, 2009. Retrieved 2010-05-18.
- ^ Aizpurua-Olaizola O, Ormazabal M, Vallejo A, Olivares M, Navarro P, Etxebarria N, et al. (January 2015). "Optimization of supercritical fluid consecutive extractions of fatty acids and polyphenols from Vitis vinifera grape wastes". Journal of Food Science. 80 (1): E101-7. doi:10.1111/1750-3841.12715. PMID 25471637.
- ^ Breuer B, Stuhlfauth T, Fock HP (July 1987). "Separation of fatty acids or methyl esters including positional and geometric isomers by alumina argentation thin-layer chromatography". Journal of Chromatographic Science. 25 (7): 302–6. doi:10.1093/chromsci/25.7.302. PMID 3611285.
- ^ Breuer, B.; Stuhlfauth, T.; Fock, H. P. (1987). "Separation of Fatty Acids or Methyl Esters Including Positional and Geometric Isomers by Alumina Argentation Thin-Layer Chromatography". Journal of Chromatographic Science. 25 (7): 302–6. doi:10.1093/chromsci/25.7.302. PMID 3611285.
- ^ "Fatty Acids: Building Blocks for Industry" (PDF). aciscience.org. American Cleaning Institute. Retrieved 22 Apr 2018.