림프성 사상충증
Lymphatic filariasis| 림프성 사상충증 | |
|---|---|
| 기타이름 | 열대우림,[1] 열대우림, 열대우림[1] |
 | |
| 사상충증으로 인한 다리의 코끼리증. | |
| 전문 | 감염병 |
| 증상 | 팔, 다리, 유방 또는 생식기의[2] 심한 부종은 없습니다. |
| 원인들 | 모기에[3] 의해 전염되는 사상충 |
| 진단방법 | 혈액의[4] 현미경 검사 |
| 예방 | 모기장, 집단탈충[2] |
| 약 | 이버멕틴 또는 디에틸카르바마진이[2] 포함된 알벤다졸 |
| 빈도수. | 4천만(2022) |
림프성 사상충증은 사상충증으로 알려진 기생충에 의해 발생하는 인간의 질병입니다.[2][3] 대개 어린 시절에 획득되는 그것은 전 세계적으로 영구적인 장애의 주요 원인이며, 1억 명 이상의 사람들에게 영향을 미치고 다양한 심각한 임상적 병리에 나타납니다[6][7]. 대부분의 경우에는 증상이 없지만, 일부 사람들은 팔, 다리, 유방에 심각한 부종이 나타나는 엘리펀트리아증이라고 불리는 증후군이 발생합니다. 생식기. 피부도 두꺼워지고 통증이 생길 수 있습니다.[2] 피해를 입은 사람들은 일을 할 수 없는 경우가 많고, 그들의 기형과 장애 때문에 다른 사람들로부터 외면을 받거나 거절을 당하는 경우가 많습니다.[7]
모기 매개 질병 중 최초로 확인된 것입니다.[8] 그 벌레들은 감염된 모기에 물려 퍼집니다.[2] 세 가지 종류의 벌레가 이 병을 일으키는 것으로 알려져 있습니다. 우체리아 반크로프티, 브루기아 말레이, 브루기아 티모리가 가장 흔하며, 우체리아 반크로프티가 가장 흔합니다.[2] 이 벌레들은 림프관 내에 둥지를 틀고 시스템의 정상적인 기능을 방해함으로써 림프계를 손상시킵니다. 벌레는 혈액을 순환하는 수백만 마리의 유충을 번식시키면서 인체 내에서 최대 8년까지 생존할 수 있습니다.[9] 밤사이 채취한 혈액을 현미경으로 검사해 질병을 진단합니다. 일반적으로 김사 염색을 한 후 혈액을 도말로 검사합니다. 혈액에서 질병에 대한 항체를 검사하는 것도 진단을 허용할 수 있습니다.[4] 같은 가족의 다른 회충들도 강맹의 원인이 됩니다.[10]
예방은 집단 탈충증으로 알려진 질병이 존재하는 전체 그룹을 치료함으로써 달성될 수 있습니다.[2] 이것은 매년 약 6년 동안 질병 인구를 완전히 제거하기 위한 노력으로 이루어집니다.[2] 약물에는 보통 알벤다졸, 이버멕틴, 디에틸카르바마진 등 2가지 이상의 구충제 조합이 포함됩니다.[11] 모기 개체 수를 줄이고 모기장 사용을 촉진하는 등 모기에 물리지 않도록 하는 노력도 권장합니다.[2]
2022년 기준으로 약 4천만 명이 감염되었고, 47개국에서 약 8억 6천 3백만 명이 질병의 위험에 처해 있습니다.[5] 열대 아프리카와 아시아에서 가장 흔합니다.[2] 림프성 사상충증은 방치된 열대성 질환과 4대 주요 지렁이 감염증 중 하나로 분류됩니다.[10] 질병의 영향으로 연간 수십억 달러의 경제적 손실이 발생합니다.[2]
징후 및 증상

림프관 사상충증에 걸린 사람들은 종종 성충 뿐만 아니라 미세 사상충에 대한 면역학적 부작용을 경험합니다.[12]: 665 사상충증은 림프관의 심각한 염증 반응에 따른 복수와도 관련이 있을 수 있습니다.[13]: 818
엘레판티아증(Elephantiasis tropica)[14]: 438 은 림프관 사상충증의 진행 단계를 극적으로 보여주는 징후입니다. 코끼리증은 림프부종의 진행 단계로, 하반신의 피부와 기저 조직이 두꺼워져 코끼리처럼 보이는 것이 특징입니다. 성충이 림프계에 머물면서 림프의 흐름을 방해하기 때문에 발생합니다. 다른 종의 사상충은 신체의 다른 부분에 영향을 미치는 경향이 있습니다. Wucherria bancrofti는 팔, 유방, 다리, 음낭, 외음부에 영향을 줄 수 있는 반면, Brugia timori는 생식기에 거의 영향을 주지 않습니다.[citation needed]
원인들
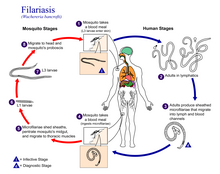
모두 Onchocercidae 과에 속하는 세 종의 사상충 회충은 인간의 림프관 사상충증을 유발합니다. Wucherria bancrofti (가장 흔한 원인종), Brugia malayi, 그리고 Brugia timori. 사상충 회충은 아데스속, 아노펠레스속, 쿨렉스속 또는 만소니아속의 감염된 모기에 물려 전염됩니다. 림프성 사상충증이 발병하려면 몇 달 또는 몇 년에 걸쳐 모기에 여러 번 물려야 합니다.[15] 모기는 L3(감염기) 유충을 인간 숙주의 피부에 침착시켜 물린 상처에 침투시킵니다. 거기서 유충은 림프관으로 들어가 성충으로 발전합니다.[7] 유충은 림프관과 폐 조직에 거주하면서 호흡을 방해하고 병이 진행되면서 흉통을 일으킵니다.[16] 이 질환은 회충과 관련된 결핵,[17] 천식 또는 기침과 혼동될 수 있습니다.[18]
질병 자체는 여러 요인, 즉 벌레, 벌레 내부의 공생적인 볼바흐균, 숙주의 면역 반응, 그리고 발생하는 수많은 기회주의적 감염과 장애 사이의 복잡한 상호 작용의 결과입니다. 성충은 인간의 림프계에 살며 몸 전체의 림프 흐름을 방해합니다. 이로 인해 주로 하체(일반적으로 다리와 생식기)에서 발견되는 만성 림프 부종이 발생합니다.[19] 이 벌레들은 혈액을 통해 순환하는 수백만 마리의 유충을 번식시키면서 인체 내에서 최대 8년까지 생존할 수 있습니다.[9]
진단.
림프성 사상충증을 진단하는 바람직한 방법은 혈액의 현미경 검사를 통해 미세 사상충을 찾는 것입니다. 혈액 샘플은 일반적으로 김사 염색으로 염색된 두꺼운 도말 형태입니다. 혈액 도말을 분석하는 기술자는 W. bancrofti와 잠재적으로 존재하는 다른 기생충을 구별할 수 있어야 합니다. 혈액 도말은 미세 사상체가 말초 순환에 있을 때 혈액 샘플을 채취하는 경우 간단하고 상당히 정확한 진단 도구입니다. 미세모충은 밤에만 혈액 속을 순환하기 때문에 밤에는 혈액 검체를 채취해야 합니다.[20]
진행된 경우에도 말초혈액에서 원인균을 검출하기 어렵거나 불가능한 경우가 많습니다.[12] 이러한 경우, 혈액 혈청에서 질병에 대한 항체를 검사하는 것도 사용할 수 있습니다.[4] 필라리아 DNA의 최소 1pg의 미세 분획을 검출하기 위해 중합효소 연쇄 반응 테스트도 수행할 수 있습니다.[21] X선 검사로 죽은 석회화된 벌레를 탐지할 수 있습니다. 초음파 검사를 통해 성충의 움직임으로 인한 움직임과 소음을 감지할 수도 있습니다.[22]
감별진단
림프성 사상충증은 자극성 알칼리성 점토 토양에 맨발이 노출되어 발생하는 비감염성 질환인 포도코니증(비 사상충증이라고도 함)과 혼동될 수 있습니다.[23][24] 그러나 족저증은 일반적으로 양쪽 다리에 영향을 미치는 반면, 사상체증은 일반적으로 일방적입니다.[23] 또한 족저증은 사타구니에 영향을 미치는 경우가 매우 드물지만 사상충증은 사타구니를 자주 침범합니다. 지리적 위치는 또한 이 두 질병을 구별하는 데 도움이 될 수 있습니다: 족집게증은 일반적으로 계절적 강우량이 높은 고지대에서 발견되는 반면, 사상충증은 모기가 만연한 저지대에서 흔히 발견됩니다.[23]
예방
풍토병 지역에서 모기에 물리지 않도록 보호하는 것은 림프 사상충증 예방에 매우 중요합니다. 방충제와 모기장(특히 델타메트린이나 퍼메트린과 같은 살충제로 처리되는 경우)[25]은 림프성 사상충증의 전염을 감소시키는 것으로 입증되었습니다.[26][27] 또한 잔여 분사 및 개인 보호 장비는 벡터를 제어하는 방법으로 알려져 있습니다.[9]
전 세계적인 림프성 사상충 퇴치가 최종 목표입니다. 이 질병은 알려진 동물 저장소가 없기 때문에 가능한 것으로 간주됩니다.[26] 세계보건기구(WHO)는 사상충을 근절하기 위한 전 세계적인 노력을 조정하고 있습니다. 이 프로그램의 주요 내용은 항우연성 약물로 위험에 처한 사람들의 전체 집단을 대량으로 제거하는 것입니다. 특정 치료법은 림프성 사상충증과 다른 사상충병의 동반 풍토병에 달려 있습니다. WHO의 연간 MDA 지침은 아래와 같습니다.
- 루아시스와 동반 유행하는 부위의 경우 알벤다졸 400 mg을 투여해야 합니다
- 온코세르시아시스와 공동 유행하는 국가의 경우, 200 mcg/kg의 이버멕틴을 400 mg의 알벤다졸과 함께 투여해야 합니다.
- 장구균증이 없는 국가에서는 디에틸카르바마진 구연산염(DEC) 6 mg/kg과 알벤다졸 400 mg을 사용해야 합니다.
- 소아마비가 없는 국가에서는 200 mcg/kg의 이버멕틴과 400 mg의 알벤다졸을 사용해야 하며, 소아마비가 없는 국가에서는 200 mcg/kg의 이버멕틴을 사용해야 합니다.[9][11]
기생충은 번식을 위해 인간 숙주를 필요로 하기 때문에 위험에 처한 집단을 일관되게 치료([2]매년 4~6년)하면 전염 주기가 끊어지고 원인 유기체의 멸종을 초래할 것으로 예상됩니다.[26]
2011년, 스리랑카는 WHO로부터 림프성 사상충증을 퇴치했다는 인증을 받았습니다. 2017년 7월, WHO는 통가에서 이 질병이 제거되었다고 발표했습니다. 캄보디아, 중국, 쿡 제도, 이집트, 키리바시, 몰디브, 마셜 제도, 니우에, 팔라우, 한국, 태국, 바누아투, 베트남, 왈리스와 후투나에서도 병균이 제거되었습니다.[28] 2020년 WHO는 이 프로그램의 2030년 목표가 풍토병 국가의 80%에서 림프성 사상충증이 제거될 것이라고 발표했습니다.[29]
백신은 아직 출시되지 않았지만, 2013년 일리노이 대학교 의과 대학은 쥐를 대상으로 B. malayi에 대한 테스트에서 95%의 효능을 보고했습니다.[30]
치료
림프성 사상충증의 치료는 부분적으로 질병이 획득된 지역의 지리적 위치에 따라 다르지만 거의 항상 2가지 이상의 구충제(알벤다졸, 이버멕틴 및 디에틸카르바마진)의 조합을 포함합니다. 사하라 이남 아프리카에서는 보통 알벤다졸과 이버멕틴으로 병을 치료하는 반면, 서태평양 지역에서는 구충제 3종을 모두 사용합니다. 디에틸카르바마진은 알벤다졸과 함께 사용되는 경우가 많지만, 다른 조합만큼 특정적이지는 않습니다.[11]
월바치아는 림프관 사상충증을 담당하는 기생충의 내장 안에 서식하는 내공생균으로, 이들의 생존에 필요한 영양분을 공급합니다. 독시사이클린은 이 박테리아들을 죽이고, 이것은 다시 성충으로 가는 미세모충의 성숙을 막습니다. 또한 성충의 수명을 단축시켜 정상 수명인 10~14년이 아닌 1~2년 안에 죽게 합니다.[31] 독시사이클린은 림프성 사상충증 치료에 효과적입니다. 이 항생제 프로토콜의 한계로는 구충제 1회 투여가 아닌 4~6주 정도의 치료가 필요하고, 어린 아이와 임산부에게 독시사이클린을 사용해서는 안 된다는 점, 광독성이 있다는 점 등이 있습니다.[32]
알벤다졸은 구충제로 분류되는데, 구충제는 특별히 구충제를 죽이는 작용을 합니다.[33] 이 약은 벌레가 포도당을 흡수하는 것을 막아서 분명히 배고픔과 피로로 인한 죽음을 초래합니다. 알벤다졸 단독의 효과는 다양한 결과를 가지고 있지만, DEC 약물과 병용하면 더 효과적인 것으로 밝혀졌습니다.[34] 이버멕틴은 알벤다졸과 함께 투여되며, 기생충의 신경세포와 결합하여 작용하고, 이후 이들을 염화물에 투과시킵니다. 이것은 마비로 사망에 이릅니다. 그러나 이버멕틴은 생명의 초기 단계에서 기생충을 죽일 뿐 성충인 살아있는 벌레는 죽이지 못하는 것으로 밝혀졌습니다. 따라서 이 약은 보통 DEC와 결합하여 미세모충과 성충을 모두 죽입니다.[35]
음낭성 상피증 및 수핵의 경우 수술적 치료가 도움이 될 수 있습니다. 하지만 수술은 일반적으로 팔다리의 코끼리증을 교정하는 데는 효과가 없습니다.[36] 림프부종, 하이드로셀로 인한 급성 염증 반응은 좋은 위생, 피부 관리, 운동 및 감염된 팔다리의 상승을 실천함으로써 감소 또는 예방할 수 있습니다.[9]
역학

임파선성 사상충증은 아프리카, 아시아, 중앙아메리카, 카리브해, 남아메리카의 열대 및 아열대 지역과 일부 태평양 섬 국가에서 발생합니다. 림프관 사상충증에 의한 코끼리증은 세계에서 가장 흔한 영구장애의 원인 중 하나입니다.[7] 2018년 기준 5100만 명이 림프성 사상충증에 감염됐고 50개국에서 최소 8억 6300만 명이 감염 확산을 막기 위해 예방적 항암치료가 필요한 지역에 살고 있습니다. 2022년까지 유병률은 약 4천만 명으로 감소했으며 이 질병은 47개국에서 풍토병으로 남아 있습니다. 이러한 개선은 WHO의 림프성 사상충증 제거를 위한 글로벌 프로그램의 직접적인 결과입니다.[5] 시행 이후 7억 4천만 명의 사람들이 더 이상 질병을 치료하기 위해 예방적 항암 치료를 필요로 하지 않습니다.[9]
W. bancrofti는 림프 사상충증의 90%를 담당합니다. 브루기아 말레이는 나머지 대부분의 경우를 유발하지만 브루기아 티모리는 드문 원인입니다.[5] W. bancrofti는 넓은 적도대(아프리카, 나일강 삼각주, 튀르키예, 인도, 동인도 제도, 동남아시아, 필리핀, 대양주 제도 및 남아메리카 일부)에 크게 영향을 미칩니다. 임파선성 사상충증은 관광으로 인한 감염 확산에 수개월에서 수년에 걸쳐 모기를 여러 번 물어야 하기 때문에 발생률이 낮습니다.[37] W. bancrofti의 모기 매개체는 사람의 혈액을 선호합니다. 사람은 분명히 W. bancrofti에 자연적으로 감염된 유일한 동물입니다. 알려진 저장소 호스트가 없습니다.[38] 림프성 사상충증은 미국에서 극히 드물며, 1900년대 초 사우스 캐롤라이나에서 보고된 사례는 단 한 건뿐입니다.[7]
남미에서는 브라질, 도미니카 공화국, 가이아나, 아이티로 구성된 4개의 풍토병 국가가 림프구 사상충증 발병을 막기 위해 노력하고 있습니다.[39] 라틴 아메리카에서 림프성 사상충증의 확산은 W. brancrofti를 통해 이루어지는데, W. brancrofti는 이 지역 내의 유일한 인류인 culex quinquefasciatus를 통해 이루어집니다. [40] MDA 프로그램 개발을 통해 미주 지역의 기하급수적인 발전 속도를 계산하고 있습니다. 3단계 약물 투여 프로그램인 MDA 프로그램을 통해 약물 프로그램의 필요성이 67% 감소했습니다.[39] 브라질은 질병으로 가장 큰 피해를 입은 지역사회에 MDA 프로그램을 통해 DEC 약물을 투여함으로써 증가하는 풍토병을 목표로 삼았습니다. 브라질은 매년 이러한 약물을 제공하고 사후 관리를 제공함으로써 가족들에게 질병을 치료하는 방법을 보여주고 일자리를 위한 인맥을 형성하는 것은 물론 환자들을 사회에 통합하기 위한 소셜 네트워크를 제공함으로써 치료를 제공하기 위해 가장 많은 노력을 기울였습니다.[41] 도미니카 공화국은 2002년부터 2007년까지 5년 동안 매년 5회의 DEC 약물을 투여해 왔습니다. 초기의 극단적인 조치 이후, 도미니카는 또 다른 세 차례의 MDA를 투여했습니다. 가이아나는 또한 2003년부터 2007년까지 DEC 강화 소금을 사용하고 궁극적으로 2014년부터 현재까지 DEC와 함께 MDA로 전환하면서 질병의 확산을 막는 데 초점을 맞추기 위해 DEC 약물을 사용했습니다. 환자 교육 및 치료 접근성을 목표로 합니다.[42] 아이티는 그 후 2002년에 DEC 약품을 시행함으로써 그 질병에 집중했습니다. 2012년까지 완전한 지리적 범위에 도달했으며, 이후 2014년에는 약 20개 커뮤니티에서 MDA의 필요성을 제거했습니다.
족저증 풍토병 지역에서는 유병률이 5% 이상일 수 있습니다.[43] 림프성 사상충증이 풍토병인 지역에서는 여성의 10%가 수족이 부어올라 영향을 받을 수 있고, 남성의 50%는 생식기 돌연변이 증상이 발생할 수 있습니다.[44]
역사


4000년 전의 림프성 사상충증의 증거가 있습니다.[45] 기원전 1500년 - 기원전 1200년경에 작곡된 고대 베다 텍스트인 리그 베다는 코끼리 공포증에 대한 가능한 언급을 하고 있습니다. 리그베다 7권의 50번째 찬송가는 미트라, 바루나, 아그니 신들에게 "안에 둥지를 틀고 부풀어 오르는 것"에 대한 보호를 요청합니다. 찬송가의 저자는 신들에게 벌레가 발을 다치지 않게 해달라고 애원합니다. 이 질병은 발목과 무릎에 발진이 생기는 것으로 설명됩니다.[46] 고대 이집트 (기원전 2000년)와 서아프리카의 녹 문명 (기원전 500년)의 유물은 가능한 코끼리증 증상을 보여줍니다. 이 질병에 대한 최초의 명확한 언급은 고대 그리스 문헌에서 발견되는데, 학자들은 종종 유사한 림프성 사상충증의 증상을 나병의 증상과 구별하여 나병을 엘레판티아시스 그레이코룸으로, 림프성 사상충증을 엘레판티아시스 아라붐으로 설명했습니다.[45]
증상에 대한 최초의 기록은 16세기에 얀 후이겐 반 린쇼텐(Jan Huygen van Linschoten)이 고아(Goa)를 탐험하는 동안 이 질병에 대해 썼습니다. 아시아와 아프리카 지역의 탐험가들도 비슷한 증상을 보고했지만, 그 질병에 대한 이해는 수세기가 지나서야 시작되었습니다.[citation needed]
원인 물질은 19세기 후반에 처음 확인되었습니다.[47] 1866년, 티모시 루이스(Timothy Lewis)는 장 니콜라스 데마르콰이(Jean Nicolas Demarquay와 오토 헨리 우체러(Otto Henry Wucherer)의 연구를 기반으로 미세모충증과 엘리펀트리아증 사이의 연관성을 확립하고 궁극적으로 이 질병을 설명하는 연구 과정을 수립했습니다. 1876년, 조셉 밴크로프트는 그 벌레의 성체를 발견했습니다.[48] 1877년, 절지동물 벡터를 포함하는 라이프사이클은 패트릭 맨슨에 의해 이론화되었고, 그는 모기에 벌레가 존재한다는 것을 계속해서 증명했습니다. 맨슨은 모기가 알을 낳은 물과의 피부 접촉을 통해 질병이 전염된다는 잘못된 가설을 세웠습니다.[49] 1900년, 조지 카마이클 로우는 모기 매개체의 주둥이에서 벌레의 존재를 발견함으로써 실제 전염 방법을 알아냈습니다.[45]
말라바르, 나야르, 그리고 브라만과 그들의 아내들의 많은 사람들이, 사실 가장 낮은 계급의 사람들을 포함하여, 전체 인구의 약 4분의 1이나 5분의 1이, 아주 큰 다리를 가지고 있습니다. 그리고 그들은 이것 때문에 죽습니다. 이것은 보기 흉한 일입니다. 그들은 이것이 그들이 통과하는 물 때문이라고 말합니다, 왜냐하면 그 나라는 습지이기 때문입니다. 이것을 현지어로 심낭이라고 하는데, 무릎 아래부터 붓기가 모두 같고, 통증도 없고, 이 병에 대해서도 전혀 눈치채지 못합니다.
— Portuguese diplomat Tomé Pires, Suma Oriental, 1512–1515.[50]
연구방향
시카고 일리노이대(UIC) 연구진이 림프구 사상충증 예방을 위한 새로운 백신을 개발했습니다. 이 백신은 림프 사상충 감염의 마우스 모델에서 강력하고 보호적인 면역 반응을 이끌어내는 것으로 나타났습니다. 이 백신에 의해 유도된 면역 반응은 마우스 모델에서 W. bancrofti 및 B. malayi 감염 모두에 대해 보호적인 것으로 입증되었으며 인간에게 유용할 수 있습니다.[51]
2007년 9월 20일, 유전학자들은 림프 사상충증을 일으키는 회충 중 하나인 브루기아 말레이의 완전한 유전체(유전적 내용)의 초안을 발표했습니다.[52] 이 프로젝트는 1994년에 시작되었고 2000년까지 게놈의 80%가 결정되었습니다. 유전자의 함량을 결정하는 것은 신약과 백신의 개발로 이어질 수 있습니다.[53]
수의병
온초카오천기는 소의 림프성 사상충증을 유발합니다.[54][55]
참고문헌
- ^ a b James WD, Berger T, Elston D (2015). Andrews' Diseases of the Skin: Clinical Dermatology. Elsevier Health Sciences. p. 432. ISBN 9780323319690. Archived from the original on 12 October 2016.
- ^ a b c d e f g h i j k l m "Lymphatic filariasis Fact sheet N°102". World Health Organization. March 2014. Archived from the original on 25 March 2014. Retrieved 20 March 2014.
- ^ a b "Lymphatic filariasis". World Health Organization. Retrieved 7 May 2016.
- ^ a b c "Parasites – Lymphatic Filariasis Diagnosis". CDC. 14 June 2013. Archived from the original on 22 February 2014. Retrieved 21 March 2014.
- ^ a b c d "Lymphatic filariasis". www.who.int. Retrieved 4 October 2019.
- ^ Chakraborty, Sanjukta; Gurusamy, Manokaran; Zawieja, David C.; Muthuchamy, Mariappan (July 2013). "Lymphatic filariasis: Perspectives on lymphatic remodeling and contractile dysfunction in filarial disease pathogenesis". Microcirculation (New York, N.Y. : 1994). 20 (5): 349–364. doi:10.1111/micc.12031. ISSN 1073-9688. PMC 3613430. PMID 23237232.
- ^ a b c d e Centers for Disease Control and Prevention (22 October 2018). "Lymphatic Filariasis". Parasites. Retrieved 10 December 2022.
- ^ "Lymphatic filariasis". Health Topics A to Z. World Health Organization. Retrieved 25 September 2011.
- ^ a b c d e f "Lymphatic filariasis". www.who.int. Retrieved 17 November 2023.
- ^ a b "Working to overcome the global impact of neglected tropical diseases – Summary" (PDF). Relevé Épidémiologique Hebdomadaire. 86 (13): 113–20. March 2011. PMID 21438440.
- ^ a b c "Global programme to eliminate lymphatic filariasis: progress report, 2022". www.who.int. Retrieved 20 November 2023.
- ^ a b Pfarr KM, Debrah AY, Specht S, Hoerauf A (November 2009). "Filariasis and lymphoedema". Parasite Immunology. 31 (11): 664–72. doi:10.1111/j.1365-3024.2009.01133.x. PMC 2784903. PMID 19825106.
- ^ Lizaola B, Bonder A, Trivedi HD, Tapper EB, Cardenas A (November 2017). "Review article: the diagnostic approach and current management of chylous ascites". Alimentary Pharmacology & Therapeutics. 46 (9): 816–24. doi:10.1111/apt.14284. hdl:2027.42/138889. PMID 28892178.
- ^ James WD, Berger TG, et al. (2006). Andrews' Diseases of the Skin: clinical Dermatology. Saunders Elsevier. ISBN 978-0-7216-2921-6.
- ^ Prevention, CDC-Centers for Disease Control and (17 September 2020). "CDC - Lymphatic Filariasis - General Information - Frequently Asked Questions". www.cdc.gov. Retrieved 17 November 2023.
- ^ Jha, Suman K.; Karna, Bibek; Mahajan, Kunal (2020), "Tropical Pulmonary Eosinophilia", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 32491456, retrieved 1 December 2020
- ^ "Pulmonary Eosinophilia". Retrieved 16 April 2011.
- ^ "ICD-10 Classification". Retrieved 16 April 2011.
- ^ Saladin K (2007). Anatomy & Physiology: The Unity of Form and Function. McGraw-Hill. ISBN 978-0-07-287506-5.
- ^ van Hoegaerden M, Ivanoff B (1986). "A rapid, simple method for isolation of viable microfilariae". Am J Trop Med Hyg. 35 (1): 148–51. doi:10.4269/ajtmh.1986.35.148. PMID 3456213.
- ^ Zhong M, McCarthy J, Bierwert L, Lizotte-Waniewski M, Chanteau S, Nutman TB, Ottesen EA, Williams SA (1996). "A polymerase chain reaction assay for detection of the parasite Wuchereria bancrofti in human blood samples". Am J Trop Med Hyg. 54 (4): 357–63. doi:10.4269/ajtmh.1996.54.357. PMID 8615447.
- ^ Amaral F, Dryer G, Figueredo-Silva J, Noroes J, Cavalcanti A, Samico SC, Santos A, Coutinho A (1994). "Live adult worms detected by ultrasonography in human Bancroftian filariasis". Am J Trop Med Hyg. 50 (6): 753–7. doi:10.4269/ajtmh.1994.50.753. PMID 8024070.
- ^ a b c Korevaar DA, Visser BJ (2012). "Podoconiosis, a neglected tropical disease". The Netherlands Journal of Medicine. 70 (5): 210–14. PMID 22744921.
- ^ Davey G, Tekola F, Newport MJ (2007). "Podoconiosis: non-infectious geochemical elephantiasis". Transactions of the Royal Society of Tropical Medicine and Hygiene. 101 (12): 1175–80. doi:10.1016/j.trstmh.2007.08.013. PMID 17976670.
- ^ Swales, Jay (2006). "Malaria: Fever Wars". CDC.
- ^ a b c The Carter Center. "Lymphatic Filariasis Elimination Program" (PDF). Retrieved 28 November 2015.
- ^ U.S. Centers for Disease Control and Prevention. "Lymphatic". Retrieved 8 July 2010.
- ^ World Health Organization (31 July 2017). "Congratulations, Tonga! Pacific island state eliminates lymphatic filariasis as a public health problem". Retrieved 10 December 2022.
- ^ World Health Organization (29 October 2020). "Lymphatic filariasis: reporting continued progress towards elimination as a public health problem". News. World Health Organization. Retrieved 10 December 2022.
- ^ Dakshinamoorthy G, Samykutty AK, Munirathinam G, Reddy MV, Kalyanasundaram R (March 2013). "Multivalent fusion protein vaccine for lymphatic filariasis". Vaccine. 31 (12): 1616–22. doi:10.1016/j.vaccine.2012.09.055. PMC 3554871. PMID 23036503.
- ^ Landmann F, Voronin D, Sullivan W, Taylor MJ (November 2011). "Anti-filarial activity of antibiotic therapy is due to extensive apoptosis after Wolbachia depletion from filarial nematodes". PLOS Pathogens. 7 (11): e1002351. doi:10.1371/journal.ppat.1002351. PMC 3207916. PMID 22072969.
- ^ Taylor MJ, Hoerauf A, Townson S, Slatko BE, Ward SA (2014). "Anti-Wolbachia drug discovery and development: safe macrofilaricides for onchocerciasis and lymphatic filariasis". Parasitology. 141 (1): 119–27. doi:10.1017/s0031182013001108. PMC 3884836. PMID 23866958.
- ^ Prevention, CDC-Centers for Disease Control and (26 October 2020). "CDC - Lymphatic Filariasis - Resources for Health Professionals - Guidance for Evaluation and Treatment". www.cdc.gov. Retrieved 12 December 2023.
- ^ "Lymphatic filariasis". www.who.int. Retrieved 12 December 2023.
- ^ Brown, K. R.; Ricci, F. M.; Ottesen, E. A. (2000). "Ivermectin: effectiveness in lymphatic filariasis". Parasitology. 121 Suppl: S133–146. doi:10.1017/s0031182000006570. ISSN 0031-1820. PMID 11386685. S2CID 19933533.
- ^ Gloviczki P (1995). "The management of lymphatic disorders". In Rutherford RB (ed.). Vascular surgery (4th ed.). Philadelphia: WB Saunders. pp. 1883–1945.
- ^ Prevention, CDC-Centers for Disease Control and (26 August 2021). "CDC - Lymphatic Filariasis - Epidemiology & Risk Factors". www.cdc.gov. Retrieved 20 November 2023.
- ^ King CL, Freedman DP (2000). "Filariasis". In G.T. Strickland (ed.). Hunter's tropical medicine and emerging infectious diseases (8th ed.). Philadelphia: E.B. Saunders. pp. 740–53. ISBN 978-0-7216-6223-7.
- ^ a b Fontes, Gilberto; da Rocha, Eliana Maria Mauricio; Scholte, Ronaldo Guilherme Carvalho; Nicholls, Rubén Santiago (22 December 2020). "Progress towards elimination of lymphatic filariasis in the Americas region". International Health. 13 (Suppl 1): S33–S38. doi:10.1093/inthealth/ihaa048. ISSN 1876-3405. PMC 7753170. PMID 33349876.
- ^ Fontes, G.; Rocha, E. M.; Brito, A. C.; Fireman, F. A.; Antunes, C. M. (June 2000). "The microfilarial periodicity of Wuchereria bancrofti in north-eastern Brazil". Annals of Tropical Medicine and Parasitology. 94 (4): 373–379. doi:10.1080/00034983.2000.11813552. ISSN 0003-4983. PMID 10945047. S2CID 9316265.
- ^ Fontes, Gilberto; Leite, Anderson Brandão; de Lima, Ana Rachel Vasconcelos; Freitas, Helen; Ehrenberg, John Patrick; da Rocha, Eliana Maria Mauricio (26 November 2012). "Lymphatic filariasis in Brazil: epidemiological situation and outlook for elimination". Parasites & Vectors. 5: 272. doi:10.1186/1756-3305-5-272. ISSN 1756-3305. PMC 3545725. PMID 23181663.
- ^ McPherson, T (24 January 2003). "Impact on the quality of life of lymphoedema patients following introduction of a hygiene and skin care regimen in a Guyanese community endemic for lymphatic filariasis: A preliminary clinical intervention study". Filaria Journal. 2 (1): 1. doi:10.1186/1475-2883-2-1. ISSN 1475-2883. PMC 149435. PMID 12605723.
- ^ Deribe K, Tomczyk S, Tekola-Ayele F (2013). Phillips RO (ed.). "Ten years of podoconiosis research in Ethiopia". PLOS Neglected Tropical Diseases. 7 (10): e2301. doi:10.1371/journal.pntd.0002301. PMC 3794913. PMID 24130908.
- ^ The Carter Center. "Lymphatic Filariasis Elimination Program". Retrieved 17 July 2008.
- ^ a b c "Lymphatic Filariasis Discovery". Retrieved 21 November 2008.
- ^ "HYMN L. Various Deities".
- ^ Otsuji, Y. (2011). "History, Epidemiology and Control of Filariasis". Tropical Medicine and Health. 39 (1 Suppl 2): 3–13. doi:10.2149/tmh.39-1-suppl_2-3 (inactive 1 August 2023). PMC 3153148. PMID 22028595.
{{cite journal}}: CS1 maint: 2023년 8월 기준 DOI 비활성화 (링크) - ^ Grove, David I (1990). A history of human helminthology. Wallingford: CAB International. pp. 1–848. ISBN 0-85198-689-7.
- ^ Grove, David I (2014). Tapeworms, lice and prions: a compendium of unpleasant infections. Oxford: Oxford University Press. pp. 1–602. ISBN 978-0-19-964102-4.
- ^ Burma D.P. (2010). Project Of History Of Science, Philosophy And Culture In Indian Civilization, Volume Xiii Part 2: From Physiology And Chemistry To Biochemistry. Pearson Education India. p. 49. ISBN 978-81-317-3220-5.
- ^ Dakshinamoorthy G, Samykutty AK, Munirathinam G, Reddy MV, Kalyanasundaram R (March 2013). "Multivalent fusion protein vaccine for lymphatic filariasis". Vaccine. 31 (12): 1616–22. doi:10.1016/j.vaccine.2012.09.055. PMC 3554871. PMID 23036503. (1차 출처)
- ^ Ghedin E, Wang S, Spiro D, Caler E, Zhao Q, Crabtree J, et al. (September 2007). "Draft genome of the filarial nematode parasite Brugia malayi". Science. 317 (5845): 1756–60. Bibcode:2007Sci...317.1756G. doi:10.1126/science.1145406. PMC 2613796. PMID 17885136.
- ^ Williams SA, Lizotte-Waniewski MR, Foster J, Guiliano D, Daub J, Scott AL, Slatko B, Blaxter ML (April 2000). "The filarial genome project: analysis of the nuclear, mitochondrial and endosymbiont genomes of Brugia malayi". International Journal for Parasitology. 30 (4): 411–19. doi:10.1016/s0020-7519(00)00014-x. PMID 10731564.
- ^ Bain, Odile (2002). "Evolutionary Relationships Among Filarial Nematodes". World Class Parasites. Vol. 5. Boston: Kluwer. pp. 21–9. doi:10.1007/0-306-47661-4_3. ISBN 1-4020-7038-1. ISBN 978-1-4020-7038-9. ISBN 978-1-4757-7600-3. ISBN 978-0-306-47661-7.
- ^ Taylor, Mark J.; Bandi, Claudio; Hoerauf, Achim (2005). "Wolbachia Bacterial Endosymbionts of Filarial Nematodes". Advances in Parasitology. Vol. 60. Elsevier. pp. 245–84. doi:10.1016/s0065-308x(05)60004-8. ISBN 9780120317608. ISSN 0065-308X. PMID 16230105. S2CID 39363217.



