오렐라닌
Orellanine | |
| 이름 | |
|---|---|
| IUPAC 이름 3,3µ, 4,4µ-테트라히드록시-2,2µ-비피리딘-N,Nµ-이산화물 | |
| 기타 이름 오렐라닌 2,2-비피리딘-3,3-4,4-테트롤-1,1-이산화물 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.232.424 |
PubChem CID | |
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| C10H8N2O6 | |
| 몰 질량 | 252.182 g/160−1 |
| 위험 요소 | |
| 산업안전보건(OHS/OSH): | |
주요 위험 요소 | 독성의 시작이 늦어지는 고독성 |
| GHS 라벨링: | |
  | |
| 위험. | |
| H300, H370 | |
| P260, P264, P270, P301+P310, P307+P311, P321, P330, P405, P501 | |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
오렐라닌 또는 오렐라닌은 코르티나리아과의 [1]오렐라니로 알려진 버섯 군에서 발견되는 마이코톡신이다.구조적으로 제초제 디쿼트와 다소 관련이 있는 비피리딘 N-옥사이드 화합물이다.
역사
오렐라닌은 1957년 폴란드 비드고시츠에서 135명의 집단 중독으로 19명이 [2][3][4]사망했을 때 처음으로 사람들의 관심을 끌었다.오렐라닌은 코르티나리우스에 속하는 버섯의 한 종류에서 유래한다.이 속의 모든 종이 독성이 있거나 오렐라닌을 포함하고 있는 것은 아니지만, 코티나리우스 오렐라누스, 루벨루스, 헨리시, 레이네렌시스, 브루노풀부스가 오렐라닌을 함유하고 있는 것으로 밝혀졌다.북미에서도 오렐라닌 중독 사례가 있지만, 이 버섯과 관련된 독극물은 주로 유럽에서 먹이가 주요 영양 공급원이었다.오렐라닌은 급성 신장 손상을 일으키는 것으로 밝혀졌으며 사람들이 환각작용을 [5]일으키는 것으로 오인하여 이 버섯을 복용한 사례가 많다.
1962년이 되어서야 오렐라닌의 첫 분리가 이루어졌다.최초의 메타놀 추출과 오렐라닌의 분리는 Staniswaw Grzymala에 의해 이루어졌고 버섯 Cortinarius [4][6]orellanus에서 분리되었습니다.오렐라닌의 분리와 함께, Grzymala는 또한 코르티나리우스 오렐라누스의 신독성을 입증하고 오렐라닌의 다양한 물리적, 화학적 특성을 결정할 수 있었다.그는 버섯의 독성이 지연과 급성 신장 손상 둘 다 때문이라는 것을 발견했다.그는 또한 분리된 백색 결정성 물질이 150°C 이상에서 가열되면 서서히 [3][4]분해되기 시작했다고 언급했다.오렐라닌의 첫 번째 분리 후,[3][6] 오렐라닌의 구조는 1979년 Antkowiak와 Gessner에 의해 처음으로 추론되었다.오렐라닌의 구조는 3,3', 4,4'-테트라히드록시-2,2'-비피리딘-1,1'-이산화물로 밝혀졌다.또한 Antkowiak와 Gessner는 오렐리닌의 분해 생성물인 오렐린의 모노 N-옥사이드라는 것을 확인할 수 있었다.또한 오렐린은 독성이 없는 것으로 밝혀졌다.오렐라닌의 첫 번째 성공적인 합성은 1985년에 이루어졌다.Tiecco, M. et al.는 시판되는 3-히드록시피리딘을 [3]사용하여 오렐라닌의 총합성을 완료했다.첫 번째 성공적인 합성 후, 1987년 코헨-아다드 등에 의해 X선 결정학에 [6]의해 구조가 확인되었다.
합성
오렐라닌의 화학적 구성은 1970년대 후반 폴란드의 화학자 Antkowiak와 Gessner가 그것이 [7][8]이산화 비피리딘이라는 것을 발견하기 전까지 알려지지 않았다.오렐라닌은 호변이성체를 거치며, 보다 안정적인 호변이성체는 산화아민 형태이다.오렐라닌의 흥미로운 특징은 알루미늄 이온을 결합시켜 킬레이트 [9]복합체를 형성하는 능력이다.
오렐라닌의 첫 합성은 1985년에 이루어졌으며, 티에코 등은 3-히드록시 피리딘에서 오렐렌을 합성할 수 있었다.이 합성은 79-87%의 수율로 8단계로 완료되었다.두 개의 피리딜 고리가 합성될 때 거의 수직이고 분자는 [4]키랄이다.버섯으로부터 분리될 때, 그것은 광학적으로 비활성화된 라세미 혼합물입니다.다른 통합 전략도 시도되었다.예를 들어, 1985년 Dehmlow와 Schulz에 의해 3-아미노피리딘을 사용하여 9단계에 걸쳐 오렐라닌을 합성하여 원하는 제품을 30%의 [2]수율로 합성하였다.
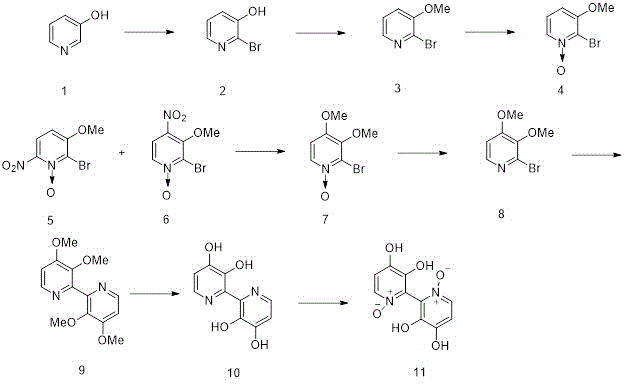
Tiecco에 의해 수행된 합성에서는 M. 등이 아래의 스킴에서 볼 수 있다.제1공정에서는 먼저 3-히드록시피리딘을 알칼리성 용액 중 브롬으로 처리하여 2를 얻는다.그런 다음 DMF를 용매로 사용하여 O-알킬화를 수행하여 3을 클로로포름의 m-클로로페록시벤조산으로 산화하여 4를 얻는다.그 후 질산과 황산으로 질화시켜 5와 6의 혼합물을 얻었다.이 두 분자는 물과 산물의 혼합물을 결합함으로써 분리되었다.5는 물에 녹지 않는 반면 6은 물에 녹는다.이어서 메탄올에서 6을 메톡시드나트륨으로 하여 제품 7에서 볼 수 있는 다른 메톡시기를 얻고, 7을 트리브롬화 인을 사용하여 탈산소하여 8을 얻는다.테트라메틸오렐린, 구조 9, 트리페닐포스핀, NiCl2·6을 얻기 위해HO 및 아연 분말은 니켈-포스핀 복합체를 사용하여 할로피리딘의 호모커플링을 수행하는데 사용되었다2.일단 비피리딜 구조의 8을 얻으면, 오렐라닌의 합성을 수행할 수 있었다.8번 비피리딜 생성물은 수소 브롬산으로 탈알킬화되어 오렐린을 생성하는데, 오렐린은 노란색 결정성 고체(10)로 밝혀졌다.다음으로 오렐린을 열을 이용하여 과산화수소로 산화하여 원하는 생성물인 오렐란인(11)을 얻는다.
9에서 오렐라닌을 합성하는 또 다른 방법은 클로로포름에서 과도한 m-클로로페록시벤조산을 투여하여 12, 테트라메틸 오렐라닌을 얻는 것이었다.그런 다음 테트라메틸 오렐렌을 하이드로브롬산을 사용하여 탈메틸화시켜 오렐란을 생성했다.
독성
양전하를 띤 질소 원자를 가진 비피리딘은 오렐라닌의 구조가 밝혀지기 전에 이미 독성이 있는 것으로 알려져 있었다.제초제 파라코트와 디쿼트는 식물뿐만 아니라 인간과 가축에게도 독성이 있다.하전된 질소 원자를 가진 비피리딘은 유기체의 중요한 산화환원반응을 방해하고, 한두 개의 전자를 '도둑질'하고, 때로는 다른, 종종 바람직하지 않은 산화환원반응으로 전자를 우회시킨다.최종 생성물은 과산화물 또는 과산화물 이온일 수 있으며, 후자는 세포에 유해합니다.비록 교란된 산화환원 반응에서 심각한 신장 손상으로 이어지는 과정이 적절하게 해결되지 않았지만, 오렐라닌은 같은 방식으로 작동할 가능성이 있다.
인간의 경우, 네프로톡신 오렐라닌에 의한 중독의 특징은 긴 잠복기이다. 첫 증상은 보통 섭취 후 2~3일 후에 나타나며 경우에 따라서는 3주까지 걸릴 수 있다.오렐라닌 중독의 첫 증상은 일반적인 독감(콧물, 구토, 복통, 두통, 근육통 등)과 유사하며, 이러한 증상들은 신부전 초기 단계(과도한 갈증, 빈뇨, 신장 주변 통증)와 함께 결국 소변량이 감소하거나 존재하지 않거나 신장 fa의 다른 증상들이다.일루어가 발생하다.치료하지 않고 방치하면 죽음이 뒤따를 것이다.
생쥐의 오렐라닌 LD는50 체중 [10][11]1kg당 12~20mg이다. 이는 2주 이내에 사망에 이르는 용량이다.인간의 오렐라닌 관련 버섯 중독 사례로 볼 때 인간의 치사량은 상당히 낮은 것으로 보인다.
치료
비록 오렐라닌 중독에 대한 알려진 해독제는 없지만, 조기 입원은 때때로 심각한 부상을 예방하고 보통 죽음을 예방할 수 있습니다.연구가 진행 중입니다.일부 치료법은 항산화제 치료와 코르티코스테로이드를 사용하여 환자들이 신장 기능 [12]부전으로부터 회복하도록 돕는다.
「 」를 참조해 주세요.
레퍼런스
- ^ Oubrahim H.; Richard J.-M.; Cantin-Esnault D.; Seigle-Murandi F.; Trecourt F (1997). "Novel methods for identification and quantification of the mushroom nephrotoxin orellanine". Journal of Chromatography. 758 (1): 145–157. doi:10.1016/S0021-9673(96)00695-4. PMID 9181972.
- ^ a b Dehmlow, Eckehard V.; Schulz, Hans-Joachim (1985). "Synthesis of orellanine the lethal poison of a toadstool - ScienceDirect". Tetrahedron Letters. 26 (40): 4903–4906. doi:10.1016/S0040-4039(00)94981-5.
- ^ a b c d Tiecco, Marcello; Tingoli, Macro; Testaferri, Lorenzo; Chianelli, Donatella; Wenkert, Ernest (1985). "Total synthesis of orellanine : The lethal toxin of Cortinarius orellanus fries mushroom - ScienceDirect". Tetrahedron. 42 (5): 1475–1485. doi:10.1016/S0040-4020(01)87367-1.
- ^ a b c d Dinis-Oliveira, Ricardo Jorge; Soares, Mariana; Rocha-Pereira, Carolina; Carvalho, Félix (2015). "Human and experimental toxicology of orellanine". Human & Experimental Toxicology. 35 (9): 1016–1029. doi:10.1177/0960327115613845. PMID 26553321. S2CID 7230959.
- ^ Deutsch, Christopher J.; Swallow, Daniel (24 September 2012). "Deliberate ingestion of "magic" mushrooms may also cause renal failure". BMJ. 345: e6388. doi:10.1136/bmj.e6388. ISSN 1756-1833. PMID 23008206. S2CID 32430024.
- ^ a b c Richard, Jean-Michel; Louis, Josette; Cantin, Danielle (1 March 1988). "Nephrotoxicity of orellanine, a toxin from the mushroom Cortinarius orellanus". Archives of Toxicology. 62 (2–3): 242–245. doi:10.1007/BF00570151. ISSN 0340-5761. PMID 3196164. S2CID 36515278.
- ^ Antkowiak W.Z., Gessner W. P. (1975). "Isolation and characteristics of toxic components of Cortinarius orellanus, Fries". Bulletin de l'Académie Polonaise des Sciences, Série des Sciences Chimiques. 23: 729–733.
- ^ Antkowiak Wieław Z., Gessner Wiesł P. (1979). "The structures of orellanine and orelline". Tetrahedron Letters. 20 (21): 1931–1934. doi:10.1016/s0040-4039(01)86882-9.
- ^ Høiland K (1994). "Suppression of the toxic effect of soluble aluminium on fungi by dermocybin-1-ß-D-glucopyranoside and orellanine from Cortinarius sanguineus and C. orellanoides". Nord. J. Bot. 14 (2): 221–228. doi:10.1111/j.1756-1051.1994.tb00591.x.
- ^ Prast H; Werner ER; Pfaller W; Moser M. (1988). "Toxic properties of the mushroom Cortinarius orellanus. I. Chemical characterization of the main toxin of Cortinarius orellanus (Fries) and Cortinarius speciosissimus (Kuhn & Romagn) and acute toxicity in mice". Archives of Toxicology. 62 (1): 81–8. doi:10.1007/bf00316263. PMID 3190463. S2CID 24495871.
- ^ Holmdahl, J (2001). Mushroom poisoning: Cortinarius speciosissimus nephrotoxicity (PDF). Göteborg University. Archived from the original (PDF) on February 4, 2012.
- ^ Rachael G. Kilner; et al. (1999). "Acute renal failure from intoxication by Cortinarius orellanus: recovery using anti-oxidant therapy and steroids". Nephrology Dialysis Transplantation. 14 (11): 2779–2780. doi:10.1093/ndt/14.11.2779-a. PMID 10534536.
외부 링크
- 코티나리우스 루벨루스 태평양 북서쪽 균류, 특징적인 균류 4번 4