단백질 어그리게이션
Protein aggregation단백질 응집이란 본질적으로 무질서한 단백질이나 잘못 접힌 단백질이 세포내 또는 세포외에서 [1][2]응집(즉, 축적 및 뭉쳐짐)되는 생물학적 현상이다.잘못 접힌 단백질 집합체는 종종 질병과 관련이 있다.사실, 단백질 집합체는 ALS, 알츠하이머, 파킨슨병,[3][4] 프리온병을 포함한 아밀로이드스로 알려진 다양한 질병과 관련이 있습니다.
합성 후, 단백질은 전형적으로 열역학적으로 가장 유리한 특정한 3차원 구조, 즉 본래의 상태로 [5]접힙니다.이러한 접힘 과정은 소수성 효과에 의해 추진됩니다: 단백질의 소수성(물을 두려워하는) 부분이 단백질의 내부에 묻음으로써 세포의 친수성(물을 좋아하는) 환경으로부터 스스로를 보호하는 경향입니다.따라서 단백질의 외부는 전형적으로 친수성인 반면, 내부는 전형적으로 소수성이다.
단백질 구조는 2개의 시스테인 잔기 사이의 비공유 상호작용 및 디술피드 결합에 의해 안정화된다.비공유 상호작용에는 이온 상호작용과 약한 반데르발스 상호작용이 포함된다.이온 상호작용은 음이온과 양이온 사이에서 형성되고 단백질을 안정시키는 데 도움을 주는 소금 다리를 형성합니다.Van der Waals 상호작용에는 비극성 상호작용(예: 런던 분산력)과 극성 상호작용(예: 수소 결합, 다이폴-다이폴 결합)이 포함된다.이것들은 알파나선이나 베타시트를 형성하는 것과 같은 단백질의 2차 구조와 3차 구조에서 중요한 역할을 한다.특정 단백질의 아미노산 잔류물 간의 상호작용은 단백질의 최종 구조에서 매우 중요하다.
아미노산 배열의 변화와 함께 발생할 수 있는 비공유 상호작용에 변화가 있을 때, 단백질은 잘못 접히거나 전개되기 쉽다.이 경우 세포가 단백질의 재접힘을 돕지 않거나 전개된 단백질을 분해하지 않으면 전개된/잘못 접힌 단백질이 응집되어 단백질의 노출된 소수성 부분이 다른 [6][7]단백질의 노출된 소수성 패치와 상호작용할 수 있다.형성될 수 있는 단백질 집합체에는 세 가지 주요 유형이 있습니다: 비정질 집합체, 올리고머, 그리고 아밀로이드 섬유입니다.[8]
원인들
단백질 응집 현상은 다양한 원인에 의해 발생할 수 있다.이러한 원인을 분류할 수 있는 4가지 클래스가 있습니다.이러한 클래스는 다음과 같습니다.
돌연변이
DNA 염기서열에서 발생하는 돌연변이는 단백질의 아미노산 염기서열에 영향을 줄 수도 있고 그렇지 않을 수도 있다.배열이 영향을 받을 때, 다른 아미노산은 단백질의 접힘에 영향을 미치는 측쇄 사이의 상호작용을 바꿀 수 있다.이는 단백질의 소수성 영역을 노출시켜 동일한 잘못 접힌/접히지 않은 단백질 또는 [citation needed]다른 단백질과 결합시킬 수 있다.
영향을 받은 단백질 자체의 돌연변이 외에도 단백질 응집은 리폴딩 경로(분자 샤페론) 또는 유비퀴틴 단백질 경로(유비퀴틴 연결효소)[9]와 같은 조절 경로의 단백질 돌연변이를 통해 간접적으로 발생할 수 있다.샤페론은 단백질이 접히는 안전한 환경을 제공함으로써 단백질 리폴딩을 돕는다.유비퀴틴은 유비퀴틴 [citation needed]변형을 통해 분해하기 위해 표적 단백질을 결합시킨다.
단백질 합성에 관한 문제
단백질 어그리게이션은 전사 또는 번역 중에 발생하는 문제로 인해 발생할 수 있습니다.전사 중에 DNA는 mRNA로 복사되어 mRNA를 형성하기 [10]위해 RNA 처리를 거치는 pre-mRNA 가닥을 형성한다.번역하는 동안, 리보솜과 tRNA는 mRNA 서열을 아미노산 [10]서열로 변환하는 것을 돕는다.두 단계 중 문제가 발생하여 잘못된 mRNA 가닥 및/또는 잘못된 아미노산 배열을 만들면 단백질이 잘못 접혀 단백질 응집을 [citation needed]초래할 수 있습니다.
환경적 스트레스
극단적인 온도와 pH 또는 산화적 스트레스와 같은 환경적 스트레스도 단백질 [11]응집을 초래할 수 있습니다.그러한 질병 중 하나가 클리오글로불린혈증이다.
극단적인 온도는 아미노산 잔류물 사이의 비공유 상호작용을 약화시키고 불안정하게 할 수 있다.단백질의 pH 범위를 벗어나는 pHs는 아미노산의 양성자화 상태를 변화시켜 비공유 상호작용을 증가시키거나 감소시킬 수 있다.이것은 또한 덜 안정적인 상호작용으로 이어질 수 있고 단백질이 전개되는 결과를 초래할 수 있다.
산화 스트레스는 활성산소종(ROS)과 같은 라디칼에 의해 발생할 수 있습니다.이러한 불안정한 라디칼은 아미노산 잔류물을 공격하여 측쇄(예: 방향족 측쇄, 메티오닌 측쇄)의 산화 및/또는 폴리펩타이드 [12]결합의 분열을 초래할 수 있습니다.이것은 단백질을 올바르게 함께 고정시키는 비공유 상호작용에 영향을 미칠 수 있고, 이것은 단백질의 불안정성을 야기할 수 있고, 단백질이 [11]펼쳐지는 것을 야기할 수 있습니다.
에이징
세포는 단백질 응집체를 되감거나 분해할 수 있는 메커니즘을 가지고 있다.그러나 세포가 노화됨에 따라 이러한 제어 메커니즘은 약해지고 세포는 [11]집계를 분해할 수 없게 됩니다.
단백질 집적이 노화의 원인 과정이라는 가설은 지연 노화의 일부 모델이 있기 때문에 현재 시험할 수 있다.단백질 골재의 개발이 노화에 의존하지 않는 과정이었다면, 노화를 늦추는 것은 시간이 지남에 따라 단백질 독성의 속도에 영향을 주지 않을 것이다.그러나 노화가 단백질 독성에 대한 보호 메커니즘의 활동 감소와 관련이 있는 경우, 느린 노화 모델은 응집 및 단백질 독성의 감소를 나타낼 것이다.이 문제를 해결하기 위해 C. elegans에서 몇 가지 독성 검사가 수행되었습니다.이러한 연구는 노화 조절 경로인 인슐린/IGF 신호(IIS)의 활성을 감소시키는 것이 신경변성 관련 독성 단백질 응집으로부터 보호하는 것으로 나타났다.IGF-1 신호 경로의 활성을 감소시키는 것이 알츠하이머 모델 쥐를 [13]질병과 관련된 행동 및 생화학적 손상으로부터 보호함으로써 이 접근법의 타당성이 포유동물에서 테스트되고 확인되었다.
집약 현지화
여러 연구에서 단백질 집적에 대한 세포 반응이 잘 조절되고 체계적이라는 것이 밝혀졌다.단백질 집단은 세포 내의 특정 영역에 국한되며, 원핵생물(E.coli)과 진핵생물(east, 포유동물 세포)[citation needed]에서 이러한 국소화에 대한 연구가 이루어졌다.
박테리아
박테리아의 응집체는 비대칭적으로 세포의 극 중 하나인 "나이든 극"에 도달한다.세포가 분열된 후, 나이가 많은 극을 가진 딸 세포는 단백질 집적을 얻고, 그 집적이 없는 딸 세포보다 더 느리게 성장한다.이는 세균 [14]집단에서 단백질 응집체를 감소시키기 위한 자연 선택 메커니즘을 제공합니다.
효모균
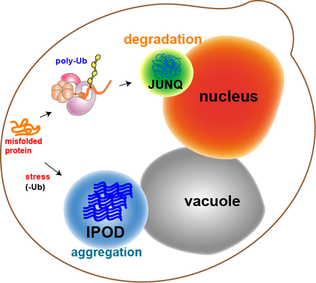
효모세포에 있는 대부분의 단백질 응집체는 분자 샤페론에 의해 다시 형성된다.그러나 산화적으로 손상된 단백질이나 분해로 표시된 단백질과 같은 일부 응집물은 리폴딩할 수 없다.오히려, 그들이 최종적으로 들어갈 수 있는 두 개의 칸이 있다.단백질 응집체는 핵막 근처인 죽탄핵품질관리실(JUNQ) 또는 효모세포 [11]내 액포 근처인 불용성 단백질 퇴적물(IPod)에서 국재할 수 있다.단백질 응집체는 유비쿼터스화되어 분해의 대상이 될 때 JUNQ에서 국부화된다.응집된 불용성 단백질은 보다 영구적인 퇴적물로 아이팟에서 국소화된다.여기 있는 단백질이 [15]자가파지에 의해 제거될 수 있다는 증거가 있다.이 두 경로는 단백질이 과로할 [15]때 단백질이 아이팟으로 오는 경향이 있다는 점에서 함께 작용한다.
포유류의 세포
포유동물 세포에서, 이러한 단백질 집합체는 "아그레솜"이라고 불리며 세포가 병에 걸렸을 때 형성된다.이는 세포가 변이될 때 발생할 수 있는 이종 단백질이 세포에 존재할 때 응집체가 형성되는 경향이 있기 때문이다.동일한 단백질의 다른 돌연변이는 수용성 종의 확산에서 다른 병원성을 [16]갖는 큰 점까지 다양한 형태의 어그롬을 형성할 수 있다.E3 유비퀴틴 연결효소는 잘못 접힌 단백질을 인식하고 그것들을 유비퀴틴화할 수 있다.그런 다음 HDAC6는 유비퀴틴 및 운동단백질 다인(dynein)에 결합하여 표시된 골재를 마이크로튜브 조직센터(MTOC)로 가져올 수 있습니다.거기서, 그것들은 MTOC를 둘러싼 구 모양으로 뭉쳐진다.그들은 샤페론과 프로테아솜을 가져와 자가포기를 [17]활성화시킨다.
소거
세포에는 단백질 응집체를 제거하는 두 가지 주요 단백질 품질 관리 시스템이 있습니다.잘못 접힌 단백질은 바이샤페론 시스템에 의해 리폴드되거나 유비퀴틴 프로테아솜 시스템 또는 오토파지에 [18]의해 분해될 수 있습니다.
리폴드
본 발명의 바이샤페론 시스템은 Hsp70(대장균 내 DnaK-DnaJ-GrpE, 효모 내 Ssa1-Ydj1/Sis1-Se1/Fe1) 및 Hsp100(대장균 내 ClpB 및 효모 내 Hsp104)을 이용하여 단백질 분해한다.[19]
Hsp70은 단백질 집합체와 상호작용하여 Hsp100을 모집한다.Hsp70은 활성화된 Hsp100을 안정화시킨다.Hsp100 단백질은 단일 폴리펩타이드를 분해하는 스레드 활성에 사용되는 방향족 모공 루프를 가지고 있습니다.이 스레드화 활성은 N-말단, C-말단 또는 폴리펩타이드 중간에서 시작할 수 있습니다.폴리펩타이드는 일련의 단계에서 Hsp100을 통해 각 [19]단계에서 ATP를 이용하여 전위됩니다.폴리펩타이드가 펼쳐지고 나서 스스로 또는 열충격 [20]단백질의 도움을 받아 다시 팔 수 있게 됩니다.
열화
잘못 접힌 단백질은 유비퀴틴단백질계(UPS)를 통해 제거될 수 있다.이것은 단백질의 분해를 표시하기 위해 단백질을 유비쿼터스화하는 E1-E2-E3 경로로 구성된다.진핵생물에서 단백질은 26S 프로테아솜에 의해 분해된다.포유동물 세포에서 E3 연결효소인 카르복시 말단 Hsp70 상호작용단백질(CHIP)은 Hsp70 결합단백질을 표적으로 한다.효모에서 E3 연결효소 Doa10 및 Hrd1은 소포체 [21]단백질에 대해 유사한 기능을 가진다.분자 수준에서, 골재의 분해율은 단백질마다 다르며, 이는 단백질 분해효소 [22]분자의 접근성이 다르기 때문이다.
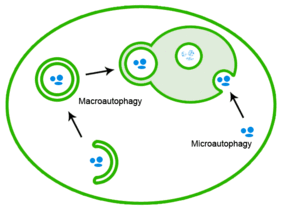
잘못 접힌 단백질은 또한 단백질 집합체가 [21]리소좀으로 전달되는 자동 파지를 통해 제거될 수 있다.
독성
성숙한 단백질 집합체 자체가 독성이 있다고 여겨졌지만, 사실은 가장 [23][24]독성이 강한 것은 미성숙한 단백질 집합체라는 증거가 있다.이러한 집합체의 소수성 패치는 세포의 다른 구성요소와 상호작용하여 손상시킬 수 있다.단백질 응집체의 독성은 세포성분 격리, 활성산소종의 생성 및 막 내 특정 수용체에 대한 결합 또는 [25]막 파괴와 관련이 있다는 가설이다.정량적 분석을 사용하여 고분자량 종이 막 [26]투과성을 담당한다는 것을 확인했습니다.체외 단백질 응집체는 인공 인지질 이중층을 불안정하게 하여 [citation needed]막의 투과성을 초래할 수 있는 것으로 알려져 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ Aguzzi, A.; O'Connor, T. (March 2010). "Protein aggregation diseases: pathogenicity and therapeutic perspectives". Nature Reviews Drug Discovery. 9 (3): 237–48. doi:10.1038/nrd3050. PMID 20190788. S2CID 5756683.
- ^ Stefani, M.; Dobson, CM. (November 2003). "Protein aggregation and aggregate toxicity: new insights into protein folding, misfolding diseases and biological evolution". J Mol Med (Berl). 81 (11): 678–99. doi:10.1007/s00109-003-0464-5. PMID 12942175. S2CID 23544974.
- ^ De Felice, FG.; Vieira, MN.; Meirelles, MN.; Morozova-Roche, LA.; Dobson, CM.; Ferreira, ST. (July 2004). "Formation of amyloid aggregates from human lysozyme and its disease-associated variants using hydrostatic pressure". FASEB J. 18 (10): 1099–101. doi:10.1096/fj.03-1072fje. PMID 15155566. S2CID 13647147.
- ^ Tanzi, RE.; Bertram, L. (February 2005). "Twenty years of the Alzheimer's disease amyloid hypothesis: a genetic perspective". Cell. 120 (4): 545–55. doi:10.1016/j.cell.2005.02.008. PMID 15734686. S2CID 206559875.
- ^ Brüning, Ansgar; Jückstock, Julia (2015-01-01). "Misfolded proteins: from little villains to little helpers in the fight against cancer". Frontiers in Oncology. 5: 47. doi:10.3389/fonc.2015.00047. PMC 4338749. PMID 25759792.
- ^ Gething, MJ.; Sambrook, J. (January 1992). "Protein folding in the cell". Nature. 355 (6355): 33–45. Bibcode:1992Natur.355...33G. doi:10.1038/355033a0. PMID 1731198. S2CID 4330003.
- ^ Roberts, CJ. (December 2007). "Non-native protein aggregation kinetics". Biotechnol Bioeng. 98 (5): 927–38. doi:10.1002/bit.21627. PMID 17705294. S2CID 21787377.
- ^ Cox, David L.; Nelson, Michael M. (2013). Lehninger Principles of Biochemistry. New York: W.H. Freeman. p. 143. ISBN 978-1-4292-3414-6.
- ^ Berke, Sarah J Shoesmith; Paulson, Henry L (2003-06-01). "Protein aggregation and the ubiquitin proteasome pathway: gaining the UPPer hand on neurodegeneration". Current Opinion in Genetics & Development. 13 (3): 253–261. doi:10.1016/S0959-437X(03)00053-4. PMID 12787787.
- ^ a b Weaver, Robert F. (2012). Molecular Biology. New York: McGraw-Hill. pp. 122–156, 523–600. ISBN 978-0-07-352532-7.
- ^ a b c d Tyedmers, Jens; Mogk, Axel; Bukau, Bernd (November 2010). "Cellular strategies for controlling protein aggregation". Nature Reviews Molecular Cell Biology. 11 (11): 777–788. doi:10.1038/nrm2993. PMID 20944667. S2CID 22449895.
- ^ Stadtman, E. R.; Levine, R. L. (2003-07-29). "Free radical-mediated oxidation of free amino acids and amino acid residues in proteins". Amino Acids. 25 (3–4): 207–218. doi:10.1007/s00726-003-0011-2. ISSN 0939-4451. PMID 14661084. S2CID 26844881.
- ^ Morley JF, Brignull HR, Weyers JJ, Morimoto RI (2002). "The threshold for polyglutamine-expansion protein aggregation and cellular toxicity is dynamic and influenced by aging in Caenorhabditiselegans". PNAS. 99 (16): 10417–10422. Bibcode:2002PNAS...9910417M. doi:10.1073/pnas.152161099. PMC 124929. PMID 12122205.
- ^ Bednarska, Natalia G.; Schymkowitz, Joost; Rousseau, Frederic; Van Eldere, Johan (2013-01-01). "Protein aggregation in bacteria: the thin boundary between functionality and toxicity". Microbiology. 159 (9): 1795–1806. doi:10.1099/mic.0.069575-0. PMID 23894132.
- ^ a b Takalo, Mari; Salminen, Antero; Soininen, Hilkka; Hiltunen, Mikko; Haapasalo, Annakaisa (2013-03-08). "Protein aggregation and degradation mechanisms in neurodegenerative diseases". American Journal of Neurodegenerative Disease. 2 (1): 1–14. ISSN 2165-591X. PMC 3601466. PMID 23516262.
- ^ Wan, Wang; Zeng, Lianggang; Jin, Wenhan; Chen, Xinxin; Shen, Di; Huang, Yanan; Wang, Mengdie; Bai, Yulong; Lyu, Haochen; Dong, Xuepeng; Gao, Zhenming (2021). "A Solvatochromic Fluorescent Probe Reveals Polarity Heterogeneity upon Protein Aggregation in Cells". Angewandte Chemie International Edition. 60 (49): 25865–25871. doi:10.1002/anie.202107943. ISSN 1521-3773. PMID 34562048. S2CID 237626399.
- ^ Garcia-Mata, Rafael; Gao, Ya-Sheng; Sztul, Elizabeth (2002-06-01). "Hassles with Taking Out the Garbage: Aggravating Aggresomes". Traffic. 3 (6): 388–396. doi:10.1034/j.1600-0854.2002.30602.x. ISSN 1600-0854. PMID 12010457. S2CID 305786.
- ^ Gregersen, Niels; Bolund, Lars; Bross, Peter (2005-10-01). "Protein misfolding, aggregation, and degradation in disease". Molecular Biotechnology. 31 (2): 141–150. doi:10.1385/MB:31:2:141. ISSN 1073-6085. PMID 16170215. S2CID 36403914.
- ^ a b Mogk, Axel; Kummer, Eva; Bukau, Bernd (2015-01-01). "Cooperation of Hsp70 and Hsp100 chaperone machines in protein disaggregation". Frontiers in Molecular Biosciences. 2: 22. doi:10.3389/fmolb.2015.00022. ISSN 2296-889X. PMC 4436881. PMID 26042222.
- ^ Liberek, Krzysztof; Lewandowska, Agnieszka; Ziętkiewicz, Szymon (2008-01-23). "Chaperones in control of protein disaggregation". The EMBO Journal. 27 (2): 328–335. doi:10.1038/sj.emboj.7601970. ISSN 0261-4189. PMC 2234349. PMID 18216875.
- ^ a b Chen, Bryan; Retzlaff, Marco; Roos, Thomas; Frydman, Judith (2011-08-01). "Cellular Strategies of Protein Quality Control". Cold Spring Harbor Perspectives in Biology. 3 (8): a004374. doi:10.1101/cshperspect.a004374. ISSN 1943-0264. PMC 3140689. PMID 21746797.
- ^ Wan, Wang; Zeng, Lianggang; Jin, Wenhan; Chen, Xinxin; Shen, Di; Huang, Yanan; Wang, Mengdie; Bai, Yulong; Lyu, Haochen; Dong, Xuepeng; Gao, Zhenming (2021). "A Solvatochromic Fluorescent Probe Reveals Polarity Heterogeneity upon Protein Aggregation in Cells". Angewandte Chemie International Edition. 60 (49): 25865–25871. doi:10.1002/anie.202107943. ISSN 1521-3773. PMID 34562048. S2CID 237626399.
- ^ Zhu, YJ.; Lin, H.; Lal, R. (June 2000). "Fresh and nonfibrillar amyloid beta protein(1-40) induces rapid cellular degeneration in aged human fibroblasts: evidence for AbetaP-channel-mediated cellular toxicity". FASEB J. 14 (9): 1244–54. doi:10.1096/fasebj.14.9.1244. PMID 10834946. S2CID 42263619.
- ^ Nilsberth, C.; Westlind-Danielsson, A.; Eckman, CB.; Condron, MM.; Axelman, K.; Forsell, C.; Stenh, C.; Luthman, J.; Teplow, DB.; et al. (September 2001). "The 'Arctic' APP mutation (E693G) causes Alzheimer's disease by enhanced Abeta protofibril formation". Nat Neurosci. 4 (9): 887–93. doi:10.1038/nn0901-887. PMID 11528419. S2CID 13516479.
- ^ Soto C (2003). "Unfolding the role of protein misfolding in neurodegenerative diseases". Nat. Rev. Neurosci. 4 (1): 49–60. doi:10.1038/nrn1007. PMID 12511861. S2CID 205499427.
- ^ Flagmeier P, De S, Wirthensohn DC, Lee SF, Vincke C, Muyldermans S, Knowles TPJ, Gandhi S, Dobson CM, Klenerman D (2017). "Ultrasensitive Measurement of Ca2+Influx into Lipid Vesicles Induced by Protein Aggregates". Angew. Chem. Int. Ed. Engl. 56 (27): 7750–7754. doi:10.1002/anie.201700966. PMC 5615231. PMID 28474754.