에산화티타늄
Titanium ethoxide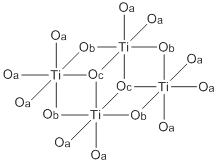 티타늄의 축약 구조()IV) 이산화질소. 이산화질소 리간드는 O's로 대표된다. 이산화 말단 리간드는 오아가, 이중 브리징 리간드는 오브가, 삼각 브리지는 오크가 각각 지정한다. | |
| 이름 | |
|---|---|
| IUPAC 이름 에탄올산염; 티타늄(4+) | |
| 체계적 IUPAC 이름 테트라에탄올레이트 티타늄(4+) | |
| 기타 이름 에틸 타이타네이트, 테트라에틸 타이타네이트 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.019.464 |
| EC 번호 |
|
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| 초티3280164 | |
| 어금질량 | 228.1987 g/mb |
| 외관 | 무색의 액체 |
| 밀도 | 1.088 |
| 비등점 | 150–152 (@10 mmHg) |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
이산화티타늄은 Ti4(OCHCH23)라는 공식을 가진 화학 화합물이다.16 유기용제에 용해되지만 쉽게 가수분해되는 무색의 액체다. 무색 용액으로 상업적으로 판매되고 있다. 티타늄의 알크산화물(IV) 및 지르코늄().IV)는 유기합성 및 재료과학에 사용된다. 그들은 경험적 공식에서 제시된 것보다 더 복잡한 구조를 채택한다.[1]
합성
에산화티타늄은 아민이 존재하는 곳에서 테트라클로라이드 티타늄을 에탄올로 처리하여 제조된다.[2]
- TiCl4 + 4 EtOH + 4 EtN3 → Ti(OTT)4 + 4 EtNHCl3
에산화티타늄의 순도는 일반적으로 양성자 NMR 분광법에 의해 측정된다. Ti(OTT)4 1H NMR(90MHz, 클로로포름-d, ppm): 4.36(쿼터, 8H, CH2), 1.27(트리플릿, 12H, CH3)이다.[3]
구조
두 Ti(OTT)4는 주로 금속 중심 주위에 팔면 조정 환경을 가진 테트라머로 존재한다. 티타늄 중심은 단자 대 알카산화 리간드 브리지에 따라 두 종류가 있다. Zr(OET)4은 구조적으로 비슷하다.[2][4] 이들 화합물의 테트라머 구조를 위한 MO416 코어 구조의 가상 대칭은 C이다2h.[5]
관련 화합물
티타늄메톡사이드
이산화티타늄처럼 티타늄 메톡사이드 Ti(OMe)4는 각 TiIV 금속 센터가 팔면 조정 환경을 갖는 테트라머로서 존재한다.[6]
이소프로산화 티타늄
부피가 큰 알키 그룹과 대조적으로 Ti(OPRi)4는 Ti 센터 주변에 사면체 환경을 가진 모노머로 존재한다. 금속 중심에 대한 이 낮은 수준의 조정은 Pr 그룹의 강체 부피 대 n-alkyl 그룹에 기인하며, 이는 금속 중심 간의 교호작용을 방지하는 역할을 한다.[7]
에산화 지르코늄
에산화 지르코늄은 티타늄 화합물과 유사하지만 동일하지는 않은 방식으로 제조할 수 있다.[8]
- ZrCl4 + 5 NaOEt + EtOH → NaH[Zr(OET)]6 + 4 NaCl
- NaH[Zr(OET)]6 + HCl → Zr(OET)4 + NaCl + 2 Et오호
에산화지르코늄에 대한 보다 일반적인 합성법은 원하는 알코올과 암모니아로 지르코늄 테트라클로라이드를 처리하는 것이다.[8]
- ZrCl4 + 4 ROH + 4 NH3 → Zr(OR)4 + 4 NHCl4
에산화지르코늄은 또한 지르코노세 디클로로이드와 함께 준비될 수 있다.[9]
- CpZrCl22 + 4 EtOH + 2 EtN3 → 2 CpH + 2 EtNHCl3 + Zr(OTT)4
프로포사이드 지르코늄
Zr(OPRn)4도 티타늄 에산화 구조를 채택하고 있다.[4][5]
반응
Ti와 Zr 알코시드는 모두 TiO2 또는 ZrO의2 마이크로 구조 필름을 보관하는 데 사용할 수 있다.
- M(OET)4 + 2 HO2 → MO2 + 4 Et오호
이 필름들은 알카산화물의 가수분해를 통해 형성된다. 그 결과 발생하는 산화물은 화학적으로 회복력이 있다.[10] 이 물질에서 자라는 금속 산화막의 구조는 가수분해를 위한 염기 또는 산성 촉매의 존재에 의해 영향을 받는다. 일반적으로 산성투석은 폴리머 체인의 방향이 무작위이고 선형인 솔을 산출한다. 베이스 매개 변수인 경우 부쉬 클러스터 또는 교차 링크된 네트워크가 생성되는 경우, 이러한 구조물은 용매와 반응 부산물을 가둘 수 있고 젤 코팅을 형성할 수 있다.[11] Ti와IV ZrIV 알코시드는 알켄 중합에 사용되는 지글러-나타 촉매의 잠재적 시동 물질이기도 하다.[10] 가수분해에서 매개체가 결정화되었다. 그들은 성단 외관에는 에토산화물 외에 내부 산화물도 특징으로 한다.[12]
참조
- ^ Ram C. Mehrotra; Singh, Anirudh (1997). "Recent Trends in Metal Alkoxide Chemistry". In Kenneth D. Karlin (ed.). Progress in Inorganic Chemistry. Vol. 46. John Wiley & Sons. pp. 239–454. doi:10.1002/9780470166475.ch4. ISBN 9780470167045.
- ^ a b F. Albert Cotton; Geoffrey Wilkinson; Murillo, C.; Bochmann, M. (1999). Advanced Inorganic Chemistry (6th ed.). New York: John Wiley & Sons. ISBN 978-0-471-19957-1.
- ^ 유기화합물의 통합 스펙트럼 데이터베이스 시스템, 버전 2011. AIST: 일본, 2011년 (2011년 10월 3일 접속)
- ^ a b James A. Ibers (1963). "Crystal and Molecular Structure of Titanium(IV) Ethoxide". Nature. 197 (4868): 686–687. Bibcode:1963Natur.197..686I. doi:10.1038/197686a0. S2CID 4297907.
- ^ a b Day, Victor W.; Klemperer, Walter G.; Pafford, Margaret M. (2001). "Isolation and Structural Characterization of Tetra-n-propyl Zirconate in Hydrocarbon Solution and the Solid State". Inorg. Chem. 40 (23): 5738–5746. doi:10.1021/ic010776g. PMID 11681880.
- ^ Wright, D. A.; Williams, D. A. (1968). "The Crystal and Molecular Structure of Titanium Tetramethoxide". Acta Crystallographica B. 24 (8): 1107–1114. doi:10.1107/S0567740868003766.
- ^ Ghosh, Rajshekhar; Nethaji, Munirathinam; Samuelson, Ashoka G. (2005). "Reversible double insertion of aryl isocyanates into the Ti–O bond of titanium(IV) isopropoxide". J. Organomet. Chem. 690 (5): 1282–1293. doi:10.1016/j.jorganchem.2004.11.038.
- ^ a b Bradley, D. C.; Wardlaw, W. (1951). "Zirconium alkoxides". J. Chem. Soc.: 280–285. doi:10.1039/jr9510000280.
- ^ Gray, Donald R.; Brubaker, Carl H. (1971). "Preparation and characterization of a series of chloroalkoxobis(cyclopentadienyl)zirconium(IV) and dialkoxobis(cyclopentadienyl)zirconium(IV) compounds". Inorg. Chem. 10 (10): 2143–2146. doi:10.1021/ic50104a010.
- ^ a b Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ Schubert, U. (2003). "Sol–Gel Processing of Metal Compounds". In McCleverty, J. A.; Meyer, T. J. (eds.). Comprehensive Coordination Chemistry II. Reference Module in Chemistry, Molecular Sciences and Chemical Engineering. Vol. 7. Pergamon. pp. 629–656. doi:10.1016/B0-08-043748-6/06213-7. ISBN 978-0-12-409547-2.
- ^ Coppens, Philip; Chen, Yang; Trzop, Elżbieta (2014). "Crystallography and Properties of Polyoxotitanate Nanoclusters". Chemical Reviews. 114 (19): 9645–9661. doi:10.1021/cr400724e. PMID 24820889.


