테트라브로마이드 티타늄
Titanium tetrabromide | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 티타늄()IV)브로마이드 | |
| 기타 이름 테트라브로마이드 티타늄 | |
| 식별자 | |
3D 모델(JSmol) | |
| ECHA InfoCard | 100.029.259 |
| EC 번호 |
|
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| 티브르4 | |
| 어금질량 | 367.483 g/1983 g/1973 |
| 외관 | 갈색 결정체 흡습성의 |
| 밀도 | 3.25 g/cm3 |
| 녹는점 | 39°C(102°F, 312K) |
| 비등점 | 230°C(446°F, 503K) |
| 수력화 | |
| 기타 용매의 용해성 | 클로로카본, 벤젠 |
| 구조 | |
| 세제곱, Pa3, Z = 8 | |
| 사면체 | |
| 0 D | |
| 위험 | |
| 산업안전보건(OHS/OSH): | |
주요 위험 | 부식성의 |
| GHS 라벨 표시:[1] | |
 | |
| 위험 | |
| H314 | |
| P260, P264, P280, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P310, P363, P405 | |
| NFPA 704(화재 다이아몬드) | |
| 플래시 포인트 | 불연성 |
| 관련 화합물 | |
기타 음이온 | 티타늄()IV) 염화물 티타늄()IV) 플루오르화 티타늄()IV) 요오드화합물 |
관련 화합물 | 티타늄(III)브로마이드 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
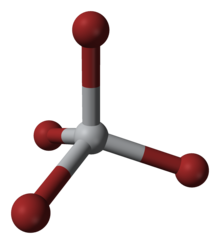
테트라브로마이드는 TiBr이라는 공식을4 가진 화학 화합물이다. 그것은 가장 휘발성이 강한 전이 금속 브롬화물이다. TiBr의4 속성은 TiCl과4 TiI의4 평균이다. 이 4개의 조화된 Ti(IV) 종의 주요 특성으로는 높은 루이스 산도와 비극성 유기 용매에서의 높은 용해성이 있다. TiBr은4 금속 중심부의 d 구성을0 반영하는 직경이다.[2]
준비 및 구조
이 4개의 조정된 복합체는 사면 기하학을 채택한다. 원소로부터 (i), (ii) 카본과 브롬을 이용한2 TiO의 반응을 통해 (kroll 공정 참조), (iii) HBr로 TiCl을4 처리하여 준비할 수 있다.
반응
티타늄 사트라브로마이드는 TiBr4(TiBr)2 및 [TiBr5]−[3]과 같은 인덕트를 형성한다. 2-메틸피리딘(2-Mepy)과 같은 부피가 큰 기증자 리간드를 사용하여 5개의 조정된 유도체를 형성한다. TiBr4(2-MePy)은 적도 평면에서 피리딘과 삼각형이다.[4]
티브르는4 유기합성에 루이스 산화물 촉매로 사용되어 왔다.[5]
티타늄의 사트라브로마이드와 사트라클로라이드는 혼합 사트라할라이드인 TiBrCl4−xx (x = 0-4)의 통계적 혼합물을 주기 위해 반응한다. 이 재분배 반응의 메커니즘은 불확실하다. 하나의 제안된 통로는 조광기의 중간을 유발한다.[6]
안전
TiBr은4 히드로브롬산으로 알려진 브롬화수소를 방출하기 위해 잠재적으로 위험할 수 있는 수소를 급수화한다.
참조
- ^ "Titanium tetrabromide". pubchem.ncbi.nlm.nih.gov. Retrieved 12 December 2021.
- ^ Holleman, A.F.; Wiberg, E. "In 유기화학" 학술언론: 샌디에이고, 2001. ISBN 0-12-352651-5.
- ^ Colin S. Creaser & J. Alan Creighton (1975). "Pentachloro- and pentabromo-titanate(IV) ions". J. Chem. Soc., Dalton Trans. (14): 1402–1405. doi:10.1039/DT9750001402.
- ^ Hensen, K.; Lemke, A.; Bolte, M. (2000). "Tetrabromo(2-methylpyridine-N)-titanate(IV)". Acta Crystallographica. C56 (12): e565–e566. doi:10.1107/S0108270100015407.
- ^ B. Patterson, S. Marumoto & S. D. Rychnovsky (2003). "Titanium(IV)-Promoted Mukaiyama Aldol-Prins Cyclizations". Org. Lett. 5 (17): 3163–3166. doi:10.1021/ol035303n. PMID 12917007.
- ^ S. P. Webb & M. S. Gordon (1999). "Intermolecular Self-Interactions of the Titanium Tetrahalides TiX4 (X = F, Cl, Br)". J. Am. Chem. Soc. 121 (11): 2552–2560. doi:10.1021/ja983339i.