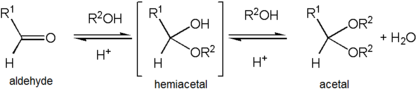
아세탈
Acetal아세탈은 연결2 RC(OR')2를 가진 기능군입니다.여기서, R군은 유기 조각(탄소 원자, 임의의 다른 원자가 부착된 수소) 또는 수소가 될 수 있으며, R군은 수소가 아닌 유기 조각이어야 한다.두 개의 R' 그룹은 서로 동등하거나('대칭 아세탈'), 그렇지 않을 수 있습니다('혼합 아세탈').아세탈은 알데히드 또는 케톤에서 형성되며, 알데히드 또는 케톤으로 변환되며, 중심탄소에서의 산화상태는 동일하지만 유사한 카르보닐 화합물과 비교하여 화학적 안정성과 반응성이 크게 다르다.중심 탄소 원자는 4개의 결합을 가지고 있으며, 따라서 포화 상태이며 사면체 형상을 가지고 있습니다.
케탈이라는 용어는 알데히드가 아닌 케톤(수소가 아닌 R 그룹 유기 조각)과 관련된 구조를 식별하기 위해 사용되기도 하며, 역사적으로 아세탈이라는 용어는 알데히드 관련 사례(중앙 [1]탄소 위에 R 대신 최소 1개의 수소를 포함)에 대해 특별히 사용되었다.IUPAC는 당초 케탈이라는 단어의 사용을 전면 폐지했으나 그 이후 결정을 번복했다.그러나 역사적 사용과는 달리 케탈은 이제 알데히드 및 케톤 유래 구조를 모두 포함하는 용어인 아세탈의 하위 집합이다.
R기 중 하나가 첫 번째 원자로 산소를 갖는 경우(즉, 중앙 탄소에 단결합된 산소가 2개 이상 있음), 관능기는 대신 오르토에스터이다.R의 변화와는 대조적으로, 두 R' 그룹은 모두 유기 조각이다.1개의 R'이 수소일 경우, 관능기는 헤미아세탈이며, 양쪽이 H일 경우 관능기는 케톤 하이드레이트 또는 알데히드 하이드레이트이다.
아세탈의 형성은 헤미아세탈의 수산기가 양성자가 되어 물로서 소실될 때 발생한다.생성된 탄수화물은 알코올 분자에 의해 빠르게 공격됩니다.부착된 알코올로 인해 양성자가 손실되면 아세탈이 생성됩니다.
아세탈은 헤미아세탈에 비해 안정적이지만 그 형성은 에스테르와 마찬가지로 가역적 평형이다.아세탈을 생성하기 위한 반응으로, 예를 들어 Dean-Stark 장치를 사용하여 반응 혼합물에서 물을 제거하여 제품이 헤미아세탈로 가수 분해되지 않도록 해야 합니다.아세탈의 형성은 존재하는 총 분자 수를 감소시키므로(글루소닐 + 2 알코올 → 아세탈 + 물) 엔트로피와 관련하여 일반적으로 바람직하지 않다.장내적으로 바람직하지 않은 한 가지 상황은 두 개의 분리된 알코올 분자(디올 + 디올 → 아세탈 + 물)가 아닌 단일 디올 분자를 사용하는 경우이다.엔트로피 비용을 회피하는 또 다른 방법은 알코올 자체를 단순 첨가하는 것이 아니라 기존의 아세탈형 시약을 OR'기 공여체로 사용하여 아세탈 교환에 의한 합성을 수행하는 것입니다.이 방법에 사용되는 시약 중 하나가 오르토에스테르입니다.이 경우 잔류 오르토에스테르 분자를 가수분해하면 아세탈 생성물과 함께 생성된 물이 파괴되고, 이 부작용으로 인해 알코올이 많아져 주반응에 이용된다.
아세탈은 염기에 의한 가수분해 및 많은 산화 및 환원제에 대해 안정적이기 때문에 유기합성에서 카르보닐기의 보호기로 사용된다.그들은 분자 내의 카르보닐을 보호할 수 있고 (알코올과 일시적으로 반응시켜) 디올을 보호할 수 있다.즉, 카르보닐이나 알코올, 또는 둘 다 반응성을 조절해야 하는 분자의 일부가 될 수 있습니다.
다양한 특정 카르보닐 화합물은 아세탈 형태에 대한 특별한 이름을 가지고 있다.예를 들어, 포름알데히드에서 형성된 아세트(중앙 탄소에 부착된 두 개의 수소)는 때때로 포름[2] 또는 메틸렌디옥시기라고 불립니다.아세톤에서 생성된 아세탈은 아세톤화물이라고도 합니다.
좀 더 일반적인 의미로 사용되는 X,Y-acetal이라는 용어는 또한 두 개의 헤테로아톰 X와 Y를 가진 탄소로 구성된 모든 기능기를 가리킵니다.예를 들어 N,O-acetal은 RRC(OR)(NR')(2R,R' ≠ H)형12 화합물, S,S-acetal은 RRC(SR)(SR')(R,R ≠ H)형12 화합물, S-acetal은 Thio라고도 한다.
아세탈화
아세탈화는 아세탈(또는 케탈)의 형성을 수반하는 유기 반응이다.아세탈 형성의 한 가지 방법은 케톤 또는 알데히드에 알코올을 친핵적으로 첨가하는 것입니다.아세탈화는 가역적인 반응이기 때문에 보호기를 만들기 위해 유기 합성에 종종 사용된다.
아세탈화는 물의 제거와 함께 산성 촉매 작용을 합니다. 아세탈은 기본 조건에서는 형성되지 않습니다.반응 시스템에서 물을 제거하거나 분자 체 또는 산화 알루미늄으로 물을 가두면 반응이 아세탈로 유도될 수 있습니다.
1의 카르보닐기는 하이드로늄에서 양성자를 얻는다.프로톤화 카르보닐기 2는 알코올의 친핵 첨가를 위해 활성화된다.구조 2a와 2b는 중합체이다.물에 의한 3의 탈양성 후 헤미아세탈 또는 헤미케탈 4를 형성한다.4의 히드록실기는 양성자화되며 옥소늄 이온 6은 두 번째 알코올기를 수용하여 아세탈 8로 최종 탈양성된다.역반응은 같은 산성배지에 물을 첨가함으로써 일어난다.아세탈은 기본 배지에 대해 안정적입니다.아세탈화 또는 교차 아세탈화에서 디올은 아세탈과 반응하거나 두 개의 다른 아세탈이 서로 반응합니다.이것은 모든 반응 단계가 평형이기 때문에 가능하다.
예
- 벤질리덴 아세탈, 보호군
- 디메톡시메탄, 용매, 메틸알, a.k.a. 포르말
- 다이옥소란
- 금속알데히드
- 파라알데히드
- 1,3,5-트리옥산
- 페닐술포닐에틸리덴(PSE) 아세탈은 아릴술포닐 아세탈의 일례이며,[3] 예를 들어 보호기를 선택적으로 도입 및 제거하는 내산 가수분해성과 같은 비정형 특성을 가진다.
- 탄수화물과 다른 다당류에 있는 대부분의 글리코시드 결합은 아세탈 [4]결합이다.
- 셀룰로오스는 폴리아세탈의 흔한 예이다.
많은 화합물이 아세탈 관능기를 포함하고 있지만, 적어도 두 가지 아세탈 화합물은 줄여서 "아세탈"이라고 불립니다.
- "아세탈" 또는 "폴리아세탈"이라고도 알려진 폴리옥시메틸렌(POM) 플라스틱은 폴리아세탈(및 폴리에테르)과 포름알데히드의 중합체입니다.
- 1,1-디에톡시에탄(아세트알데히드 디에틸 아세탈)은 증류 [5]음료의 중요한 향미 화합물이다.
「 」를 참조해 주세요.
레퍼런스
- ^ IUPAC, 화학 용어집, 제2판('골드북') (1997).온라인 수정판: (2006–) "ketals" . doi : 10.1351 / goldbook . K03376
- ^ 모리슨, 로버트 T.와 보이드, 로버트 N., "유기화학(6th ed)" p683.프렌티스 홀 주식회사(1992)
- ^ Chéry, Florence; Rollin, Patrick; De Lucchi, Ottorino; Cossu, Sergio (2000). "Phenylsulfonylethylidene (PSE) acetals as atypical carbohydrate-protective groups". Tetrahedron Letters. 41 (14): 2357–2360. doi:10.1016/s0040-4039(00)00199-4. ISSN 0040-4039.
- ^ IUPAC, 화학 용어집, 제2판('골드북') (1997).온라인 수정판: (2006–) glycosides.doi:10.1351/goldbook.G02661
- ^ 식음료 내 휘발성 화합물, ISBN 0-8247-8390-5, https://books.google.com/books?id=_OvXjhLUz-oC, 페이지 554