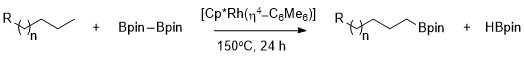보릴레이션
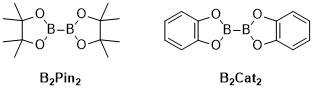
Borylation금속으로 분석된 C-H 보릴레이션 반응은 전환 금속 촉매 유기 반응으로, 편향적이고 방향성 있는 C-H 본드의 기능화를 통해 오르간오보론 화합물을 생성하므로 탄소-수소 본드 활성화에 유용한 반응이다.[1]금속으로 분석된 C-H 보릴레이션 반응은 전환 금속을 활용하여 C-H 결합을 C-B 결합으로 직접 변환한다.이 경로는 값싸고 풍부한 탄화수소 시작 물질을 사용하고 사전 기능화된 유기화합물을 제한하며 독성 부산물을 줄이고 생물학적으로 중요한 분자의 합성을 합리화함으로써 기존의 보릴레이션 반응에 비해 유리할 수 있다.[2][3]붕소산과 붕소 에스테르는 보릴화 반응을 통해 유기 분자로 통합된 흔한 보릴 그룹이다.[4]붕소산은 3가 붕소를 함유한 유기 화합물로, 알킬 대체물 1개와 히드록실 2개를 함유하고 있다.마찬가지로 붕소 에스테르는 알킬 대체물 1개와 에스테르 그룹 2개를 보유하고 있다.붕소산과 에스테르는 붕소에 직접 결합된 탄소군(R)의 종류에 따라 분류되는데, 예를 들어 알킬-, 알케닐-, 알킬-, 아릴-보론 에스테르 등이 그것이다.전이 금속 촉매 보릴레이션 반응을 위해 유기 화합물에 붕소 에스테르를 통합하는 가장 일반적인 유형의 시동 물질은 일반 공식(RO)2B-B(OR)를 가지고 있다.2예를 들어 bis(피나콜라토)diboron(BPin22)과 bis(카테콜라토)diborane(BCAT22)은 이 일반 공식의 일반적인 붕소 공급원이다.[5]
붕소 에스테르나 산의 붕소 원자는 빈 p 궤도(pootal orbit)를 가지고 혼합되어 이들2 집단이 루이스 산으로 활동할 수 있게 한다.붕소산과 에스테르의 C-B 결합은 1.55-1.59 å 범위의 일반적인 C-C 단일 결합보다 약간 길다.C-C 채권에 비해 긴 C-B 결합은 또한 C-C 채권의 결합 에너지(C–B의 경우 323 kJ/mol 대 C–C의 경우 358 kJ/mol)보다 약간 적은 결합 에너지를 초래한다.[6]탄소-수소 결합은 약 1.09 09의 결합 길이를 가지며, 결합 에너지는 약 413 kJ/mol이다.따라서 C-B 채권은 일반적으로 비활동적인 C-H 채권을 대체하는 채권으로서 유용한 중간이다.
오르가노보론 화합물은 탄소보론 결합을 포함하는 유기 화합물이다.오르가노보론 화합물은 C-X(X = Br, Cl), C-O, C–N 또는 C–C 결합으로 쉽게 변환될 수 있기 때문에 화학 합성에 광범위하게 응용된다.C-B 결합의 다용성 때문에 유기 화합물에 통합하기 위한 수많은 프로세스가 개발되었다.[7]오르간오보론 화합물은 전통적으로 그리그나드 시약으로부터 수력보존 또는 이변반응을 통해 합성된다.[8]보릴레이션은 대안을 제시한다.
금속성 C-H 보릴레이션 반응
알리파카틱 C-H 보릴레이션
하트비히에서 처음 설명한 바와 같이, 1차 C-H 본드에 대해 높은 선택성으로 선택적으로 알칸을 Cp*Rh(--CMe466)를 촉매로 사용하여 보릴링할 수 있다.[9]특히 1차 C-H 본드의 선택성은 탄소-수소 체인의 이질성 존재에서도 배타적이다.메틸 C-H 결합의 로듐 촉매 보릴레이션은 이형 원자의 위치에 의존하지 않고 선택적으로 발생한다.보릴화는 아세탈, 에테르, 아민, 알킬 플루오르화물의 범위에서 최소 강직적으로 방해를 받고 최소 전자가 풍부한 일차 C-H 결합에서 선택적으로 발생한다.[10]또한 일차 C-H 본드가 없을 경우, 예를 들어 사이클로헥산이 기질인 경우 어떠한 반응도 나타나지 않는다.
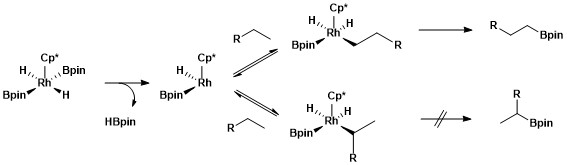
1차 알카인 결합의 선택적 기능화는 2차 알킬-금속 복합체의 형성에 비해 운동학적, 열역학적으로 유리한 1차 알킬-금속 복합체가 형성되기 때문이다.[11]
1차 알킬 콤플렉스와 2차 알킬 콤플렉스의 안정성은 몇 가지 요인에 기인할 수 있다.첫째, 1차 알킬 콤플렉스는 2차 알킬 콤플렉스보다 강직하게 선호된다.둘째, 금속-알킬 복합체의 α-탄소에 부분 음전하가 존재하는 경우가 많으며 1차 알킬 리간드는 2차 알킬 리간드보다 부분 음전하를 더 잘 지지한다.로듐 촉매를 이용한 알리파틱 C-H 보릴화의 선택성의 기원은 수소-중수소 교환이라고 하는 기계론적 연구의 한 유형을 사용하여 조사되었다.교환된 H/D는 2차 C-H 본드에 대한 1차 금속-알킬 중간물에 대한 1차 금속-알킬 중간의 선택적 세분화와 2차 금속-알킬 중간의 1차 금속-알킬 중간의 선택적 기능화에 의해 아래에 제시된 전체 공정의 재열성을 보여주었다.[12]
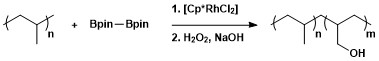
알리파틱 C–H 보릴레이션의 합성 효용성이 보릴화를 통한 폴리머의 개조에 적용되어 산화에 이어 히드록실 기능화된 폴리머를 형성하고 있다.[13]
방향제 C-H 보릴레이션
스테릭 지시 아레네스의 C-H 보릴레이션
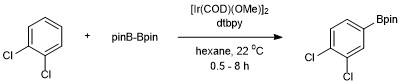
활성화되지 않은 탄화수소(벤젠)의 촉매 C-H 보리의 첫 번째 예는 Smith와 Iverson이 Ir(Cp*)(H)(Bpin)을 촉매로 사용하여 보고하였다.그러나 이 시스템의 효율은 낮아서 150 °C에서 120시간 후 3회만 턴오버할 수 있었다.[14]하트비히와 동료들에 의한 수많은 후속 개발은 아렌 보릴레이션을 위한 효율적이고 실용적인 조건들로 이어졌다.아로마틱 C-H 보릴레이션은 존 F에 의해 개발되었다. 하르트비히와 이시야마는 디보론 시약 비스(피나콜라토)디보론을 사용하여 4,4'-디-티르트-부틸비피리딘(dtbpy)과 [Ir(COD)(OME)]2[15] 촉매제를 사용했다.이 촉매 시스템을 사용하여 방향족 C-H 결합의 보릴레이션은 시작 아레네의 강직 효과에 의해 제어되는 섭열성과 함께 발생한다.방향족 C-H 본드의 기능화를 위한 선택성은 정형 대체물이 없는 C-H 본드를 사용할 수 있을 때 대체물질에 대한 반응이 발생하지 않는다는 일반적인 규칙에 따른다.[11]기능 그룹이 하나만 존재할 경우 2:1의 통계 비율(메타:파라)에서 메타 및 파라 위치에서 보리가 발생한다.대체제의 강직 효과로 인해 정형 이소머가 검출되지 않는다.[16]
Bpin의 추가는 대칭으로 대체된 1,2-와 1,4-대체 아레네에 대한 한 위치에서만 발생한다.대칭 또는 비대칭 1,3-대칭 아레네도 선택적으로 보릴레이션되는데, 이는 단 하나의 C-H 결합만이 강직적으로 접근할 수 있기 때문이다.
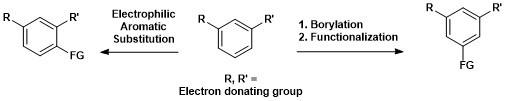
이것은 섭열성이 전자적 효과에 의해 지배되는 Electrophilic 방향족 치환과는 대조적이다.[17]
방향족 C-H 보릴레이션의 합성 중요도는 아래에 나타나 있으며, 여기서 1,3 분해 방향족 화합물을 1,3,5-오르가노보란 화합물로 직접 변환하여 그 후에 기능화할 수 있다.[15]
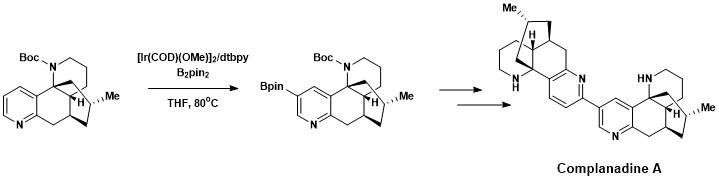
방향족 C-H 기능화는 신경성장인자(NGF)에 대한 mRNA 발현과 인간 용혈세포의 NGF 생성을 강화한 리코포듐알칼로이드인 콤파나딘A의 총합성에 성공적으로 접목되었다.새로운 신경망의 성장을 촉진하는 천연물들이 알츠하이머병 등 질병 치료에 관심사다.[18]콤파나딘 A는 하트비히와 이시야마가 개발한 다이렉트 방향족 C-H 보릴레이션의 조합을 이용하여 성공적으로 합성되었고, 그 다음 스즈키-미야우라 교차 결합, 보크 보호 그룹의 갈라짐이 뒤따랐다.
이성애자의 C-H 보릴레이션
헤테로아레네는 이리듐을 분석한 조건에서도 보리를 사용할 수 있지만, 이 경우 현장 선택성은 전자적 효과에 의해 제어되며, 푸란, 피롤 및 티오페네는 이질 원자에 대한 C-H 결합 알파에서 반응을 겪는다.이 경우 선택성은 가장 산성 C-H 결합이며 따라서 가장 반응성이 높기 때문에 C-H 결합 알파에서 이형 원자까지 C-H 결합을 통해 발생하는 것으로 제안된다.[11]
방향직교 C-H 보릴레이션
동일한 촉매 시스템을 사용하여 스테릭 매개체로 대체되지 않고 섭정성을 달성하도록 그룹을 고용할 수 있다.예를 들어, Boebel과 Hartwig는 Arene의 dimethyl-hydrosilyl directing group이 C–H 본드 직교에서 iridium 촉매 보리를 받는 정형-보리화를 수행하는 방법을 보고하였다.[19]하이드로실릴 지시군을 사용하는 경우 직교 위치의 선택성은 금속 중심에 Si-H 결합을 가역적으로 추가함으로써 하이드로실 대체물에 C-H 본드 정형화가 우선 분할되기 때문이다.아레네의 정형-보리화를 달성하기 위한 몇 가지 다른 전략들은 다양한 연출 그룹을 사용하여 개발되었다.[20][21][22]
C-H 붕리화를 위한 기계론적 세부사항
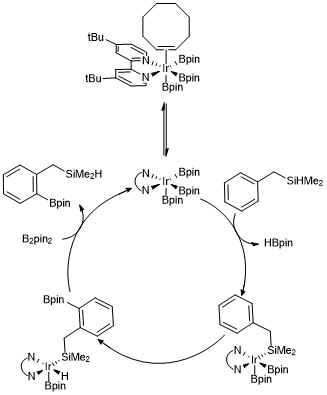
아레네와 헤테로아레네의 C-H 보리를 유발하는 이러한 각각의 반응에 대한 메커니즘을 용이하게 하기 위해 트리스보릴 이리듐 복합체가 제안되었다.운동 연구와 동위원소 라벨링 연구는 Ir(III) 트리보릴 복합체가 촉매 과정에서 아레네와 반응한다는 것을 밝혀냈다.[23]하이드로실레인 화합물의 정형화 보릴레이션에 대한 촉매 주기의 버전은 아래에 제시되어 있다.운동 데이터는 관측된 트리스보릴 콤플렉스가 사이클로옥틴과 빠르고 역전적으로 분리되어 16 전자 트리스보릴 콤플렉스를 형성한다는 것을 보여준다.벤질디메틸실레인을 디렉팅 그룹으로 사용하는 경우, 벤질디메틸실레인은 금속 중심에 Si-H 본드를 가역적으로 첨가하여 트리스보릴 이리듐 촉매와 반응한 후 산화 첨가 및 환원 제거를 통한 선택적 Ortho-C–H 본드 활성화가 제안된다.[24]
메타 선택 보릴레이션:메타선택형 C-H 보릴레이션은 미국 미시간 주립대학의 스미스 3세에 의해 2002년에 발견된 중요한 합성 변형이다. 그러나 이 메타 보릴레이션은 완전히 강직하게 지시되어 1,3개의 분해가 있는 벤젠에 한정되었다.약 12년 후, 인도 U.P. 생물 의학 연구 센터의 Chattopadhyy 박사와 그의 팀은 메타 선택 C-H 본드 활성화와 보리를 위한 우아한 기술을 발견했다.연구팀은 같은 기질을 사용하면 리간드를 바꾸는 것만으로도 다른 위치 선택도를 바꿀 수 있다는 것을 보여주었다.메타 선택성의 원점은 1) 정전기 상호작용, 2) 이차 B-N 상호작용과 같은 두 가지 매개변수에 의해 정의되었다.[25]
이와 동시에, 일본의 카나이 박사팀은 2차 상호작용에 기초한 메타 선택적 보릴레이션의 놀라운 개념을 보고했다.이 방법은 다양한 카보닐 화합물 보리를 포함한다.[26]
오르간오보론 화합물과의 감소반응
코리-박시-시바타 감소(CBS 감소)
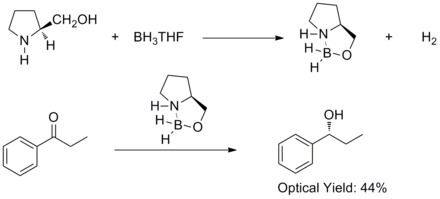
1981년, 히라오와 동료들은 치랄 아미노 알코올과 붕소를 함유한 프로치랄 방향제 케톤이 비대칭적으로 감소하여 해당 2차 알코올에 60% ee를 공급한다는 것을 발견했다.그들은 치랄 아미노 알코올이 보란과 반응하여 알록실-아민-보레인 복합체를 형성한다는 것을 알아냈다.이 단지는 열 및 수력학적 안정성과 다양한 양성 용매와 무화합 용매에 용해성을 제공하는 비교적 견고한 5개 멤버링 시스템을 포함할 것을 제안한다.[27]
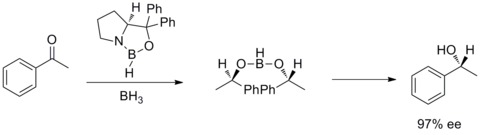
1987년 엘리아스 제임스 코레이와 동료들은 붕소와 치랄 아미노 알코올에서 옥사보리딘의 형성을 알아냈다.그리고 옥사보롤리딘은 BH3가 있는 곳에서 프로치랄 케톤이 빠르고 높은 항억제적 감소를 촉진하는 것으로 밝혀졌다.THF. 촉매 옥사보리딘을 함유한 아치랄 케톤에 대한 이러한 항저항성 감소를 코리-박시-시바타 감소 또는 CBS 감소라고 한다.[28][29]
미들랜드 알파인-보레인 감소(미들랜드 감소)
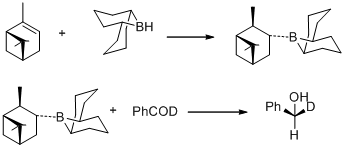
In 1977, M. M. Midland and co-workers reported a surprising observation that B-3-alpha-Pinanyl-9-borabicyclo [3,3,1] nonane, readily prepared by hydroboration of (+)-alpha-pinene with 9-borobicyclo[3,3,1] nonane, rapidly reduces benzaldehyde-alpha-d to (S)-(+)-benzyl-alpha-d alcohol with an essentially quantitative asymmetric induction.[30]
같은 해 M. M. M. M. M. M. Midland는 B-3-alpha-pinanyl-9-BBN을 환원제로 발견했는데, 이 환원제는 (+-alpha-pinene을 9-BBN과 반응시키면 쉽게 구할 수 있다.이 새로운 환원제는 나중에 알프스 보레인이라는 이름으로 알드리히사에 의해 상용화되었고 알프스-보레인 에나토머를 가진 카보닐 그룹의 비대칭 환원제는 미들랜드 알프스-보레인 환원제로 알려져 있다.[31]
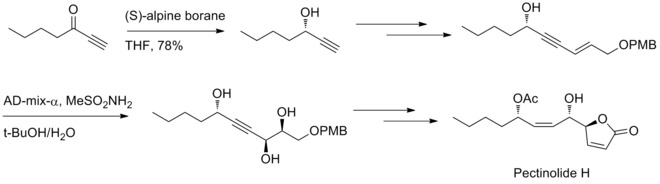
2012년, U. R. Y. 벤카테스워루와 동료들은 펙티놀라이드 H. 미들랜드 감소와 샤를리스 디히드록실화 반응이 C–4, C–5, C–1에 3개의 치랄 센터를 생성하는 데 관여한다고 보고했다.[32]
오르간오보론 화합물과의 결합 반응
페타시스 붕산-만니치 반응
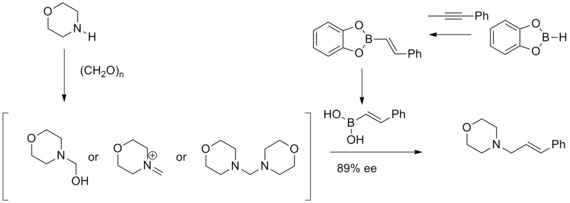
1993년 N. A. 페타시스와 I.Akrtopoulou는 변형된 Mannich 반응으로 동맹성 아민의 효율적인 합성을 보고했다.이 변형된 마니치 반응에서, 그들은 비닐 붕산이 기하학적으로 순수한 아리아민을 주기 위해 핵물질로 참여할 수 있다는 것을 발견했다.이러한 변형된 만니치 반응은 페타시스 보론산-만니치 반응으로 알려져 있었다.[33][34]
루쉬 비대칭 동맹화
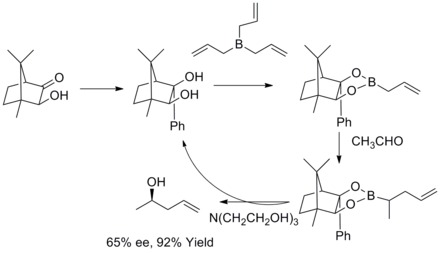
1978년 R. W. 호프만과 T.헤럴드는 키랄 비인두증 에스테르를 통한 2차 호모알콜의 항항체적 합성에 대해 보고했다.호모알코올은 뛰어난 수율과 적당한 항우울제로 형성되었다.[35]
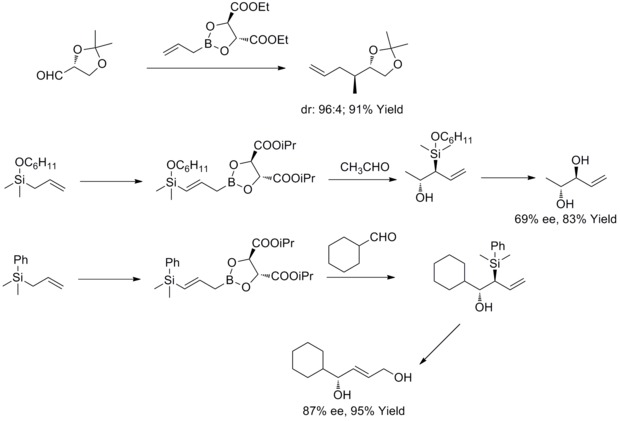
1985년, W. R. R. R. Roush와 동료들은 치랄과 아치랄 알데히드와의 반응에서 타르트레이트 변형 동맹 붕소나이트가 얼굴 선택성 제어에 간단하고 매우 매력적인 접근법을 제공한다는 것을 발견했다.이듬해 W.R. Roussh와 동료들은 이 전략을 but-2-ene-1,4-diols와 Anti-diolls의 합성까지 확장했다.이런 종류의 반응은 루치 비대칭 동맹이라고 알려져 있다.[36][37][38][39]
2011년, R. A. 페르난데스와 P. 카탕구루는 (8S, 11R, 12R)와 (8R, 11R, 12R)-탑센톨라이드 B2 디스트로이드의 개선된 총합성을 8단계로 완료하였다.논문에서는 두 개의 치랄 중간을 도입하기 위한 총합성의 핵심 반응으로 이질회수성 루스 아일화 반응이 사용되었다.그리고 나서 저자들은 이 두 개의 치랄 매개체를 통해 두 개의 이질제거기를 합성했다.[40]
스즈키-미야우라 교차커플링
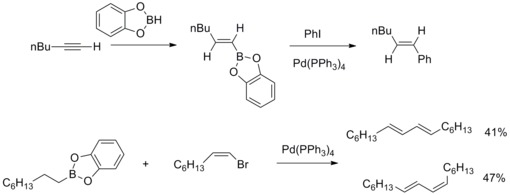
1979년 N. 미야우라, A.스즈키는 아릴 할리드로부터 높은 수율의 아릴화(E)-알켄의 합성을 알킬-1-에닐보레인(alkyl-1-enylboranes)과 테트라키스(tetrakis, triphelphosine) 팔라듐과 베이스로 촉매 처리했다고 보고했다.그러면 A.스즈키와 동료들은 이런 종류의 반응을 다른 오르가노보론 화합물과 다른 알케닐, 아릴, 알킬 할로겐화물과 트리플플라이트에까지 확장시킨다.팔라듐 촉매 교차 결합 반응 오르간오보론 화합물과 탄소-탄소 결합을 형성하기 위한 유기 할로겐화물은 스즈키-미야우라 교차 결합으로 알려져 있다.[41][42]
2013년 요아힘 포들렉과 동료들은 NMR 분광 분석으로 알테뉴산 3의 구조를 파악해 합성을 완료했다.합성 전략에서는 기능성이 높은 붕소산염과 부테놀라이드를 사용한 스즈키-미야우라 크로스커플링 반응을 사용해 수율이 높은 천연물의 전구체를 합성했다.[43]
수정된 울만 바이아릴 에테르 및 바이아릴 아민 합성
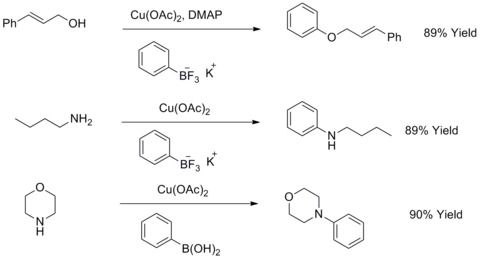
1904년 프리츠 울만은 구리 가루가 아릴 할로겐과 페놀의 반응을 크게 개선시켜 바이오 에테르를 공급할 수 있다는 사실을 알아냈다.이 반응은 울만 응결이라고 알려져 있다.1906년 I. 골드버그는 아릴 할리드를 탄산화칼륨과 CuI가 존재하는 곳에서 아릴 할리드를 아미드와 반응시킴으로써 아릴아민을 합성하기 위해 이 반응을 연장했다.이 반응은 골드버그가 울만 응결제를 변형시킨 것으로 알려져 있다.[44]2003년 R. A. Batey와 T. D. Quach는 아릴 에테르나 아릴 아민을 합성하기 위해 아릴 아민이나 아일린과 반응하기 위해 오가노트리플루오보레이트 염을 사용하여 이러한 종류의 반응을 수정했다.[45][46]
참고 항목
참조
- ^ Hartwig, John F. (2012). "Borylation and Silylation of C–H Bonds: A Platform for Diverse C–H Bond Functionalizations". Accounts of Chemical Research. 45 (6): 864–873. doi:10.1021/ar200206a. ISSN 0001-4842. PMID 22075137.
- ^ Cho, J. Y.; Tse, M. K.; Holmes, D.; Maleczka, R. E.; Jr; Smith, M. R. (2001). "Remarkably Selective Iridium Catalysts for the Elaboration of Aromatic C-H Bonds". Science. 295 (5553): 305–8. doi:10.1126/science.1067074. PMID 11719693. S2CID 21096755.
- ^ 이시야마, T., 노부타, Y., 하트비히, J. F., 미야우라, N. Chem. 코뮌.2003, 2924.
- ^ 브라운, H. C.; 크레이머, 레비, A. B.; 보란스를 통한 M. M. 유기합성; 와일리-인터사이언스:1975년 뉴욕; 제1권
- ^ Braunschweig, H.; Guethlein, F. (2011). "Transition-Metal-Catalyzed Synthesis of Diboranes(4)". Angewandte Chemie International Edition. 50 (52): 12613–12616. doi:10.1002/anie.201104854. PMID 22057739.
- ^ Hall, D. G. (2011) Structure, Properties, and Preparation of Boronic Acid Derivatives, in Boronic Acids: Preparation and Applications in Organic Synthesis, Medicine and Materials (Volume 1 and 2), Second Edition (ed D. G. Hall), Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, Germany. doi:10.1002/9783527639328.ch1
- ^ Mkhalid, Ibraheem A. I.; Barnard, Jonathan H.; Marder, Todd B.; Murphy, Jaclyn M.; Hartwig, John F. (2010). "C–H Activation for the Construction of C–B Bonds". Chemical Reviews. 110 (2): 890–931. doi:10.1021/cr900206p. PMID 20028025.
- ^ Wade, L. G. 유기화학.Upper Saddle River: Pearson Education, Inc., 2010.
- ^ Chen, H.; Schlecht, S.; Semple, T. C.; Hartwig, J. F. (2000). "Thermal, Catalytic, Regiospecific Functionalization of Alkanes". Science. 287 (5460): 1995–1997. Bibcode:2000Sci...287.1995C. doi:10.1126/science.287.5460.1995. PMID 10720320.
- ^ Lawrence, J. D.; Takahashi, M.; Bae, C.; Hartwig, J. F. (2004). "Regiospecific Functionalization of Methyl C−H Bonds of Alkyl Groups in Reagents with Heteroatom Functionality". J. Am. Chem. Soc. 126 (47): 15334–15335. doi:10.1021/ja044933x. PMID 15563132.
- ^ a b c Hartwig, J. F. (2011). "Regioselectivity of the borylation of alkanes and arenes". Chem. Soc. Rev. 40 (4): 1992–2002. doi:10.1039/C0CS00156B. PMID 21336364.
- ^ Wei, C. S.; Jimenez-Hoyos, C. A.; Videa, M.F.; Hartwig, J. F.; Hall, M. B. (2010). "Origins of the Selectivity for Borylation of Primary over Secondary C−H Bonds Catalyzed by Cp*-Rhodium Complexes". J. Am. Chem. Soc. 132 (9): 3078–91. doi:10.1021/ja909453g. PMID 20121104.
- ^ Kondo, Y.; Garcia-Cuadrado, D.; Hartwig, J. F.; Boaen, N. K.; Wagner, N. L.; Hillmyer, M. A. (2002). "Rhodium-Catalyzed, Regiospecific Functionalization of Polyolefins in the Melt". J. Am. Chem. Soc. 124 (7): 1164–5. doi:10.1021/ja016763j. PMID 11841273.
- ^ Iverson, Carl N.; Smith, Milton R. (1999-08-06). "Stoichiometric and Catalytic B−C Bond Formation from Unactivated Hydrocarbons and Boranes". Journal of the American Chemical Society. 121 (33): 7696–7697. doi:10.1021/ja991258w.
- ^ a b Hartwig, J.F. (2012). "Borylation and silylation of C-H bonds: a platform for diverse C-H bond functionalizations". Accounts of Chemical Research. 45 (6): 864–873. doi:10.1021/ar200206a. PMID 22075137.
- ^ Ishiyama, T.; Takagi, J.; Ishida, K.; Miyaura, N.; Anastasi, N.; Hartwig, J.F. (2002). "Mild Iridium-Catalyzed Borylation of Arenes. High Turnover Numbers, Room Temperature Reactions, and Isolation of a Potential Intermediate". J. Am. Chem. Soc. 124 (3): 390–391. doi:10.1021/ja0173019. PMID 11792205.
- ^ 리스트키, C.Iridium-Catalysised Borylation of Arimatic 및 Aliphatic C–H 결합: 방법론과 메커니즘.일리노이 대학의 논문.우르반 샴페인.2013.
- ^ Fischer, D.F; Sarpong, R. (2010). "Total Synthesis of (+)-Complanadine A Using an Iridium-Catalyzed Pyridine C−H Functionalization". J. Am. Chem. Soc. 132 (17): 5926–5927. doi:10.1021/ja101893b. PMC 2867450. PMID 20387895.
- ^ Boebel, T. A.; Hartwig, J. F. (2008). "Silyl-Directed, Iridium-Catalyzedortho-Borylation of Arenes. A One-Potortho-Borylation of Phenols, Arylamines, and Alkylarenes". J. Am. Chem. Soc. 130 (24): 7534–5. doi:10.1021/ja8015878. PMID 18494474.
- ^ Ishiyama, T.; Miyaura, N.; Isou, H.; Kikuchi, T. (2010). "Ortho-C–H borylation of benzoate esters with bis(pinacolato)diboron catalyzed by iridium–phosphine complexes". Chem. Commun. 46 (1): 159–61. doi:10.1039/b910298a. hdl:2115/44631. PMID 20024326.
- ^ Kawamorita, S.; Ohmiya, H.; Hara, K.; Fukuoka, A.; Sawamura, M. (2009). "Directed Ortho Borylation of Functionalized Arenes Catalyzed by a Silica-Supported Compact Phosphine−Iridium System". J. Am. Chem. Soc. 131 (14): 5058–9. doi:10.1021/ja9008419. PMID 19351202.
- ^ 로스, 에스테파, B, 로페즈-로드리케스, 알바레스, 페르난데스, R, 라살레타, J.M. 안젤레즈. 화학. 인트. 2011년 12월 50일, 1일.
- ^ 볼러, 티엠, 머피, 제이엠, 합케, 이시야마, 티, 미야우라, 하트비히, 제이프 제이엠. 화학. Soc. 2005; 127, 14263.
- ^ Boebel, T.A.; Hartwig, J.F. (2008). "Silyl-Directed, Iridium-Catalyzedortho-Borylation of Arenes. A One-Potortho-Borylation of Phenols, Arylamines, and Alkylarenes". J. Am. Chem. Soc. 130 (24): 7534–7535. doi:10.1021/ja8015878. PMID 18494474.
- ^ Bisht, R.; Chattopadhyay, B. (2016). "Formal Ir-Catalyzed Ligand-Enabled Ortho and Meta Borylation of Aromatic Aldehydes via in Situ-Generated Imines". J. Am. Chem. Soc. 138 (1): 84–7. doi:10.1021/jacs.5b11683. PMID 26692251.
- ^ Kanai; et al. (2015). "A meta-selective C–H borylation directed by a secondary interaction between ligand and substrate". Nat. Chem. 7 (9): 712–7. Bibcode:2015NatCh...7..712K. doi:10.1038/nchem.2322. PMID 26291942.
- ^ Hirao, Akira; Itsuno, Shinichi; Nakahama, Seiichi; Yamazaki, Noboru (1981). "Asymmetric reduction of aromatic ketones with chiral alkoxy-amineborane complexes". Journal of the Chemical Society, Chemical Communications (7): 315. doi:10.1039/c39810000315.
- ^ Corey, E. J.; Bakshi, Raman K.; Shibata, Saizo (September 1987). "Highly enantioselective borane reduction of ketones catalyzed by chiral oxazaborolidines. Mechanism and synthetic implications". Journal of the American Chemical Society. 109 (18): 5551–5553. doi:10.1021/ja00252a056.
- ^ Corey, E. J.; Bakshi, Raman K.; Shibata, Saizo; Chen, Chung Pin; Singh, Vinod K. (December 1987). "A stable and easily prepared catalyst for the enantioselective reduction of ketones. Applications to multistep syntheses". Journal of the American Chemical Society. 109 (25): 7925–7926. doi:10.1021/ja00259a075.
- ^ Midland, M.Mark; Tramontano, Alfonso; Zderic, Stephen A (July 1977). "The facile reaction of B-alkyl-9-borabicyclo[3.3.1]nonanes with benzaldehyde". Journal of Organometallic Chemistry. 134 (1): C17–C19. doi:10.1016/S0022-328X(00)93625-8.
- ^ Midland, M. Mark; Tramontano, Alfonso; Zderic, Stephen A. (June 1977). "Preparation of optically active benzyl-.alpha.-d alcohol via reduction by B-3.alpha.-pinanyl-9-borabicyclo[3.3.1]nonane. A new highly effective chiral reducing agent". Journal of the American Chemical Society. 99 (15): 5211–5213. doi:10.1021/ja00457a068.
- ^ Ramesh, D.; Shekhar, V.; Chantibabu, D.; Rajaram, S.; Ramulu, U.; Venkateswarlu, Y. (March 2012). "First stereoselective total synthesis of pectinolide H". Tetrahedron Letters. 53 (10): 1258–1260. doi:10.1016/j.tetlet.2011.12.122.
- ^ Petasis, Nicos A.; Akritopoulou, Irini (January 1993). "The boronic acid mannich reaction: A new method for the synthesis of geometrically pure allylamines". Tetrahedron Letters. 34 (4): 583–586. doi:10.1016/S0040-4039(00)61625-8.
- ^ Yu, Tao; Li, Hui; Wu, Xinyan; Yang, Jun (2012). "Progress in Petasis Reaction". Chinese Journal of Organic Chemistry. 32 (10): 1836. doi:10.6023/cjoc1202092.
- ^ Herold, Thomas; Hoffmann, Reinhard W. (October 1978). "Enantioselective Synthesis of Homoallyl Alcoholsvia Chiral Allylboronic Esters". Angewandte Chemie International Edition in English. 17 (10): 768–769. doi:10.1002/anie.197807682.
- ^ Roush, William R.; Walts, Alan E.; Hoong, Lee K. (December 1985). "Diastereo- and enantioselective aldehyde addition reactions of 2-allyl-1,3,2-dioxaborolane-4,5-dicarboxylic esters, a useful class of tartrate ester modified allylboronates". Journal of the American Chemical Society. 107 (26): 8186–8190. doi:10.1021/ja00312a062.
- ^ Roush, William R.; Ando, Kaori; Powers, Daniel B.; Halterman, Ronald L.; Palkowitz, Alan D. (January 1988). "Enantioselective synthesis using diisopropyl tartrate modified (E)- and (Z)-crotylboronates: Reactions with achiral aldehydes". Tetrahedron Letters. 29 (44): 5579–5582. doi:10.1016/S0040-4039(00)80816-3.
- ^ Roush, William R.; Grover, Paul T. (January 1990). "Diisopropyl tartrate (E)-γ-(dimethylphenylsilyl)allylboronate, a chiral allylic alcohol β-carbanion equivalent for the enantioselective synthesis of 2-butene-1,4-diols from aldehydes". Tetrahedron Letters. 31 (52): 7567–7570. doi:10.1016/S0040-4039(00)97300-3.
- ^ Roush, William R.; Gover, Paul T.; Lin, Xiaofa (January 1990). "Diisopropyl tartrate modified (E)-γ-[(cyclohexyloxy)dimethylsilyl-allylboronate, a chiral reagent for the stereoselective synthesis of anti 1,2-diols via the formal α-hydroxyallylation of aldehydes". Tetrahedron Letters. 31 (52): 7563–7566. doi:10.1016/S0040-4039(00)97299-X.
- ^ Fernandes, Rodney A.; Kattanguru, Pullaiah (November 2011). "Total synthesis of (8S,11R,12R)- and (8R,11R,12R)-topsentolide B2 diastereomers and assignment of the absolute configuration". Tetrahedron: Asymmetry. 22 (20–22): 1930–1935. doi:10.1016/j.tetasy.2011.10.020.
- ^ Miyaura, Norio; Suzuki, Akira (1979). "Stereoselective synthesis of arylated (E)-alkenes by the reaction of alk-1-enylboranes with aryl halides in the presence of palladium catalyst". Journal of the Chemical Society, Chemical Communications (19): 866. doi:10.1039/C39790000866.
- ^ Miyaura, Norio; Yamada, Kinji; Suzuki, Akira (January 1979). "A new stereospecific cross-coupling by the palladium-catalyzed reaction of 1-alkenylboranes with 1-alkenyl or 1-alkynyl halides" (PDF). Tetrahedron Letters. 20 (36): 3437–3440. doi:10.1016/S0040-4039(01)95429-2. hdl:2115/44006.
- ^ Nemecek, Gregor; Thomas, Robert; Goesmann, Helmut; Feldmann, Claus; Podlech, Joachim (October 2013). "Structure Elucidation and Total Synthesis of Altenuic Acid III and Studies towards the Total Synthesis of Altenuic Acid II". European Journal of Organic Chemistry. 2013 (28): 6420–6432. doi:10.1002/ejoc.201300879.
- ^ Kürti, László; Czakó, Barbara (2007). Strategic applications of named reactions in organic synthesis : background and detailed mechanisms ; 250 named reactions (Pbk. ed., [Nachdr.]. ed.). Amsterdam [u.a.]: Elsevier Academic Press. pp. 464–465. ISBN 978-0-12-429785-2.
- ^ Quach, Tan D.; Batey, Robert A. (April 2003). "Copper(II)-Catalyzed Ether Synthesis from Aliphatic Alcohols and Potassium Organotrifluoroborate Salts". Organic Letters. 5 (8): 1381–1384. doi:10.1021/ol034454n. PMID 12688764.
- ^ Quach, Tan D.; Batey, Robert A. (1 November 2003). "Ligand- and Base-Free Copper(II)-Catalyzed C−N Bond Formation: Cross-Coupling Reactions of Organoboron Compounds with Aliphatic Amines and Anilines". Organic Letters. 5 (23): 4397–4400. doi:10.1021/ol035681s. PMID 14602009.