그루브 촉매
Grubbs catalyst | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 벤질리덴-비스(트리시클록시엘포시노)-디클로로루테늄 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
펍켐 CID | |
| 유니 | |
| |
| |
| 특성. | |
| C43H72CL2P2루 | |
| 어금질량 | 822.97 g·197−1 |
| 외관 | 보라색 고체 |
| 녹는점 | 153 °C(307 °F; 426 K)(위치) |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 [1,3-bis-2,4-6-6ethylphenyl)-2-이미다졸리디닐리덴]inylloro(phenylmethylene)(트리시클로헥실포스피노)ruthenium | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
펍켐 CID | |
| |
| |
| 특성. | |
| C46H65CL2N2P루 | |
| 어금질량 | 848.98 g·190−1 |
| 외관 | 핑크빛 갈색의 솔리드 |
| 녹는점 | 143.5 ~ 148.5°C(290.3 ~ 299.3°F, 416.6 ~ 421.6K) |
| 위험 | |
| GHS 라벨 표시: | |
 | |
| 경고 | |
| H228 | |
| P210, P240, P241, P280, P378 | |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 디클로로(o-isopropoxyphenylmethylene)(트리시클로헥실인산)루테늄(ruthenium)II) | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
펍켐 CID | |
| |
| |
| 특성. | |
| C28H45CL2OP루 | |
| 어금질량 | 600.61 g·190−1 |
| 외관 | 브라운 솔리드 |
| 녹는점 | 195~197°C(383~387°F, 468~470K) |
| 위험 | |
| GHS 라벨 표시: | |
 | |
| 경고 | |
| H228 | |
| P210, P240, P241, P280, P378 | |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 [1,3-Bis-(2,4,6-트리메틸페닐)-2-이미다졸리디닐리덴)디클로로(o-이소프로포시페닐메틸렌)루테늄 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| EC 번호 |
|
펍켐 CID | |
| |
| |
| 특성. | |
| C31H38CL2N2O루 | |
| 어금질량 | 626.63 g·162−1 |
| 외관 | 그린솔리드 |
| 녹는점 | 216 ~ 220 °C(421 ~ 428 °F, 489 ~ 493 K) |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
그럽스 촉매란 올레핀 메타텍스 촉매로 사용되는 일련의 전이 금속 카베네 콤플렉스다.그것들은 그들의 합성을 감독한 화학자인 로버트 H. 그루브스의 이름을 따서 지어졌다.그 촉매는 몇 세대에 걸쳐 개발되었다.[1][2]그럽스 촉매들은 알켄 기질 내의 많은 기능 그룹을 견디고, 공기에 내성이 있으며, 광범위한 용매와 호환된다.[3][4]이러한 이유로, 그럽스 촉매들은 합성 유기 화학에서 인기를 끌었다.[5]그럽스, 리처드 R과 함께. 슈록과 이브 차우빈은 올레핀 메타텍스 개발에 기여한 공로를 인정받아 노벨 화학상을 수상했다.
1세대 촉매
1960년대에 루테늄 트리클로라이드는 올레핀 메타테이프스를 촉매로 만드는 것이 발견되었다.이러한 발견을 바탕으로 공정이 상용화되었다.이러한 정의되지 않았지만 매우 활동적인 균질 촉매들은 산업용에 남아 있다.[6]최초의 잘 정의된 루테늄 촉매는 1992년에 보고되었다.[7]그것은 루클2(PPH3)4과 디페닐사이클로프로펜에서 준비되었다.
이 최초의 루테늄 촉매는 현재 1세대 그루브스 촉매로 알려진 것에 의해 1995년에 뒤따랐다.루클2(PPH3),3 페닐디아조메탄, 트리시클로헥실인산염에서 원팟 합성으로 합성된다.[8][9]
1세대 그루브스 촉매는 최초의 잘 정의된 루 기반 촉매였다.다른 모든 그루브형 촉매의 전구로서도 중요하다.
2세대 촉매
2세대 촉매는 1세대 촉매와 유기합성에 동일한 용도를 가지지만 일반적으로 활동량이 더 높다.이 촉매는 습기와 공기에 안정적이어서 실험실에서 다루기 쉽다.
2세대 그루브스 촉매 발견 직전인 1999년 3월 놀란과[10] 그루브스에[11] 의해 불포화 N-헤테로사이클릭 카베네(2,4-bis(2,4,6-트리메틸페닐)이미다졸)에 기초한 매우 유사한 촉매가 독립적으로 보고되었고, 같은 해 6월에는 퓌스트너가[12] 보고하였다.그 직후인 1999년 8월 그루브스는 포화 N-헤테로사이클릭 카베네(2,3-bis(2,4,6-트리메틸페닐) 디히드로이미다졸)에 근거하여 2세대 촉매를 보고하였다.[13]
포화 및 불포화 사례 모두에서 인산 리간드는 모든 2세대 유형의 촉매의 특징인 N-헤로사이클릭 카베네(NHC)로 대체된다.[3]
1세대와 2세대 촉매 모두 2세대 촉매의 많은 파생 모델과 함께 상업적으로 이용할 수 있다.
호비다-그럽스 촉매
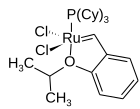
호비다-그럽스 촉매에서 벤질리덴 리간드는 벤젠 링에 부착된 킬레이트 정형외과-이소프로포시 그룹을 가지고 있다.정형외과-이소프로포시벤질리덴 모이에티는 때때로 호비다 킬레이트라고 불린다.킬레이트 산소 원자는 인산 리간드를 대체하는데, 2세대 촉매의 경우 인산 없는 구조를 준다.1세대 호비다-그럽스 촉매제는 1999년 아미르 H. 호비다의 그룹에 의해 보고되었고,[14] 이듬해 2세대 호비다-그럽스 촉매제가 블리처트와[15] 호비다[16] 연구소의 거의 동시 출판물에 설명되었다.지그프리드 블리처트의 이름은 일반적으로 eponymous 촉매 이름에 포함되지 않는다.호비다-그럽스 촉매들은 그것들이 파생된 그루브스 촉매보다 더 비싸고 시작하기도 더 느리지만, 그들의 안정성이 향상되었기 때문에 인기가 있다.[3]첼레이트(chelate)의 steric 및 전자적 특성을 변경함으로써, 촉매는 Zhan Catalyst([17][18]Zhan Catalyst)에서와 같이 시작률을 변조할 수 있다.호비다-그럽스 촉매들은 해당 그럽스 촉매로부터 첼레이트 리간드를 첨가하고 염화 구리(I)와 같은 인광 스캐빈저를 사용함으로써 쉽게 형성된다.[16]
2세대 Hoveyda-Grubbs 촉매도 NHC를 추가하여 1세대 Hoveyda-Grubbs 촉매로부터 준비될 수 있다.[15]
한 연구에서는 폴리에틸렌 글리콜 체인을 이미다졸리딘 그룹에 부착하여 수용성 그럽스 촉매가 준비된다.[19]이 촉매는 암모늄 염분을 운반하는 디엔의 물의 링 클로징 메타텍스 반응에도 사용되어 수용성이 높다.
3세대 그럽스 촉매(급속 개시 촉매)
그럽스 촉매의 속도는 인광 리간드를 더 많은 라빌리딘 피리딘 리간드로 대체함으로써 바뀔 수 있다.3-브로모피리딘을 사용함으로써 시작률이 백만 배 이상 증가한다.[20]피리딘과 3-브로모피리딘이 공통적으로 사용되며, 브로모- 버전이 4.8배 더 많은 라일리로 더욱 빠른 속도를 낸다.[21]촉매는 전통적으로 두 개의 피리딘 콤플렉스로 격리되지만, 한 개의 피리딘은 용해 후 손실되어 모든 화학 반응에서 루테늄 중심을 역방향으로 억제한다.
빠르게 개시되는 촉매의 주요 적용은 링 개방 메타텍스 중합(ROMP)을 위한 개시자 역할을 한다.ROMP에서의 유용성 때문에 이러한 촉매를 3세대 그럽스 촉매라고 부르기도 한다.[22]전파 속도에 대한 시작 비율의 높은 비율은 이러한 촉매를 살아있는 중합에 유용하게 만들고, 낮은 다분산성을 가진 중합체를 산출한다.[23]
적용들
올레핀 메타텍스에는 그루브 촉매제가 관심사다.그것은 주로 미세한 화학 합성에 적용된다.올레핀 메타텍스트의 대규모 상업적 응용은 거의 항상 이질적인 촉매나 루테늄 트리클로라이드에 기초한 잘못 정의된 시스템을 채택한다.[6]
참조
- ^ Grubbs, Robert H. (2003). Handbook of Metathesis (1st ed.). Weinheim: Wiley-VCH. ISBN 978-3-527-30616-9.
- ^ Grubbs, R. H.; Trnka, T. M. (2004). "Ruthenium-Catalyzed Olefin Metathesis". In Murahashi, S. (ed.). Ruthenium in Organic Synthesis. Weinheim: Wiley-VCH. pp. 153–177. doi:10.1002/3527603832.ch6. ISBN 9783527603831.
- ^ a b c Vougioukalakis, G. C.; Grubbs, R. H. (2010). "Ruthenium-Based Heterocyclic Carbene-Coordinated Olefin Metathesis Catalysts". Chemical Reviews. 110 (3): 1746–1787. doi:10.1021/cr9002424. PMID 20000700.
- ^ Trnka, T. M.; Grubbs, R. H. (2001). "The Development of L2X2Ru=CHR Olefin Metathesis Catalysts: An Organometallic Success Story". Accounts of Chemical Research. 34 (1): 18–29. doi:10.1021/ar000114f. PMID 11170353.
- ^ Cossy, Janine; Arseniyadis, Stellios; Meyer, Christophe (2010). Metathesis in Natural Product Synthesis: Strategies, Substrates and Catalysts (1st ed.). Weinheim: Wiley-VCH. ISBN 978-3-527-32440-8.
- ^ a b Lionel Delaude, Alfred F. Noels (2005). "Metathesis". Kirk-Othmer Encyclopedia of Chemical Technology. Weinheim: Wiley-VCH. doi:10.1002/0471238961.metanoel.a01. ISBN 978-0471238966.
{{cite encyclopedia}}: CS1 maint: 작성자 매개변수 사용(링크) - ^ Nguyen, S. T.; Johnson, L. K.; Grubbs, R. H.; Ziller, J. W. (1992). "Ring-opening metathesis polymerization (ROMP) of norbornene by a Group VIII carbene complex in protic media" (PDF). Journal of the American Chemical Society. 114 (10): 3974–3975. doi:10.1021/ja00036a053.
- ^ Schwab, P.; France, M. B.; Ziller, J. W.; Grubbs, R. H. (1995). "A Series of Well-Defined Metathesis Catalysts – Synthesis of [RuCl2(=CHR′)(PR3)2] and Its Reactions". Angew. Chem. Int. Ed. 34 (18): 2039–2041. doi:10.1002/anie.199520391.
- ^ Schwab, P.; Grubbs, R. H.; Ziller, J. W. (1996). "Synthesis and Applications of RuCl2(=CHR′)(PR3)2: The Influence of the Alkylidene Moiety on Metathesis Activity". J. Am. Chem. Soc. 118 (1): 100–110. doi:10.1021/ja952676d.
- ^ Huang, J.-K.; Stevens, E. D.; Nolan, S. P.; Petersen, J. L. (1999). "Olefin Metathesis-Active Ruthenium Complexes Bearing a Nucleophilic Carbene Ligand". J. Am. Chem. Soc. 121 (12): 2674–2678. doi:10.1021/ja9831352.
- ^ Scholl, M.; Trnka, T. M.; Morgan, J. P.; Grubbs, R. H. (1999). "Increased Ring Closing Metathesis Activity of Ruthenium-Based Olefin Metathesis Catalysts Coordinated with Imidazolin-2-ylidene Ligands". Tetrahedron Letters. 40 (12): 2247–2250. doi:10.1016/S0040-4039(99)00217-8.
- ^ Ackermann, L.; Fürstner, A.; Weskamp, T.; Kohl, F. J.; Herrmann, W. A. (1999). "Ruthenium Carbene Complexes with Imidazolin-2-ylidene Ligands Allow the Formation of Tetrasubstituted Cycloalkenes by RCM". Tetrahedron Lett. 40 (26): 4787–4790. doi:10.1016/S0040-4039(99)00919-3.
- ^ Scholl, M.; Ding, S.; Lee, C. W.; Grubbs, R. H. (1999). "Synthesis and Activity of a New Generation of Ruthenium-Based Olefin Metathesis Catalysts Coordinated with 1,3-Dimesityl-4,5-dihydroimidazol-2-ylidene Ligands". Org. Lett. 1 (6): 953–956. doi:10.1021/ol990909q. PMID 10823227.
- ^ Kingsbury, Jason S.; Harrity, Joseph P. A.; Bonitatebus, Peter J.; Hoveyda, Amir H. (1999). "A Recyclable Ru-Based Metathesis Catalyst". Journal of the American Chemical Society. 121 (4): 791–799. doi:10.1021/ja983222u.
- ^ a b Gessler, S.; Randl, S.; Blechert, S. (2000). "Synthesis and metathesis reactions of phosphine-free dihydroimidazole carbene ruthenium complex". Tetrahedron Letters. 41 (51): 9973–9976. doi:10.1016/S0040-4039(00)01808-6.
- ^ a b Garber, S. B.; Kingsbury, J. S.; Gray, B. L.; Hoveyda, A. H. (2000). "Efficient and Recyclable Monomeric and Dendritic Ru-Based Metathesis Catalysts". Journal of the American Chemical Society. 122 (34): 8168–8179. doi:10.1021/ja001179g.
- ^ Engle, Keary M.; Lu, Gang; Luo, Shao-Xiong; Henling, Lawrence M.; Takase, Michael K.; Liu, Peng; Houk, K. N.; Grubbs, Robert H. (2015). "Origins of Initiation Rate Differences in Ruthenium Olefin Metathesis Catalysts Containing Chelating Benzylidenes". Journal of the American Chemical Society. 137 (17): 5782–5792. doi:10.1021/jacs.5b01144. PMID 25897653.
- ^ Luo, Shao-Xiong; Engle, Keary M.; Deng, Xiaofei; Hejl, Andrew; Takase, Michael K.; Henling, Lawrence M.; Liu, Peng; Houk, K. N.; Grubbs, Robert H. (2018). "An Initiation Kinetics Prediction Model Enables Rational Design of Ruthenium Olefin Metathesis Catalysts Bearing Modified Chelating Benzylidenes". ACS Catalysis. 8 (5): 4600–4611. doi:10.1021/acscatal.8b00843. PMC 7289044.
- ^ Hong, Soon Hyeok; Grubbs, Robert H. (2006). "Highly Active Water-Soluble Olefin Metathesis Catalyst" (PDF). Journal of the American Chemical Society. 128 (11): 3508–3509. doi:10.1021/ja058451c. PMID 16536510.
- ^ Love, J. A.; Morgan, J. P.; Trnka, T. M.; Grubbs, R. H. (2002). "A Practical and Highly Active Ruthenium-Based Catalyst that Effects the Cross Metathesis of Acrylonitrile". Angew. Chem. Int. Ed. Engl. 41 (21): 4035–4037. doi:10.1002/1521-3773(20021104)41:21<4035::AID-ANIE4035>3.0.CO;2-I. PMID 12412073.
- ^ Walsh, Dylan J.; Lau, Sii Hong; Hyatt, Michael G.; Guironnet, Damien (2017-09-25). "Kinetic Study of Living Ring-Opening Metathesis Polymerization with Third-Generation Grubbs Catalysts". Journal of the American Chemical Society. 139 (39): 13644–13647. doi:10.1021/jacs.7b08010. ISSN 0002-7863. PMID 28944665.
- ^ Leitgeb, Anita; Wappel, Julia; Slugovc, Christian (2010). "The ROMP toolbox upgraded". Polymer. 51 (14): 2927–2946. doi:10.1016/j.polymer.2010.05.002.
- ^ Choi, T.-L.; Grubbs, R. H. (2003). "Controlled Living Ring-Opening-Metathesis Polymerization by a Fast-Initiating Ruthenium Catalyst". Angewandte Chemie International Edition. 42 (15): 1743–1746. doi:10.1002/anie.200250632. PMID 12707895.