랑무어 흡착 모델
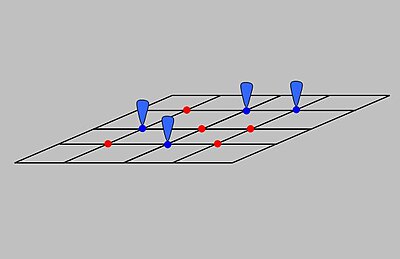
Langmuir adsorption modelLangmuir 흡착 모델은 흡착제가 등온 조건에서 이상적인 기체로 작용한다고 가정하여 흡착을 설명한다.모델에 따르면 흡착과 탈착은 되돌릴 수 있는 과정이다.이 모델은 압력의 영향, 즉 이러한 조건에서 흡착제의 부분 압력인 p 은 그것의 부피, V, 고체 흡착제에 흡착된 것과 관련이 있다.그림에서 표시한 대로 흡착제는 흡착제를 결합할 수 있는 일련의 구별되는 부위로 구성된 이상적인 고체 표면으로 가정한다.흡착제 결합은 흡착제 기체 분자 와 비어 있는 흡착 사이트 S 사이의 화학 반응으로 처리된다.이 반응은 연관된 평형 상수 }을(를) 가진 {\ A_{\eq을(를) 생성한다
이러한 기본적인 가설에서 Langmuir 흡착 이소템의 수학적 공식은 다양한 독립적 및 보완적 방법으로 도출될 수 있다: 각각 운동학, 열역학 및 통계 역학 접근방식(다양한 시연에 대해서는 아래 참조).
Langmuir 흡착 방정식은 다음과 같다.
여기서 는 흡착 부지의 부분 점유, 즉 V의 비율, 고체에 흡착된 기체의 와 Vm {\V_{\},고체의 전체 표면을 덮고 완전히 흡착된 기체 분자의 부피이다.균일한 평면 고체 표면을 덮고 있는 흡착 분자의 연속적인 단열재는 이 흡착 모델의 개념적 기초가 된다.[1]
배경 및 실험
1916년, 어빙 랭무어는 단순한 표면에 종을 흡착하기 위한 그의 모델을 제시했다.랑무어는 표면 화학에 관한 연구로 1932년 노벨상을 받았다.그는 주어진 표면에는 물리치료나 화학요법에 의해 한 종이 "붙일 수 있는" 일정한 수의 동등한 부위가 있다고 가설을 세웠다.그의 이론은 기체 분자가 표면에서 탄성적으로 반동하지 않고 고체의 분자 집단과 유사한 방식으로 그 분자가 가지고 있다고 가정했을 때 시작되었다.[2]
랑무어는 흡착된 필름이 두께가 한 분자를 넘지 않는다는 가정을 확증한 두 개의 논문을 발표했다.첫 번째 실험은 가스의 가열된 필라멘트로부터의 전자 방출 관찰을 포함했다.[3]두 번째, 보다 직접적인 증거는 액체의 필름을 흡착 표면 층에 대고 검사하고 측정했다.그는 또한 일반적으로 표면과 흡착물질의 첫 번째 층 사이의 매력적인 강도는 첫 번째 층과 두 번째 층 사이의 강도보다 훨씬 더 크다고 지적했다.그러나 온도 및 압력의 적절한 조합을 고려할 때 후속 레이어가 응축될 수 있는 경우가 있다.[4]
모형의 기본 가정
이 모델에 내재된 다음과 같은 가정은[5] 특히 가장 단순한 경우에 유효하다: 고체의 표면에 일련의 동등한 부위로 단일 흡착하는 것이다.
- 흡착 부위가 포함된 표면은 골판이 없는 완벽하게 평평한 평면이다(표면이 균질하다고 가정한다).그러나 화학적으로 이질적인 표면은 흡착제가 표면의 기능 그룹의 한 유형에만 결합되는 경우 균질하다고 간주할 수 있다.
- 흡착 가스는 움직이지 않는 상태로 흡착한다.
- 모든 부지는 정력적으로 동등하며 흡착의 에너지는 모든 부지에 동등하다.
- 각 부위는 A의 분자를 최대 1개까지 수용할 수 있다(단층 커버리지만 해당).
- 인접 부위의 흡착 분자 사이의 (또는 이상적인) 상호작용 없음.교호작용이 이상적인 경우, 측면 교호작용의 에너지는 표면 점유에 관계 없이 모든 현장에 대해 동일하다.
Langmuir 흡착의 파생은 다른 것이다.
오직 하나의 흡착종만을 포함하는 Langmuir 흡착의 수학적 표현은 각각 운동학적 접근법, 열역학 접근법, 통계역학 접근법 등 다양한 방법으로 증명될 수 있다.경쟁적으로 흡착되는 두 종의 경우 경쟁 흡착 모델이 필요한 반면, 흡착된 종은 두 개의 뚜렷한 개체로 분리될 때, 분리 흡착 모델을 사용할 필요가 있다.
운동 유도
이 섹션은[5] 단일 흡착제 케이스에 대한 운동적 파생을 제공한다.다중 흡착 케이스는 경쟁 흡착 하위 섹션에서 다룬다.모델은 흡착과 탈착이 기본 공정이라고 가정하며, 여기서 흡착 r의ad 비율과 탈착 r의d 비율은 다음과 같다.
여기서 p는A 표면상 A의 부분압력이고, [S]는 수/m의2 자유현장의 농도, [Aad]는 분자/m의2 표면농도(점유현장의 농도)이며, k와ad k는 상기d 반응에서 전방흡착반응과 후방탈착반응의 상수다.
평형상태에서 흡착률은 탈착률과 동일하다.설정ad r = r 및d 재배치를 통해
부지 농도는 전체 표면을 덮고 있는 부지(S0)의 총수를 흡착제 면적(a)으로 나눈 값이다.
그런 다음 자유 사이트[S]와 점유 사이트의 농도를 합산하여 모든 사이트의 농도를 계산할 수 있다.
이걸 평형 방정식과 결합하면
이제 A, θ으로A 덮인 표면 부위의 분율을 정의한다.
이는 부지 균형과 평형을 결합한 이전 방정식에 적용되며, Langmuir 흡착 등식을 산출한다.
열역학적 유도
응축된 단계(솔루션)에서 고체 표면으로의 흡착은 결합 부지를 점유하기 위한 용매(A)와 용매(B) 사이의 경쟁적 과정이다.열역학적 평형은 다음과 같이 설명된다.
용제 (경계) + 솔류트 (무료) £ (무료) + 솔류트 (경계)
우리가 첨자 "1"로 용제를 지정하고 용제를 "2"로 용제를 지정하며, 위첨자 "s"(표면/경계)로 바운드 상태를 "b"(불크 용액/무료)로 지정하면, 평형 상수는 다음과 같은 과잉 반응제 간의 비율로 기록할 수 있다.
묽은 용액의 경우 b} 1} 및 활성 계수( 도 표면에서 이상적인 것으로 가정한다.Thus, , , and . ( : , X X: 몰 분율 ) 에 대한 평형 상수와 해결방법 다시 쓰기
용액 흡착제의 농도를 활성 계수 대신 사용할 수 있다는 점에 유의하십시오.그러나 평형 상수는 더 이상 치수가 없고 대신 1/농도 단위를 가질 것이다.Langmuir 모델의 운동학적 및 열역학적 파생 간의 차이는 열역학이 활동을 출발점으로 사용하는 반면 운동적 파생은 반응 속도를 사용한다는 것이다.열역학 파생은 결합 및 자유 상태의 흡착제의 활성 계수를 포함하도록 허용한다.열역학적 파생은 보통 "랑쥐르 같은 방정식"[6][7]이라고 불린다.
통계적 기계적 파생
통계역학에 기초한 이 파생은[8][9] 1925년 볼머와 마너트에[10] 의해 원래 제공되었다.표준 앙상블에서 표면에 흡착된 흡착제의 한정된 개수의 파티션 함수는 다음과 같다.
여기서 는 단일 흡착 분자의 파티션 함수, 은 흡착 지점 수(점유 및 비점유)이며, A 은 보다 작거나 같아야 하는 흡착 분자의 수입니다 괄호 안의 용어는 개별 파티션 함수의 제품을 취함으로써 흡착된 분자의 총 파티션 함수를 제공한다(하위부의 파티션 함수 참조)./ 인자는 흡착제의 구별할 수 없는 성질로 인해 발생하는 과대 계수를 설명한다.표준 파티션 함수는 다음과 같다.
는 흡착 분자의 화학적 잠재력이다.이항계열의 형태를 띠기 때문에 합이 로 줄어든다.
여기서 = L ( A ). x
평균 사용 사이트 수를 계산하는 기준
취재할 수 있게 해 주는 건
이제, 시스템이 평형 상태라는 조건, 즉 흡착 분자의 화학적 잠재력이 가스 단계의 분자와 동일하다는 조건을 불러올 때, 우리는
이상적인 가스의 화학적 잠재력은
여기서 =- k 는 파티션 기능을 가진 이상적인 기체의 헬름홀츠 자유 에너지다.
은(는) 볼륨에서 단일 입자의 파티션 함수(여기서는 변환 자유만 고려)이다.
μg =- k B T ( / ){\을(를 사용하며스털링의 근사치를 사용한다.
{\ \를 {\의 표현에 연결하면 다음과 같은 결과를 얻을 수 있다
취재할 수 있게 해 주는 건
정의
그리고 ID = N 을를) 사용하여 마지막으로
그림에는 흡착제의 부분 압력에 따라 표면 커버리지가 상당히 빠르게 증가하지만 P가 P에0 도달한 후에는 레벨이 해제된다는 것을 보여 주는 그림이 표시된다.
경쟁적 흡착
이전의 파생들은 표면으로 흡착되는 A 종만이 있다고 가정했다.이 절에서는[11] 시스템에 두 개의 뚜렷한 흡착제가 있는 경우를 고려한다.동일한 흡착 사이트에서 경쟁하는 두 종 A와 B를 고려하십시오.여기서 다음과 같은 가설이 만들어진다.
- 모든 사이트는 동등하다.
- 각 부위는 A의 최대 한 분자 또는 B의 한 분자를 포함할 수 있지만 동시에 둘 다 포함할 수는 없다.
- 인접 부위의 흡착분자 사이에는 상호작용이 없다.
운동적 고려사항을 사용하여 도출된 것처럼, A와 B 모두의 평형 상수는 다음에 의해 주어진다.
그리고
현장 잔액에는 총 현장[S0]의 농도가 자유 현장, A가 점유한 현장, B가 점유한 현장의 합계와 동일하다고 명시되어 있다.
평형 방정식을 삽입하고 단일종 흡착에 대해 했던 것과 같은 방식으로 재배열하면 we과A θB 모두에 대해 비슷한 표현을 얻게 된다.
분리 흡착
특별한 중요한 또 다른 경우는 분자2 D가 흡착시 두 개의 원자로 분리되는 경우다.[11]여기서 다음과 같은 가정이 유효하게 유지될 것이다.
- D는2 흡착시 D의 두 분자를 완전히 분리한다.
- D 원자는 고체의 표면에 있는 서로 다른 부위로 흡착한 다음 주위를 이동하여 평형화한다.
- 모든 사이트는 동일하다.
- 각 부지는 최대 D 원자 1개까지 수용할 수 있다.
- 인접 부위의 흡착분자 사이에는 상호작용이 없다.
유사한 운동적 고려를 사용하여, 우리는
p의D2 1/2 지수는 가스상 분자 하나가 흡착된 두 종을 생성하기 때문에 발생한다.위와 같이 사이트 밸런스를 적용하고,
등방성 고려사항
표면에 흡착에 의한 랑무어 단열체의 형성은 분자계의 엔트로피를 극적으로 감소시킨다.이는 고립된 시스템에서 엔트로피가 증가할 것이라는 열역학 제2법칙과 상충된다.이것은 또 다른 국소 활성 힘이 열역학적 전위보다 강하거나 또는 시스템의 엔트로피에 대한 우리의 표현이 불완전하다는 것을 암시한다.
엔트로피 감소량을 찾기 위해 우리는 흡착 상태일 때 분자의 엔트로피를 발견한다.[12]
스털링의 근사치를 이용해서
반면에 이상적인 기체의 분자의 엔트로피는
여기서 은 가스 분자의 열 de Broglie 파장이다.
모델의 제한 사항
Langmuir 흡착 모델은 주로 흡착제의 표면 거칠기를 설명하지 못하기 때문에 많은 경우 크게 편차된다.거친 비균종 표면은 흡착에 사용할 수 있는 여러 가지 현장 유형을 가지며, 흡착열과 같은 일부 매개변수는 현장마다 다르다.또한, 특정 표면적은 척도 의존적인 수량이며 이 매개변수에 대한 단일 참 값이 존재하지 않는다.[1]따라서 대체 탐침 분자를 사용하면 표면적에 대해 획득한 수치가 다를 수 있으므로 비교에 문제가 있을 수 있다.
이 모델은 또한 흡착제/흡착제 교호작용도 무시한다.실험적으로 흡착 데이터의 열에서 흡착/흡착 상호작용에 대한 명확한 증거가 있다.흡착작용에는 직접적 상호작용과 간접적 상호작용의 두 종류가 있다.직접적 상호작용은 인접한 흡착 분자 간에 이루어지는데, 이것은 다른 흡착 분자 근처에서 흡착하는 것을 다소 유리하게 만들 수 있고 높은 탐지 가능 행동에 큰 영향을 미칠 수 있다.간접 상호작용에서 흡착제는 흡착된 부위 주위의 표면을 변화시키며, 이는 다시 근처의 다른 흡착 분자의 흡착에 영향을 미친다.
수정
수정은 표면 거칠기, 비균질성 및 흡착-아도체 상호작용과 같이 위 절에서 언급된 점을 설명하려고 한다.
2-메커니즘 Langmuir 유사 방정식(TMLLE)
두 사이트 랭무어 방정식으로도 알려져 있다.이 방정식은 둘 이상의 고유한 유형의 흡착 사이트에 대한 한 흡착제의 흡착을 설명한다.각 바인딩 사이트 유형의 흡착이 나머지 유형과 독립적이기만 하면 각 바인딩 사이트는 자체 Langmuir 표현으로 설명할 수 있다.
a : 주어진 흡착제 농도에서 흡착된 총량
x : 사이트 유형 1의 최대 용량
x : 사이트 유형 2의 최대 용량
}: 대지 유형 1의 평형(선호도) 상수
}}: 부지 유형 2의 평형(선호도) 상수
: 평형 상태에서 용액에서 흡착 활성
이 방정식은 일부 약물 분자가 수소 결합과 상호작용하는 활성탄소로 흡착하는 데 효과적이며, 다른 분자는 소수성 상호작용(수소효과)을 통해 표면의 다른 부분과 상호작용한다.이 방정식은 소수성 효과(엔트로피 주도 흡착이라고도 함)를 설명하기 위해 수정되었다.[13]
효과는 2 .a } 이래 농도와 무관하다 따라서 소수성 상호작용에 대한 흡착제의 용량( B 는 피팅에서 실험 데이터에 이르기까지 얻을 수 있다.엔트로피 구동 흡착은 흡착제에 의해 대량 물 분자의 변환 운동을 제한하여 흡착 시 완화되는 것에서 비롯된다.
프룬드리히 흡착 이소템
Freundlich isotherm은 거친 표면에서 가장 중요한 다중 사이트 흡착이다.
여기서 α와F C는F 매개변수를 적합시킨다.[14]이 방정식은 흡착 데이터의 로그 로그 그림을 만들면 데이터가 직선에 적합함을 의미한다.프룬드리히 이소템은 두 개의 매개변수를 가지고 있는 반면 랑무르의 방정식은 단 하나의 매개변수를 가지고 있다. 그 결과 랑무르의 방정식보다 거친 표면의 데이터에 더 잘 적합하는 경우가 많다.그러나 Freundlich 방정식은 독특하다. 따라서 데이터가 방정식에 적합한다면 표면이 이질적이라는 것은 입증되지 않을 것이다.표면의 이질성은 칼로리 측정으로 확인할 수 있다.균질 표면(또는 균질 흡착을 보이는 이기종 표면(단일 현장)은 점유율이 %인 현장의 함수로서 일정한 H의 흡착을 가진다.한편, 이기종 흡착(다중 사이트)은 점유된 사이트의 비율에 따라 Δ H 의 흡착이 가변적이다.흡착 압력(또는 농도)이 낮을 때 높은 에너지 부지가 점유될 것이며, 압력(또는 농도)이 증가함에 따라 적은 에너지 부지가 점유되어 낮은 의 흡착이 발생할 것이다.[15]
관련 방정식은 토스 방정식이다.Langmuir 방정식을 재정렬하여 다음을 얻을 수 있다.
Toth는[16] Toth 방정식을 공식화하기 위해 α와T0 C라는T0 두 파라미터를 추가하여 이 방정식을 수정했다.
템킨 흡착 이소템
이 다른 방법은 흡착등에서의 간접 흡착-어드소브 상호작용을 고려한다.Temkin은[17] 실험적으로 흡착열은 커버리지가 증가함에 따라 증가하는 것보다 감소하는 경우가 더 많다고 지적했다.
흡착열 ΔH는ad 다음과 같이 정의된다.
그는 표면이 흡착제로 가득 차면 층 내 모든 분자의 흡착 열은 흡착과 아도르베이트 상호작용에 의해 커버리지에 따라 선형적으로 감소한다고 가정하는 모델을 도출했다.
여기서 α는T 적합한 매개변수다.Langmuir 흡착이 흡착층에도 여전히 적용된다고 가정하면 K A 은(는) 다음과 같이 커버리지에 따라 달라질 것으로 예상된다.
Langmuir의 Isotherm은 다음과 같은 형태로 재배열할 수 있다.
평형 상수의 식을 대체하고 자연 로그 취하기:
BET 방정식
브루나우어, 에멧, 텔러(BET)[18]는 다층 흡착을 위한 최초의 등심도를 도출했다.그것은 옆에 그림처럼 비어 있거나 1개의 단일 레이어, 2개의 레이어 등으로 덮인 사이트의 무작위 분포를 가정한다.이 모델의 주요 방정식은 다음과 같다.
어디에
그리고 [A]는 표면의 분자 총농도로서, 다음과 같이 주어진다.
어디에
여기서 [A]0는 맨 부위의 수이고, [A]i는 i 분자에 의해 덮인 표면 부위의 수입니다.
고체에 2진액 흡착
이 절에서는 흡착제가 액체 위상이고 이항 혼합물인 경우 표면 커버리지를 설명한다.[19]
이상적인 두 단계 - 측면 상호작용 없음, 균질 표면 - 고체 표면과 접촉하는 이항 액체 시스템의 표면 위상의 구성은 구성 요소가 변경 없이 상호 교환 가능한 고전적인 Everett isotherm 방정식(Langmuir 방정식의 단순한 아날로그)에 의해 주어진다(즉 "1"을 "2"로 교환할 수 있다).등식 형식의:
다중 구성요소 시스템의 정상적인 정의가 다음과 같이 유효할 경우:
간단한 재배열로 우리는
이 방정식은 성분 "1"과 "2"의 경쟁을 설명한다.
참고 항목
- 힐 방정식(생물화학)
- Michaelis-Menten 운동학(동일한 수학 형식과 동일)
- 모노드 방정식(동일한 수학 형식과 동일)
- 표면에서의 반응
참조
- ^ a b Hanaor, D. A. H.; Ghadiri, M.; Chrzanowski, W.; Gan, Y. (2014). "Scalable Surface Area Characterization by Electrokinetic Analysis of Complex Anion Adsorption" (PDF). Langmuir. 30 (50): 15143–15152. arXiv:2106.03411. doi:10.1021/la503581e. PMID 25495551.
- ^ Langmuir, Irving (June 1918). "The Adsorption of Gases on Plane Surface of Glass, Mica and Platinum". Journal of the American Chemical Society. 40 (9): 1361–1402. doi:10.1021/ja02242a004.
- ^ Langmuir, Irving (1916). "Part I". The Research Laboratory of the General Electric Company: 2221.
- ^ Langmuir, Irving (1918). "Part II". The Research Laboratory of the General Electric Company: 1848.
- ^ a b Masel, Richard (1996). Principles of Adsorption and Reaction on Solid Surfaces. Wiley Interscience. p. 240. ISBN 978-0-471-30392-3.
- ^ 아서 W. 아담슨표면의 물리적 화학.제6판.
- ^ Kleman, Maurice; Lavrentovich, Oleg D.; Laverntovich, Oleg D. (2004). "Surface Phenomena". Soft Matter Physics: An Introduction. Partially Ordered Systems. pp. 472–518. doi:10.1007/978-0-387-21759-8_13. ISBN 978-0-387-95267-3.
- ^ Masel, Richard (1996). Principles of Adsorption and Reaction on Solid Surfaces. Wiley Interscience. p. 242. ISBN 978-0-471-30392-3.
- ^ Cahill, David (2008). "Lecture Notes 5 Page 2" (pdf). University of Illinois, Urbana Champaign. Retrieved 2008-11-09.
- ^ Volmer, M. A.; Mahnert, P. (1925). "Solution of Solid Substances in Liquid Surfaces and the Characteristics of Layers Thus Produced". Z. Phys. Chem. 115: 253.
- ^ a b Masel, Richard (1996). Principles of Adsorption and Reaction on Solid Surfaces. Wiley Interscience. p. 244. ISBN 978-0-471-30392-3.
- ^ Cahill, David (2008). "Lecture Notes 5 Page 13" (pdf). University of Illinois, Urbana Champaign. Retrieved 2008-11-09.
- ^ 활성탄 Kirk A에 의한 수용액에서의 흡착 모델링에 대한 수정된 Langmuir 유사 모델반더캄프, 동메이치앙, 악탐아부럽, 데일 에릭 워스터 랭무어 2005년 21(1), 217-224 DOI: 10.1021/la040093o
- ^ Freundlich, H. (1909). "Eine darstellung der chemie der kolloide und verwanter gebiete". Kapillarchemie.
- ^ Adamson, A.W (1997). Physical chemistry of surfaces. p. 699.
- ^ Toth, J (1971). "State equations of the solid gas interface layer". Acta Chim. Acad. Sci. Hung. 69: 311.
- ^ Temkin, M. I.; Pyzhev, V. (1940). "Kinetics of ammonia synthesis on promoted iron catalyst". Acta Phys. Chim. USSR. 12: 327.
- ^ Brunauer, Stephen; Emmett, P. H.; Teller, Edward (1938). "Adsorption of gases in multimolecular layers". Journal of the American Chemical Society. 60 (2): 309–319. Bibcode:1938JAChS..60..309B. doi:10.1021/ja01269a023. ISSN 0002-7863.
- ^ Marczewski, A.W. (2002). "Basics of liquid adsorption". www.adsorption.org. Retrieved 2008-11-24.

 비어 있는 흡착
비어 있는 흡착 



 흡착 부지의 부분 점유, 즉
흡착 부지의 부분 점유, 즉 
![{\displaystyle r_{\text{ad}}=k_{\text{ad}}\,p_{A}\,[S],}](https://wikimedia.org/api/rest_v1/media/math/render/svg/34d7054e60ae2df6c859a214624d2d6a8eda3874)
![{\displaystyle r_{\text{d}}=k_{d}\,[A_{\text{ad}}],}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5ac4fa47126279a157264328cfc2c81da6e57099)
![{\displaystyle {\frac {[A_{\text{ad}}]}{p_{A}[S]}}={\frac {k_{\text{ad}}}{k_{\text{d}}}}=K_{\text{eq}}^{A}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/077e4f35eb173fa77f1f27dcd94fdf47658f02a7)
![{\displaystyle [S_{0}]=S_{0}/a.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5fe9664e61e335f5c0bbcc81a358265311f7f161)
![{\displaystyle [S_{0}]=[S]+[A_{\text{ad}}].}](https://wikimedia.org/api/rest_v1/media/math/render/svg/eb8d8534715cbf6040c177b81ef8d33a1987ac42)
![{\displaystyle [S_{0}]={\frac {[A_{\text{ad}}]}{K_{\text{eq}}^{A}\,p_{A}}}+[A_{\text{ad}}]={\frac {1+K_{\text{eq}}^{A}\,p_{A}}{K_{\text{eq}}^{A}\,p_{A}}}\,[A_{\text{ad}}].}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3d9c9e224cd6608b0437fc4d1ddec5340b3bf2ef)
![{\displaystyle \theta _{A}={\frac {[A_{\text{ad}}]}{[S_{0}]}}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b5f9192fa33b5270a9b86dbd1150194bf4a93f67)











![{\displaystyle Z(N_{A})=\left[\zeta _{L}^{N_{A}}{\frac {N_{S}!}{(N_{S}-N_{A})!}}\right]{\frac {1}{N_{A}!}},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/910aa4b31aea7fb2f942337a9ec81ea8b930ce44)
 단일 흡착 분자의 파티션 함수,
단일 흡착 분자의 파티션 함수, 

























![{\displaystyle {\frac {[A_{\text{ad}}]}{p_{A}\,[S]}}=K_{\text{eq}}^{A}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/44725625437993196a9a4165a46c99d75b4c333d)
![{\displaystyle {\frac {[B_{\text{ad}}]}{p_{B}\,[S]}}=K_{\text{eq}}^{B}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/663952feea387641f3370a99098080af7d12f37b)
![{\displaystyle [S_{0}]=[S]+[A_{\text{ad}}]+[B_{\text{ad}}].}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e5bf2a031efc95eaa90507d63b5417751e8f896a)


![{\displaystyle {\frac {[D_{\text{ad}}]}{p_{D_{2}}^{1/2}[S]}}=K_{\text{eq}}^{D}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/49ecd2d98dc50f2b619138e97c70576250ffff70)







 가스 분자의 열
가스 분자의 열 













![\frac{[A_{ad}]}{p_A\,[S]} = K^A_{eq} \propto \mathrm{e}^{-\Delta G_{ad}/RT} = \mathrm{e}^{\Delta S_{ad}/R}\,\mathrm{e}^{-\Delta H_{ad}/RT}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7dbc94e40b167be07b05da7e35e29caa4ccf065b)






![\frac{[A]}{S_0} = \frac{c_B \, x_B}{(1-x_B)\,[1 + (c_B - 1)\,x_B]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b41253c511d35f3b9adfa62d013de963a2a63441)

![[A] = \sum^{\infty}_{i=1} i\,[A]_i = \sum^{\infty}_{i=1}i \, K_1 \, K^{i-1}_m \, p^i_A \, [A]_0](https://wikimedia.org/api/rest_v1/media/math/render/svg/3bb2ab62d2be4dacaf2c502432368bc772df8812)
![K_i = \frac{[A]_i}{p_A\,[A]_{i-1}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0441d825bd3700721ce23e2a0cd1b851ed37bd5b)


![x_1^s \, = \, \frac{K[x_1^l/(1-x_1^l)]}{1+K[x_1^l/(1-x_1^l)]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/cc24fa2cadff29cfed92458d3afa5d84e9b58b14)


