기질 표시
Substrate presentation기질 표시는 단백질을 활성화시키는 생물학적 과정이다. 단백질은 기질로부터 격리된 후 단백질을 방출하고 기질에 노출시킴으로써 활성화된다.[1][2] 기질은 일반적으로 효소가 작용하는 물질이지만 리간드가 결합하는 단백질 표면이 될 수도 있다. 기질은 작용하는 물질이다. 효소와 상호작용하는 경우, 단백질이나 유기 기질은 일반적으로 화학적 형태를 바꾼다. 기질 표시는 효소가 촉매분석을 시작하기 위해 순응을 변경할 필요가 없다는 점에서 고환성 조절과 다르다. 기질 표시는 나노경사 거리(<100nm)에 대해 가장 잘 설명된다.
예
아밀로이드 전구단백질
아밀로이드 전구단백질(APP)은 베타 및 감마시크레이아제에 의해 분해되어 알츠하이머병과 관련된 베타 아밀로이드 플라크를 담당하는 40-42 아미노산 펩타이드를 생산한다. 효소는 기질 발현에 의해 조절된다.[3] 기질 APP는 아스트로사이테 콜레스테롤에 반응하여 GM1 지질 뗏목을 들락날락한다. 아폴리포프로테인 E(ApoE)에 의해 전달된 콜레스테롤은 APP를 GM1 지질 뗏목과 연결하도록 유도한다. 콜레스테롤이 낮으면 단백질이 탈선 부위로 밀거래되고 알파 분비물에 의해 분해되어 비아밀 유발 제품을 만든다. 효소는 콜레스테롤에 반응하는 것처럼 보이지 않고 기질만 움직인다.
친수성은 분자의 분할을 촉진한다. 세포 안에서, 이것은 세포 내부와 세포막 안에서 구획화를 일으킨다. 지질 뗏목의 경우, 팜티토일화는 대부분의 뗏목 단백질에 대한 뗏목 친화력을 조절한다.[4] 뗏목 규제는 콜레스테롤 신호에 의해 조절된다.
인산리파제 D2
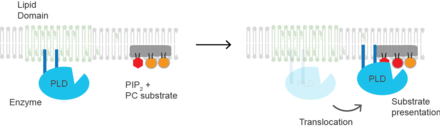
(PLD2)는 기질 발현에 의해 활성화되는 효소의 잘 정의된 예다.[5] 이 효소는 팜토이롤링되어 효소가 GM1 지질 영역이나 "지질 뗏목"으로 이동하게 된다. 인산리파제 D의 기질은 불포화인 인산염(PC)으로 지질 뗏목이 풍부하지 않다. PC는 다불포화 지방질인산염 4,5-비스인산염(PIP2)과 함께 세포의 불순부위로 국소화한다. PLD2에는 PIP2 바인딩 도메인이 있다. 멤브레인 내 PIP2 농도가 증가하면 PLD2는 GM1 도메인을 떠나 PIP2에 바인딩되며, PLD2는 기질 PC에 접근하여 기질 표시에 기반한 강직화를 시작한다. 아마도 이 효소는 지질 뗏목에서 반응을 촉진시킬 수 있지만 활동을 위한 기질이 부족하다.
염증
TACE라고도 불리는 (ADAM17)는 기질인 막결합종양 괴사인자(mTNF)에서 떨어진 지질 뗏목으로 격리된다.콜레스테롤은 mTNF가 지질 뗏목에 ADAM17과 군집하게 하고, 염증성 사이토카인 수용성 TNF(sTNF)를 떨어뜨린다.
사스-코브-2
(후린) (생성세포, 복제) 세포에 콜레스테롤 퓨린 트래핑을 싣고 사스-CoV-2의 팜토이틀화 스파이크 단백질로 국부화된 GM1 뗏목으로 옮겨 바이러스 유입을 위해 프리밍한다.[7]
(ACE2) (대상 세포, 바이러스 유입) SARS-CoV-2 ACE2의 수용체 SARS-CoV-2를 GM1 지질 뗏목으로 내포되어 갈라짐과 최적의 세포 융합을 위해 카테핀에 노출된다.[8] 저콜레스테롤 ACE2에서는 바이러스를 TMPRSS2로 밀거래하는데, TMPRSS2는 바이러스를 분해하여 바이러스 유입을 허용하지만 훨씬 효율적이지 않은 표면 메커니즘을 통해서도 바이러스를 유입시킨다. 콜레스테롤에 대한 ACE2의 민감성은 어린이들에게 덜 심각한 COVID19 증상에 기여하는 것으로 생각된다.
활성화 메커니즘
격리
혈장막 내에서 격리 작용은 주로 포화 지방질을 콜레스테롤과 함께 포장하거나 매우 작은 거리(< 100 nm)에서 위상 분리를 통해 이루어진다. 거시적으로 볼 때, 오르가넬과 베실체는 기질에 대한 효소의 접근을 제한할 수 있다. 효소의 기질이 움직일 수도 있다. 이동은 일반적으로 팜티테이트 매개 지방화 또는 오르가넬 밀매의 중단이다. palmitoylated와 bind PIP2 둘 다인 단백질의 경우, PIP2의 농도를 증가시키면 pip2는 poly 불포화 효소가 pip2로 밀거래되는 것을 선호한다. PIP2는 주로 poly 불포화 되어 lipid 뗏목에서 떨어져서 localization을 유발하고 pip2가 palitate med localized localized localization을 반대하도록 한다.[9]
규정
콜레스테롤
콜레스테롤과 다불포화지방산(PUFA)은 지질 뗏목 형성을 조절해 뗏목의 생물학적 기능을 조절한다. 막에서 포화 지방질과 콜레스테롤이 증가하면 지질 뗏목은 팜토이틀린 단백질에 대한 친화력을 높인다.[10] PUFA는 반대 효과가 있다. 그들은 막을 유동화한다.
PUFA
PUFA는 신호 지질의 농도를 증가시킬 수도 있다. 뇌에서 매우 흔한 PUFA인 아라키돈산은 PC에 통합된다.[11] 아라키도닐 PC는 셀의 PA 양을 증가시킬 가능성이 있는 PLD의 선호 기질이다. 콜레스테롤에 의한 뗏목 기능의 조절은 기질 발현과 기질 발현을 활성화의 메커니즘으로 활용하는 많은 팜티토일화 단백질을 효과적으로 조절한다. 추측이 가능하지만, 콜레스테롤과 PUFA가 인간의 건강에 미치는 심오한 영향은 세포 내 지질 뗏목 기능의 생리학적 조절을 통해 나타날 가능성이 높다.
생물학에서의 역할
기계화
기계적 힘(날개 또는 팽창)은 독립적으로 패킹과 지질 뗏목에 대한 팜티테이트의 결과적 친화력을 방해할 수 있다. 이러한 혼란은 또한 PLD2가 PIP2 도메인으로의 인신매매에 찬성하게 만든다.[12]
마취
일반 마취제 프로포폴과 흡입한 마취제 제논, 클로로포름, 이소플루란, 디에틸에테르가 PLD2에서 지질 래프트에 대한 팜티테 매개 국산화 등 지질 래프트 기능을 방해한다.[13][14] PLD의 활성화는 TREK-1 채널을 활성화한다. 멤브레인 매개 PLD2 활성화는 마취 불감증 호몰로그 TRAK로 전달되어 채널 마취 민감성을 회복시킬 수 있다.
참조
- ^ Petersen, EN; Pavel, MA; Wang, H; Hansen, SB (28 October 2019). "Disruption of palmitate-mediated localization; a shared pathway of force and anesthetic activation of TREK-1 channels". Biochimica et Biophysica Acta (BBA) - Biomembranes. 1862 (1): 183091. doi:10.1016/j.bbamem.2019.183091. PMC 6907892. PMID 31672538.
- ^ Robinson, CV; Rohacs, T; Hansen, SB (September 2019). "Tools for Understanding Nanoscale Lipid Regulation of Ion Channels". Trends in Biochemical Sciences. 44 (9): 795–806. doi:10.1016/j.tibs.2019.04.001. PMC 6729126. PMID 31060927.
- ^ Wang, Hao; Kulas, Joshua A.; Wang, Chao; Holtzman, David M.; Ferris, Heather A.; Hansen, Scott B. (17 August 2021). "Regulation of beta-amyloid production in neurons by astrocyte-derived cholesterol". Proceedings of the National Academy of Sciences. 118 (33): e2102191118. doi:10.1073/pnas.2102191118. ISSN 0027-8424. PMC 8379952. PMID 34385305.
- ^ Levental, I; Lingwood, D; Grzybek, M; Coskun, U; Simons, K (21 December 2010). "Palmitoylation regulates raft affinity for the majority of integral raft proteins". Proceedings of the National Academy of Sciences of the United States of America. 107 (51): 22050–4. Bibcode:2010PNAS..10722050L. doi:10.1073/pnas.1016184107. PMC 3009825. PMID 21131568.
- ^ Petersen, EN; Chung, HW; Nayebosadri, A; Hansen, SB (15 December 2016). "Kinetic disruption of lipid rafts is a mechanosensor for phospholipase D." Nature Communications. 7: 13873. Bibcode:2016NatCo...713873P. doi:10.1038/ncomms13873. PMC 5171650. PMID 27976674.
- ^ Tellier, Edwige; Canault, Matthias; Rebsomen, Laure; Bonardo, Bernadette; Juhan-Vague, Irène; Nalbone, Gilles; Peiretti, Franck (10 December 2006). "The shedding activity of ADAM17 is sequestered in lipid rafts". Experimental Cell Research. 312 (20): 3969–3980. doi:10.1016/j.yexcr.2006.08.027. PMID 17010968.
- ^ Wang, Hao; Yuan, Zixuan; Pavel, Mahmud Arif; Hansen, Scott B. (29 May 2020). "The role of high cholesterol in age-related COVID19 lethality". bioRxiv: 2020.05.09.086249. doi:10.1101/2020.05.09.086249. PMC 7263494. PMID 32511366.
- ^ Wang, Hao; Yuan, Zixuan; Pavel, Mahmud Arif; Hansen, Scott B. (29 May 2020). "The role of high cholesterol in age-related COVID19 lethality". bioRxiv: 2020.05.09.086249. doi:10.1101/2020.05.09.086249. PMC 7263494. PMID 32511366.
- ^ Hansen, SB (May 2015). "Lipid agonism: The PIP2 paradigm of ligand-gated ion channels". Biochimica et Biophysica Acta (BBA) - Molecular and Cell Biology of Lipids. 1851 (5): 620–8. doi:10.1016/j.bbalip.2015.01.011. PMC 4540326. PMID 25633344.
- ^ Levental, I; Lingwood, D; Grzybek, M; Coskun, U; Simons, K (21 December 2010). "Palmitoylation regulates raft affinity for the majority of integral raft proteins". Proceedings of the National Academy of Sciences of the United States of America. 107 (51): 22050–4. Bibcode:2010PNAS..10722050L. doi:10.1073/pnas.1016184107. PMC 3009825. PMID 21131568.
- ^ Petersen, E. Nicholas; Gudheti, Manasa; Pavel, Mahmud Arif; Murphy, Keith R.; Ja, William W.; Jorgensen, Erik M.; Hansen, Scott B. (5 September 2019). "Phospholipase D Transduces Force to TREK-1 Channels in a Biological Membrane". bioRxiv 10.1101/758896.
- ^ Petersen, EN; Pavel, MA; Wang, H; Hansen, SB (28 October 2019). "Disruption of palmitate-mediated localization; a shared pathway of force and anesthetic activation of TREK-1 channels". Biochimica et Biophysica Acta (BBA) - Biomembranes. 1862 (1): 183091. doi:10.1016/j.bbamem.2019.183091. PMC 6907892. PMID 31672538.
- ^ Petersen, EN; Pavel, MA; Wang, H; Hansen, SB (1 January 2020). "Disruption of palmitate-mediated localization; a shared pathway of force and anesthetic activation of TREK-1 channels". Biochimica et Biophysica Acta (BBA) - Biomembranes. 1862 (1): 183091. doi:10.1016/j.bbamem.2019.183091. PMC 6907892. PMID 31672538.
- ^ Pavel, Mahmud Arif; Petersen, E. Nicholas; Wang, Hao; Lerner, Richard A.; Hansen, Scott B. (19 June 2019). "Studies on the mechanism of membrane mediated general anesthesia". bioRxiv 10.1101/313973.



