셸 상위 올레핀 공정
Shell higher olefin process셸 고등 올레핀 공정은 로얄 더치 셸이 발명하고 착취한 올레핀 메타텍스 및 에틸렌 올리고머화를 통한 선형 알파 올레핀 생산을 위한 화학 공정이다.[1] 올레핀 제품은 지방 알데히드로 변환된 다음 지방 알코올로 변환되는데, 이는 전구체 가소제 및 세제다. 이 방법을 통한 올레파인 연간 세계 생산량은 100만톤이 넘는다.[2]
역사
이 과정은 1968년 쉘 개발 에머리빌의 화학자들에 의해 발견되었다. 당시 생태학적 고려는 세제에 널리 사용되는 갈기 지방 알코올을 선형 지방 알코올로 대체할 것을 요구했는데, 갈기 화합물의 생물분해가 느려서 표면 수분의 거품이 발생했기 때문이다.[2] 동시에 새로운 가스오일 크래커가 위탁되고 에틸렌 공급이 수요를 앞지르고 있었다.[2] 이 공정은 1977년 로열더치셸에 의해 상용화되었으며, 2002년 루이지애나주 게이샤르(Geismar, 미국) 공장 증설에 이어 전 세계 연간 생산능력은 120만 톤이었다.[3]
과정
에틸렌은 촉매에 의해 반응하여 더 긴 사슬을 준다. 매우 긴 폴리머 생산을 목표로 하는 지글러-나타 공정과 달리 과점체는 에틸렌 1~10단위를 반복한 후 성장을 멈춘다. C12~C올레핀18(40~50%)이 함유된 분수는 세제 생산에서 직접적인 상업적 가치를 지녀 제거된다.[2] 나머지 부분이 상업적 이익이 되려면 두 단계를 더 진행해야 한다. 첫 번째 단계는 알칼리성 알루미나 촉매를 이용한 액체 위상 이소머라이징으로 내부 이중 결합을 유도하는 것이다. 예를 들어 1옥틴은 4옥틴으로, 1에코센(C20 탄화수소)은 10에코센으로 전환된다. 두 번째 단계에서 올레핀 메타텍스전구는 이와 같은 혼합물을 C14 성분인 2-테트라데센으로 변환하고 다시 상용 범위 내에서 변환한다.[2]
또한 내부 올레핀은 알루미나에 지원되는 레늄(VII) 산화물 함유 에틸렌의 과잉으로 반응할 수 있으며, 이는 내부 이중 결합을 분열시켜 원하는 분자 중량의 홀수 및 짝수 탄소 체인 길이와 α-올레핀의 혼합물을 형성하게 한다.[4]
C에서12 C18 올레핀은 이후 알데히드를 주기 위해 하이드로폼화(옥소 공정)를 받는다. 알데히드는 수소를 첨가해 지방성 알코올을 공급하는데, 이 알코올은 세제 제조에 적합하다.[4]
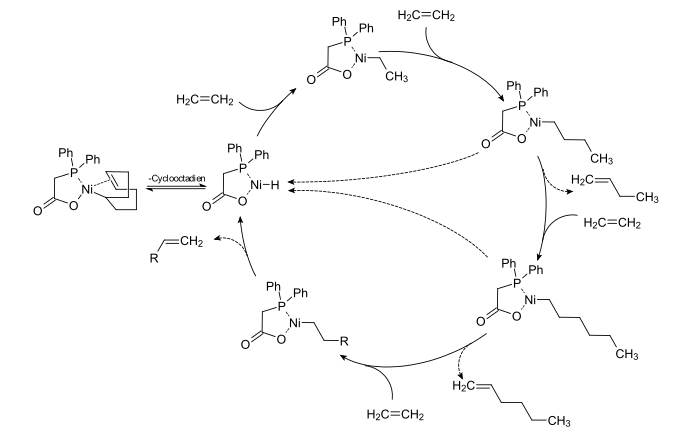
촉매 사이클
이 프로세스의 첫 번째 단계는 니켈-인산 복합체에 의해 촉매된 80~120℃와 70~140bar(7~14 MPa)의 짝수 α-olefin 혼합물에 대한 에틸렌 과점이다. 그러한 촉매들은 (CH65)2PCHCCOH와22 같은 일지 인산 카복실산으로부터 일반적으로 준비된다.[5] 그 과정과 그 메커니즘은 처음에는 Shell에서 그리고 나중에는 RWTH Aachen에서 Wilhelm Keim 그룹에 의해 설명되었다.[6]
대체 경로
또 다른 올레핀 적용에서 쉘 사이클로데카트리엔은 부분적으로 사이클로데켄에 수소를 공급한 후 단자 선형 오픈 체인 디엔에 대한 에테노리시스(Ethernolysis)를 받는다. 이 과정은 심각한 폭발이 일어날 때까지 Essar Stanlow 정제소에서 계속 사용되었고, 화재 이후 2018년에 공장 폐쇄와 그것이 공급한 알코올 유닛으로 이어졌다.
참조
- ^ 산업 유기 화학, 클라우스 와세르멜, 한스 주르겐 아르페 존 와일리 & 선스, 1997년 3차 ISBN3-527-28838-4
- ^ a b c d e Keim, W.(2013), 에틸렌을 α-올레핀에 대한 올리고머화: Shell High Olefin Process(Shell High Olefin Process)의 발견 및 개발. 안젤라, 화학. Ed. 52: 12492–12496. doi:10.1002/anie.201305308
- ^ Mol, J. C. (2004). "Industrial applications of olefin metathesis". Journal of Molecular Catalysis A: Chemical. 213: 39–45. doi:10.1016/j.molcata.2003.10.049.
- ^ a b Reuben, Bryan; Wittcoff, Harold (1988). "The SHOP process: An example of industrial creativity". J. Chem. Educ. 65 (7): 605. Bibcode:1988JChEd..65..605R. doi:10.1021/ed065p605.
- ^ Kuhn, P.; Semeril, D.; Matt, D.; Chetcuti, M. J.; Lutz, P. (2007). "Structure–Reactivity Relationships in SHOP-Type Complexes: Tunable Catalysts for the Oligomerisation and Polymerisation of Ethylene". Dalton Trans. (5): 515–528. doi:10.1039/B615259G. PMID 17225902.
- ^ Gadi Rothenberg (17 March 2008). Catalysis: Concepts and Green Applications (Google Books excerpt). p. 97. ISBN 9783527318247.