계피산
Cinnamic acid | |
 | |
 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 (2E)-3-페닐프로프-2-에노산 | |
| 기타 이름 | |
| 식별자 | |
3D 모델(JSmol) | |
| 3 DMet | |
| 1905952 | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.004.908 |
| EC 번호 |
|
| 3731 | |
| 케그 | |
PubChem CID | |
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| C9H8O2 | |
| 몰 질량 | 148.140 g/140−1 |
| 외모 | 백색 단사정계 결정 |
| 냄새 | 꿀[2] 같은 |
| 밀도 | 1.2475g/cm3[3] |
| 녹는점 | 133 °C (271 °F, 406 [3]K) |
| 비등점 | 300 °C (572 °F, 573 [3]K) |
| 500 mg/L[3] | |
| 산도(pKa) | 4.44 |
자화율(δ) | - 7.836×10cm−53/세로 |
| 위험 요소 | |
| GHS 라벨링: | |
 | |
| 경고 | |
| H315, H319, H335 | |
| P261, , , , , , , , , , , | |
| NFPA 704(파이어 다이아몬드) | |
| 플래시 포인트 | > 100 °C (212 °F, 373 [3]K) |
| 관련 화합물 | |
관련 화합물 | 벤조산, 페닐아세트산, 페닐프로판산 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
계피산은 식 CH-CH65=CH-COOH의 유기화합물이다.물에 약간 녹고 많은 유기 [4]용제에 자유롭게 녹는 하얀 결정성 화합물입니다.불포화 카르본산으로 분류되며, 많은 식물에서 자연적으로 발생합니다.시스 이성질체와 트랜스 이성질체로 존재하지만, 트랜스 이성질체가 더 [5]흔하다.
발생 및 생산
생합성
계피산은 리그놀, 플라보노이드, 이소플라보노이드, 쿠마린, 오론, 스틸벤, 카테킨 및 페닐프로파노이드를 포함한 수많은 천연물의 생합성에 있어 중심 중간체이다.그것의 생합성에는 페닐알라닌에 [6]대한 페닐알라닌 암모니아분해효소(PAL)의 작용이 포함된다.
자연발생
그것은 계피 기름이나 스토락스 [4]같은 발사암에서 얻습니다.그것은 또한 시어버터에서도 발견된다.계피산은 꿀 같은 [2]냄새를 가지고 있으며, 계피산과 그 휘발성이 더 높은 에틸에스테르(계피산 에틸)는 관련된 계피알데히드가 주요 성분인 계피 에센셜 오일의 향미 성분이다.
합성
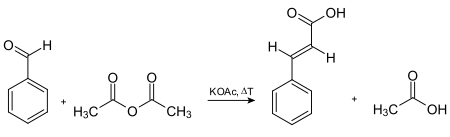
계피산은 염화아세틸과 벤즈알데히드의 염기 촉매 축합에 의해 먼저 합성된 후 염산 [5]생성물의 가수 분해에 의해 합성되었다.1890년, 라이너 루드비히 클라이젠은 나트륨의 존재 [7]하에서 아세트산에틸과 벤즈알데히드의 반응을 통해 계피산에틸의 합성을 설명했습니다.계피산을 조제하는 또 다른 방법은 크노에베나겔 축합 반응에 [8]의한 것이다.이에 대한 반응물은 약한 염기의 존재 하에서 벤즈알데히드와 말론산이며, 이어서 산 촉매 탈탄산이다.계피알데히드의 산화, 염화벤잘과 아세트산나트륨의 응축(그 후 산 가수분해), 퍼킨 반응을 통해서도 제조할 수 있다.계피산에 대한 가장 오래된 상업적으로 사용되는 경로는 퍼킨 반응을 수반하며, 이는 다음[5] 체계에서 주어진다.
대사
계피알데히드의 자동산화에서 얻은 계피산은 [10]간에서 벤조산나트륨으로 대사된다.
사용하다
계피산은 조미료, 합성 인디고, 특정 의약품에 사용된다.주요 용도는 향수 [4]산업을 위한 계피산메틸, 계피산 에틸 및 계피산벤질 제조의 전구체이다.계피산은 페닐알라닌을 [5]생성하기 위해 효소 촉매 아미노화를 통해 감미료 아스파탐의 전구체이다.계피산은 비극성 용매에서 이합체를 형성하여 서로 다른 선형 자유 에너지 [11]관계를 형성할 수 있습니다.
레퍼런스
- ^ . Encyclopædia Britannica. Vol. 6 (11th ed.). 1911. p. 376.
- ^ a b "Cinnamic acid". flavornet.org.
- ^ a b c d e 산업안전보건연구소 GESTIS 물질 데이터베이스 기록
- ^ a b c Budavari, Susan, ed. (1996), The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (12th ed.), Merck, ISBN 0911910123
- ^ a b c d Garbe, Dorothea (2012). "Cinnamic Acid". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a07_099.
- ^ Vogt, T. (2010). "Phenylpropanoid Biosynthesis". Molecular Plant. 3 (1): 2–20. doi:10.1093/mp/ssp106. PMID 20035037.
- ^ Claisen, L. (1890). "Zur Darstellung der Zimmtsäure und ihrer Homologen" [On the preparation of cinnamic acid and its homologues]. Berichte der Deutschen Chemischen Gesellschaft. 23: 976–978. doi:10.1002/cber.189002301156.
- ^ Tieze, L. (1988). Reactions and Synthesis in the Organic Chemistry Laboratory. Mill Vall, CA. p. 1988.
- ^ F. K. Thayer (1925). "m-Nitrocinnamic Acid". Organic Syntheses. 5: 83. doi:10.15227/orgsyn.005.0083.
- ^ Jana A, Modi KK, Roy A, Anderson JA, van Breemen RB, Pahan K (June 2013). "Up-regulation of neurotrophic factors by cinnamon and its metabolite sodium benzoate: therapeutic implications for neurodegenerative disorders". Journal of Neuroimmune Pharmacology. 8 (3): 739–55. doi:10.1007/s11481-013-9447-7. PMC 3663914. PMID 23475543.
- ^ Bradley, J.-C.; Abraham, M. H.; Acree, W. E.; Lang, A.; Beck, S. N.; Bulger, D. A.; Clark, E. A.; Condron, L. N.; Costa, S. T.; Curtin, E. M.; Kurtu, S. B.; Mangir, M. I.; McBride, M. J. (2015). "Determination of Abraham model solute descriptors for the monomeric and dimeric forms of trans-cinnamic acid using measured solubilities from the Open Notebook Science Challenge". Chemistry Central Journal. 9: 11. doi:10.1186/s13065-015-0080-9. PMC 4369286. PMID 25798191.