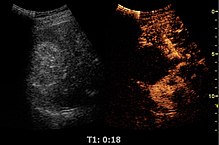
조영증진 초음파
Contrast-enhanced ultrasound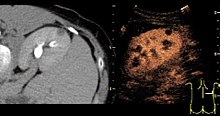
조영 증강 초음파(CEUS)는 초음파 조영제를 기존의 의료 소노그래피에 적용한 것이다. 초음파 조영제는 물질들 사이의 인터페이스에서 음파가 반사되는 다른 방법에 의존한다. 이것은 작은 공기 방울의 표면일 수도 있고 더 복잡한 구조일 수도 있다. 상업적으로 이용 가능한 조영제는 가스를 가득 채운 미세 거품이며, 계통 순환에 정맥으로 투여된다. 마이크로버블은 높은 수준의 초음파 발생성(물체의 초음파 반사 능력)을 가지고 있다. 마이크로 버블에 있는 기체와 신체의 연조직 주위에는 초음파생성에 큰 차이가 있다. 따라서 마이크로 버블 조영제를 사용한 초음파 영상촬영은 초음파 백스캐터(반사)를 강화시켜 초음파 발생도 차이가 높아 대비를 높인 초음파 촬영법을 만든다. 대조 강화 초음파는 장기의 혈액 관류를 영상화하고, 심장과 다른 장기의 혈류량을 측정하며, 다른 용도로 사용할 수 있다.
혈관내 질환의 특징인 수용체와 결합하는 리간드를 대상으로 하는 것은 마이크로버블(microbubbles)으로 결합할 수 있어 마이크로버블 복합체가 병든 조직이나 비정상 조직 등 관심 영역에 선택적으로 축적될 수 있다. 표적 대비 강화 초음파라고 알려진 이러한 형태의 분자 영상촬영은 표적 마이크로버블이 관심 영역에 결합할 경우에만 강력한 초음파 신호를 발생시킬 것이다. 표적 대조 강화 초음파는 의료 진단과 의료 치료 모두에 많은 응용이 있을 수 있다. 그러나 이 표적 기술은 아직 FDA로부터 미국 내 임상 사용을 승인받지 못했다.
조영 증강 초음파는 성인에게 안전한 것으로 간주되며, MRI 조영제의 안전성에 비견되며, 조영 CT 스캔에 사용되는 방사선 조영제보다 우수하다. 어린이의 안전 데이터가 더 제한적일수록 그러한 사용은 성인 인구만큼 안전하다는 것을 시사한다.[2]
버블 심초음파
심초음파란 초음파를 이용한 심장에 대한 연구다. 버블 심초음파(bubble echoardio)는 이 연구의 연장선으로 간단한 기포를 조영제로 사용하며 종종 구체적으로 요청해야 한다.
색 도플러(Color Doppler)를 사용하여 심방 사이의 비정상적인 흐름을 감지할 수 있지만(예: 아멘 오발레에 대한 지속성(특허성)) 감도는 제한적이다. 이와 같은 결함을 구체적으로 찾을 때는 작은 기포를 조영제로 사용하고 정맥주사를 통해 심장의 우측으로 이동할 수 있다. 이 검사는 기포가 심장의 좌측으로 지나가는 것이 보이면 비정상적인 의사소통에 양성반응을 보일 것이다.(보통 기포가 폐동맥을 통해 심장을 빠져나와 폐에 의해 정지된다.) 이러한 형태의 거품 조영제는 주입 직전 시험 임상의사가 일반 식염수(예를 들어 연결된 두 주사기 사이에 식염수를 빠르고 반복적으로 전달함)를 자극하여 임시로 생성한다.[citation needed]
마이크로버블 콘트라스트제
일반 기능
다양한 미세 버블 콘트라스트제가 있다. 마이크로버블은 쉘 메이크업, 가스코어 메이크업, 대상 여부 등에서 차이가 난다.[citation needed]
- 마이크로 버블 껍질: 껍질 물질의 선택은 마이크로 버블이 면역체계에 의해 얼마나 쉽게 흡수되는지를 결정한다. 더 많은 친수성 물질은 더 쉽게 흡수되는 경향이 있고, 이것은 순환하는 미세 거품들의 거주 시간을 줄여준다. 이렇게 하면 조영 영상촬영에 사용할 수 있는 시간이 줄어든다. 셸 재료는 또한 미세 버블 기계적 탄성에도 영향을 미친다. 소재에 탄력이 있을수록 터지기 전에 버틸 수 있는 음향 에너지가 많아진다.[3] 현재 마이크로버블 껍질은 알부민, 갈락토스, 지질, 폴리머로 구성되어 있다.[4]
- 마이크로 버블 가스 코어: 가스 코어는 초음파 대비 마이크로 버블에서 가장 중요한 부분이다. 왜냐하면 그것은 초음파 대비 마이크로 버블을 측정하기 때문이다. 기포가 초음파 주파수장에 잡히면 기포가 압축, 진동, 특성 에코를 반영해 대조 강화 초음파에서 강하고 독특한 초음파 초음파를 생성한다. 가스 코어는 공기 또는 과불화탄소 또는 질소와 같은 무거운 기체로 구성될 수 있다.[4] 무거운 가스는 수용성이 낮기 때문에 미세 버블에서 빠져나와 미세 버블 해체로 이어질 가능성이 적다.[3] 그 결과 가스 코어가 무거운 마이크로 버블이 더 오래 유통된다.
셸이나 가스 코어 구성과 상관없이 마이크로 버블 크기는 상당히 균일하다. 그것들은 지름 1~4마이크로미터의 범위 안에 놓여 있다. 그렇게 되면 적혈구보다 크기가 작아져 미세순환뿐만 아니라 혈액순환을 통해 쉽게 흐를 수 있게 된다.
특정 에이전트
- 과플루트렌 지질 마이크로스피어(브랜드명 Definity, Luminity)는 외부 지질 껍질에 캡슐화된 옥타플루오로프로판(Octafluoropropane)으로 구성된 과불화탄소 유화액이다.[5][6]
- 알부민 껍질이 있는 옥타플루오로프로판 가스코어(Optison)는 또 다른 과불화탄소 에멀젼으로 식품의약국(FDA)이 승인하고 GE헬스케어가 만든 마이크로버블이다.
- 헥사플루오린드 마이크로 버블(SonoVue Bracoon(회사)) 재래식(b-모드) 초음파로는 제대로 식별할 수 없는 간 병변의 특성화에 주로 쓰인다. 3~8분 동안 혈액 속에 잘 보이고 폐에 의해 소멸된다.[7]
- 지질/갈락토스 껍질 내의 공기(이전의 레보비스트, 스크링에 의해 만들어진 FDA 승인 마이크로 버블).[4]
- Perflexane Lipid microspects(구 Imagent 또는 Imavist)는 심장의 좌심실 시각화 개선, 차최적 심초음파 환자의 심내막경계선을 디라인화하기 위해 FDA가 승인한 (2002년 6월) 얼라이언스 제약사가 개발한 주입식 중지제였다. 심장 기능과 관류를 평가하는 데 사용되는 것 외에도, 그것은 전립선, 간, 신장 및 다른 장기의 영상의 강화제로도 사용된다.[8]
표적형 마이크로 버블
표적형 미세 기포가 임상 전 개발 중에 있다. 이들은 미획득 미세거품들과 같은 일반적인 특징을 가지고 있지만 염증 세포나 암세포와 같이 세포유형에 의해 표현되는 특정 수용체를 묶는 리간드를 가지고 있다. 현재 개발 중인 마이크로 버블은 과불화탄소 가스 코어를 가진 지질 단열재 껍질로 구성되어 있다. 지질 껍질은 폴리에틸렌 글리콜(PEG) 층으로도 덮여 있다. PEG는 마이크로 버블 집적을 방지하고 마이크로 버블을 더 비활성화시킨다. 그것은 일시적으로 면역 체계의 미세 버블을 "숨겨서" 순환 시간을 증가시키고, 따라서 영상 시간을 증가시킨다.[9] PEG층 외에도 특정 수용체를 묶는 리간드를 부착할 수 있는 분자로 껍질이 변형된다. 이 리간드는 카르보디미드, 말레미드 또는 비오틴-스트렙타비딘 결합을 사용하여 마이크로 버블에 부착된다.[9] 비오틴-스트렙타비딘은 비오틴의 스트렙타비딘 친화력이 매우 강하고 리간드에 비오틴을 붙이기 쉽기 때문에 가장 인기 있는 커플링 전략이다. 현재 이들 리간드는 특별히 대상 세포 유형에 의해 표현된 수용체와 분자와 결합하는 동물 세포 배양으로부터 생성된 단세포 항체다. 항체는 인간화되지 않기 때문에 인간 치료에 사용될 때 면역 반응을 이끌어낼 것이다. 항체를 인간화하는 것은 비용이 많이 들고 시간이 많이 걸리는 과정이기 때문에, 같은 기능을 수행하지만 면역 문제는 없는 펩타이드들을 대상으로 합성적으로 제조되는 것과 같은 리간드의 대체 원천을 찾는 것이 이상적일 것이다.[citation needed]
종류들
조영제 강화 초음파에는 두 가지 형태가 있는데, 두 가지 형태는 비수술(오늘날의 클리닉에서 사용)과 표적 초음파(임상 전 발달)이다. 그 두 가지 방법은 서로 약간 다르다.
언타겟 CEUS
앞서 말한 소노뷰, 옵티슨 또는 레보비스트와 같은 미생물의 미세 거품이 작은 볼루스 안에서 정맥주사로 전신 순환에 주입된다. 마이크로 버블은 일정 기간 동안 시스템 순환에 남을 것이다. 그 기간 동안 초음파는 관심 영역을 향한다. 혈액 속의 미세 기포가 영상 창을 지나 흐를 때 초음파 기사에서 설명한 고주파 소닉 에너지장에 반응하여 미세 기체의 압축 가스 코어가 진동한다. 마이크로버블은 미세버블과 조직계유성의 크기 불일치 순서에 따라 주변 조직과 극명한 대조를 이루는 독특한 메아리를 반영한다. 초음파 시스템은 강한 초음파생성을 대조적으로 강화된 관심 영역의 이미지로 변환한다. 이렇게 하면 혈류의 메아리가 높아져 임상의가 혈액을 주변 조직과 구별할 수 있게 된다.[citation needed]
타겟 CEUS
표적 대조 강화 초음파도 비슷한 방식으로 작동하며, 몇 가지 변경사항이 있다. 이미징 관심 영역에 의해 표현되는 특정 분자 표지를 묶는 리간드로 표적이 된 마이크로버블은 여전히 작은 볼러스에 시스템적으로 주입된다. 마이크로 버블은 이론적으로 순환계를 통해 이동하며, 결국 각자의 목표를 찾고 구체적으로 구속력을 갖는다. 초음파 파장은 관심 영역으로 향할 수 있다. 만약 충분한 수의 마이크로 버블이 그 영역에 결합되어 있다면, 그들의 압축 가능한 가스 코어는 초음파 기사에서 설명한 고주파 소닉 에너지장에 반응하여 진동한다. 대상 마이크로버블은 마이크로버블과 조직계유전성의 크기 불일치 순서에 따라 주변 조직과 극명한 대조를 이루는 독특한 에코도 반영한다. 초음파 시스템은 강한 초음파생성을 관심 영역의 대비 강화 영상으로 변환해 결합 미세 거품의 위치를 밝힌다.[10] 결합 마이크로 버블의 검출은 관심 영역이 특정 질병 상태를 나타내거나 관심 영역의 특정 세포를 식별할 수 있는 특정 분자 마커를 표현하고 있음을 보여줄 수 있다.[citation needed]
적용들
초음파 검사는 초음파 초음파 검사 및 방사선 검사에서 실시되고 있다. 표적 대조 강화 초음파는 다양한 의료 용도에 대해 개발되고 있다.
언타겟 CEUS
Optison이나 Levovist와 같은 미생물의 미세 분비가 현재 심장 초음파 검사에서 사용되고 있다. 또한 병변 특성화를 위해 방사선학에서도 소노뷰[11] 초음파 조영제가 사용된다.
- 기관 가장자리 디라인레이션: 미세 거품은 조직과 혈액 사이의 인터페이스에서 대비를 향상시킬 수 있다. 이 인터페이스의 더 선명한 그림은 임상의에게 장기 구조에 대한 더 나은 그림을 제공한다. 심초음파에서 조직구조는 중요한데 심장벽의 얇아지거나 두꺼워지거나 불규칙한 상태가 관찰이나 치료가 필요한 심각한 심장 상태를 나타낸다.
- 혈액 용적과 관류: 대조 강화 초음파에는 (1) 장기 또는 관심 영역의 혈액 관류 정도를 평가하고 (2) 장기 또는 관심 영역의 혈액량을 평가하는 약속이 들어 있다. 도플러 초음파와 함께 사용하면 미세 기포가 심근 유량을 측정해 밸브 문제를 진단할 수 있다. 그리고 미세 버블 메아리의[12] 상대적인 강도 또한 혈액량에 대한 정량적인 추정치를 제공할 수 있다.
- 병변 특성화: 대조 강화 초음파는 양성 간 병변과 악성 초점 간 병변의 분화에 역할을 한다. 이 분화는 병변 내 동적 혈관 패턴의 관찰[13] 또는 처리와[14][15] 관련된 주변 조직 실질에 의존한다.
타겟 CEUS
- 염증: 조영제는 크론병, 아테롬성 동맥경화증, 심지어 심장마비 같은 염증성 질환에서 발현되는 특정 단백질에 결합하도록 설계될 수 있다. 이러한 경우에 관심 있는 세포는 혈관의 내피세포와 백혈구다.
- 염증이 생긴 혈관은 VCAM-1, ICAM-1, E-selectin과 같이 세포 접착 분자로 기능하면서 특정 수용체를 구체적으로 표현한다. 미세 분자를 묶는 리간드로 미세 분자를 표적으로 삼으면 대조 초음파 검사로 염증 발발을 감지할 수 있다. 조기 발견은 더 나은 치료의 설계를 가능하게 한다. 마이크로버블을 P-selectin, ICAM-1, VCAM-1을 결합하는 단핵항체로 장착하려는 시도가 있었지만 분자표적에 대한 접착력이 떨어지고 특히 생리학적 관련성의 높은 전단응력에서 대상과 결합되는 미세버블의 상당 부분이 급속하게 분리되었다.[4][16]
- 백혈구는 이중 리거 및 셀렉틴 일체형 세포 구속 시스템에 의해 부분적으로 높은 접착 효율을 가지고 있다.[17] 1리간드:리셉터 쌍(PSGL-1:selectin)은 고속 결합을 통해 백혈구를 느리게 하고, 두 번째 쌍(integrin:immunoglobulin superfamily)은 온 레이트가 느리지만 오프 레이트가 느린 것을 허용하여 백혈구를 구속함으로써 동역학적으로 접착력을 강화시킨다. 시도는 조영제와 같은 ligands에 결합을 만들기 위해 뚜렷한 감각 기관의 백혈구의selectin-integrin 세포 체포의 중합체 microspheres,[18][19]과 생체 모방에dual-ligand 타깃이 같은 system,[20]지만, 아직 충분히 있을 거의 임상 사용할 수 있도록 효율적이지 않아 증가된 부착력 효율성을 보여 준 것 기법으로 만들어졌다.cont rgeted염증을 위한 초음파 검사
- 혈전증 및 혈전분해: 활성 혈소판은 혈전(트롬비)의 주요 성분이다. 마이크로버블은 가장 풍부한 혈소판 표면 수용체인 활성 당단백질 IIb/IIIa(GPIB/IIIa) 전용의 재조합형 단일 체인 변수 조각으로 결합할 수 있다. 혈전 부위의 높은 전단 응력에도 불구하고 GPIB/IIIa 표적 미세 분자 분자는 활성화 혈소판에 구체적으로 결합하고 심근경색 등 혈전증의 실시간 분자 영상촬영은 물론 약리학적 혈전분해증의 성패를 감시할 수 있게 된다.[21]
- 암: 암세포도 특정 수용체 집합을 나타내며, 주로 혈관신생을 촉진하는 수용체, 즉 새로운 혈관의 성장을 촉진하는 수용체를 나타낸다. 만약 마이크로 버블이 VEGF나 활성화된 당단백질 IIb/IIIa와 같은 수용체를 결합하는 리간드로 표적이 된다면, 그들은 비침습적으로 그리고 구체적으로 암의 영역을 식별할 수 있다.[22]
- 유전자 전달: 벡터 DNA는 마이크로 버블에 결합될 수 있다. 마이크로버블은 관심 세포 유형에 의해 표현되는 수용체와 결합하는 리간드로 표적이 될 수 있다. 표적 마이크로 버블이 DNA 페이로드로 세포 표면에 축적되면 초음파를 이용해 마이크로 버블을 터뜨릴 수 있다. 파열과 관련된 힘은 일시적으로 주변 조직에 스며들어 DNA가 세포 안으로 더 쉽게 들어갈 수 있게 할 수 있다. AAA의 체내 개발을 중지하기 위해 miR126을 사전 임상적 설정으로 전달하기 위해 대상 불가지역 마이크로버블(VCAM-1에서 지시)을 채용했다.[23]
- 약물 전달: 약물은 마이크로 버블의 지질 껍질에 통합될 수 있다. 리포솜과 같은 다른 약물 전달 차량과 비교했을 때 마이크로 버블의 큰 사이즈는 차량당 더 많은 양의 약물이 전달되도록 할 수 있다. 특정 세포 타입에 묶이는 리간드로 약물을 탑재한 마이크로 버블을 표적으로 삼음으로써 마이크로 버블은 약물을 구체적으로 전달할 뿐만 아니라 초음파를 이용해 그 부위를 이미징하면 약물이 전달된다는 검증도 제공할 수 있다.[24]
이점
의료 소노그래피 입력에서 언급된 강점에 더하여 대조 강화 초음파에는 다음과 같은 추가적인 장점이 추가된다.
- 몸은 73%의 물이고, 따라서 음향학적으로 균일하다. 혈액과 주변조직은 초음파 발생이 비슷해 기존 초음파로는 혈류 정도, 관류 정도, 조직과 혈액의 접점을 명확히 구분하기도 어렵다.[4]
- 초음파 영상을 통해 혈류를 실시간으로 평가할 수 있다.[25]
- 영상 평면에서 초음파에[26] 의한 미세 분비를 파괴하면 조직 관류를 절대적으로 계량화할 수 있다.[27]
- 초음파 분자 이미징은 방사선을 수반하지 않기 때문에 방사성핵종 이미징과 같은 분자 이미징 양식에 비해 안전하다.[25]
- MRI, PET, SPECT와 같은 대체 분자 영상 촬영 양식은 비용이 많이 든다. 반면에 초음파는 매우 비용 효율적이고 널리 이용 가능하다.[10]
- 마이크로버블은 이처럼 강한 신호를 발생시킬 수 있기 때문에 정맥내 투약량이 낮아야 하기 때문에 MRI 조영제 등 다른 분자 영상 촬영 양식에 비해 마이크로버블 마이크로그램이 필요하다.[10]
- 마이크로 버블에 대한 타겟팅 전략은 다용도적이고 모듈적이다. 새로운 지역을 목표로 하는 것은 새로운 리간드를 만드는 것만을 수반한다.
- 능동 타겟팅은 2D-모드와 3D-모드의 임상 초음파 영상 시스템을 사용하여 음향 복사력에 의해[28][29] 증가(향상된 마이크로 버블 접착)할 수 있다.[32]
단점들
조영 증강 초음파는 의료 소노그래피 항목에서 언급된 약점 외에도 다음과 같은 단점을 가지고 있다.
- 마이크로 버블은 유통되는 데 그리 오래가지 못한다. 이들은 PEG로 코팅된 상태에서도 면역체계 세포에 의해 흡수되거나 간이나 비장에 의해 흡수되기 때문에 순환거주 시간이 짧다.[10]
- 초음파는 주파수가 증가할수록 더 많은 열을 발생시키므로 초음파 주파수를 주의 깊게 관찰해야 한다.
- 마이크로버블은 낮은 초음파 주파수와 높은 기계 지수(MI)에서 폭발하는데, 이는 초음파 영상 시스템의 음의 음향 압력을 측정하는 것이다. MI를 증가시키면 영상 화질은 높아지지만 미세 버블 파괴와 트레이드오프가 있다. 미세한 거품 파괴는 국소적인 미세생물체 파열과 용혈증을 유발할 수 있다.[9]
- 리간드 타겟팅은 면역성을 유발할 수 있는데, 이는 전임상 실험에 사용되는 리간드 타겟팅이 동물 배양에서 파생되기 때문이다.[9]
- 낮은 표적 마이크로 버블 접착 효율, 즉 주입된 미세 버블의 소부분이 관심 영역에 결합됨을 의미한다.[16] 이는 표적 조영 증강 초음파가 임상 전 발달 단계에 머물러 있는 주요 이유 중 하나이다.
참고 항목
참조
- ^ a b 처음에 복사한 내용: Hansen, Kristoffer; Nielsen, Michael; Ewertsen, Caroline (2015). "Ultrasonography of the Kidney: A Pictorial Review". Diagnostics. 6 (1): 2. doi:10.3390/diagnostics6010002. ISSN 2075-4418. PMC 4808817. PMID 26838799.(CC-BY 4.0)
- ^ Sidhu, Paul; Cantisani, Vito; Deganello, Annamaria; Dietrich, Christoph; Duran, Carmina; Franke, Doris; Harkanyi, Zoltan; Kosiak, Wojciech; Miele, Vittorio; Ntoulia, Aikaterini; Piskunowicz, Maciej; Sellars, Maria; Gilja, Odd (2016). "Role of Contrast-Enhanced Ultrasound (CEUS) in Paediatric Practice: An EFSUMB Position Statement". Ultraschall in der Medizin – European Journal of Ultrasound. 38 (1): 33–43. doi:10.1055/s-0042-110394. ISSN 0172-4614. PMID 27414980.
- ^ a b McCulloch M.; Gresser C.; Moos S.; Odabashian J.; Jasper S.; Bednarz J.; Burgess P.; Carney D.; Moore V.; Sisk E.; Waggoner A.; Witt S.; Adams D. (2000). "Ultrasound contrast physics: A series on contrast echocardiography, article 3". J Am Soc Echocardiogr. 13 (10): 959–67. doi:10.1067/mje.2000.107004. PMID 11029724.
- ^ a b c d e Lindner J.R. (2004). "Microbubbles in medical imaging: current applications and future directions". Nat Rev Drug Discov. 3 (6): 527–32. doi:10.1038/nrd1417. PMID 15173842. S2CID 29807146.
- ^ "Definity- perflutren injection, suspension". DailyMed. 19 August 2020. Retrieved 22 October 2020.
- ^ "Luminity EPAR". European Medicines Agency (EMA). Retrieved 22 October 2020.
- ^ "SonoVue, INN-sulphur hexafluoride - Annex I - Summary of Product Characteristics" (PDF). European Medicines Agency. Retrieved 2019-02-24.
- ^ "Perflexane: (AF0150, AFO 150, Imagent, Imavist™)". Drugs in R&D, Volume 3, Number 5, 2002, pp. 306–309(4). Adis International. Retrieved 2010-03-08.
- ^ a b c d Klibanov A.L. (2005). "Ligand-carrying gas-filled microbubbles: ultrasound contrast agents for targeted molecular imaging". Bioconjug. Chem. 16 (1): 9–17. doi:10.1021/bc049898y. PMID 15656569.
- ^ a b c d Klibanov A.L. (1999). "Targeted delivery of gas-filled microspheres, contrast agents for ultrasound imaging". Adv Drug Deliv Rev. 37 (1–3): 139–157. doi:10.1016/s0169-409x(98)00104-5. PMID 10837732.
- ^ Schneider, M (November 1999). "SonoVue, a new ultrasound contrast agent". Eur. Radiol. 9 (3 Supplement): S347–S348. doi:10.1007/pl00014071. PMID 10602926. S2CID 19613214.
- ^ Rognin, NG; Frinking, P.; Costa, M.; Arditi, M. (November 2008). "In-vivo perfusion quantification by contrast ultrasound: Validation of the use of linearized video data vs. Raw RF data". 2008 IEEE Ultrasonics Symposium. pp. 1690–1693. doi:10.1109/ULTSYM.2008.0413. ISBN 978-1-4244-2428-3. S2CID 45679140.
- ^ Claudon, M; Dietrich, CF.; Choi, BI.; Cosgrove, DO.; Kudo, M.; Nolsøe, CP.; Piscaglia, F.; Wilson, SR.; Barr, RG.; Chammas, MC.; Chaubal, NG.; Chen, MH.; Clevert, DA.; Correas, JM.; Ding, H.; Forsberg, F.; Fowlkes, JB.; Gibson, RN.; Goldberg, BB.; Lassau, N.; Leen, EL.; Mattrey, RF.; Moriyasu, F.; Solbíatí, L.; Weskott, HP.; Xu, HX (February 2013). "Guidelines and Good Clinical Practice Recommendations for Contrast Enhanced Ultrasound (CEUS) in the Liver-Update 2012: A WFUMB-EFSUMB Initiative in Cooperation With Representatives of AFSUMB, AIUM, ASUM, FLAUS and ICUS". Ultrasound Med Biol. 39 (2): 187–210. doi:10.1016/j.ultrasmedbio.2012.09.002. PMID 23137926.
- ^ Rognin, NG; Arditi, M.; Mercier, L.; Frinking, P.J.A.; Schneider, M.; Perrenoud, G.; Anaye, A.; Meuwly, J.; Tranquart, F. (November 2010). "Parametric imaging for characterizing focal liver lesions in contrast-enhanced ultrasound". IEEE Transactions on Ultrasonics, Ferroelectrics and Frequency Control. 57 (11): 2503–2511. doi:10.1109/TUFFC.2010.1716. PMID 21041137. S2CID 19339331.
- ^ Anaye, A; Perrenoud, G.; Rognin, N.; Arditi, M.; Mercier, L.; Frinking, P.; Ruffieux, C.; Peetrons, P.; Meuli, R.; Meuwly, JY. (October 2011). "Differentiation of focal liver lesions: usefulness of parametric imaging with contrast-enhanced US". Radiology. 261 (1): 300–310. doi:10.1148/radiol.11101866. PMID 21746815.
- ^ a b Takalkar A.M.; Klibanov A.L.; Rychak J.J.; Lindner J.R.; Ley K. (2004). "Binding and detachment dynamics of microbubbles targeted to P-selectin under controlled shear flow". J. Control. Release. 96 (3): 473–482. doi:10.1016/j.jconrel.2004.03.002. PMID 15120903.
- ^ Eniola A.O.; Willcox P.J.; Hammer D.A. (2003). "Interplay between rolling and firm adhesion elucidated with a cell-free system engineered with two distinct receptor-ligand pairs". Biophys. J. 85 (4): 2720–31. Bibcode:2003BpJ....85.2720E. doi:10.1016/s0006-3495(03)74695-5. PMC 1303496. PMID 14507735.
- ^ Eniola A.O.; Hammer D.A. (2005). "In vitro characterization of leukocyte mimetic for targeting therapeutics to the endothelium using two receptors". Biomaterials. 26 (34): 7136–44. doi:10.1016/j.biomaterials.2005.05.005. PMID 15953632.
- ^ Weller G.E.; Villanueva F.S.; Tom E.M.; Wagner W.R. (2005). "Targeted ultrasound contrast agents: In vitro assessment of endothelial dysfunction and multi-targeting to ICAM-1 and sialyl Lewis(x)". Biotechnol. Bioeng. 92 (6): 780–8. doi:10.1002/bit.20625. PMID 16121392.
- ^ Rychak J.J. A.L. Klibanov, W. Yang, B. Li, S. Acton, A.L. Klibanov, W. Li, S. Acton, A. Li, A.L. Klibanov, W. Yang, B. Li. Li, 레파넨, R.D. 커밍스, K. 레이. 2005년 3월 미국 캘리포니아 주 샌디에이고 방사선학에서 제10회 초음파 대비 연구 심포지엄 "생리학적으로 조정된 타겟팅 리간드로 P-selectin에 대한 마이크로버블 접착 강화"
- ^ Wang, X; Hagemeyer, CE; Hohmann, JD; Leitner, E; Armstrong, PC; Jia, F; Olschewski, M; Needles, A; Peter, K; Ingo, A (June 2012). "Novel single-chain antibody-targeted microbubbles for molecular ultrasound imaging of thrombosis: Validation of a unique non-invasive method for rapid and sensitive detection of thrombi and monitoring of success or failure of thrombolysis in mice". Circulation. 125 (25): 3117–3126. doi:10.1161/CIRCULATIONAHA.111.030312. PMID 22647975.
- ^ Yap, ML; McFadyen, JD; Wang, X; Hohmann, JD; Ziegler, M; Yao, Y; Pham, A; Harris, M; Donnelly, PS; Hogarth, PM; Pietersz, GA; Lim, B; Peter, K (June 2017). "Targeting Activated Platelets: A Unique and Potentially Universal Approach for Cancer Imaging". Theranostics. 7 (10): 2565–2574. doi:10.7150/thno.19900. PMID 28819447.
- ^ Wang, X; Searle, AK; Hohmann, JD; Liu, AO; Abraham, MK; Palasubramaniam, J; Lim, B; Yao, Y; Wallert, M; Yu, E; Chen, YC; Peter, K (April 2018). "Dual-Targeted Theranostic Delivery of miRs Arrests Abdominal Aortic Aneurysm Development". Molecular Therapy. 25 (4): 1056–1065. doi:10.1016/j.ymthe.2018.02.010. PMID 2952574.
- ^ Wang, X; Gkanatsas, Y; Palasubramaniam, J; Hohmann, JD; Chen, YC; Lim, B; Hagemeyer, CE; Peter, K (March 2016). "Thrombus-Targeted Theranostic Microbubbles: A New Technology towards Concurrent Rapid Ultrasound Diagnosis and Bleeding-free Fibrinolytic Treatment of Thrombosis". Theranostics. 6 (5): 726–738. doi:10.7150/thno.14514. PMID 27022419.
- ^ a b 린드너, J.R., A.L. 클리아노프, K. 레이. 표적 염증, 인: 약물 표적의 생물의학적 측면. (무지칸토프, V.R., 토틸린, V.P. 에드) 2002년 보스턴 클루워; 페이지 149-172.
- ^ Wei, K; Jayaweera, AR; Firoozan, S; Linka, A; Skyba, DM; Kaul, S (February 1998). "Quantification of myocardial blood flow with ultrasound-induced destruction of microbubbles administered as a constant venous infusion". Circulation. 97 (5): 473–483. doi:10.1161/01.cir.97.5.473. PMID 9490243.
- ^ Arditi, M; Frinking, PJA.; Zhou, X.; Rognin, NG. (June 2006). "A new formalism for the quantification of tissue perfusion by the destruction-replenishment method in contrast ultrasound imaging". IEEE Transactions on Ultrasonics, Ferroelectrics and Frequency Control. 53 (6): 1118–1129. doi:10.1109/TUFFC.2006.1642510. PMID 16846144. S2CID 6328131.
- ^ Rychak, JJ; Klibanov, AL; Hossack, JA (March 2005). "Acoustic radiation force enhances targeted delivery of ultrasound contrast microbubbles: in vitro verification". IEEE Transactions on Ultrasonics, Ferroelectrics and Frequency Control. 52 (3): 421–433. doi:10.1109/TUFFC.2005.1417264. PMID 15857050. S2CID 25032596.
- ^ Dayton, P; Klibanov, A; Brandenburger, G; Ferrara, K (October 1999). "Acoustic radiation force in vivo: a mechanism to assist targeting of microbubbles". Ultrasound Med Biol. 25 (8): 1195–1201. doi:10.1016/s0301-5629(99)00062-9. PMID 10576262.
- ^ Frinking, PJ; Tardy, I; Théraulaz, M; Arditi, M; Powers, J; Pochon, S; Tranquart, F (August 2012). "Effects of acoustic radiation force on the binding efficiency of BR55, a VEGFR2-specific ultrasound contrast agent". Ultrasound Med Biol. 38 (8): 1460–1469. doi:10.1016/j.ultrasmedbio.2012.03.018. PMID 22579540.
- ^ Gessner, RC; Streeter, JE; Kothadia, R; Feingold, S; Dayton, PA (April 2012). "An in vivo validation of the application of acoustic radiation force to enhance the diagnostic utility of molecular imaging using 3-d ultrasound". Ultrasound Med Biol. 38 (4): 651–660. doi:10.1016/j.ultrasmedbio.2011.12.005. PMC 3355521. PMID 22341052.
- ^ Rognin, NG; Unnikrishnan, S.; Klibanov, AL. (September 2013). "Molecular Ultrasound Imaging Enhancement by Volumic Acoustic Radiation Force (VARF): Pre-clinical in vivo Validation in a Murine Tumor Model". Abstracts of the 2013 World Molecular Imaging Congress. Archived from the original on 2013-10-11.