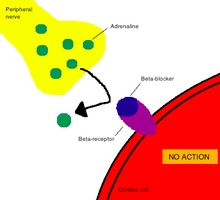
작용 메커니즘
Mechanism of action약리학에서 작용 메커니즘(MOA)이라는 용어는 약물이 약리학적 [2]효과를 내는 특정한 생화학적 상호작용을 말한다.작용 메커니즘은 보통 효소 또는 [3]수용체와 같은 약물이 결합하는 특정 분자 표적에 대한 언급을 포함한다.수용체 부위는 약물의 화학적 구조뿐만 아니라 그곳에서 발생하는 특정 작용에 기초한 약물에 대한 특정 친화력을 가진다.
수용체에 결합하지 않는 약물은 단순히 신체의 화학적 또는 물리적 특성과 상호작용함으로써 그에 상응하는 치료 효과를 낸다.이런 방식으로 작용하는 약의 일반적인 예는 제산제와 설사약이다.[2]
반대로 행동모드(MoA)는 세포 수준에서 기능적 또는 해부학적 변화를 기술하며, 이는 살아있는 유기체의 물질에 대한 노출에서 비롯된다.
중요성
새로운 약물과 의약품의 작용 메커니즘을 설명하는 것은 여러 가지 이유로 중요하다.
- 항감염제 개발의 경우 이 정보를 통해 임상 안전과 관련된 문제를 예측할 수 있다.예를 들어 세포질막 또는 전자전달망을 교란하는 약물은 [4][5]세포벽(펩티도글리칸 또는 β-글루칸) 또는 70S 리보솜의 구성 요소를 대상으로 하는 약물보다 독성 문제를 일으킬 가능성이 높다.
- 약물의 특정 부위와 수용체 사이의 상호작용을 아는 것으로, 다른 약물을 이 상호작용을 재현하는 방법으로 조제할 수 있어 같은 치료 효과를 얻을 수 있다.사실, 이 방법은 신약을 만들기 위해 사용된다.
- 어떤 환자가 치료에 가장 잘 반응하는지를 확인하는 데 도움이 될 수 있습니다.유방암 치료제인 트라스트주맙은 예를 들어 단백질 HER2를 대상으로 하는 것으로 알려져 있기 때문에 종양이 이 분자의 존재 여부를 스크리닝하여 환자가 트라스트주맙 치료를 [6][7]받을 수 있는지 여부를 결정할 수 있다.
- 표적 경로에 대한 약물의 효과를 환자에서 모니터링할 수 있기 때문에 더 나은 투여를 가능하게 할 수 있습니다.예를 들어, 스타틴 복용량은 보통 환자의 혈중 콜레스테롤 수치를 [6]측정함으로써 결정된다.
- 그것은 약물 내성이 나타날 가능성을 낮추도록 약물을 결합할 수 있게 한다.항감염제 또는 항암제가 어떤 세포 구조에 작용하는지 알면 여러 표적을 동시에 억제하는 칵테일을 투여할 수 있어 미생물 또는 종양 DNA의 단일 돌연변이가 약물 내성과 [4][8][9][10]치료 실패로 이어질 위험을 줄일 수 있다.
- 이는 약물의 식별을 위한 다른 징후를 허용할 수 있다.예를 들어 실데나필이 포스포디에스테라아제-5(PDE-5) 단백질을 억제한다는 발견은 PDE-5가 폐고혈압 [11][12]폐에서 발현되기 때문에 폐동맥고혈압 치료에 이 약물을 용도 변경할 수 있게 했다.
결정.
현미경을 이용한 방법

생체활성화합물은 표적세포의 표현형 변화, 현미경으로 관찰할 수 있는 변화,[13] 화합물의 작용 메커니즘에 대한 통찰력을 줄 수 있는 변화를 유도한다.
항균제에 의해 표적세포의 구상세포로의 전환은 펩티도글리칸 합성이 억제되고 있음을 나타낼 수 있으며 표적세포의 필라멘테이션은 PBP3, FTSZ 또는 DNA 합성이 억제되고 있음을 나타낼 수 있다.다른 항균제 유도 변화로는 난형 세포 형성, 의사 적혈구 형성, 국소적 팽창, 팽대 형성, 블링 및 펩티도글리칸 [4]비후화가 있다.항암제의 경우 Bleb 형성은 화합물이 혈장막을 [14]교란하고 있음을 나타낼 수 있다.
현재 이 접근법의 한계는 수동으로 데이터를 생성하고 해석하는 데 필요한 시간이지만 자동 현미경 검사 및 이미지 분석 소프트웨어의 진보가 [4][13]이 문제를 해결하는 데 도움이 될 수 있습니다.
직접 생화학적 방법
직접 생화학적 방법에는 약물 후보와 같은 단백질 또는 소분자가 라벨로 표시되어 [15]몸 전체에 걸쳐 추적되는 방법이 포함된다.이것은 약물의 약효소를 식별하기 위해 약 윤곽의 기본적인 표현과 같이 관심 있는 작은 표적과 결합하는 표적 단백질을 찾는 가장 직접적인 접근법임이 증명된다.라벨 부착 분자와 단백질 사이의 물리적 상호작용으로 인해 생화학적 방법은 약물의 독성, 효능 및 작용 메커니즘을 결정하기 위해 사용될 수 있다.
계산 추론 방법
일반적으로 계산 추론 방법은 주로 컴퓨터 기반 패턴 인식에 [15]기반하여 소분자 약물에 대한 단백질 표적을 예측하는 데 사용된다.그러나 이 방법은 기존 또는 새로 개발된 약물에 대한 새로운 표적 발굴에도 사용될 수 있다.약제 분자의 약초를 동정함으로써 새로운 타깃이 [15]동정되는 패턴 인식의 프로파일링 방법을 실시할 수 있다.이것은 단백질의 특정 영역과 상호작용할 때 약물의 특정 기능 성분이 어떤 역할을 하는지 알려져 있기 때문에 가능한 작용 메커니즘에 대한 통찰력을 제공합니다.
OMIC 기반 메서드
오믹스 기반 방법은 화학단백질학, 역유전학 및 유전체학, 전사체학, 프로테오믹스와 같은 오믹스 기술을 사용하여 관심 [16]화합물의 잠재적 대상을 식별합니다.예를 들어 역유전학 및 유전체학 접근법은 유전자 섭동(예: CRISPR-Cas9 또는 siRNA)을 화합물과 결합하여 사용하여 해당 화합물의 약리학적 효과를 파괴하는 유전자를 식별한다.한편, 화합물의 전사체학 및 프로테오믹스 프로파일은 알려진 타겟을 가진 화합물의 프로파일과 비교하기 위해 사용될 수 있다.계산 추론 덕분에 화합물의 작용 메커니즘에 대한 가설을 세울 수 있으며, 이는 후속적으로 [16]시험될 수 있다.
MOA가 알려진 약물
작용 메커니즘이 알려진 많은 약들이 있다.한 예로 아스피린을 들 수 있다.
아스피린
아스피린의 작용 메커니즘은 시클로옥시게나아제 [17]효소의 돌이킬 수 없는 억제를 포함한다. 따라서 프로스타글란딘과 트롬복산의 생성을 억제하여 통증과 염증을 감소시킨다.이 작용 메커니즘은 아스피린에 고유하며 모든 비스테로이드성 항염증제(NSAIDs)에 대해 일정하지 않습니다.오히려 아스피린은 COX-1을 [18]불가역적으로 억제하는 유일한 NSAID이다.
MOA를 알 수 없는 약물
일부 약물 작용 메커니즘은 아직 알려지지 않았다.하지만, 어떤 약물의 작용 메커니즘은 알려져 있지 않지만, 그 약은 여전히 기능한다; 단지 그 약물이 수용체와 어떻게 상호작용하고 치료 효과를 내는지는 알려지지 않았거나 불분명하다.
동작 모드
일부 문헌 기사에서는 "작용 메커니즘"과 "작용 방식"이라는 용어가 번갈아 사용되며, 일반적으로 약물이 상호작용하고 의학적 효과를 생성하는 방식을 가리킨다.그러나 실제로 작용 모드는 세포 수준에서 기능적 또는 해부학적 변화를 기술하며,[19] 이는 살아있는 유기체의 물질에 대한 노출에 기인한다.이것은 억제, 활성화, 작용 또는 길항작용을 통해 약물과 효소 또는 수용체 사이의 상호작용 및 상호작용의 특정 형태에 초점을 맞춘 보다 구체적인 용어이기 때문에 작용 메커니즘과는 다르다.게다가, "작용 메커니즘"이라는 용어는 주로 약리학에서 사용되는 주요 용어이며, "작용 방식"은 미생물학 또는 생물학의 특정 측면에 더 자주 나타날 것이다.
「 」를 참조해 주세요.
레퍼런스
- ^ Ogrodowczyk, M.; Dettlaff, K.; Jelinska, A. (2016). "Beta-blockers: Current state of knowledge and perspectives". Mini Reviews in Medicinal Chemistry. 16 (1): 40–54. doi:10.2174/1389557515666151016125948. PMID 26471965.
- ^ a b Spratto, G.R.; Woods, A.L. (2010). Delmar Nurse's Drug Handbook. Cengage Learning. ISBN 978-1-4390-5616-5.
- ^ 그랜트, R.L.; 콤스, A.B.;Acosta, D. (2010) "독성 메커니즘 조사를 위한 실험 모델"C.A. 종합 독물학 McQueen (제2판).옥스퍼드:엘세비어, 페이지 204ISBN 978-0-08-046884-6.
- ^ a b c d e Cushnie, T.P.; O’Driscoll, N.H.; Lamb, A.J. (2016). "Morphological and ultrastructural changes in bacterial cells as an indicator of antibacterial mechanism of action". Cellular and Molecular Life Sciences. 73 (23): 4471–4492. doi:10.1007/s00018-016-2302-2. hdl:10059/2129. PMID 27392605. S2CID 2065821.
- ^ Chang, C.C.; Slavin, M.A.; Chen, S.C. (2017). "New developments and directions in the clinical application of the echinocandins". Archives of Toxicology. 91 (4): 1613–1621. doi:10.1007/s00204-016-1916-3. PMID 28180946. S2CID 31029386.
- ^ a b No authors listed (2010). "Mechanism matters". Nature Medicine. 16 (4): 347. doi:10.1038/nm0410-347. PMID 20376007.
- ^ Joensuu, H. (2017). "Escalating and de-escalating treatment in HER2-positive early breast cancer". Cancer Treatment Reviews. 52: 1–11. doi:10.1016/j.ctrv.2016.11.002. PMID 27866067.
- ^ Cihlar, T.; Fordyce, M. (2016). "Current status and prospects of HIV treatment". Current Opinion in Virology. 18: 50–56. doi:10.1016/j.coviro.2016.03.004. PMID 27023283.
- ^ Antony, H.A.; Parija, S.C. (2016). "Antimalarial drug resistance: An overview". Tropical Parasitology. 6 (1): 30–41. doi:10.4103/2229-5070.175081. PMC 4778180. PMID 26998432.
- ^ Bozic, I.; Reiter, J.G.; Allen, B.; Antal, T.; Chatterjee, K.; Shah, P.; Moon, Y.S.; Yaqubie, A.; Kelly, N.; Le, D.T.; Lipson, E.J.; Chapman, P.B.; Diaz, L.A.; Vogelstein, B.; Nowak, M.A. (2013). "Evolutionary dynamics of cancer in response to targeted combination therapy". eLife. 2: Article ID e00747. doi:10.7554/eLife.00747. PMC 3691570. PMID 23805382.
- ^ Tari, L.; Vo, N.; Liang, S.; Patel, J.; Baral, C.; Cai, J. (2012). "Identifying novel drug indications through automated reasoning". PLOS ONE. 7 (7): Article e40946. Bibcode:2012PLoSO...740946T. doi:10.1371/journal.pone.0040946. PMC 3402456. PMID 22911721.
- ^ Hayardeny, L. (2014). Why is it important to know the mode of action of drugs? (Conference presentation). New Frontiers in Neuroscience and Methods of Transdisciplinary Education Workshop, Tel Aviv University, Israel: Tel Aviv University. Retrieved 18 March 2017.
- ^ a b Fetz, V.; Prochnow, H.; Brönstrup, M.; Sasse, F. (2016). "Target identification by image analysis" (PDF). Natural Product Reports. 33 (5): 655–667. doi:10.1039/c5np00113g. hdl:10033/621283. PMID 26777141.
- ^ Dubovskii, P.V.; Vassilevski, A.A.; Kozlov, S.A.; Feofanov, A.V.; Grishin, E.V.; Efremov, R.G. (2015). "Latarcins: versatile spider venom peptides". Cellular and Molecular Life Sciences. 72 (23): 4501–4522. doi:10.1007/s00018-015-2016-x. PMID 26286896. S2CID 14177431.
- ^ a b c Schenone, M.; Dančík, V.; Wagner, B.K.; Clemons, P.A. (2013). "Target identification and mechanism of action in chemical biology and drug discovery". Nature Chemical Biology. 9 (4): 232–240. doi:10.1038/nchembio.1199. ISSN 1552-4450. PMC 5543995. PMID 23508189.
- ^ a b Wecke, T.; Mascher, T. (2011). "Antibiotic research in the age of omics: from expression profiles to interspecies communication". Journal of Antimicrobial Chemotherapy. 66 (12): 2689–2704. doi:10.1093/jac/dkr373. PMID 21930574.
- ^ Tóth, L.; Muszbek, L.; Komaromi, I. (2013). "Mechanism of the irreversible inhibition of human cyclooxygenase-1 by aspirin as predicted by QM/MM calculations". Journal of Molecular Graphics and Modelling. 40: 99–109. doi:10.1016/j.jmgm.2012.12.013. PMID 23384979.
- ^ Sharma, S.; Sharma, S. C. (1997). "An update on eicosanoids and inhibitors of cyclooxygenase enzyme systems". Indian Journal of Experimental Biology. 35 (10): 1025–1031. ISSN 0019-5189. PMID 9475035.
- ^ "Mechanisms and mode of dioxin action" (PDF). U.S. Environmental Protection Agency. Retrieved 11 June 2012.