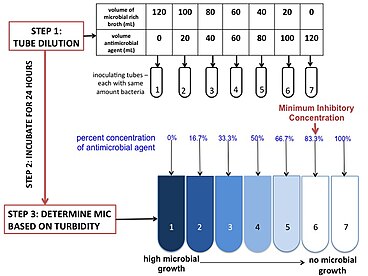
최소 억제 농도
Minimum inhibitory concentration미생물학에서 최소억제농도(MIC)는 박테리아나 박테리아의 눈에 보이는 성장을 막는 화학약품의 최저농도이다.MIC는 미생물, 영향을 받는 사람(체내에만 해당) 및 항생제 [1]자체에 의존합니다.종종 밀리리터당 마이크로그램(μg/mL) 또는 리터당 밀리그램(mg/L)으로 표현된다.
총무성은 화학약품의 시험관내용액을 농도증가로 조제하여 배양균의 별도 배치로 배양한 후 한천희석 또는 육수미량희석법으로 측정하여 결정한다.결과는 브레이크포인트를 사용하여 민감성(종종 민감성이라고 함), 노출 증가 또는 특정 항균제에 대한 내성으로 분류되었습니다.중단점은 미국 임상 및 실험실 표준 연구소(CLSI), 영국 항균 화학 치료 협회(BSAC) 또는 유럽 항균 감수성 검사 위원회(EUCAST)[2]와 같은 참조 기관의 지침에 발표된 값에 대해 합의된다.수년간 다양한 유럽 국가의 중단점과 유럽 항균 감수성 시험 위원회(EUCAST)와 미국 임상 및 실험실 표준 연구소(CLSI)[3]의 중단점 사이에 큰 차이가 있었다.
MIC는 눈에 보이는 성장을 억제하는 데 필요한 항균제의 최저 농도인 반면, 최소 살균 농도(MBC)는 세균을 죽게 하는 항균제의 최소 농도이다.총무성이 MBC에 가까울수록 [4]살균력이 높아진다.
약물 발견의 첫 단계는 [5]관심 박테리아에 대한 MIC의 라이브러리 약물 후보자의 선별이다.따라서 MIC는 일반적으로 새로운 항균제에 [6]대한 대규모 임상 전 평가의 출발점이다.최소 억제 농도를 측정하는 목적은 항생제를 효율적으로 선택하여 치료의 성공을 높이는 것입니다.
배경
역사
항생제의 발견과 상용화 이후 미생물학자, 약학자, 의사 알렉산더 플레밍이 육수의 탁도를 이용하여 [7]육수 희석 기술을 개발하였다.이것은 일반적으로 최소 억제 [8]농도의 착상점으로 여겨진다.이후 1980년대에 임상 및 실험실 표준 연구소는 MIC 결정 및 임상 사용을 위한 방법과 표준을 통합했습니다.새로운 항균, 병원균 및 그 진화의 발견에 따라 CLSI에 의한 프로토콜도 지속적으로 갱신되어 그 [9]변화를 반영하고 있다.CLSI에 의해 설정된 프로토콜과 매개변수는 미국에서 "금본위제"로 간주되며 FDA와 같은 규제 당국이 평가를 [10]위해 사용한다.
임상 사용
현재 MIC는 항균 감수성 테스트에 사용되고 있습니다.MIC는 각 항생제 옆에 감수성 해석을 제공함으로써 보고됩니다.다양한 민감도 해석은 S(민감), I(중간) 및 R(저항)입니다.이러한 해석은 CLSI(Clinical and Laboratory Standards Institute)에 의해 작성 및 구현되었다.클리닉에서는 대개 환자의 증상으로 정확한 병원균을 쉽게 알아낼 수 없다.그 후 병원체가 결정되어도 황색포도상구균과 같은 병원체의 혈청형은 항균제에 대한 내성이 다르다.따라서 올바른 항균제를 [11]처방하는 것은 어렵다.이러한 경우 MIC는 환자로부터 격리된 병원균을 접시 또는 육수에 배양하여 결정하며,[12] 나중에 검사에 사용됩니다.따라서 MIC에 대한 지식은 의사에게 처방전을 작성하기 위한 귀중한 정보를 제공할 것입니다.항균제의 정확하고 정확한 사용 또한 다제내성 박테리아와 관련하여 중요하다.박테리아와 같은 미생물은 이전에 [13]감염되기 쉬웠던 항균제에 대한 내성을 얻고 있다.양립할 수 없는 수준의 항균제를 사용하면 세균 [14]병원체의 저항성 방향과 진화를 주도하는 선택적 압력을 제공합니다.이것은 항생제의 [15]서브MIC 수준에서 관찰되었다.따라서 항균제 처방에 있어서 최선의 선택을 하기 위해 MIC를 결정하는 것이 점점 더 중요해지고 있다.
MIC는 임상적으로 MBC보다 더 쉽게 [9]결정되기 때문에 MIC를 사용합니다.최소 살균 농도(MBC)는 미생물의 죽음을 초래하는 최소 항균 농도이며 박테리아를 재배양할 수 없는 것으로 정의된다.또한, 숙주 면역체계가 세균 증식이 [16]멈춘 상태에서 병원체를 배출할 수 있기 때문에 총무성과 MBC 농도 모두에서 약물 효과는 일반적으로 유사하다.MBC가 정통부보다 훨씬 높으면 약물 독성이 MBC를 복용하는 것은 환자에게 해가 된다.항균성 독성은 면역 과민증이나 표적외 [17]독성 등 여러 가지 형태로 나타날 수 있다.
방법들
육수 희석 분석
이 검사를 실행하는 데 필요한 세 가지 주요 시약이 있습니다. 매체, 항균제 및 검사 중인 미생물입니다.가장 일반적으로 사용되는 매체는 대부분의 병원균의 성장을 지원하는 능력과 일반적인 항생제에 [18]대한 억제제가 부족하기 때문에 양이온 조정된 뮬러 힌튼 브로스이다.검사 중인 병원체 및 항생제에 따라 미디어를 변경하거나 조정할 수 있습니다.원료 항균제와 배지를 혼합하여 항균 농도를 올바른 농도로 조정합니다.조절된 항균제를 여러 튜브(또는 웰)로 직렬로 희석하여 구배를 구합니다.희석 속도는 중단점과 시술자의 필요에 따라 조정할 수 있습니다.미생물, 즉 접종제는 동일한 콜로니 형성 단위에서 추출되어야 하며 정확한 농도로 제조되어야 한다.이는 배양 시간과 희석으로 조정할 수 있습니다.검증을 위해 정대조제를 100배 희석하여 콜로니 형성 단위를 계수한다.미생물들은 튜브(또는 접시)에 접종하고 16-20시간 동안 배양된다.MIC는 일반적으로 [18]탁도에 의해 결정됩니다.
테스트
에테스는 또한 전 세계 미생물학 실험실에서 널리 사용되고 있는 다른 유기체 그룹에 대해 광범위한 항균제의 최소 억제 농도 값을 결정하기 위한 대체 방법으로 사용될 수 있다.바이오메리우가 제조한 Etests는 즉시 사용할 수 있는 비다공성 플라스틱 시약 스트립으로 항생제의 구배가 미리 정의되어 있으며 연속 농도 범위를 [19]커버합니다.
「 」를 참조해 주세요.
- 커비-바우어 검정
- Arthur Thomas Palin, 식수 염소 처리 및 테스트의 선구자
레퍼런스
- ^ McKinnon PS, Davis SL (April 2004). "Pharmacokinetic and pharmacodynamic issues in the treatment of bacterial infectious diseases". European Journal of Clinical Microbiology & Infectious Diseases. 23 (4): 271–88. doi:10.1007/s10096-004-1107-7. PMID 15015030. S2CID 28455936.
- ^ Andrews JM (July 2001). "Determination of minimum inhibitory concentrations". The Journal of Antimicrobial Chemotherapy. 48 Suppl 1 (suppl 1): 5–16. doi:10.1093/jac/48.suppl_1.5. PMID 11420333.
- ^ Diene SM, Abat C, Rolain JM, Raoult D (July 2017). "How artificial is the antibiotic resistance definition?". The Lancet Infectious Diseases. 17 (7): 690. doi:10.1016/S1473-3099(17)30338-9. PMID 28653629.
- ^ Tripathi KD (2013). Essentials of Medical Pharmacology (7th ed.). New Delhi, India: Jaypee Brothers Medical Publishers. pp. 696, 697. ISBN 9789350259375.
- ^ Turnidge JD, Ferraro MJ, Jorgensen JH (2003). "Susceptibility Test Methods: General Considerations". In Murray PR, Baron EJ, Jorgensen JH, Pfaller MA, Yolken RH (eds.). Manual of Clinical Microbiology (8th ed.). Washington: American Society of Clinical Microbiology. p. 1103. ISBN 1-55581-255-4.
- ^ O'Neill AJ, Chopra I (August 2004). "Preclinical evaluation of novel antibacterial agents by microbiological and molecular techniques". Expert Opinion on Investigational Drugs. 13 (8): 1045–63. doi:10.1517/13543784.13.8.1045. PMID 15268641. S2CID 24016698.
- ^ Fleming A (1944). On the antibacterial action of cultures of a penicillium, with special reference to their use in the isolation of B. influenzae. H.K. Lewis. OCLC 25424051.
- ^ Wheat PF (July 2001). "History and development of antimicrobial susceptibility testing methodology". The Journal of Antimicrobial Chemotherapy. 48 Suppl 1 (suppl_1): 1–4. doi:10.1093/jac/48.suppl_1.1. PMID 11420332.
- ^ a b Cockerill FR (2012). Methods for dilution antimicrobial susceptibility tests for bacteria that grow aerobically : approved standard (9th ed.). Wayne, Pa: Clinical and Laboratory Standards Institute. ISBN 978-1562387846. OCLC 1016466655.
- ^ Cockerill F (2012). Performance standards for antimicrobial susceptibility testing : twenty-second informational supplement. Wayne, PA: Clinical and Laboratory Standards Institute. ISBN 978-1562387853. OCLC 795927370.
- ^ Cameron DR, Howden BP, Peleg AY (September 2011). "The interface between antibiotic resistance and virulence in Staphylococcus aureus and its impact upon clinical outcomes". Clinical Infectious Diseases. 53 (6): 576–82. doi:10.1093/cid/cir473. PMID 21865195.
- ^ Schwalbe R, Steele-Moore L, Goodwin AC (2007). Antimicrobial susceptibility testing protocols. Boca Raton: CRC Press. ISBN 9781420014495. OCLC 666899344.
- ^ World Health Organization (2015-12-15). Global antimicrobial resistance surveillance system : manual for early implementation. World Health Organization. Geneva, Switzerland. ISBN 978-9241549400. OCLC 950637154.
- ^ Geisinger E, Isberg RR (February 2017). "Interplay Between Antibiotic Resistance and Virulence During Disease Promoted by Multidrug-Resistant Bacteria". The Journal of Infectious Diseases. 215 (suppl_1): S9–S17. doi:10.1093/infdis/jiw402. PMC 5853982. PMID 28375515.
- ^ Gullberg E, Cao S, Berg OG, Ilbäck C, Sandegren L, Hughes D, Andersson DI (July 2011). "Selection of resistant bacteria at very low antibiotic concentrations". PLOS Pathogens. 7 (7): e1002158. doi:10.1371/journal.ppat.1002158. PMC 3141051. PMID 21811410.
- ^ Gallagher JC (2016-11-21). Antibiotics simplified. ISBN 9781284111293. OCLC 952657550.
- ^ Guengerich FP (2011). "Mechanisms of drug toxicity and relevance to pharmaceutical development". Drug Metabolism and Pharmacokinetics. 26 (1): 3–14. doi:10.2133/dmpk.DMPK-10-RV-062. PMC 4707670. PMID 20978361.
- ^ a b Cockerill F (2015). Methods for dilution antimicrobial susceptibility tests for bacteria that grow aerobically : approved standard (Tenth ed.). Wayne, Pa.: Clinical and Laboratory Standards Institute. ISBN 978-1562387839. OCLC 932608948.
- ^ "ETEST". bioMérieux. Retrieved 2019-04-23.