작은 간섭 RNA
Small interfering RNAsiRNA(small interferencing RNA)는 짧은 간섭 RNA 또는 소음 RNA로 알려지기도 하며, 일반적으로 길이가 20-24(보통 21)인 최초의 비코드 RNA 분자에 있는 이중 가닥 RNA의 한 종류이며, miRNA와 유사하며 RNA 간섭 경로 내에서 작동합니다.전사 후 mRNA를 분해하여 특정 유전자의 상보적 뉴클레오티드 배열 발현을 방해하여 [1][2]번역을 방해한다.
구조.
자연적으로 발생하는 siRNA는 인산화 5' 말단과 두 개의 돌출된 뉴클레오티드를 가진 히드록실화 3' 말단을 가진 짧은 (보통 20~24-bp) 이중 가닥 RNA(dsRNA)인 잘 정의된 구조를 가지고 있다.Dicer 효소는 긴 dsRNA와 작은 머리핀 RNA에서 [3]siRNA의 생성을 촉매한다. siRNA는 또한 트랜스펙션에 의해 세포에 도입될 수 있다.원칙적으로 어떤 유전자도 상보적인 염기서열을 가진 합성 siRNA에 의해 쓰러질 수 있기 때문에, siRNA는 포스트 게놈 시대에 유전자 기능과 약물 표적을 검증하는 중요한 도구이다.
역사
1998년, 워싱턴 DC에 있는 카네기 과학 연구소의 앤드류 파이어와 우스터에 있는 매사추세츠 대학의 크레이그 멜로는 선충류인 [4]케노하브디스의 유전자 발현을 연구하던 중 RNAi 메커니즘을 발견했다.그들은 2006년 RNAi를 이용한 연구로 노벨상을 수상했다. siRNA와 전사 후 유전자 사일런싱(PTGS)에서의 그들의 역할은 영국 노리치의 세인즈베리 연구소에 있는 데이비드 바울컴의 그룹에 의해 식물에서 발견되었고 [5]1999년에 사이언스에 보고되었다.Thomas Tuschl과 동료들은 곧 Nature에서 합성 siRNA가 [6]포유류의 세포에서 RNAi를 유도할 수 있다고 보고했다.2001년에는 포유류 세포에 화학적으로 합성된 siRNA를 도입함으로써 특정 유전자의 발현을 성공적으로 침묵시켰다(Tuschl et al).이러한 발견은 생물의학 연구와 약물 개발을 위해 RNAi를 이용하는 것에 대한 관심의 급증으로 이어졌다.siRNA 치료법은 유기(탄소 기반) 나노입자와 무기(비탄소 기반) 나노입자 모두에서 상당한 발전을 이루었으며, 이는 인간 피험자에게 치료제를 전달할 수 있는 유망한 방법을 제공한다.그러나 siRNA의 인간 적용은 성공에 상당한 한계를 가지고 있다.그 중 하나는 표적이 [2]빗나간 거야이러한 치료법이 선천적인 [4]면역력을 유발할 가능성도 있다.동물 모형은 인간에게서 이러한 반응의 정도를 정확하게 표현하는데 성공하지 못했다.따라서 siRNA 치료의 효과를 연구하는 것은 어려운 과제였다.
최근 몇 년 동안, siRNA 치료법이 승인되었고 이러한 문제들을 극복하기 위한 새로운 방법들이 확립되었다.상업적으로 사용할 수 있는 승인된 치료법이 있으며,[citation needed][7] 현재 승인을 받기 위해 대기 중인 치료법도 있다.
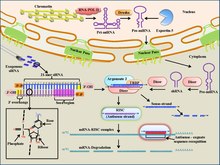
메커니즘
자연 siRNA가 번역 억제를 통해 유전자 침묵을 유발하는 메커니즘은 다음과 같습니다.
- 긴 dsRNA는 Dicer라고 불리는 엔도리보핵산가수분해효소에 의해 분해된다.다이서는 긴 dsRNA를 짧게 간섭하는 RNA 또는 siRNA를 형성하기 위해 절단합니다. 이것이 분자가 RNA 유도 사일런싱 복합체(RISC)를 형성할 수 있도록 합니다.
- 일단 siRNA가 세포에 들어가면 그것은 다른 단백질에 통합되어 RISC를 형성한다.
- 일단 siRNA가 RISC 복합체의 일부가 되면, siRNA는 풀려서 단일 가닥 siRNA를 형성합니다.
- 5' 끝의 염기쌍으로 인해 열역학적으로 안정성이 떨어지는 가닥은 RISC 복합체의 일부로 선택됩니다.
- RISC 복합체의 일부인 단일 가닥 siRNA를 스캔하여 상호 보완적인 mRNA를 찾을 수 있게 되었습니다.
- 단일 가닥 siRNA(RISC 복합체의 일부)가 표적 mRNA에 결합하면 mRNA 분열을 유도한다.
- 이제 mRNA가 절단되어 세포에 의해 비정상적인 것으로 인식됩니다.이것은 mRNA의 분해를 유발하고, 결과적으로 mRNA가 아미노산과 단백질로 변환되지 않는다.mRNA를 암호화하는 유전자를 침묵시키는 거죠
siRNA는 miRNA와 유사하지만 miRNA는 짧은 스템루프 RNA 생성물로부터 파생되며, 일반적으로 번역 억제에 의해 유전자를 침묵시키고, 작용의 특이성이 더 넓은 반면, siRNA는 일반적으로 번역 전에 mRNA를 분해함으로써 작용하며, 100% 상보성을 가지므로 표적 특이성이 매우 엄격하다.[8][9]
siRNA 또는 그 생합성 전구체를 이용한 RNAi 유도

외인성 siRNA의 트랜스펙션에 의한 유전자 녹다운은 특히 빠르게 분열하는 세포에서 효과가 일시적이기 때문에 만족스럽지 못한 경우가 많다.이는 siRNA의 발현 벡터를 생성함으로써 극복할 수 있습니다.siRNA 시퀀스는 두 가닥 사이에 짧은 루프를 도입하도록 수정됩니다.결과물은 짧은 머리핀 RNA(shRNA)로, Dicer에 의해 통상적인 [10]방법으로 기능성 siRNA로 처리될 수 있다.일반적인 전사 카세트는 RNA 중합효소 III 프로모터(예: U6 또는 H1)를 사용하여 작은 핵 RNA(snRNA)의 전사를 지시합니다(U6은 유전자 스플라이싱에 관여하고 H1은 인간 RNAase P의 RNase 성분).그 결과 생성된 siRNA 전사물은 Dicer에 의해 처리된다는 이론이 있다.
유전자 녹다운 효율은 세포 [11]압착을 통해서도 향상될 수 있다.
RNAi에서 siRNA의 활성은 RNA 유도 사일런싱 복합체(RISC)에 대한 결합 능력에 크게 좌우된다.이중 siRNA가 RISC에 결합하는 것은 엔도핵산가수분해효소에 의한 센스스트랜드의 풀림 및 절단이다.나머지 안티센스 스트랜드-RISC 복합체는 전사 사일런싱을 [12]시작하기 위해 표적 mRNA에 결합할 수 있다.
RNA활성화
dsRNA는 또한 "작은 RNA 유도 유전자 활성화" 또는 RNAa로 불려온 메커니즘인 유전자 발현을 활성화시킬 수 있다는 것이 발견되었다.유전자 촉진제를 대상으로 하는 dsRNA가 관련 유전자의 강력한 전사 활성화를 유도하는 것으로 나타났다.RNAa는 "소형 활성화 RNA(saRNA)"라고 불리는 합성 dsRNA를 사용하여 인간 세포에서 입증되었다.RNAa가 다른 [13]유기체에서 얼마나 보존되는지는 현재 알려져 있지 않다.이집트 모기의 한 보고서는 RNAa에 대한 몇 가지 증거가 있으며 프로모터 [14]지역을 대상으로 하는 짧고 긴 dsRNA에 의해 달성될 수 있다는 것을 보여주었다.
전사 후 유전자 사일런트화
siRNA 유도 전사 후 유전자 소음은 RNA 유도 소음 복합체(RISC)의 조립으로 시작됩니다.복합체는 표적 유전자를 코드하는 mRNA 분자를 절단함으로써 특정 유전자 발현을 침묵시킨다.프로세스를 시작하기 위해 두 개의 siRNA 스트랜드 중 하나인 가이드 스트랜드(안티 센스 스트랜드)가 RISC에 로드되고 다른 한 개의 스트랜드인 조수석 스트랜드(센스 스트랜드)가 저하됩니다.특정 다이서 효소는 가이드 가닥을 RISC에 [15]로드하는 역할을 할 수 있습니다.그런 다음, siRNA는 mRNA [16]분자의 완벽한 상보적 배열로 RISC를 스캔하고 지시합니다.mRNA 분자의 분할은 RISC의 아르고나이트 단백질의 Piwi 도메인에 의해 촉매되는 것으로 생각된다.mRNA 분자는 siRNA 잔기 10과 11에 쌍을 이루는 표적 뉴클레오티드 사이의 포스포디에스테르 결합을 분해하여 5'[17] 말단부터 정확하게 절단된다.이 분열은 세포핵산분해효소에 의해 더욱 분해되는 mRNA 단편을 만든다.5' fragment는 3' 말단에서 엑소솜에 의해 분해되고, 3' fragment는 5' 말단에서 5' - 3' 엑시보핵산가수분해효소 1(XRN1)[18]에 의해 분해된다.분할 후 표적 mRNA 가닥을 RISC에서 분리하면 더 많은 mRNA를 무음화할 수 있다.이 해리 과정은 ATP 가수 [17]분해에 의해 구동되는 외부 인자에 의해 촉진될 가능성이 있다.
때때로 표적 mRNA 분자의 분열이 일어나지 않는다.경우에 따라서는 포스포디에스테르 골격의 핵내분열은 절단 부위 부근의 siRNA와 타깃 mRNA의 불일치에 의해 억제될 수 있다.다른 경우 RISC의 Argonaute 단백질은 표적 mRNA와 siRNA가 완벽하게 [17]쌍을 이룬 경우에도 엔도핵산가수분해효소 활성이 결여된다.이러한 경우, 유전자 발현은 대신 miRNA 유도 메커니즘에 의해 침묵될 것이다.
Piwi 상호작용 RNA는 트랜스포존의 소음에 책임이 있으며 siRNA가 [19]아닙니다.PIWI-상호작용 RNA(piRNA)는 길이가 21-35뉴클레오티드의 작은 비코드 RNA(ncRNA)의 최근 발견된 클래스입니다.그들은 유전자 발현 조절, 트랜스포존 사일링, 바이러스 감염 억제에 역할을 한다.한때 ncRNA의 "암흑 물질"로 여겨졌던 piRNA는 서로 [20]다른 유기체의 다세포 기능에서 중요한 주체로 떠올랐다.
전사 유전자 사일런싱
또는 siRNA를 RNA 유도 전사 사일런싱(RITS) 복합체에 포함할 수 있다.활성 RITS 복합체는 siRNA와 일치하는 DNA 주위에 헤테로크로마틴의 형성을 유발하여 DNA의 해당 영역의 유전자를 효과적으로 침묵시킵니다.
응용 프로그램:대립유전자특이적유전자
siRNA의 강력한 적용 중 하나는 단일 뉴클레오티드 차이로 표적 배열과 비표적 배열을 구별할 수 있는 능력이다.이 접근법은 돌연변이 대립 유전자가 단일 뉴클레오티드(nt)에 의해 wt-alle과 다른 GOF(기능성 이득) 장애에 치료적으로 중요한 것으로 간주되어 왔다.단일 nt 차이를 구별할 수 있는 능력을 가진 이러한 유형의 siRNA를 대립 유전자 특이적 siRNA라고 한다.[2]
ASP-RNAi는 지배적인 돌연변이 대립 유전자를 억제하는 것을 목적으로 하는 RNAi의 혁신적인 범주이며,[2] 두 가지 사이의 단일 핵산 차이의 특이성과 함께 대응하는 정상 대립 유전자의 발현을 피한다.ASP-siRNA는 특히 헌팅턴병(HD), DYT1 디스토니아(Gonzalez-Alegre et al. 2003, 2005), 알츠하이머병(Parkinson's et al. 2011)과 같은 유기체 생존에 중요한 경우 상염색체 우성 유전 질환 치료에 대한 새롭고 더 나은 교정 대안이다.질병(PD) (타카하시 외 2015), 아밀로이드 측삭경화증(ALS) (Schwarz 외 2006), 마차도-요셉병(Alves 외 2008)이 그것이다.또한 이들의 치료 잠재력은 표피용해성 황소단백증(Atkinson 등 2011), 표피성 손바닥 각질피증(EPPK) 및 격자 각막디스트로피증(LCDI 등 2014)[2]과 같은 다양한 피부 질환에 대해서도 평가되었다.
과제: 비특이적 효과 회피
RNAi는 많은 다른 경로와 교차하기 때문에, 때때로 siRNA의 [21][22]실험적인 도입에 의해 비특이적 효과가 유발되는 것은 놀라운 일이 아니다.포유류 세포가 siRNA와 같은 이중가닥 RNA를 만나면 바이러스 부산물로 착각해 면역반응을 일으킬 수 있다.또한 구조적으로 관련된 마이크로RNA는 주로 표적 mRNA와의 불완전한 상보성 염기쌍 상호작용을 통해 유전자 발현을 변조하기 때문에 siRNA의 도입은 의도하지 않은 표적이탈을 일으킬 수 있다.siRNA의 화학적 변형은 단일 뉴클레오티드 [23]특이성의 손실을 초래하는 열역학 특성을 변화시킬 수 있다.
선천성 면역
너무 많은 siRNA의 도입은 선천적인 면역 [24]반응의 활성화로 인해 비특이적인 사건을 야기할 수 있다.레티노인산유도유전자I(RIG-I)도 관련될 [25]수 있지만, 현재까지 대부분의 증거는 이것이 아마도 dsRNA 센서 PKR의 활성화에 기인한다고 시사한다.Toll-like receptor 7(TLR7)을 통한 사이토카인 유도도 설명되었다.유전자 기능 및 치료 응용에 대한 선천적 면역반응 활성화를 감소시키기 위해 siRNA의 화학적 변형을 사용한다.비특이적 효과를 감소시키는 하나의 유망한 방법은 siRNA를 마이크로RNA로 [26]변환하는 것이다.마이크로RNA는 자연적으로 발생하며, 이 내생 경로를 이용함으로써 상대적으로 낮은 농도의 siRNA에서 유사한 유전자 녹다운을 달성할 수 있을 것이다.이렇게 하면 비특이적인 영향을 최소화할 수 있습니다.
오프타깃팅
유전자 녹다운 [22]도구로 siRNA를 사용하는 것에 대한 또 다른 도전이다.여기서, 불완전한 상보성을 가진 유전자는 의도치 않게 siRNA에 의해 하향 조절되며(실제로 siRNA는 miRNA로 작용함), 데이터 해석 및 잠재적 독성에 문제를 일으킨다.그러나 이는 적절한 제어 실험을 설계함으로써 부분적으로 해결할 수 있으며, 현재 siRNA 설계 알고리즘은 오프타깃팅으로부터 자유로운 siRNA를 생산하기 위해 개발되고 있다.그 후, 예를 들어 마이크로 어레이 기술에 의한 게놈 전체의 발현 분석을 사용하여 이를 검증하고 알고리즘을 더욱 정교하게 만들 수 있다.Khvorova 박사의 2006년 논문은 위치 2에서 6 또는 7의 염기쌍 길이가 3'과 일치하는 siRNA에 포함된다고 한다.표적에서 벗어난 [27]유전자의 UTR 영역.siRNA 오프타깃 프리딕션 도구는 http://crdd.osdd.net/servers/aspsirna/asptar.php에서 구할 수 있으며 ASPSiRNA [28]리소스로 게시됩니다.
적응 면역 반응
일반 RNA는 면역력이 떨어질 수 있지만, RNA-단백질 복합체에 대한 항체는 쉽게 만들어질 수 있다.많은 자가면역질환들은 이런 종류의 항체를 본다.단백질에 결합된 siRNA에 대한 항체에 대한 보고는 아직 없다.siRNA 송달을 위한 몇 가지 방법은 올리고뉴클레오티드에 폴리에틸렌 글리콜(PEG)을 인접시켜 배설량을 줄이고 순환 반감기를 개선한다.그러나 최근 인자 IX에 대한 PEGyllated RNA 압타머의 대규모 3상 시험은 RNA의 PEG 부분에 대한 심각한 아나필락시 반응 때문에 Regado Biosciences에 의해 중단되어야 했다.이러한 반응은 일부 경우에 사망으로 이어졌으며 PEGylated 올리고뉴클레오티드가 관여할 [29]때 siRNA 전달에 대한 상당한 우려를 제기한다.
RNAi 기계의 포화도
세포로의 siRNA 전달은 전형적으로 많은 유전자의 발현을 감소시키지만, 유전자의 상향 조절 또한 관찰된다.유전자 발현의 상향 조절은 내인성 miRNA의 예측된 유전자 표적에 의해 부분적으로 설명될 수 있다.150개 이상의 siRNA 트랜스펙션 실험에 대한 컴퓨터 분석은 외인성 siRNA가 내인성 RNAi 기구를 포화시켜 내인성 miRNA 조절 [30]유전자의 억제 해제를 초래할 수 있는 모델을 뒷받침한다.따라서, siRNA는 원하지 않는 오프타깃 효과, 즉 siRNA와 표적 사이의 부분 배열 일치를 통해 mRNA의 의도하지 않은 하향 조절을 발생시킬 수 있는 반면, RNAi 기계의 포화는 또 다른 뚜렷한 비특이적 효과이며, 이는 miRNA 조절 유전자의 억제 해제와 데이터 해석과 유사한 문제를 야기한다.잠재적 [31]독성
화학적 수식
siRNA는 활성 강화, 혈청 안정성 증가, 표적 이탈 감소 및 면역학적 활성화 감소와 같은 치료 특성을 강화하기 위해 화학적으로 수정되었습니다.일반적으로 siRNA는 혈액의 분해를 방지하기 위해 나노지질 입자에 캡슐화되어 있다.그러한 모든 화학적 수정에 대한 자세한 데이터베이스는 과학 [32]문헌에서 siRNAmod로 수동으로 큐레이션된다.또한 siRNA의 화학적 변형은 의도치 않게 단일 핵산 [33]특이성의 손실을 초래할 수 있다.
치료 응용 프로그램 및 과제
본질적으로 관심 있는 유전자를 쓰러뜨릴 수 있는 능력을 감안할 때, siRNA를 통한 RNAi는 기초 생물학과 응용 생물학 모두에[34] 큰 관심을 불러일으켰다.
siRNA 및 RNAi 기반 치료의 가장 큰 어려움 중 하나는 세포 내 [35]전달이다. siRNA는 또한 약한 안정성과 약동학적 [36]행동을 가지고 있다.생체 내 siRNA올리고스는 혈장 및 조직핵산분해효소 및 엑소핵산가수분해효소에[37] 의한 분해에 [35]취약하며, [38]사람의 눈과 같은 국소적 전달부위에서는 미미한 효과만을 보였다.순수한 DNA를 표적 유기체에 전달하는 것은 그것의 큰 크기와 구조 때문에 [35]어렵다. siRNA올리고는 21-23올리고의 [39]작은 크기 때문에 이 문제를 회피한다.이것은 [38]나노벡터라고 불리는 나노스케일 배달 차량을 통해 배달할 수 있게 해준다.
siRNA 전달을 위한 좋은 나노벡터는 siRNA를 열화로부터 보호하고 표적 기관의 siRNA를 풍부하게 하며 siRNA의 [37]세포 흡수를 촉진해야 한다.siRNA 나노 벡터의 세 가지 주요 그룹은 지질 기반, 비지질 유기 기반 및 [37]무기입니다.지질 기반 나노 벡터는 고형 [37]종양에 siRNA를 전달하는 데 탁월하지만, 다른 암의 경우 시클로덱스트린 기반 나노 [37][40]입자와 같은 다른 비지질 기반 유기 나노 벡터가 필요할 수 있습니다.
지질 기반 나노 입자를 통해 전달되는 siRNA는 중추신경계 [41]장애에 대한 치료 잠재력을 가지고 있는 것으로 나타났다.중추 신경 장애,지만 혈액 뇌 장벽(BBB)자주 잠재적인 치료법의 뇌에 대한 접근을 차단하기 드문 일이 아니다.[41]siRNAs 그 목표와 BBB표면에 대해 침묵 유출 단백질 BBB투과성의 증가를 만드는 것으로 나타났다.[41]siRNA 지질을 통해 바탕으로 나노 입자 완전히 BBB를 가로질러 들어갈 수 있다 배달했다.[41]
siRNA 전달의 큰 어려움은 목표물을 벗어나는 [35][38]문제이다.유전자는 쌍방향으로 읽히기 때문에 의도한 안티센스 siRNA 가닥이 읽혀져 목표 mRNA가 녹아웃되어도 감지 siRNA 가닥은 다른 [42]기능에 관여하는 다른 단백질을 목표로 할 가능성이 있다.
2005년 말 첫 번째 두 가지 치료용 RNAi 시험 결과(노화 관련 황반변성, 일명 AMD)는 siRNA가 잘 견디고 적절한 약동학적 [43]특성을 가지고 있다고 보고했다.
1상 임상시험에서는 간으로 전이된 진행암 환자 41명에게 지질 나노입자를 통해 전달된 RNAi를 투여했다.RNAi는 암세포의 성장에 핵심 단백질을 코드하는 두 유전자, 혈관내피성장인자(VEGF)와 키네신방추단백질(KSP)을 대상으로 했다.그 결과 6개월 후 암이 안정되거나 일부 환자의 전이가 퇴보하는 임상적 이점이 나타났다.환자의 생체검사 검체에 대한 약역학 분석 결과, 검체 내 RNAi 구조의 존재가 밝혀져 분자가 의도한 [44][45]목표에 도달했음을 입증했습니다.
개념 증명 시험은 에볼라 표적 siRNA가 인간 노출 후 예방책으로 효과적일 수 있으며, 비인간 영장류의 100%가 가장 치명적인 [46]변종인 자이르 에볼라 바이러스의 치사량에서 살아남았다는 것을 보여주었다.
세포내 분만
세포 내에서 siRNA를 제공하는 것은 여전히 어려운 과제입니다.siRNA에는 효율과 독성이 다른 세 가지 주요 전달 기술이 있습니다.
트랜스펙션
이 기술에서 siRNA는 먼저 표적 유전자에 대해 설계되어야 한다.일단 siRNA가 유전자에 대해 구성되면 그것은 트랜스펙션 프로토콜을 통해 효과적으로 전달되어야 한다.전달은 보통 양이온성 리포좀, 고분자 나노입자, 그리고 지질 결합에 [47]의해 이루어집니다.이 방법은 대부분의 세포에 siRNA를 전달할 수 있고, 높은 효율성과 재현성을 가지고 있으며, 상업적으로 제공되기 때문에 유리하다.siRNA의 트랜스펙션을 위한 가장 일반적인 시약은 리포펙타민과 Neon 트랜스펙션이다.그러나 모든 세포 유형과 양립할 수 없으며 생체 내 [48][49]효율이 낮다.
일렉트로포레이션
또한 전기 펄스는 세포 내에 siRNA를 전달하기 위해 사용됩니다.세포막은 인지질로 이루어져 있어 전장에 민감합니다.빠르고 강력한 전기 펄스가 시작되면 지질 분자는 가열로 인해 열상 전이를 겪는 동안 방향을 다시 잡습니다.이것은 친수성 기공을 만들고 지질 이중층 세포막의 국소적인 섭동을 야기하기도 한다.이것은 이온과 대사물과 같은 많은 세포 내 내용물의 유출과 약물, 분자 탐침, 핵산의 동시 흡수를 가능하게 한다.전기감염이 어려운 세포는 전기감염이 유리하지만 이 [50]기술에서는 세포사망 가능성이 더 높다.
이 방법은 VEGF를 표적으로 하는 siRNA를 누드 생쥐의 이종 이식 종양에 전달하기 위해 사용되어 종양의 [51]성장을 현저하게 억제했다.
바이러스 매개 전달
트랜스펙트 설계 siRNA의 유전자 소음 효과는 일반적으로 일시적이지만 RNAi 접근방식을 통해 이 어려움을 극복할 수 있다.DNA 템플릿으로부터 이 siRNA를 전달하는 것은 레트로바이러스, 아데노 관련 바이러스, 아데노 바이러스 및 렌티바이러스에 [52]기초한 여러 재조합 바이러스 벡터를 통해 이루어질 수 있다.후자는 핵을 [53]직접 겨냥할 뿐만 아니라 비분열 세포를 전달할 수 있어 표적 세포에 siRNA를 안정적으로 전달하는 가장 효율적인 바이러스다.이러한 특정 바이러스 벡터는 세포로의 전달에 사용할 수 없는 siRNA를 효과적으로 촉진하기 위해 합성되었다.또 다른 측면은 어떤 경우에 합성 바이러스 벡터가 세포 게놈에 siRNA를 통합할 수 있어 siRNA의 안정적인 발현과 장기 유전자 녹다운을 가능하게 한다.이 기술은 생체 내이며 전달하기 어려운 세포에 효과적이기 때문에 유리하다.그러나 일부 세포 유형에서 항바이러스 반응을 유발하여 돌연변이 유발 및 면역 유발 효과를 일으킬 수 있기 때문에 문제가 발생합니다.
이 방법은 헌팅턴병 [54]치료를 위한 중추신경계의 유전자 소음에 잠재적으로 사용된다.
치료법
1993년 RNAi 메커니즘이 발견된 지 10년 후, 제약 부문은 siRNA 치료법의 연구와 개발에 많은 투자를 했다.이 치료법은 작은 분자와 항체보다 몇 가지 장점이 있다.분기별 또는 6개월마다 투여할 수 있습니다.또 다른 장점은 단백질의 특정 배열을 인식할 필요가 있는 작은 분자 및 모노클로널 항체와 달리 siRNA는 Watson-Crick 염기쌍과 mRNA에 의해 기능한다는 것이다.따라서 적절한 뉴클레오티드 배열을 이용할 [36]수 있다면 높은 친화력과 특이성으로 처리되어야 하는 표적 분자를 선택할 수 있다.연구자들이 극복해야 할 가장 큰 도전 중 하나는 그 치료법이 체내에 들어갈 수 있는 전달 시스템을 식별하고 확립하는 것이었다.그리고 면역체계가 RNAi 치료법을 감염제의 잔재로 오인하는 경우가 많습니다. 면역반응을 [4]일으킬 수 있습니다.동물 모델은 투자자들이 RNAi에서 [4]분리한 치료제의 약속에도 불구하고 사람에게서 나타나는 면역 반응의 정도를 정확하게 나타내지 못했다.
그러나 인간을 위한 RNAi 치료법의 개발을 계속한 몇몇 회사들이 있었다.Alnylam Pharmacuticals, Sirna Therapeutics 및 Dicerna Pharmacuticals는 아직 RNAi 치료제를 시장에 내놓기 위해 노력하고 있는 몇몇 회사들입니다.혈류에서 투여되는 거의 모든 siRNA 요법이 간에 축적된다는 것이 밝혀졌다.그래서 초기 약물 표적이 대부분 간에 영향을 미치는 질병들이었던 것이다.반복된 개발 작업은 또한 면역 반응을 감소시키기 위해 RNA 분자의 화학적 조성을 개선하는 데 빛을 비추었고, 결과적으로 부작용을 [55]거의 또는 전혀 일으키지 않았다.아래는 승인된 치료법 또는 파이프라인 치료법 중 일부입니다.
알닐람 제약
2018년 알닐람 제약은 FDA에 의해 siRNA 치료제를 승인받은 최초의 회사가 되었습니다.온파트로(patisiran)는 성인의 유전성 트란스티레틴 매개(hATTR) 아밀로이드증의 다발성 신경병증 치료에 대해 승인되었으며, hATTR은 희귀하고 점진적으로 쇠약해지는 질환이다.그것은 전 세계 5만 명의 사람들에게 영향을 미친다.약물을 간으로 직접 전달하기 위해 siRNA를 지질 나노 입자에 담는다.siRNA 분자는 비정상적인 TTR 단백질의 RNA 생산을 방해함으로써 아밀로이드 단백질의 생산을 중단시킨다.이것은 이러한 단백질이 신체의 다른 장기에 축적되는 것을 방지하고 환자들이 이 [56][57]병을 관리하는데 도움을 준다.
hATTR의 다른 치료 방법으로는 질병이 아직 초기 단계일 경우 잠재적으로 도움이 될 수 있는 OLT(정교성 간이식)가 있습니다.하지만 OLT는 병의 진행을 늦출 수 있을 뿐 치료하지 않을 수 있다.일시적인 완화를 제공하는 작은 분자 약품들도 있다.Onpattro가 출시되기 전에는 hATTR에 대한 치료 옵션이 제한적이었다.Onpattro의 승인 후, FDA는 Alnylam에게 심각한 상태를 치료하기 위한 약물에 주어지고 사용 가능한 치료법보다 상당히 개선된 획기적인 치료법 지정을 수여했다.또한 200,000명 미만의 [58]사람들에게 영향을 미치는 상태를 안전하게 치료하기 위한 치료법에 대한 Orphan Drug Designations도 수여되었습니다.
2019년 FDA는 급성 간 포르피린증(AHP) 치료에 사용되는 두 번째 RNAi 치료제인 기블라리(기보시란)를 승인했다.이 병은 헴 생산 과정에서 형성된 독성 포르포빌리노겐(PBG) 분자의 축적으로 인해 발생한다.이 분자들은 다른 장기에 축적되고 이것은 AHP의 증상이나 발작을 일으킬 수 있습니다.
기블라리는 헴 생산의 초기 단계에 관여하는 간 효소인 아미노레불린산 합성효소 1(ALS1)의 발현을 하향 조절하는 siRNA 약물이다.AHAS1의 하향조절은 AHP [36]증상을 일으키는 신경독성 중간체 수치를 낮춘다.
수년에 걸친 연구는 간에 영향을 미치는 것 이상의 siRNA 치료법에 대한 더 많은 이해를 이끌어냈다.알닐람 제약은 현재 헌팅턴병이나 알츠하이머병과 [4]같은 아밀로이드증과 CNS 질환을 치료할 수 있는 치료법에 관여하고 있다.그들은 또한 최근 CNS, 눈 및 간 질환에 대한 치료법을 개발하기 위해 Regeneron Pharmacuticals와 파트너 관계를 맺고 있습니다.
2020년 현재 ONPATRO와 GIVLAARI는 상용 적용이 가능하며, 신약 적용을 위해 루마시란(ALN-GO1)과 인클리시란(inclisiran)의 2가지 siRNA가 FDA에 제출되었다.몇몇 siRNA는 3단계 임상 연구를 진행 중이며, 더 많은 후보들이 초기 발달 [36]단계에 있다.2020년 알닐람과 버 제약회사는 파트너십을 발표했고 COVID-19의 [59]심각한 환자를 치료할 RNAi 치료법을 연구하기 시작했다.
siRNA 치료제의 파이프라인 개발에 성공한 기업으로는 Eli Lily와 제휴한 Dicerna Pharmacuticals와 Johnson과 제휴한 Arrowhead Pharmacuticals가 있습니다.Amgen과 AstraZeneca와 같은 몇몇 다른 대형 제약 회사들도 생물학적 [60]약물의 잠재적인 성공을 보고 siRNA 치료에 많은 투자를 했습니다.
「 」를 참조해 주세요.
레퍼런스
- ^ Laganà A, Veneziano D, Russo F, Pulvirenti A, Giugno R, Croce CM, Ferro A (2015). "Computational design of artificial RNA molecules for gene regulation". RNA Bioinformatics. Methods in Molecular Biology. Vol. 1269. pp. 393–412. doi:10.1007/978-1-4939-2291-8_25. ISBN 978-1-4939-2290-1. PMC 4425273. PMID 25577393.
- ^ a b c d e f Monga 1세, 쿠레시 A, 인도의 N, 굽타 AK, 쿠마르 M(2017년)."ASPsiRNA:A자원 ASP-siRNAs는 치료적 잠재력 인간 유전자 Disorders과 알고리즘의 그들의 Inhibitory 성능 예측".G3(베데스다, md입니다). 7(9):2931–2943. doi:10.1534/g3.117.044024.PMC 5592921.PMID 28696921.텍스트는 창조적 공용 귀인 4.0국제 라이센스 하에 가능하다 이 원본에서 복사되었다.
- ^ Bernstein E, Caudy AA, Hammond SM, Hannon GJ (January 2001). "Role for a bidentate ribonuclease in the initiation step of RNA interference". Nature. 409 (6818): 363–6. Bibcode:2001Natur.409..363B. doi:10.1038/35053110. PMID 11201747. S2CID 4371481.
- ^ a b c d e Eisenstein M (16 October 2019). "Pharma's roller-coaster relationship with RNA therapies". Nature. 574 (7778): S4–S6. Bibcode:2019Natur.574S...4E. doi:10.1038/d41586-019-03069-3. S2CID 204741280.
- ^ Hamilton AJ, Baulcombe DC (October 1999). "A species of small antisense RNA in posttranscriptional gene silencing in plants". Science. 286 (5441): 950–2. doi:10.1126/science.286.5441.950. PMID 10542148. S2CID 17480249.
- ^ Elbashir SM, Harborth J, Lendeckel W, Yalcin A, Weber K, Tuschl T (May 2001). "Duplexes of 21-nucleotide RNAs mediate RNA interference in cultured mammalian cells". Nature. 411 (6836): 494–8. Bibcode:2001Natur.411..494E. doi:10.1038/35078107. PMID 11373684. S2CID 710341.
- ^ "New Kind of Drug, Silencing Genes, Gets FDA Approval". The Wall Street Journal. 10 August 2018. Retrieved 26 March 2021.
{{cite news}}: CS1 maint :url-status (링크) - ^ Qureshi A, Thakur N, Monga I, Thakur A, Kumar M (1 January 2014). "VIRmiRNA: a comprehensive resource for experimentally validated viral miRNAs and their targets". Database. 2014: bau103. doi:10.1093/database/bau103. PMC 4224276. PMID 25380780.
- ^ Mack GS (June 2007). "MicroRNA gets down to business". Nature Biotechnology. 25 (6): 631–8. doi:10.1038/nbt0607-631. PMID 17557095. S2CID 35357127.
- ^ "RNA Interference (RNAi)". Retrieved 27 July 2018.
- ^ Sharei A, Zoldan J, Adamo A, Sim WY, Cho N, Jackson E, et al. (February 2013). "A vector-free microfluidic platform for intracellular delivery". Proceedings of the National Academy of Sciences of the United States of America. 110 (6): 2082–7. Bibcode:2013PNAS..110.2082S. doi:10.1073/pnas.1218705110. PMC 3568376. PMID 23341631.
- ^ Daneholt, B. (2006). "Advanced Information: RNA interference". The Novel Prize in Physiology or Medicine.
- ^ Li L (2008). "Small RNA-Mediated Gene Activation". In Morris KV (ed.). RNA and the Regulation of Gene Expression: A Hidden Layer of Complexity. Caister Academic Press. ISBN 978-1-904455-25-7.
- ^ De Hayr L, Asad S, Hussain M, Asgari S (2020). "RNA activation in insects: The targeted activation of endogenous and exogenous genes". Insect Biochem Mol Biol. 119: 103325. doi:10.1016/j.ibmb.2020.103325. PMID 31978586. S2CID 210891954.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Lee YS, Nakahara K, Pham JW, Kim K, He Z, Sontheimer EJ, Carthew RW (April 2004). "Distinct roles for Drosophila Dicer-1 and Dicer-2 in the siRNA/miRNA silencing pathways". Cell. 117 (1): 69–81. doi:10.1016/s0092-8674(04)00261-2. PMID 15066283. S2CID 6683459.
- ^ a b Carthew RW, Sontheimer EJ (February 2009). "Origins and Mechanisms of miRNAs and siRNAs". Cell. 136 (4): 642–55. doi:10.1016/j.cell.2009.01.035. PMC 2675692. PMID 19239886.
- ^ a b c Tomari Y, Zamore PD (March 2005). "Perspective: machines for RNAi". Genes & Development. 19 (5): 517–29. doi:10.1101/gad.1284105. PMID 15741316.
- ^ Orban TI, Izaurralde E (April 2005). "Decay of mRNAs targeted by RISC requires XRN1, the Ski complex, and the exosome". RNA. 11 (4): 459–69. doi:10.1261/rna.7231505. PMC 1370735. PMID 15703439.
- ^ Ozata DM, Gainetdinov I, Zoch A, Phillip D, Zamore PD (2019). "PIWI-interacting RNAs: small RNAs with big functions" (PDF). Nature Reviews Genetics. 20 (2): 89–108. doi:10.1038/s41576-018-0073-3. PMID 30446728. S2CID 53565676.
- ^ Monga I, Banerjee I (2019). "Computational Identification of piRNAs Using Features Based on RNA Sequence, Structure, Thermodynamic and Physicochemical Properties". Current Genomics. 20 (2): 508–518. doi:10.2174/1389202920666191129112705. PMC 7327968. PMID 32655289.
- ^ Jackson AL, Linsley PS (January 2010). "Recognizing and avoiding siRNA off-target effects for target identification and therapeutic application". Nature Reviews Drug Discovery. 9 (1): 57–67. doi:10.1038/nrd3010. PMID 20043028. S2CID 20903257.
- ^ a b Woolf TM, Melton DA, Jennings CG (August 1992). "Specificity of antisense oligonucleotides in vivo". Proceedings of the National Academy of Sciences of the United States of America. 89 (16): 7305–9. Bibcode:1992PNAS...89.7305W. doi:10.1073/pnas.89.16.7305. PMC 49698. PMID 1380154.
- ^ Dua P, Yoo JW, Kim S, Lee DK (September 2011). "Modified siRNA structure with a single nucleotide bulge overcomes conventional siRNA-mediated off-target silencing". Molecular Therapy. 19 (9): 1676–87. doi:10.1038/mt.2011.109. PMC 3182346. PMID 21673662.
- ^ Whitehead KA, Dahlman JE, Langer RS, Anderson DG (17 June 2011). "Silencing or stimulation? siRNA delivery and the immune system". Annual Review of Chemical and Biomolecular Engineering. 2 (1): 77–96. doi:10.1146/annurev-chembioeng-061010-114133. PMID 22432611. S2CID 28803811.
- ^ Matsumiya T, Stafforini DM (2010). "Function and regulation of retinoic acid-inducible gene-I". Critical Reviews in Immunology. 30 (6): 489–513. doi:10.1615/critrevimmunol.v30.i6.10. PMC 3099591. PMID 21175414.
- ^ Barøy T, Sørensen K, Lindeberg MM, Frengen E (June 2010). "shRNA expression constructs designed directly from siRNA oligonucleotide sequences". Molecular Biotechnology. 45 (2): 116–20. doi:10.1007/s12033-010-9247-8. PMID 20119685. S2CID 24309609.
- ^ Birmingham A, Anderson EM, Reynolds A, Ilsley-Tyree D, Leake D, Fedorov Y, et al. (March 2006). "3' UTR seed matches, but not overall identity, are associated with RNAi off-targets". Nature Methods. 3 (3): 199–204. doi:10.1038/nmeth854. PMID 16489337. S2CID 52809577.
- ^ Monga I, Qureshi A, Thakur N, Gupta AK, Kumar M (2017). "ASPsiRNA: A Resource of ASP-siRNAs Having Therapeutic Potential for Human Genetic Disorders and Algorithm for Prediction of Their Inhibitory Efficacy". G3 (Bethesda, Md.) . 7 (9): 2931–2943. doi:10.1534/g3.117.044024. PMC 5592921. PMID 28696921.
- ^ Wittrup A, Lieberman J (September 2015). "Knocking down disease: a progress report on siRNA therapeutics". Nature Reviews. Genetics. 16 (9): 543–52. doi:10.1038/nrg3978. PMC 4756474. PMID 26281785.
- ^ Khan AA, Betel D, Miller ML, Sander C, Leslie CS, Marks DS (June 2009). "Transfection of small RNAs globally perturbs gene regulation by endogenous microRNAs". Nature Biotechnology. 27 (6): 549–55. doi:10.1038/nbt.1543. PMC 2782465. PMID 19465925.
- ^ Grimm D, Streetz KL, Jopling CL, Storm TA, Pandey K, Davis CR, et al. (May 2006). "Fatality in mice due to oversaturation of cellular microRNA/short hairpin RNA pathways". Nature. 441 (7092): 537–41. Bibcode:2006Natur.441..537G. doi:10.1038/nature04791. PMID 16724069. S2CID 15118504.
- ^ Dar SA, Thakur A, Qureshi A, Kumar M (January 2016). "siRNAmod: A database of experimentally validated chemically modified siRNAs". Scientific Reports. 6 (1): 20031. Bibcode:2016NatSR...620031D. doi:10.1038/srep20031. PMC 4730238. PMID 26818131.
- ^ Hickerson RP, Smith FJ, Reeves RE, Contag CH, Leake D, Leachman SA, et al. (March 2008). "Single-nucleotide-specific siRNA targeting in a dominant-negative skin model". The Journal of Investigative Dermatology. 128 (3): 594–605. CiteSeerX 10.1.1.465.8240. doi:10.1038/sj.jid.5701060. PMID 17914454.
- ^ Alekseev OM, Richardson RT, Alekseev O, O'Rand MG (May 2009). "Analysis of gene expression profiles in HeLa cells in response to overexpression or siRNA-mediated depletion of NASP". Reproductive Biology and Endocrinology. 7 (1): 45. doi:10.1186/1477-7827-7-45. PMC 2686705. PMID 19439102.
- ^ a b c d Petrocca F, Lieberman J (February 2011). "Promise and challenge of RNA interference-based therapy for cancer". Journal of Clinical Oncology. 29 (6): 747–54. doi:10.1200/JCO.2009.27.6287. PMID 21079135. S2CID 15337692.
- ^ a b c d Hu B, Zhong L, Weng Y, Peng L, Huang Y, Zhao Y, Liang XJ (June 2020). "Therapeutic siRNA: state of the art". Signal Transduction and Targeted Therapy. 5 (1): 101. doi:10.1038/s41392-020-0207-x. PMC 7305320. PMID 32561705.
- ^ a b c d e Shen H, Sun T, Ferrari M (June 2012). "Nanovector delivery of siRNA for cancer therapy". Cancer Gene Therapy. 19 (6): 367–73. doi:10.1038/cgt.2012.22. PMC 3842228. PMID 22555511.
- ^ a b c Burnett JC, Rossi JJ (January 2012). "RNA-based therapeutics: current progress and future prospects". Chemistry & Biology. 19 (1): 60–71. doi:10.1016/j.chembiol.2011.12.008. PMC 3269031. PMID 22284355.
- ^ Elbashir SM, Lendeckel W, Tuschl T (January 2001). "RNA interference is mediated by 21- and 22-nucleotide RNAs". Genes & Development. 15 (2): 188–200. doi:10.1101/gad.862301. PMC 312613. PMID 11157775.
- ^ Heidel JD, Yu Z, Liu JY, Rele SM, Liang Y, Zeidan RK, et al. (April 2007). "Administration in non-human primates of escalating intravenous doses of targeted nanoparticles containing ribonucleotide reductase subunit M2 siRNA". Proceedings of the National Academy of Sciences of the United States of America. 104 (14): 5715–21. doi:10.1073/pnas.0701458104. PMC 1829492. PMID 17379663.
- ^ a b c d Gomes MJ, Dreier J, Brewer J, Martins S, Brandl M, Sarmento B (April 2016). "A new approach for a blood-brain barrier model based on phospholipid vesicles: Membrane development and siRNA-loaded nanoparticles permeability". Journal of Membrane Science. 503: 8–15. doi:10.1016/j.memsci.2016.01.002.
- ^ Shukla RS, Qin B, Cheng K (October 2014). "Peptides used in the delivery of small noncoding RNA". Molecular Pharmaceutics. 11 (10): 3395–408. doi:10.1021/mp500426r. PMC 4186677. PMID 25157701.
- ^ Tansey B (11 August 2006). "Promising eye drug from S.F. firm / Macular degeneration treatment interferes with RNA messages". SFGATE.
- ^ "First-in-man study demonstrates the therapeutic effect of RNAi gene silencing in cancer treatment" (Press release). Vall d'Hebron Institute of Oncology. 11 February 2013.
- ^ Tabernero J, Shapiro GI, LoRusso PM, Cervantes A, Schwartz GK, Weiss GJ, et al. (April 2013). "First-in-humans trial of an RNA interference therapeutic targeting VEGF and KSP in cancer patients with liver involvement". Cancer Discovery. 3 (4): 406–17. doi:10.1158/2159-8290.CD-12-0429. PMID 23358650.
- ^ Geisbert TW, Lee AC, Robbins M, Geisbert JB, Honko AN, Sood V, et al. (May 2010). "Postexposure protection of non-human primates against a lethal Ebola virus challenge with RNA interference: a proof-of-concept study". Lancet. 375 (9729): 1896–905. doi:10.1016/S0140-6736(10)60357-1. PMC 7138079. PMID 20511019.
- ^ Fanelli A (2016). "Transfection: In Vitro Transfection". Retrieved 5 December 2017.
- ^ Jensen K, Anderson JA, Glass EJ (April 2014). "Comparison of small interfering RNA (siRNA) delivery into bovine monocyte-derived macrophages by transfection and electroporation". Veterinary Immunology and Immunopathology. 158 (3–4): 224–32. doi:10.1016/j.vetimm.2014.02.002. PMC 3988888. PMID 24598124.
- ^ Chatterjea MN (2012). Textbook of Medical Biochemistry (8th ed.). New Delhi: Jaypee Brothers Medical Publishers. p. 304.
- ^ "siRNA Delivery Methods into Mammalian Cells". 13 October 2016.
- ^ Takei Y (2014). "Electroporation-mediated siRNA delivery into tumors". Electroporation Protocols. Methods in Molecular Biology. Vol. 1121. pp. 131–8. doi:10.1007/978-1-4614-9632-8_11. ISBN 978-1-4614-9631-1. PMID 24510818.
- ^ Talwar GP, Hasnain S, Sarin SK (January 2016). Textbook of Biochemistry, Biotechnology, Allied and Molecular Medicine (4th ed.). PHI Learning Private Limited. p. 873. ISBN 978-81-203-5125-7.
- ^ Morris KV, Rossi JJ (March 2006). "Lentiviral-mediated delivery of siRNAs for antiviral therapy". Gene Therapy. 13 (6): 553–8. doi:10.1038/sj.gt.3302688. PMC 7091755. PMID 16397511.
- ^ Cambon K, Déglon N (2013). Lentiviral-mediated gene transfer of siRNAs for the treatment of Huntington's disease. Methods in Molecular Biology. Vol. 1010. pp. 95–109. doi:10.1007/978-1-62703-411-1_7. ISBN 978-1-62703-410-4. PMID 23754221.
- ^ Tiemann K, Rossi JJ (June 2009). "RNAi-based therapeutics-current status, challenges and prospects". EMBO Molecular Medicine. 1 (3): 142–51. doi:10.1002/emmm.200900023. PMC 3378126. PMID 20049714.
- ^ Yonezawa, Sei; Koide, Hiroyuki; Asai, Tomohiro (2020). "Recent advances in siRNA delivery mediated by lipid-based nanoparticles". Advanced Drug Delivery Reviews. 154: 64–78. doi:10.1016/j.addr.2020.07.022. ISSN 0169-409X. PMC 7406478. PMID 32768564.
- ^ Commissioner, Office of the (24 March 2020). "FDA approves first-of-its kind targeted RNA-based therapy to treat a rare disease". FDA. Retrieved 24 May 2021.
- ^ "FDA approves first-of-its kind targeted RNA-based therapy to treat a rare disease" (Press release). U.S. Food and Drug Administration. 10 August 2018.
- ^ "Vir and Alnylam Expand Collaboration to Advance Investigational RNAi Therapeutics Targeting Host Factors for t". Investor Relations Alnylam Pharmaceuticals, Inc. Retrieved 24 May 2021.
- ^ "Alnylam and Dicerna are pals now, which could spell trouble for Arrowhead". BioPharma Dive. Retrieved 24 May 2021.
추가 정보
- Hannon GJ, Rossi JJ (September 2004). "Unlocking the potential of the human genome with RNA interference". Nature. 431 (7006): 371–8. Bibcode:2004Natur.431..371H. doi:10.1038/nature02870. PMID 15372045. S2CID 4410723.
- Du Rietz H, Hedlund H, Wilhelmson S, Nordenfelt P, Wittrup A (April 2020). "Imaging small molecule-induced endosomal escape of siRNA". Nature Communications. 11 (1): 1809. Bibcode:2020NatCo..11.1809D. doi:10.1038/s41467-020-15300-1. PMC 7156650. PMID 32286269.