프로피오닐CoA카르복실화효소
Propionyl-CoA carboxylase| 프로피오닐CoA카르복실화효소 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
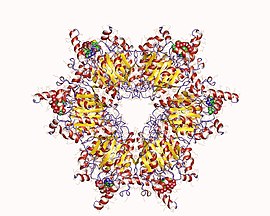
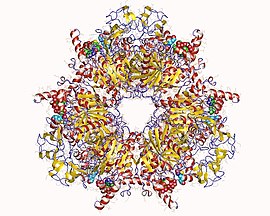 프로피오닐-CoA카르복실화효소헤테로12머, 메틸루브럼익스토르켄스 | |||||||||
| 식별자 | |||||||||
| EC 번호 | 6.4.1.3 | ||||||||
| CAS 번호 | 9023-94-3 | ||||||||
| 데이터베이스 | |||||||||
| 인텐츠 | IntEnz 뷰 | ||||||||
| 브렌다 | 브렌다 엔트리 | ||||||||
| ExPASy | NiceZyme 뷰 | ||||||||
| 케그 | KEGG 엔트리 | ||||||||
| 메타사이크 | 대사 경로 | ||||||||
| 프라이머리 | 프로필 | ||||||||
| PDB 구조 | RCSB PDB PDBe PDBum | ||||||||
| 진 온톨로지 | AmiGO / QuickGO | ||||||||
| |||||||||
프로피오닐-CoA 카르복실화효소(EC 6.4.1.3, PCC)는 미토콘드리아 매트릭스에서 프로피오닐-CoA의 카르복실화 반응을 촉매한다.PCC는 리가아제와[1] 리아제 [2]둘 다로 분류되었다.그 효소는 비오틴 의존적이다.반응 생성물은 (S)-메틸말로닐 CoA이다.
- ATP + 프로피오닐-CoA + HCO3− <=> ADP + 인산염 + (S)-메틸말로닐-CoA
(S)-메틸말로닐-CoA는 동물이 직접 이용할 수 없다.라세마아제에 의해 작용하여 (R)-메틸말로닐-CoA를 생성하고, 메틸말로닐-CoA 뮤타아제(비타민 B12를 보조 인자로 필요로 하는 몇 안 되는 대사 효소 중 하나)에 의해 숙시닐-CoA로 전환된다.크렙스 회로 중간체인 숙시닐-CoA는 푸마르산, 말산, 옥살아세트산 등으로 추가로 대사된다.옥살로아세테이트는 포스포에놀 피루브산염 및 기타 글루코네겐성 중간체를 형성하기 위해 세포 내로 운반될 수 있다.따라서 프로피오닐-CoA는 포도당의 중요한 전구체이다.
프로피오닐-CoA는 대부분의 메틸화 지방산을 포함한 홀수 사슬 지방산 대사의 최종 산물이다.아미노산 발린, 이소류신 및 메티오닌도 프로피오닐-CoA 대사의 기질이다.
구조.
프로피오닐-CoA 카르복실화효소(PCC)는 750kDa 알파(6)-베타(6)-도데카머(약 540kDa만이 토종효소)[3]이다. 알파 서브유닛은 단량체로 배열되어 중앙 베타-6 육각체 코어를 장식한다.해당 코어는 축을 따라 구멍이 뚫린 짧은 원통형이다.
PCC의 알파 서브유닛은 비오틴 카르복실화효소(BC) 및 비오틴 카르복실 캐리어 단백질(BCCP) 도메인을 포함한다.BT 도메인으로 알려진 도메인은 알파 서브유닛에 위치하고 베타 서브유닛과의 상호작용에 필수적이다.이 도메인의 8가닥 반병렬 베타 배럴 폴드는 특히 흥미롭다.베타 서브유닛은 카르복실전달효소([4]CT) 활성을 포함한다.

BC 부위와 CT 부위는 약 55Ω 떨어져 있으며,[5] 이는 프로피오닐-CoA의 카르복실화 촉매 작용 중에 BCCP 도메인 전체가 전이됨을 나타낸다.이것은 알파와 베타 서브 유닛 사이의 중요한 이합체 상호작용에 대한 명확한 증거를 제공한다.
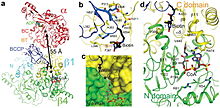
PCC의 비오틴 결합 포켓은 소수성이며 보존성이 높다.비오틴과 프로피오닐-CoA는 옥시 음이온 홀을 포함한 활성 부위에서 서로 수직으로 결합한다.비오틴에 대한 토종 효소 대 비오틴 비율은 4 [3]몰 비오틴에 대한 1 몰 토종 효소로 결정되었다.비오틴의 N1은 활성 부위 [4]염기로 생각됩니다.
D422에서의 부위 지향 돌연변이 유발은 프로피오닐-CoA 결합 부위의 기질 특이성의 변화를 나타내며, 따라서 PCC의 촉매 [6]활성에서 이 잔류물의 중요성을 나타낸다.1979년 페닐글리옥살에 의한 억제는 프로피오닐-CoA 또는 ATP 중 하나의 인산기가 촉매 작용 [7]중 활성 부위의 필수 아르기닌 잔기와 반응하는 것을 결정했다.이후(2004년) 아르기닌-338이 [8]비오틴의 최적의 카르복실화를 위해 카르복시인산 중간체의 배향 역할을 한다는 것이 제안되었다.
ATP, 프로피오닐-CoA, 중탄산염의 KM 값은 각각 0.08mM, 0.29mM, 3.0mM으로 측정되었다.등전점은 pH 5.5입니다. PCC의 구조적 건전성은 -50~37도 온도 범위와 6.2~8.8도 범위에서 유지됩니다.최적 pH는 비오틴 [3]결합 없이 7.2~8.8인 것으로 나타났다.비오틴의 경우 최적 pH는 8.0~8.[9]5이다.
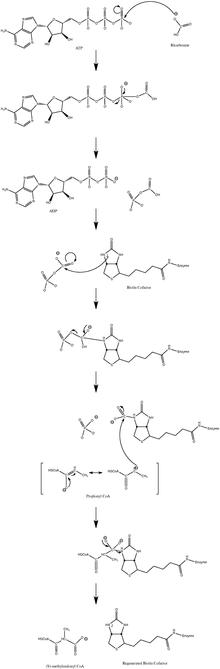
메커니즘
정상적인 촉매 반응 메커니즘은 카르보니온 중간체를 포함하며,[10] 일치된 프로세스를 거치지 않습니다.그림 3은 가능한 경로를 보여줍니다.
이 반응은 낮은 프로피오닐-CoA [11]플럭스에서 약간 가역적인 것으로 나타났다.
서브유닛유전자
인간 프로피오닐-CoA 카르복실화효소는 각각 별도의 유전자에 의해 코드되는 두 개의 서브유닛을 포함한다.
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
병리학
결핍은 프로피온산혈증과 [12][13][14]관련이 있다.
PCC 활성은 현재까지 테스트된 비오틴 상태의 가장 민감한 지표입니다.향후 임신 연구에서는 림프구 PCC 활성 데이터를 사용하여 비오틴 [15]상태를 평가할 수 있습니다.
유전자내보완
유전자에 의해 코드된 폴리펩타이드의 여러 복사본이 응집체를 형성할 때, 이 단백질 구조를 멀티머라고 한다.특정 유전자의 서로 다른 두 돌연변이 대립 유전자에 의해 생성된 폴리펩타이드로부터 멀티머가 형성될 때, 혼합 멀티머는 각각의 돌연변이만으로 형성되는 비혼합 멀티머보다 더 큰 기능 활성을 보일 수 있다.이 경우 이 현상을 유전자 내 상보라고 한다.
PCC는 αβ66 구조의 α 및 β 서브유닛으로 이루어진 헤테로폴리머이다.α 서브유닛(PCCα) 또는 β 서브유닛(PCCβ)의 PCC 돌연변이는 사람에게 프로피온산혈증을 일으킬 수 있다.PCCβ에 결함이 있는 서로 다른 돌연변이 피부 섬유아세포주가 쌍방향 결합으로 융합되었을 때, 그 결과 형성된 β 헤테로머 단백질은 종종 부모 [16]효소의 활성에 기초하여 예상한 것보다 더 높은 수준의 활성을 보였다.이러한 유전자 내 상보성의 발견은 PCC의 다량체 구조가 보다 기능적인 형태의 홀로엔자임을 생성할 수 있는 구성 PCCβ 단량체 간의 협력적 상호작용을 가능하게 한다는 것을 보여주었다.
규정
프로피오닐-CoA 카르복실화효소
a. 카르바마제핀(항간질제): 간의 효소[17] 수준을 현저하게 낮춘다.
b. 대장균 샤페로닌 단백질 GROES 및 GROEL: 인간 PCC 헤테로머 서브유닛의[18] 접힘 및 조립에 필수적
c. 중탄산염: 네거티브 협동성[8]
d2+. Mg 및 MgATP:2− 알로스테릭 활성화[19]
프로피오닐-CoA 카르복실화효소
a. 6-디옥시에리트로놀라이드 B: PCC 수치 감소로 생산량 증가
b. 췌장 베타 세포의 글루코키나아제: KM을 감소시키고 Vmax를 증가시키는 것으로 나타난 베타 PCC의 전구체; 활성화
「 」를 참조해 주세요.
레퍼런스
- ^ EC 6.4.1.3
- ^ EC 4.1.1.41
- ^ a b c Kalousek F, Darigo MD, Rosenberg LE (January 1980). "Isolation and characterization of propionyl-CoA carboxylase from normal human liver. Evidence for a protomeric tetramer of nonidentical subunits". The Journal of Biological Chemistry. 255 (1): 60–65. PMID 6765947.
- ^ a b Diacovich L, Mitchell DL, Pham H, Gago G, Melgar MM, Khosla C, et al. (November 2004). "Crystal structure of the beta-subunit of acyl-CoA carboxylase: structure-based engineering of substrate specificity". Biochemistry. 43 (44): 14027–14036. doi:10.1021/bi049065v. PMID 15518551.
- ^ a b c Huang CS, Sadre-Bazzaz K, Shen Y, Deng B, Zhou ZH, Tong L (August 2010). "Crystal structure of the alpha(6)beta(6) holoenzyme of propionyl-coenzyme A carboxylase". Nature. 466 (7309): 1001–1005. doi:10.1038/nature09302. PMC 2925307. PMID 20725044.
- ^ Arabolaza A, Shillito ME, Lin TW, Diacovich L, Melgar M, Pham H, et al. (August 2010). "Crystal structures and mutational analyses of acyl-CoA carboxylase beta subunit of Streptomyces coelicolor". Biochemistry. 49 (34): 7367–7376. doi:10.1021/bi1005305. PMC 2927733. PMID 20690600.
- ^ Wolf B, Kalousek F, Rosenberg LE (1979). "Essential arginine residues in the active sites of propionyl CoA carboxylase and beta-methylcrotonyl CoA carboxylase". Enzyme. 24 (5): 302–306. doi:10.1159/000458679. PMID 510274.
- ^ a b Sloane V, Waldrop GL (April 2004). "Kinetic characterization of mutations found in propionic acidemia and methylcrotonylglycinuria: evidence for cooperativity in biotin carboxylase". The Journal of Biological Chemistry. 279 (16): 15772–15778. doi:10.1074/jbc.M311982200. PMID 14960587.
- ^ Hsia YE, Scully KJ, Rosenberg LE (June 1979). "Human propionyl CoA carboxylase: some properties of the partially purified enzyme in fibroblasts from controls and patients with propionic acidemia". Pediatric Research. 13 (6): 746–751. doi:10.1203/00006450-197906000-00005. PMID 481943.
- ^ Stubbe J, Fish S, Abeles RH (January 1980). "Are carboxylations involving biotin concerted or nonconcerted?". The Journal of Biological Chemistry. 255 (1): 236–242. PMID 7350155.
- ^ Reszko AE, Kasumov T, Pierce BA, David F, Hoppel CL, Stanley WC, et al. (September 2003). "Assessing the reversibility of the anaplerotic reactions of the propionyl-CoA pathway in heart and liver". The Journal of Biological Chemistry. 278 (37): 34959–34965. doi:10.1074/jbc.M302013200. PMID 12824185.
- ^ Ugarte M, Pérez-Cerdá C, Rodríguez-Pombo P, Desviat LR, Pérez B, Richard E, et al. (1999). "Overview of mutations in the PCCA and PCCB genes causing propionic acidemia". Human Mutation. 14 (4): 275–282. doi:10.1002/(SICI)1098-1004(199910)14:4<275::AID-HUMU1>3.0.CO;2-N. PMID 10502773.
- ^ Desviat LR, Pérez B, Pérez-Cerdá C, Rodríguez-Pombo P, Clavero S, Ugarte M (2004). "Propionic acidemia: mutation update and functional and structural effects of the variant alleles". Molecular Genetics and Metabolism. 83 (1–2): 28–37. doi:10.1016/j.ymgme.2004.08.001. PMID 15464417.
- ^ Deodato F, Boenzi S, Santorelli FM, Dionisi-Vici C (May 2006). "Methylmalonic and propionic aciduria". American Journal of Medical Genetics. Part C, Seminars in Medical Genetics. 142C (2): 104–112. doi:10.1002/ajmg.c.30090. PMID 16602092. S2CID 21114631.
- ^ Stratton SL, Bogusiewicz A, Mock MM, Mock NI, Wells AM, Mock DM (August 2006). "Lymphocyte propionyl-CoA carboxylase and its activation by biotin are sensitive indicators of marginal biotin deficiency in humans". The American Journal of Clinical Nutrition. 84 (2): 384–388. doi:10.1093/ajcn/84.1.384. PMC 1539098. PMID 16895887.
- ^ Rodriguez-Pombo P, Pérez-Cerda C, Pérez B, Desviat LR, Santchez-Pulido L, Ugarte M.헤테로머 단백질 프로피오닐-CoA 카르복실화효소의 유전자 내 상보성을 설명하는 모델.바이오침 바이오피스 액타.2005;1740(3):489-498.doi:10.1016/j.bbbadis.2004.10.009
- ^ Rathman SC, Eisenschenk S, McMahon RJ (November 2002). "The abundance and function of biotin-dependent enzymes are reduced in rats chronically administered carbamazepine". The Journal of Nutrition. 132 (11): 3405–3410. doi:10.1093/jn/132.11.3405. PMID 12421859.
- ^ Kelson TL, Ohura T, Kraus JP (March 1996). "Chaperonin-mediated assembly of wild-type and mutant subunits of human propionyl-CoA carboxylase expressed in Escherichia coli". Human Molecular Genetics. 5 (3): 331–337. doi:10.1093/hmg/5.3.331. PMID 8852656.
- ^ McKeon C, Wolf B (1982). "Magnesium and magnesium adenosine triphosphate activation of human propionyl CoA carboxylase and beta-methylcrotonyl CoA carboxylase". Enzyme. 28 (1): 76–81. doi:10.1159/000459088. PMID 6981505.
- ^ Zhang H, Boghigian BA, Pfeifer BA (February 2010). "Investigating the role of native propionyl-CoA and methylmalonyl-CoA metabolism on heterologous polyketide production in Escherichia coli". Biotechnology and Bioengineering. 105 (3): 567–573. doi:10.1002/bit.22560. PMID 19806677. S2CID 659042.
- ^ Shiraishi A, Yamada Y, Tsuura Y, Fijimoto S, Tsukiyama K, Mukai E, et al. (January 2001). "A novel glucokinase regulator in pancreatic beta cells: precursor of propionyl-CoA carboxylase beta subunit interacts with glucokinase and augments its activity". The Journal of Biological Chemistry. 276 (4): 2325–2328. doi:10.1074/jbc.C000530200. PMID 11085976.
외부 링크
- 미국 국립의학도서관의 프로피오닐-CoA+카르복실화효소(MeSH)