다면 B세포 반응
Polyclonal B cell response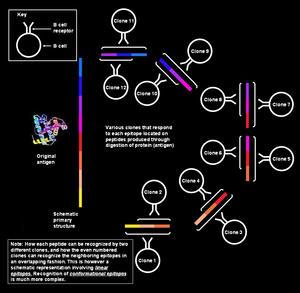
다면 B세포 반응은 포유류의 적응 면역체계에 의해 나타나는 자연적인 면역 반응 방식이다.그것은 하나의 항원이 B세포의 여러 복제에 의해, 상피라고 불리는 그것의 겹치는 부분을 통해 인식되고 공격되도록 한다.[1][2]
정상적인 면역반응 과정에서 병원균의 일부(예: 박테리아)는 면역체계에 의해 외래물질(비자체)으로 인식되어 잠재적인 손상을 줄이기 위해 제거되거나 효과적으로 중화된다.이와 같이 인지할 수 있는 물질을 항원이라고 한다.면역 체계는 항원에 다방면으로 반응할 수 있다; 이 반응의 주요 특징은 후렴 면역이라고 알려진 면역 체계의 팔을 포함하는 B 세포(또는 B 림프구)에 의한 항체의 생산이다.항체는 수용성이 있으며, 기능하기 위해 병원체와 B-세포 사이에 직접적인 세포 대 세포 접촉이 필요하지 않다.
항원은 크고 복잡한 물질일 수 있으며, 어떤 단일 항체라도 항원의 작고 특정한 영역에만 결합할 수 있다.결과적으로, 효과적인 면역 반응은 종종 같은 항원에 대해 많은 다른 B세포에 의한 많은 다른 항체의 생산을 포함한다.따라서 "폴리클론"이라는 용어는 다수를 의미하는 폴리라는 단어와 새싹이나 잔가지를 의미하는 그리스 클론에서 유래되었다.[3][4][5] 복제 세포는 공통의 "어머니" 세포에서 생겨난 세포들의 그룹이다.따라서 다면 반응에서 생성되는 항체를 다면 항체라고 한다.이질적인 다면체 항체는 단면체 항체 분자와 구별되는데, 단면체 항체 분자는 동일하며 단면체에만 반응하는 즉, 단면체 항체 분자보다 구체적이다.
다면반응은 면역체계의 장점, 특히 병원균에 대한 반응 확률이 더 높지만 숙주 내에서 생성된 고유분자에 대한 면역체계의 반응에 따른 특정 자가면역질환의 발생 가능성도 증가시킨다.
감염에 대한 유머 반응
한 유기체에서 다른 유기체로 전염될 수 있는 질병을 전염병이라고 하며, 관련된 원인 생물학적 작용제를 병원체라고 한다.병원체가 체내에 유입되는 과정을 접종이라고 하며,[note 1][6] 그것이 영향을 미치는 유기체를 생물학적 숙주라고 한다.병균이 식민지화라고 알려진 단계로 자리를 잡으면 감염을 일으켜 [7]숙주에게 직접 해를 입히거나 그로 인해 생성될 수 있는 독소라는 유해 물질을 통해 해를 입힐 수 있다.[7][7]이로 인해 폐렴이나 디프테리아와 같은 전염병의 다양한 증상과 징후가 나타난다.
다양한 전염병에 대항하는 것은 특히 취약한 유기체, 그리고 일반적으로 종의 생존에 매우 중요하다.이것은 병원체와 병원체의 독소를 제거하거나 그것들을 기능하지 못하게 함으로써 호스트들에 의해 달성된다.감염으로부터 신체를 보호하기 위한 다양한 세포, 조직, 장기의 수집은 면역 체계라고 알려져 있다.면역 체계는 특정의 백혈구의 침입 병원 균은 면역 체계의 팔이 세포성 면역, 혹은 사이트 그들은," 구하다"specifically[주 2]에 의해 병을 유발하는 세포와 독소 바인딩 생성된다에서 먼 곳으로 이사를 하게 되면 물질을 생산함으로써로 알려져 관련된 사건으로 직접적인 접촉을 통해 이 뿐이다. 흙과 함께그 과정에서 그것들을 중화시킨다. 면역 체계의 비도덕적 팔이라고 알려져 있다.그러한 물질은 수용성 항체로 알려져 있으며 감염에 대항하는 중요한 기능을 수행한다.[note 3][8]
- 백혈구 유형(WBC)
B세포반응

항체는 병원체로부터 숙주를 보호하는 다양한 기능을 한다.이러한 기능을 수행하는 그들의 수용성 형태는 백혈구의 한 종류인 혈장 B세포에 의해 생성된다.이 생산은 엄격하게 규제되고 있으며 순차적인 절차인 활성 T세포(다른 형태의 백혈구)에 의한 B세포의 활성화가 필요하다.관련된 주요 단계는 다음과 같다.[9]
- 병균이 B 세포나 대식세포에 의해 뒤엉킬 때 병원체의 특정 또는 비특정적 인식(항원 때문에).이것은 B세포의 일부만 활성화시킨다.
- 항원 처리.
- 항원 표시.
- 항원 표시 세포에 의한 T 도우미 세포의 활성화.
- 활성화 T 셀에 의한 B 셀의 공동 자극으로 완전 활성화.
- 수용성 항체의 결과적 생산으로 B세포의 증식[note 4].
병원균의 인식
병원균은 "인식 가능한" 항원 역할을 할 수 있는 단백질을 합성한다; 그들은 그들의 표면에 있는 분자들을 표현하거나 그것들을 주변으로 방출할 수 있다.이러한 물질들을 인지할 수 있게 하는 것은 항체라고 불리는 특정 숙주 단백질에 매우 구체적이고 다소 강하게 결합한다는 것이다.같은 항체가 면역체계의 세포 표면에 고정될 수 있는데, 이 경우 수용체 역할을 하거나, 수용성 항체로 알려진 혈액 속에 분비될 수 있다.분자 규모로 보면 단백질은 비교적 크기 때문에 전체적으로 인식할 수 없고 대신 에피토프라고 불리는 그들의 분절은 인식할 수 있다.[1]에피토프는 항체 분자의 매우 작은 지역(15-22개의 아미노산)과 접촉한다. 이 지역은 파라토프로 알려져 있다.[1]면역 체계에서 막 결합 항체는 B세포 수용체(BCR)이다.또한 T세포 수용체는 생화학적으로 항체로 분류되지 않지만, 특히 주요 조직적합성 복합체(MHC) 분자가 복합된 상피구에 결합한다는 점에서 유사한 기능을 한다.[note 5][10]파라토프와 그에 상응하는 항원 사이의 결합은 그 구조상 매우 구체적이며, 다른 유형의 리간드(최소한의 특이성과 강도를 가진 어떤 수용체와 결합하는 원자, 이온 또는 분자)의 결합과는 달리 다양한 비동결 결합에 의해 유도된다.바인딩의 특수성은 단단한 자물쇠와 주요 유형의 상호작용에서 발생하는 것이 아니라 파라토프와 비문 둘 다 서로의 존재에 약간의 순응적 변화를 겪도록 요구한다.[11]
B세포에 의한 상피의 구체적인 인식

왼쪽 그림에서 비문을 형성하는 다양한 부분들은 연속적으로 연속적으로 시준되는 것으로 나타났지만, 여기서 논의되고 있는 상황(즉, B세포에 의한 항원 인식)에 대해서는 이 설명이 너무 단순하다.그러한 상피들은 그 위에 있는 모든 아미노산이 같은 수열(선)에 있기 때문에 순차적 또는 선형적 상피라고 알려져 있다.이 인식 모드는 펩타이드의 크기가 작아야(약 6~8개의 아미노산) 가능하며,[1] T세포(T 림프구)에 의해 채용된다.
그러나 B 기억/생애 세포는 병원체 표면에 존재하는 온전한 단백질을 인식한다.[note 6]이런 상황에서 3차 구조의 단백질은 너무 크게 접혀 있어서 아미노산의 일부 루프가 단백질 내부에 놓여지게 되고, 그 옆을 이루는 부분들은 표면에 놓여지게 될지도 모른다.B세포 수용체에 있는 파라토프는 단백질 표면에 있는 아미노산들과만 접촉한다.표면 아미노산은 실제로 단백질의 1차 구조에서 불연속적일 수 있지만, 복잡한 단백질 접힘 패턴으로 인해 (접착된 그림에서와 같이) 병렬 처리된다.이러한 상피들은 정합성 상피로 알려져 있으며 선형 상피보다 더 긴 경향이 있다(15–22 아미노산 잔류물).[1]마찬가지로, 동일한 클론에 속하는 혈장 세포에 의해 생성된 항체는 병원체 단백질에 있는 동일한 일치성 상피에 결합될 것이다.[12][13][14][15]
해당 BCR 분자와 특정 항원의 결합은 MHC-II 분자의 생산을 증가시킨다.이것은 동일한 항원이 피노시토시스라고 불리는 비교적 비특이적인 과정에 의해 내실화될 때 동일한 항원이 B세포에 의해 작은 복실로서 "드렁크"되는 경우 동일한 현상이 발생하지 않는다는 점에서 의의를 가정한다.[16]따라서 그러한 항원은 비특정 항원으로 알려져 있으며 B세포의 활성화나 그에 대한 항체의 후속 생산으로 이어지지 않는다.
대식세포에 의한 비특정 인식
대식세포와 관련 세포는 병원체를 인식하는 다른 메커니즘을 사용한다.그들의 수용체들은 숙주세포에 존재할 가능성이 매우 낮은 침입 병원체에 존재하는 특정한 모티브를 인식한다.이와 같은 반복 모티브는 대식세포에 의해 표현되는 톨러이 수용체(TLR)와 같은 패턴인식 수용체(PRR)에 의해 인식된다.[1][17]같은 수용체가 널리 이질적인 미생물의 표면에 존재하는 주어진 모티브에 결합될 수 있기 때문에, 이러한 인식 방식은 상대적으로 비특이하며, 선천적인 면역 반응을 구성한다.
항원처리
항원을 인식한 후 대식세포나 B림프구와 같은 항원발현세포는 '파괴세포증'이라는 과정에 의해 완전히 그것을 잠식한다.삼켜진 입자는, 그것을 둘러싼 어떤 물질과 함께, 리소솜과 결합하는, 내포성 베실체(파고솜)를 형성한다.리소솜 안에서 항원은 단백질(더 큰 단백질을 분해하는 엔자임)에 의해 펩타이드라고 불리는 작은 조각으로 분해된다.개별 펩티든 다음 MHC클래스 II에 분자들은 리소 좀 –에 항원 항원 처리의 비정상적인 단백질 통신 또는의 시토졸의 내인성 pathway,[17][18][19]에 대조에 있거나 식균 작용의. 외인성 경로로 알려져 있"취급"의 이 메서드에 위치해(MHC클래스 II)시키고 있다.w 생산되MHC 등급 I 분자와 함께 세포(예: 바이러스 감염의 영향을 받거나 종양 세포에 있는 것)를 가지고 있다.
피브리노겐과 미오글로빈과 같은 특정 단백질이 변성되고 이황화 결합이 감소된 후 MHC-II 분자에 전체적으로 결합할 수 있는 내포성 처리의 대체 경로도 입증되었다.그런 다음 프로테아제는 단백질-MHC II 복합체의 노출된 부위를 저하시킨다.[19]
항원발현
처리된 항원(펩타이드)이 MHC 분자로 복합된 후, 둘 다 세포막으로 함께 이동하며, 거기서 백혈구의 일종인 CD 4+(T 도우미 세포)로 인식할 수 있는 콤플렉스로 전시(탈출)된다.[note 7][20]이것은 항원발현이라고 알려져 있다.단, B세포가 소화에 앞서 인지하는 상피(적합성 상피)는 T조력세포에 제시된 상피와 같지 않을 수 있다.또한, B 세포는 다른 MHC-II 분자에 복합된 다른 펩타이드들을 나타낼 수 있다.[16]
T 도우미 세포 자극
그들의 T세포 수용체-CD3 콤플렉스를 통한 CD 4+세포는 세포들을 제시하는 항원 표면의 비포프 결합 MHC II 분자를 인식하여 '활성화'된다.이러한 활성화에 따라 이 T세포들은 증식하여 T2세포로h 분화한다.[16][21]이것은 그들이 그들 자신의 생존을 촉진하는 가용성 화학 신호를 생산하게 한다.그러나 이들이 수행하는 또 다른 중요한 기능은 그들과 직접 신체 접촉을 함으로써 B세포의 자극을 주는 것이다.[10]
활성화된 T 도우미 셀에 의한 B 셀의 공동 자극
T 도우미 세포의 완전한 자극을 위해서는 항원에 존재하는 B7 분자가 T세포 표면에 존재하는 CD28 분자와 결합해야 한다(T세포 수용체와 근접).[10]마찬가지로 T세포 표면에 존재하는 CD40 리간드 또는 CD154(CD40L)와 B세포 표면에 존재하는 CD40 사이의 두 번째 상호작용도 필요하다.[21]T 도우미 셀을 자극하는 동일한 상호작용은 또한 B 셀을 자극하므로 비용 시뮬레이션이라는 용어가 사용된다.전체 메커니즘은 활성화된 T세포가 "비용추적" T조력세포의 T세포 수용체가 인식하는 것과 동일한 상피를 포함하는 항원을 인식하는 B세포만을 자극하도록 보장한다.B세포는 직접적인 비용측정을 떠나서 파라시린 방식으로 특정 성장인자, viz, 인터루킨 2, 4, 5, 6에 의해 자극을 받는다.이러한 요인은 대개 새로 활성화된 T 도우미 셀에 의해 생성된다.[22]그러나 이러한 활성화는 기억력에 존재하는 B세포 수용체나 순진한 B세포 그 자체가 상응하는 상피와 결합한 후에만 일어나는데, 그 없이는 Pagocytosis와 항원 처리의 시작 단계가 일어나지 않았을 것이다.
B세포의 증식과 분화
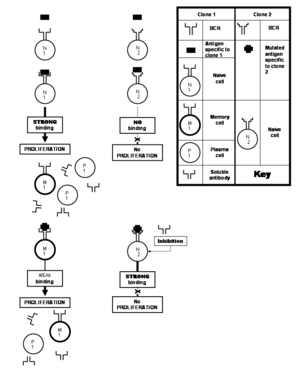
순진한(또는 경험이 없는) B 세포는 복제 세포에 속하는 세포로, 복제 세포가 특정한 비문을 접해 본 적이 없다.이와는 대조적으로 기억 B세포는 활성된 순진함 또는 기억 B세포에서 유래된 세포다.순진하거나 기억 B 세포의 활성화는 특정 B 세포의 다양성 증식에 뒤따른다. 그 발생의 대부분은 혈장 B 세포로 불규칙적으로 분화하며 나머지는 기억 B 세포로 살아남는다.[note 8]그래서 특정 클론에 속하는 순진한 세포들이 혈장세포를 발생시키기 위해 자신의 특정한 항원과 마주치게 되고, 기억세포도 몇 개 남았을 때 이것을 일차 면역반응이라고 한다.이 클론의 증식 과정에서 B세포 수용체 유전자는 항체의 파라토프에 대한 유전자 코딩에서 빈번하게 (2개의 세포분열마다 1개씩)[8] 돌연변이를 겪을 수 있다.이러한 빈번한 돌연변이를 체성 과음이라고 부른다.각각의 그러한 돌연변이는 파라토프의 상피결합 능력을 약간 변화시켜 그 과정에서 B세포의 새로운 복제본을 만들어낸다.새로 생성된 파라토프 중 일부는 (이 파라토프를 보유한 클론의 선택으로 이어짐) 같은 비피형에 더 강하게 결합되는데, 이를 친화성 성숙이라고 한다.[note 9][8][21]다른 파라토프는 증식을 자극했던 원래 에피토프와는 약간 다른 에피토프에 더 잘 결합한다.상피 구조의 변화도 항원에 대한 병원체 코딩 유전자의 돌연변이에 의해 주로 발생한다.따라서 체질의 고주화 작용은 애초에 증식을 유발한 항원에 대한 더 큰 특수성을 부여하는 것 외에도, 이후에 항원과 마주칠 때 B 세포 수용체와 수용성 항체를 항원 인식 잠재력에 더 포함시켜 항원을 더 많이 만든다.기억세포가 항원으로부터 자극을 받아 혈장세포를 생성(복제의 1차 반응에서와 마찬가지로)하고, 그 과정에서 훨씬 더 많은 기억세포를 남길 때, 이는 2차 면역반응으로 알려져 있는데,[21] 이는 혈장세포의 수가 더 많고 항체생산이 더 빠른 속도로 장기간 지속되는 것으로 해석된다.2차 반응의 일부로 생성된 기억 B 세포는 해당 항원을 더 빨리 인식하고 친화력 성숙으로 인해 그것과 더 강하게 결합한다(즉, 결합의 친화력이 더 크다).클론에서 생성되는 수용성 항체는 항원 결합의 유사한 향상을 보인다.[21]
다면성 기준
각 복제본이 주어진 상피에 대항하는 항체를 생산하는데 어느 정도 전문적이기 때문에, 그리고 각 항원은 여러 개의 상피들을 포함하고 있기 때문에 반응은 자연적으로 다면체다면체다면체인데, 그 각 항원은 B세포의 둘 이상의 복제에 의해 인식될 수 있기 때문이다.무수한 항원, 그리고 복수의 구성적 별자리에도 반응할 수 있으려면 면역체계는 모두 아주 많은 수의 별자리들을 인식할 수 있는 능력을 필요로 한다. 즉, B세포 복제의 다양성이 매우 높아야 한다.
B세포의 정합성
기억력과 순진한 B세포는 일반적으로 비교적 적은 숫자로 존재한다.인체는 다량의 잠재적 병원균에 대응할 수 있어야 하기 때문에 다양한 특이성을 가진 B세포의 풀을 유지한다.[17]결과적으로 (면역체계가 반응할 수 있는 모든 것 중에서) 어떤 주어진 비피형에 반응할 수 있는 B(영양 또는 기억력) 세포가 거의 항상 하나 이상 존재하지만, 정확한 중복은 거의 없다.그러나, 하나의 B세포가 결합할 수 있는 항원과 마주쳤을 때, 그것은 매우 빠르게 증식할 수 있다.[21]이와 같은 특이성을 가진 세포군은 복제 세포로 알려져 있으며, 공통의 "어머니" 세포에서 유래한다.모든 '딸' B세포는 상피 특이성 속에서 원래 '엄마' 세포와 일치하며, 동일한 파라토프로 항체를 분비한다.이 항체들은 동일한 모세포의 클론으로부터 파생되기 때문에 단핵항체들이다.다면반응은 여러 B세포의 클론이 동일한 항원에 반응하는 반응이다.
단일 항원에는 여러 개의 겹치는 상피들이 포함되어 있다.
하나의 항원은 여러 개의 겹치는 상피들의 배열로 생각할 수 있다.많은 독특한 B세포 복제 세포들은 개별적인 상피에 결합할 수 있을 것이다.이것은 전체 반응에 훨씬 더 큰 다중성을 부여한다.[3]이 모든 B세포가 활성화되어 혈장세포 복제의 큰 군집을 만들 수 있는데, 각각의 군집은 초당 각 비피형에 대해 최대 1000개의 항체 분자를 분비할 수 있다.[21]
여러 클론에서 단일 비피를 인식
다른 B세포가 같은 항원에 다른 상피에 반응하는 것 외에 다른 복제에 속하는 B세포도 같은 상피에 반응할 수 있을 것이다.여러 가지 다른 B세포가 공격할 수 있는 비약은 면역력이 매우 높다고 한다.이 경우 각각의 상피-파라토프 쌍에 대한 결합 친화력은 다양하며, 일부 B 세포 클론은 상피에 강하게 결합하는 항체를 생성하며, 다른 세포는 약하게 결합되는 항체를 생성한다.[1]
클론 선택
더 강한 힘으로 특정 상피에 묶인 클론은 림프절과 같은 다양한 림프조직에서 모낭의 생식선 중심에서 더 많은 증식을 위해 선택될 가능성이 더 높다.이것은 자연 선택과 다르지 않다: 복제본을 선택한 것은 마주친 병원체의 비피피(결합 강도)를 공격하기 위한 적합성 때문이다.[23]이 유추를 더욱 강하게 만드는 것은 B림프구가 생식선 중심에서 생존을 촉진하는 신호를 위해 서로 경쟁해야 한다는 점이다.
B세포 복제의 다양성
비록 많은 다양한 병원균들이 존재하지만, 이 병원균들 중 많은 것들이 끊임없이 변이되고 있지만, 대다수의 개인들이 감염으로부터 자유롭다는 것은 놀라운 일이다.그러므로 건강의 유지에는 신체가 존재할 가능성이 있는 모든 병원균(그들이 나타내거나 생산하는 항균제)을 인식해야 한다.이는 B세포의 엄청나게 큰(약 10개9) 복제의 풀을 유지함으로써 달성되는데, 각각의 복제 세포는 특정 상피에 대한 항체를 인식하고 생성함으로써 특정 상피에 반응한다.그러나, 어느 주어진 시간에, 실제로 그들의 특정한 비형에 수용적인 극소수의 복제자들만이 남아있다.따라서, 약 10개의7 다른 상이한 상피들은 결합된 모든 B 세포 복제에 의해 인식될 수 있다.[21]더구나 평생 동안 개인은 보통 신체가 인식하고 대응할 수 있는 숫자에 비해 극히 적은 수의 항원에 대한 항체의 생성을 요구한다.[21]
현상의 중요성
항원 인식 확률 증가
항원이 그 구조에서 둘 이상의 성분으로 인식될 수 있다면, 면역체계에 의해 "실종"될 가능성이 적다.[note 10]병원성 유기체의 돌연변이는 항원 구조, 즉 상피 구조를 변형시킬 수 있다.만약 면역체계가 다른 상피들이 어떻게 생겼는지 '기억'한다면 항원과 유기체는 여전히 인식되어 신체의 면역반응을 받게 될 것이다.따라서 다면 반응은 인식할 수 있는 병원균의 범위를 넓힌다.[24]
빠르게 변이되는 바이러스에 대한 면역 시스템의 제한
많은 바이러스들이 그들의 중요한 단백질의 아미노산 구성의 변화를 초래하는 빈번한 돌연변이를 겪는다.단백질에 위치한 에피토프도 그 과정에서 변화를 겪을 수 있다.이렇게 변형된 상피는 면역체계를 자극했을 수정되지 않은 상피에 특유한 항체와 덜 강하게 결합된다.이것은 유감스러운 일이다. 왜냐하면 체질의 과음술은 용해성 항체를 생산할 수 있는 복제본을 낳기 때문이다. 이는 변형된 상피를 충분히 중화시킬 수 있을 정도로 결속시킬 수 있었을 것이다.그러나 이 복제들은 이전에 자극을 받은 복제에 의해 생성된 약한 결합 항체에 의해 증식되지 않는 순진한 세포들로 구성될 것이다.이 교리는 원래 항원적 죄악으로 알려져 있다.[21]이러한 현상은 특히 인플루엔자, 뎅기, HIV 바이러스에 대한 면역 반응에 영향을 미친다.[25]그러나 이러한 한계는 다면반응 현상에 의해 부과되는 것이 아니라, 경험 많은 기억세포에 유리하게 편향된 면역반응에 의해 '노비' 순진한 세포에 대해 부과되는 것이다.
자가면역 반응 가능성 증가
자가면역에서는 면역체계가 체내의 특정 고유분자를 이물(자체항생성)으로 잘못 인식하여 면역반응을 일으킨다.이러한 고유 분자들은, 신체의 정상적인 부분으로서, 자연적으로 항상 체내에 존재할 것이기 때문에, (이차 면역 반응과 유사하게) 시간이 흐를수록 그에 대한 공격은 더 강해질 수 있다.게다가, 많은 유기체들이 분자 흉내를 내는데, 이것은 항원적으로 숙주 단백질과 유사한 항원을 표면에 보여주는 것을 포함한다.이것은 두 가지 가능한 결과를 가지고 있다: 첫째, 유기체는 자기 항원으로서 면하게 될 것이다. 둘째, 그것에 대항하여 생성된 항체들 또한 모방된 토종 단백질과 결합하게 될 것이다.항체는 자기 항체를 공격하고 세포에 의존하는 세포독성 및 보완 활성화와 같은 다양한 메커니즘을 활성화하여 항체를 보호하는 조직들을 공격할 것이다.따라서 항체 특이성의 범위가 넓어지면 한쪽이 자기 항체에 대해 반응할 가능성이 커진다(신체의 고유 분자).[26][27]
단클론 항체 생성의 어려움
단클론 항체는 구조적으로 동일한 상피 특이성을 가진 면역글로불린 분자(모두 동일한 친화력으로 동일한 상피와 결합됨)로, 동일한 상피에 대해 다양한 친화력을 갖는 다면체 상피에 대해 서로 결합한다.그것들은 대개 자연적인 면역 반응에서 만들어지는 것이 아니라, 다발성 골수종과 같이 병든 상태에서만, 또는 전문화된 실험실 기법을 통해서 만들어진다.그 특수성 때문에 특정 용도에 단핵항체가 사용되어 물질의 존재(단핵항체의 항원 역할을 하는 것)를 정량화하거나 검출하고, 개별 세포(예: 암세포)를 대상으로 한다.단핵항체는 다양한 진단양식(서양의 블롯과 면역불루오렌스 참조)과 치료법(특히 암과 자가면역성분이 있는 질병)에서 사용된다.그러나, 사실상 자연에서 모든 반응은 다면체이기 때문에, 그것은 엄청나게 유용한 단면체 항체의 생산을 덜 단순하게 만든다.[8]
역사
감염에 대항할 수 있는 혈액에 중화 물질이 존재한다는 최초의 증거는 1890년 키타사토 시바사부로와 함께 에밀 폰 베링(Emil von Behring)이 디프테리아에 대항하는 효과적인 혈청을 개발했을 때 나왔다.그들은 디프테리아 예방접종을 받은 동물들로부터 생산된 혈청을 그것으로 고통받는 동물들에게 전달함으로써 그렇게 했다.이렇게 혈청을 옮기는 것은 감염된 동물들을 치료할 수 있다.베링은 1901년에 이 작품으로 노벨상을 받았다.[28]
이 시기에는 혈액에서 정확히 어떤 것이 이 보호를 부여했는지는 알려지지 않았다.그 후 몇 십 년 안에, 보호 혈청이 독소를 중화시키고 침전시킬 수 있고, 박테리아를 뭉개버릴 수 있다는 것이 밝혀졌다.이 모든 기능은 혈청 내의 다른 물질에 기인했으며, 그에 따라 항독소, 침전물, 아글루틴으로 명명되었다.[17]세 가지 물질이 모두 하나의 실체(감마 글로불린)라는 사실은 1939년 엘빈 A. 카바트에 의해 증명되었다.그 전 해에 카바트는 말들의 세라에 대한 초밀접적 연구로 항체의 이질성을 입증했다.[29]
이때까지만 해도 세포 매개 면역과 부덕 면역은 효과적인 면역 반응을 설명하기 위해 이론을 다투는 것으로 여겨졌으나, 전자는 앞선 기술이 없어 뒤처졌다.[17]세포 매개 면역은 1942년 메릴 체이스가 백혈구를 이식해 돼지 간 결핵에 대한 면역력을 성공적으로 이전하면서 인식과 연구에 박차를 가했다.[17][30]
이후 1948년 아스트리드 파그레이우스가 박사학위 논문에서 혈장 B세포가 항체 생산에 구체적으로 관여하고 있다는 사실을 밝혀냈다.[31]세포 매개 반응과 유머 반응을 중재하는 림프구의 역할은 1959년 제임스 고완스에 의해 증명되었다.[30]
1900년 폴 에를리치는 면역체계가 인식할 수 있는 광범위한 항원을 설명하기 위해 기존의 "사슬 수용체"가 주어진 병원체를 결합하고, 이러한 상호작용은 수용체를 나타내는 세포가 증식하도록 유도하여 동일한 수용체 복사본을 더 많이 생성하게 한다는 가설을 세웠다.선택적 이론이라고 불리는 이 이론은 향후 50년 동안 증명되지 않았고 항체가 항원 주위를 접음으로써 그것의 효과적인 구조를 가정한다는 개념에 근거한 몇 가지 교육적 이론에 의해 도전을 받아왔다.[17]그러나 1950년대 후반 제른, 탈마게, 버넷 등 세 과학자의 저작은 (이론을 크게 수정한) 클론 선택 이론에 도달하게 되는데, 이는 그 작용제를 중화시킬 수 있는 특정 수용체는 수용성이 있고 막에 묶여 있지 않다는 것을 제외하고는 에를리히 가설의 모든 요소들을 증명했다.[17][30]
구스타프 노살 경은 각각의 B세포가 항상 하나의 항체만을 생산한다는 것을 보여주었을 때, clonal selection 이론이 옳다는 것이 증명되었다.[32]
1974년, 항원 표시에서 MHC의 역할은 롤프 진크나겔과 피터 C에 의해 증명되었다. 도허티[30]
참고 항목
메모들
- ^ "침입"이라는 용어는 일반적으로 능동 면역의 맥락에서, 즉 항원 물질을 숙주의 몸에 의도적으로 도입하는 경우에 사용된다.그러나 전염병에 대한 많은 논의에서, 장티푸스의 원인 유기체인 살모넬라 발진티푸스에 오염된 물을 섭취하는 것이 인체에 도입되는 결과를 초래하는 자발적(즉, 인간의 개입이 없는) 사건을 암시하기 위해 이 용어를 사용하는 것은 드문 일이 아니다.이 경우 원인 유기체 자체를 접종이라고 하며, "접종량"으로 소개되는 유기체의 수는 "접종량"으로 알려져 있다.
- ^ 특수성은 두 개의 서로 다른 병원균을 실제로 두 개의 뚜렷한 실체로 보고 서로 다른 항체 분자에 의해 반박될 것임을 암시한다.
- ^ 항체의 작용:
- 병원체를 코팅하여 숙주세포에 달라붙는 것을 방지하여 식민지화를 방지함
- 용해성 항원을 침전시키고(입자에 부착하여 "싱크"하게 함) 다양한 조직과 혈액으로부터 면역체계의 다른 세포에 의한 간극을 촉진한다.
- 병원체를 집어삼킬 수 있는 세포를 끌어들이기 위해 미생물을 코팅하는 것.이것은 opsonization이라고 알려져 있다.따라서 항체는 오포닌의 역할을 한다.삼키는 과정을 갑상샘증(문학적으론 세포식식)이라고 한다.
- 가장 중요한 것은 병원체의 외피(세포막)에 구멍을 뚫어 그 과정에서 죽이는 보완 시스템을 활성화한다.
- 항체 의존 세포 매개 세포독성(ADCC)으로 알려진 프로세스에서 바이러스에 감염된 호스트 세포의 파괴 표시
- ^ 이러한 맥락에서 확산은 세포 분열과 분화에 의한 곱셈을 의미한다.
- ^ 주요 조직적합성 복합체는 주요 조직적합성 등급 I 분자, 주요 조직적합성 등급 II 분자 및 보완 시스템(MHC 등급 III)의 기능에 관련된 기타 단백질의 합성을 위해 암호화하는 DNA의 유전자 영역이다.처음 두 제품은 항원 표시에 중요하다.MHC 호환성은 장기 이식에 있어 주요한 고려사항이며, 인간에게는 인간 백혈구 항원(HLA)으로도 알려져 있다.
- ^ 여기서 온전한 것은 소화되지 않은 단백질이 인식된다는 것을 의미하며, B 세포 수용체에 있는 파라토프가 전체 단백질 구조와 동시에 접촉하는 것은 아니다; 파라토프는 여전히 표면에 노출된 항원의 제한된 부분에만 접촉할 것이다.
- ^ 백혈구에는 많은 종류가 있다.그것들을 분류하는 일반적인 방법은 화학 염료에 의해 얼룩진 후 광현미경 아래에서의 모양에 따른 것이다.그러나 기술이 발전하면서 새로운 분류 방법이 등장했다.그 방법들 중 하나는 각 세포 유형에 특별히 결합할 수 있는 단핵 항체를 사용한다.게다가, 같은 종류의 백혈구는 다양한 발달 단계에서 세포막에 전형적인 분자를 표현할 것이다.특정 표면 분자와 특별히 결합할 수 있는 단핵 항체는 하나의 분화 군집(CD)으로 간주될 것이다.림프구의 알려진 표면 분자와 반응하지 않고, 오히려 아직 인식되지 않은 표면 분자에 반응하는 단핵 항체 또는 단핵 항체 그룹은 새로운 분화 군집으로 곤봉되고 그에 따라 번호가 매겨질 것이다.각 분화 군집은 "CD"로 약칭되며, 그 뒤에 숫자(일반적으로 발견 순서를 나타냄)가 붙는다.따라서, 분화 4의 군집에 특별히 결합하는 표면 분자(리간드라고 불림)를 가진 세포는 CD4+ 셀이라고 불릴 것이다.마찬가지로, CD8+ 셀은 CD8 리간드를 소유하고 CD8 단클론 항체에 결합되는 셀이다.
- ^ 혈장세포는 애초에 B세포 수용체에 결합하여 B세포를 자극했던 것과 같은 구조물에 결합하는 항체를 분비한다.
- ^ 친화력은 대략 라틴어에서 온 매력으로 해석된다.참고 항목:온라인 어원 사전의 친화성 정의 및 Farlex에 의한 FreeDictionary의 친화성 정의
- ^ 유사하게 사람이 붐비는 곳에서 사람을 알아보도록 되어 있다면 가능한 한 많은 신체적 특징을 아는 것이 좋다.헤어스타일로만 사람을 안다면 그 사람이 바뀌면 눈감아 줄 가능성이 있다.반면 헤어스타일과 별개로, 만약 여러분이 얼굴의 특징과 특정한 날에 어떤 옷을 입을지 알게 된다면, 여러분이 그 사람을 그리워할 가능성은 훨씬 더 낮아진다.
참조
- ^ a b c d e f g h i Goldsby, Richard; Kindt, TJ; Osborne, BA; Janis Kuby (2003). "Antigens (Chapter 3)". Immunology (Fifth ed.). New York: W. H. Freeman and Company. pp. 57–75. ISBN 978-0716749479.
- ^ "Definition of Polyclonal from MedicineNet.com". Webster's New World Medical Dictionary. Retrieved 2008-05-03.
- ^ a b Frank, Steven A. (2002). "Specificity and Cross-Reactivity (Chapter 4)". Immunology and Evolution of Infectious Disease. Princeton University. pp. 33–56. ISBN 978-0691095950. Retrieved 2008-06-23.
- ^ "Etymology of "clone"". Online etymology dictionary. Retrieved 2008-06-26.
- ^ Bansal, R.K. (2005). "Reproductive Cloning-An Act Of Human Rights Violation". Journal of Indian Association of Forensic Medicine. 27 (3): 971–973. Retrieved 2008-06-23.
- ^ "Definition of inoculation". TheFreeDictionary.com (citing Dorland's Medical Dictionary for Health Consumers. © 2007 by Saunders, an imprint of Elsevier, Inc.). Retrieved 2008-06-10.
- ^ a b c Pier, Gerald B. (2005) [1945]. "Molecular mechanisms of microbial pathogenesis (Chapter 105)". In Kasper; Braunwald; Fauci; Hauser; Longo; Jameson (eds.). Harrison's Principles of Internal Medicine. Vol. 1 (Sixteenth ed.). McGraw-Hill. p. 700. ISBN 978-0-07-123983-7.
- ^ a b c d e Goldsby (2007). "Organization and Expression of Immunoglobulin Genes (Chapter 5)". Immunology (Fifth ed.). New York. pp. 105–136. ISBN 978-0-7167-6764-0.
- ^ Nairn, Roderick (2004) [1954]. "Immunology (Chapter 8)". In Geo F. Brooks; Janet S. Butel; Stephen A. Morse (eds.). Jawetz, Melnick, & Adelberg's Medical Microbiology (Twenty-Third Edition International ed.). Lange publications/McGraw-Hill. pp. 133–135, 138–139. ISBN 978-0-07-123983-7.
- ^ a b c Goldsby (2007). "T-Cell Maturation, Activation and Differentiation (Chapter 10)". Immunology (Fifth ed.). pp. 221–246. ISBN 978-0-7167-6764-0.
- ^ Nair, Deepak; Singh Kavita; Siddiqui Zaved; Nayak Bishnu; Rao Kanury; Salunke Dinakar (2002-01-09). "Epitope Recognition by Diverse Antibodies Suggests Conformational Convergence in an Antibody Response" (PDF). The Journal of Immunology. 168 (5): 2371–2382. doi:10.4049/jimmunol.168.5.2371. PMID 11859128. S2CID 14974530. Retrieved 2008-05-03.
- ^ "Immunochemical Applications". Technical Tips. EMD biosciences. Archived from the original on 2008-04-11. Retrieved 2008-05-07.
- ^ Davis, Cheryl. "Antigens". Biology course. Western Kentucky University. Archived from the original on 2008-03-29. Retrieved 2008-05-12.
- ^ Ceri, Howard. "Antigens". Immunology course. University of Calgary. Archived from the original on 2008-10-05. Retrieved 2008-05-12.
- ^ Khudyakov, Yury; Howard A. Fields (2002). Artificial DNA: Methods and Applications. Florida: CRC Press. p. 227. ISBN 978-0-8493-1426-1.
- ^ a b c Myers, CD (1991). "Role of B cell antigen processing and presentation in the humoral immune response" (PDF). The FASEB Journal. 5 (11): 2547–2553. doi:10.1096/fasebj.5.11.1907935. PMID 1907935. S2CID 13324439. Retrieved 2008-06-20.
- ^ a b c d e f g h Goldsby (2007). "Overview of the Immune System (Chapter 1)". Immunology (Fifth ed.). pp. 1–23. ISBN 978-0-7167-6764-0.
- ^ Goldsby (2007). "Antigen Processing and Presentation (Chapter 8)". Immunology (Fifth ed.). pp. 188–194. ISBN 978-0-7167-6764-0.
- ^ a b Ojcius, DM; L Gapin; JM Kanellopoulos; P Kourilsky (September 1994). "Is antigen processing guided by major histocompatibility complex molecules?" (PDF). The FASEB Journal. 8 (5): 974–978. doi:10.1096/fasebj.8.12.8088463. PMID 8088463. S2CID 36890268. Retrieved 2008-06-20.
- ^ Goldsby (2007). "Cells and Organs of the Immune System (Chapter 2)". Immunology (Fifth ed.). pp. 24–56. ISBN 978-0-7167-6764-0.
- ^ a b c d e f g h i j k Goldsby (2007). "B-Cell Generation, Activation and Differentiation (Chapter 11)". Immunology (Fifth ed.). New York. pp. 247–275. ISBN 978-0-7167-6764-0.
- ^ McPhee, Stephen; Ganong, William (2006). Pathophysiology of Disease: An Introduction to Clinical Medicine. Lange Medical Books/McGraw-Hill. p. 39. ISBN 978-0-07-144159-9.
- ^ Cziko, Gary (1995). "The Immune System: Selection by the Enemy". Without Miracles: Universal Selection Theory and the Second Darwinian Revolution (Fifth ed.). Massachusetts: MIT Press. pp. 39–48. ISBN 978-0-262-03232-2. Retrieved 2008-05-12.
- ^ Greener, Mark (2005-02-14). "Monoclonal antibodies (MAbs) turn 30". The Scientist. 19 (3): 14. Archived from the original on 2007-08-31. Retrieved 2008-06-06.
- ^ Deem, Michael. "Michael W. Deem". Official Web Page. Rice University. Retrieved 2008-05-08.
- ^ Granholm, Norman; Tito Cavallo (1992). "Autoimmunity, Polyclonal B-Cell Activation and Infection (abstract)". Lupus. 1 (2): 63–74. doi:10.1177/096120339200100203. PMID 1301966. S2CID 27649995.
- ^ Montes CL, Acosta-Rodríguez EV, Merino MC, Bermejo DA, Gruppi A (2007). "Polyclonal B cell activation in infections: infectious agents' devilry or defense mechanism of the host? (abstract)". Journal of Leukocyte Biology. 82 (5): 1027–1032. doi:10.1189/jlb.0407214. PMID 17615380. S2CID 8054401.
- ^ "Emil von Behring: The Founder of Serum Therapy". Nobel Prize in Medicine. Archived from the original on 2008-06-12. Retrieved 2008-06-23.
- ^ Mage, Rose G.; Ten Feizi. "Elvin A. Kabat". Biographical memoirs. Retrieved 2008-06-23.
- ^ a b c d Greenberg, Steven. "A Concise History of Immunology" (PDF). Retrieved 2008-06-23.
- ^ "MTC News" (PDF). Karolinska Institutet. Retrieved 2008-06-23.
- ^ Turner, Stephen (October 2007). "One POWERFUL Idea" (PDF). Australasian Science. Archived from the original (PDF) on 2008-07-21. Retrieved 2008-06-23.
추가 읽기
- Goldsby, Richard; Kindt, TJ; Osborne, BA; Janis Kuby (2003). Immunology (Fifth ed.). New York: W. H. Freeman and Company. ISBN 978-0-7167-4947-9.
- Kishiyama, Jeffery L. (2006) [1997]. "Disorders of the Immune system (Chapter 3)". In Stephen J. McPhee; William F. Ganong (eds.). Pathophysiology of Disease: An Introduction to Clinical Medicine (5 ed.). Lange Medical Books/McGraw-Hill. pp. 32–58. ISBN 978-0-07-110523-1.
- Nairn, Roderick (2004) [1954]. "Immunology (Chapter 8)". In Geo F. Brooks; Janet S. Butel; Stephen A. Morse (eds.). Jawetz, Melnick, & Adelberg's Medical Microbiology (Twenty-Third Edition International ed.). Lange publications/McGraw-Hill. pp. 133–135, 138–139. ISBN 978-0-07-123983-7.