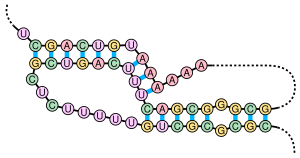
핵산 2차 구조
Nucleic acid secondary structure핵산 2차 구조는 단일 핵산 폴리머 내 또는 두 개의 폴리머 간의 염기쌍화 상호작용이다.이것은 핵산 [1]분자에서 쌍을 이루는 염기들의 목록으로 나타낼 수 있다.생물학적 DNA와 RNA의 2차 구조는 다른 경향이 있다: 생물학적 DNA는 대부분 완전히 염기쌍의 이중 나선형으로 존재하는 반면, 생물학적 RNA는 단일 가닥이고 종종 리보스의 추가적인 수산화기에서 비롯된 수소 결합을 형성하는 그것의 증가된 능력 때문에 복잡하고 복잡한 염기쌍의 상호작용을 형성한다.설탕.
비생물학적 맥락에서 2차 구조는 DNA 나노테크놀로지 및 DNA 컴퓨팅을 위한 핵산 구조의 핵산 설계에서 중요한 고려사항이며, 이는 염기쌍의 패턴이 궁극적으로 분자의 전체 구조를 결정하기 때문이다.
기본 개념
베이스 페어링
분자 생물학에서 수소 결합을 통해 연결된 상보적인 DNA 또는 RNA 가닥에 있는 두 개의 뉴클레오티드는 염기쌍이라고 불립니다.표준 왓슨-크릭 염기쌍에서 아데닌(A)은 티민(T)과 염기쌍을 형성하고 구아닌(G)은 DNA에서 시토신(C)과 염기쌍을 형성한다.RNA에서 티민은 우라실(U)로 대체된다.워블 염기쌍과 후그스틴 염기쌍과 같은 대체 수소 결합 패턴도 발생하며, 특히 RNA에서 복잡하고 기능적인 3차 구조를 발생시킨다.중요한 것은, 페어링은 전달 RNA 분자의 코돈이 단백질 번역 중에 전달 RNA의 안티코돈에 의해 인식되는 메커니즘이다.일부 DNA 또는 RNA 결합 효소는 유전자의 특정 조절 영역을 식별하는 특정 염기쌍 패턴을 인식할 수 있습니다.수소 결합은 위에서 설명한 염기쌍 구성 규칙의 기초가 되는 화학적 메커니즘입니다.수소 결합 공여체와 수용체의 적절한 기하학적 대응은 "오른쪽" 쌍만 안정적으로 형성할 수 있게 한다.GC 함량이 높은 DNA는 GC 함량이 낮은 DNA보다 안정성이 높지만, 일반적인 생각과는 달리 수소 결합은 DNA를 크게 안정시키지 못하고 안정화는 주로 적층 [2]상호작용에 의한 것이다.
더 큰 핵염기인 아데닌과 구아닌은 퓨린이라고 불리는 이중 고리 화학 구조의 구성원이고, 더 작은 핵염기인 시토신과 티민은 피리미딘이라고 불리는 단일 고리 화학 구조의 구성원입니다.퓨린은 피리미딘과 상보적이다: 피리미딘-피리미딘 쌍은 수소 결합을 확립하기에 너무 멀리 떨어져 있기 때문에 에너지적으로 바람직하지 않다; 푸린-푸린 쌍은 분자들이 너무 가깝기 때문에 에너지적으로 불리하며, 중복 거부감을 초래한다.가능한 다른 쌍은 GT와 AC뿐입니다. 수소 공여체와 수용체의 패턴이 일치하지 않기 때문에 이러한 쌍은 일치하지 않습니다.두 개의 수소 결합을 가진 GU 워블 염기쌍은 RNA에서 꽤 자주 발생합니다.
핵산 교배
교배는 상보적인 염기쌍이 결합하여 이중나선을 형성하는 과정이다.용융은 이중 나선의 가닥들 사이의 상호작용이 끊어져 두 개의 핵산 가닥이 분리되는 과정입니다.이러한 결합은 약하며 약한 가열, 효소 또는 물리적 힘에 의해 쉽게 분리된다.용융은 핵산의 [3]특정 지점에서 우선적으로 발생합니다.T 및 A의 리치 시퀀스는 C 및 G의 리치 영역보다 용융이 용이합니다.특정 염기 단계, 특히 T A 및 T G 염기 [4]단계도 DNA 용융에 취약합니다.이러한 기계적 특성은 전사를 위해 RNA 중합효소가 DNA를 녹이는 것을 돕기 위해 많은 유전자의 시작에서 TATAA와 같은 배열의 사용에 의해 반영됩니다.
분자가 약 10,000개의 염기쌍(10kbase 쌍 또는 10kbp) 미만을 가질 경우 완만한 가열에 의한 가닥 분리는 간단하다.DNA 가닥의 얽힘은 긴 부분을 분리하는 것을 어렵게 만든다.세포는 DNA를 녹이는 효소(헬리시스)가 토포이소머라아제(topoisomerase)와 동시에 작용하도록 함으로써 이 문제를 피할 수 있으며, 토포이소머라아제(topoisomerase)는 화학적으로 한 가닥의 인산염 골격을 절단하여 다른 가닥을 회전시킬 수 있다.헬리케이스는 DNA 중합효소 같은 염기서열 판독 효소의 발전을 촉진하기 위해 가닥을 푼다.
이차 구조 모티브

핵산 2차 구조는 일반적으로 나선형(연속 염기쌍)과 다양한 종류의 루프형(나선형으로 둘러싸인 짝을 이루지 않은 뉴클레오티드)으로 나뉜다.이들 요소 또는 이들 요소의 조합은 테트라루프, 의사 노트, 스템 루프 등의 추가 카테고리로 분류되는 경우가 많습니다.
이중나선
이중 나선은 분자의 2차 구조와 밀접하게 연결된 핵산 분자의 중요한 3차 구조이다.이중나선은 다수의 연속 염기쌍의 영역에 의해 형성된다.
핵산 이중 나선은 나선형 중합체로, 보통 오른손잡이이며, 염기쌍으로 구성된 두 개의 뉴클레오티드 가닥을 포함합니다.나선의 1회 회전은 약 10개의 뉴클레오티드를 구성하며, 큰 홈과 작은 홈을 포함하며, 큰 홈은 [5]작은 홈보다 넓다.큰 홈과 작은 홈의 폭의 차이로 볼 때, DNA에 결합하는 많은 단백질은 더 넓은 [6]큰 홈을 통해 그렇게 한다.DNA의 경우 생물학적으로 관련된 세 가지 형태가 A-DNA, B-DNA, Z-DNA인 반면, RNA 이중 나선형은 DNA의 A 형태와 유사한 구조를 가지고 있다.
스템 루프 구조
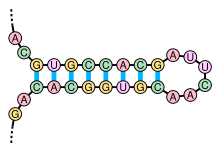
핵산 분자의 2차 구조는 종종 줄기와 고리로 독특하게 분해될 수 있다.염기쌍의 나선이 짧은 비쌍의 루프로 끝나는 스템루프 구조(흔히 "헤어핀"이라고도 함)는 매우 일반적이며 이동 RNA에서 발견되는 것과 같은 4나선 접합인 클로버 리프 구조와 같은 더 큰 구조적 모티브를 위한 구성 요소이다.내부 루프(더 긴 쌍으로 구성된 나선의 짧은 일련의 미쌍 염기) 및 팽출(나선의 한 가닥이 반대쪽 가닥에 대응물이 없는 "추가" 삽입 염기를 가진 영역)도 자주 발생한다.
생물학적 RNA에 기능적으로 중요한 많은 2차 구조 요소가 있습니다. 몇몇 유명한 예로는 Rho 독립형 터미네이터 스템 루프와 tRNA 클로버 잎이 있습니다.RNA 분자의 2차 구조를 결정하기 위한 활발한 연구가 진행 중이며, 실험 및 계산 방법을 모두 포함한다(RNA 구조 예측 소프트웨어 참조).
유사 노트
의사 노트는 적어도 2개의 스템 루프 구조를 포함한 핵산의 2차 구조이며, 그 중 한 스템의 절반이 다른 스템의 2분의 1 사이에 인터캘레이션 된다.의사 노트는 매듭 모양의 3차원 구조로 접히지만 진정한 위상 매듭은 아닙니다.pseudoknots의 베이스 페어링은 잘 중첩되지 않습니다.즉, 시퀀스 위치에서 베이스 페어가 서로 "오버랩"됩니다.이것은 핵산 시퀀스에서 일반적인 의사 노트의 존재를 동적 프로그래밍의 표준 방법으로 예측하는 것을 불가능하게 만든다. 동적 프로그래밍은 쌍을 이루는 줄기를 식별하기 위해 재귀 스코어링 시스템을 사용하고 결과적으로 공통 알고리즘으로 비내포성 염기쌍을 검출할 수 없다.단, 변경된 동적 [8]프로그램을 사용하여 의사 노트의 제한된 서브클래스를 예측할 수 있습니다.확률적 문맥이 없는 문법과 같은 새로운 구조 예측 기법 또한 의사 노트를 고려할 수 없다.
유사 노트는 촉매[9] 활성으로 다양한 구조를 형성할 수 있고 몇몇 중요한 생물학적 과정은 유사 노트를 형성하는 RNA 분자에 의존한다.예를 들어 인간 텔로머라아제의 RNA 성분은 활성에 [7]중요한 의사 노트를 포함한다.간염 델타 바이러스 리보자임은 활성 [10][11]부위에 의사 노트가 있는 촉매 RNA의 잘 알려진 예이다.DNA는 또한 의사 노트를 형성할 수 있지만, 일반적으로 표준 생리 조건에는 존재하지 않는다.
이차 구조 예측
핵산 2차 구조를 예측하는 대부분의 방법은 가장 가까운 이웃의 열역학 [12][13]모델에 의존합니다.뉴클레오티드의 시퀀스가 주어졌을 때 가장 가능성이 높은 구조를 결정하는 일반적인 방법은 낮은 자유 [14]에너지를 가진 구조를 찾는 동적 프로그래밍 알고리즘을 이용한다.동적 프로그래밍 알고리즘은 종종 pseudoknots 또는 염기쌍이 완전히 중첩되지 않은 다른 경우를 금지합니다. 이러한 구조는 작은 핵산 분자에 대해서도 계산적으로 매우 비싸기 때문입니다.확률적 문맥이 없는 문법과 같은 다른 방법도 핵산 2차 구조를 예측하는 데 사용될 수 있다.
많은 RNA 분자의 경우, 2차 구조는 RNA의 정확한 기능에 매우 중요합니다. 종종 실제 배열보다 더 중요합니다.이 사실은 때때로 "RNA 유전자"라고 불리는 비코드 RNA의 분석에 도움을 준다.생물정보학의 한 응용은 유전체를 탐색하는 데 예측된 RNA 2차 구조를 사용한다. 예를 들어, 마이크로RNA는 작은 내부 루프로 방해되는 표준적인 긴 줄기-루프 구조를 가지고 있다.
RNA 2차 구조는 특정 종에서 RNA 스플라이싱에 적용된다.사람과 다른 네발동물에서는 U2AF2 단백질이 없으면 스플라이싱 과정이 억제되는 것으로 나타났다.그러나 제브라피쉬와 다른 텔레오스트에서는 U2AF2가 없는 경우에도 특정 유전자에 RNA 스플라이싱 과정이 여전히 발생할 수 있습니다.이는 제브라피쉬의 유전자 중 10%가 각 인트론에서 각각 3' 스플라이스 부위(3'ss)와 5' 스플라이스 부위(5'ss)에 번갈아 TG와 AC 염기쌍을 가지며, 이는 RNA의 2차 구조를 변화시키기 때문일 수 있다.이것은 RNA의 2차 구조가 스플라이싱에 영향을 미칠 수 있다는 것을 암시하며, 잠재적으로 스플라이싱이 [15]일어나는데 필요한 것으로 생각되는 U2AF2와 같은 단백질을 사용하지 않아도 된다.
이차 구조 결정
RNA 2차 구조는 종종 단백질 데이터 뱅크에 축적되는 X선 결정학에 의해 얻어진 원자 좌표(teriary structure)로부터 결정될 수 있다.현재 방법에는 3DNA/[17]DSSR[16] 및 MC-notate가 있습니다.
「 」를 참조해 주세요.
- DNA나노테크놀로지
- DNA 분자 모형
- DiProDB데이터베이스는 열역학, 구조 및 기타 디뉴클레오티드 특성을 수집하고 분석하도록 설계되었다.
- RNA CoSMos
레퍼런스
- ^ Dirks, Robert M.; Lin, Milo; Winfree, Erik & Pierce, Niles A. (2004). "Paradigms for computational nucleic acid design". Nucleic Acids Research. 32 (4): 1392–1403. doi:10.1093/nar/gkh291. PMC 390280. PMID 14990744.
- ^ Yakovchuk, Peter; Protozanova, Ekaterina; Frank-Kamenetskii, Maxim D. (2006). "Base-stacking and base-pairing contributions into thermal stability of the DNA double helix". Nucleic Acids Research. 34 (2): 564–574. doi:10.1093/nar/gkj454. PMC 1360284. PMID 16449200.
- ^ Breslauer KJ, Frank R, Blöcker H, Marky LA (1986). "Predicting DNA duplex stability from the base sequence". PNAS. 83 (11): 3746–3750. Bibcode:1986PNAS...83.3746B. doi:10.1073/pnas.83.11.3746. PMC 323600. PMID 3459152.
- ^ Richard Owczarzy (2008-08-28). "DNA melting temperature - How to calculate it?". High-throughput DNA biophysics. owczarzy.net. Retrieved 2008-10-02.
- ^ Alberts; et al. (1994). The Molecular Biology of the Cell. New York: Garland Science. ISBN 978-0-8153-4105-5.
- ^ Pabo C, Sauer R (1984). "Protein-DNA recognition". Annu Rev Biochem. 53: 293–321. doi:10.1146/annurev.bi.53.070184.001453. PMID 6236744.
- ^ a b Chen JL, Greider CW (2005). "Functional analysis of the pseudoknot structure in human telomerase RNA". Proc Natl Acad Sci USA. 102 (23): 8080–5. Bibcode:2005PNAS..102.8080C. doi:10.1073/pnas.0502259102. PMC 1149427. PMID 15849264.
- ^ Rivas E, Eddy SR (1999). "A dynamic programming algorithm for RNA structure prediction including pseudoknots". J Mol Biol. 285 (5): 2053–2068. arXiv:physics/9807048. doi:10.1006/jmbi.1998.2436. PMID 9925784. S2CID 2228845.
- ^ Staple, David W.; Butcher, Samuel E. (2005-06-14). "Pseudoknots: RNA Structures with Diverse Functions". PLOS Biol. 3 (6): e213. doi:10.1371/journal.pbio.0030213. ISSN 1545-7885. PMC 1149493. PMID 15941360.
- ^ Doudna, Jennifer A.; Ferré-D'Amaré, Adrian R.; Zhou, Kaihong (October 1998). "Crystal structure of a hepatitis delta virus ribozyme". Nature. 395 (6702): 567–574. Bibcode:1998Natur.395..567F. doi:10.1038/26912. PMID 9783582. S2CID 4359811.
- ^ Lai, Michael M. C. (1995-06-01). "The Molecular Biology of Hepatitis Delta Virus". Annual Review of Biochemistry. 64 (1): 259–286. doi:10.1146/annurev.bi.64.070195.001355. ISSN 0066-4154. PMID 7574482.
- ^ Xia T, SantaLucia J Jr, Burkard ME, Kierzek R, Schroeder SJ, Jiao X, Cox C, Turner DH (October 1998). "Thermodynamic parameters for an expanded nearest-neighbor model for formation of RNA duplexes with Watson-Crick base pairs". Biochemistry. 37 (42): 14719–35. CiteSeerX 10.1.1.579.6653. doi:10.1021/bi9809425. PMID 9778347.
- ^ Mathews DH, Disney MD, Childs JL, Schroeder SJ, Zuker M, Turner DH (May 2004). "Incorporating chemical modification constraints into a dynamic programming algorithm for prediction of RNA secondary structure". PNAS. 101 (19): 7287–92. Bibcode:2004PNAS..101.7287M. doi:10.1073/pnas.0401799101. PMC 409911. PMID 15123812.
- ^ Zuker, M. (1989-04-07). "On finding all suboptimal foldings of an RNA molecule". Science. 244 (4900): 48–52. Bibcode:1989Sci...244...48Z. doi:10.1126/science.2468181. ISSN 0036-8075. PMID 2468181.
- ^ Lin, Chien-Ling; Taggart, Allison J.; Lim, Kian Huat; Cygan, Kamil J.; Ferraris, Luciana; Creton, Robert; Huang, Yen-Tsung; Fairbrother, William G. (13 November 2015). "RNA structure replaces the need for U2AF2 in splicing". Genome Research. 26 (1): 12–23. doi:10.1101/gr.181008.114. PMC 4691745. PMID 26566657.
- ^ Lu, XJ; Bussemaker, HJ; Olson, WK (2 December 2015). "DSSR: an integrated software tool for dissecting the spatial structure of RNA". Nucleic Acids Research. 43 (21): e142. doi:10.1093/nar/gkv716. PMC 4666379. PMID 26184874.
- ^ "MC-Annotate". www-lbit.iro.umontreal.ca.
외부 링크
- MDDNA: DNA의 구조생물정보학
- 전복 - DNA 모델링을 위한 상용 소프트웨어
- DNA 라이브: DNA의 물리적 특성을 계산하는 웹 인터페이스입니다.또한 UCSC Genome Browser 및 DNA Dynamics와 결과를 상호 연결할 수 있습니다.