액체.
Liquid| 시리즈의 일부 |
| 연속체 역학 |
|---|
액체(또는 초입자)는 용기의 모양과 일치하지만 압력과는 무관하게 (거의) 일정한 부피를 유지하는 거의 비압축성 유체입니다.이와 같이, 물질의 네 가지 기본 상태 중 하나이며(다른 것들은 고체, 가스, 플라즈마) 부피가 정해져 있지만 고정된 형태가 없는 유일한 상태입니다.액체는 분자간 결합에 의해 결합되는 원자와 같은 물질의 작은 진동 입자로 구성되어 있다.기체처럼 액체는 흐를 수 있고 용기의 형태를 취할 수 있다.대부분의 액체는 압축에 저항하지만 다른 액체는 압축할 수 있습니다.기체와 달리 액체는 용기의 모든 공간을 채우기 위해 흩어지지 않고 상당히 일정한 밀도를 유지합니다.액체 상태의 특징적인 특성은 표면 장력이며, 습윤 현상을 일으킵니다.물은 지구에서 단연코 가장 흔한 액체이다.
액체의 밀도는 보통 고체에 가깝고 기체의 밀도보다 훨씬 높습니다.그러므로 액체와 고체는 모두 응축 물질이라고 불린다.반면에, 액체와 기체는 흐르는 능력을 공유하기 때문에, 둘 다 유체라고 불립니다.비록 액체 상태의 물이 지구에 풍부하지만, 액체가 존재하기 위해서는 상대적으로 좁은 온도/압력 범위가 필요하기 때문에, 사실 이러한 물질의 상태는 알려진 우주에서 가장 흔하지 않습니다.우주에서 가장 많이 알려진 물질은 (검출할 수 있는 고체 물질의 흔적이 있는) 가스 형태이며, 성간 구름이나 별 안에서 나오는 플라스마입니다.
서론
액체는 물질의 네 가지 주요 상태 중 하나이며, 다른 것들은 고체, 가스, 플라즈마입니다.액체는 유체이다.고체와 달리, 액체 속의 분자는 훨씬 더 자유롭게 움직일 수 있습니다.고체에서 분자들을 결합시키는 힘은 액체 안에서만 일시적이며, 고체가 단단하게 유지되는 동안 액체가 흐를 수 있게 합니다.
기체와 같은 액체는 유체의 특성을 나타낸다.액체가 흐를 수 있고, 용기 모양을 가정할 수 있으며, 밀폐된 용기에 넣으면 용기 내의 모든 표면에 균등하게 압력이 분배됩니다.봉지에 액체를 넣으면 어떤 형태로든 짜낼 수 있습니다.기체와 달리 액체는 거의 압축할 수 없으며, 이는 광범위한 압력에 걸쳐 거의 일정한 부피를 차지한다는 것을 의미합니다. 액체는 일반적으로 용기 내의 사용 가능한 공간을 채우기 위해 팽창하지 않고 자체 표면을 형성하며, 항상 다른 액체와 쉽게 혼합되지 않을 수 있습니다.이러한 특성은 액체를 유압장치와 같은 용도에 적합하게 만듭니다.
액체 입자는 단단하지만 단단하지는 않습니다.이들은 서로 자유롭게 이동할 수 있기 때문에 입자 이동성이 제한적입니다.온도가 상승함에 따라 분자의 진동이 증가하여 분자 간의 거리가 증가하게 됩니다.액체가 끓는점에 도달하면, 분자들을 밀접하게 결합하는 응집력이 깨지고 액체는 기체 상태로 변한다(과열이 일어나지 않는 한).온도가 낮아지면 분자 사이의 거리가 작아진다.액체가 어는 지점에 도달하면, 분자는 보통 결정화라고 불리는 매우 특정한 순서로 고정되고, 그들 사이의 결합은 더 강해져 액체를 고체 상태로 변화시킵니다.
예
이 섹션은 확인을 위해 추가 인용문이 필요합니다.(2022년 7월 (이를 에 대해 학습합니다) |
온도와 압력에 대한 표준 조건에서의 액체 원소는 수은과 브롬 두 가지뿐입니다.상온보다 약간 높은 녹는점을 가진 원소는 프랑슘, 세슘, 갈륨, 루비듐 [1]등 4개입니다.상온에서 액체인 금속합금에는 NaK, 나트륨-칼륨 금속합금, 갈린스탄, 용융합금 액체 및 일부 아말감(수은을 포함한 합금)이 포함된다.
정상 조건에서 액체인 순수한 물질에는 물, 에탄올 및 기타 많은 유기 용제가 포함됩니다.액체 상태의 물은 화학과 생물학에서 매우 중요하다; 그것은 생명체의 존재에 필수적인 것으로 여겨진다.
무기 액체는 물, 마그마, 무기 비수성 용제 및 많은 산을 포함한다.
중요한 일상 액체에는 가정용 표백제와 같은 수용액, 미네랄 오일과 가솔린과 같은 다른 물질의 혼합물, 비네그레트나 마요네즈와 같은 유화액, 혈액과 같은 부유액, 페인트와 우유와 같은 콜로이드 등이 있다.
많은 기체는 액체 산소, 액체 질소, 액체 수소, 액체 헬륨과 같은 액체를 생성하면서 냉각에 의해 액화 될 수 있다.그러나 모든 가스가 대기압에서 액화될 수 있는 것은 아니다.예를 들어, 이산화탄소는 5.1atm 이상의 [2]압력에서만 액화할 수 있습니다.
어떤 재료들은 물질의 고전적인 세 가지 상태로 분류될 수 없다.예를 들어 액정(액정 디스플레이에 사용)은 고체 및 액체 양 특성을 모두 가지며 액체 또는 고체와 구별되는 물질 상태에 속합니다.
적용들

액체는 윤활제, 용제 및 냉각제로서 다양한 용도로 사용됩니다.
트라이볼로지에서는 액체가 윤활유로서의 성질을 위해 연구된다.오일과 같은 윤활제는 구성 요소의 작동 온도 범위 전체에 적합한 점도와 흐름 특성을 위해 선택됩니다.오일은 우수한 윤활 [3]특성을 위해 엔진, 기어 박스, 금속 가공 및 유압 시스템에 자주 사용됩니다.
많은 액체는 다른 액체나 고체를 용해하기 위해 용매로 사용된다.솔루션은 페인트, 실란트, 접착제 등 다양한 용도로 사용됩니다.나프타와 아세톤은 산업에서 부품과 기계에서 기름, 그리스, 타르를 제거하는 데 자주 사용됩니다.체액은 수성 용액이다.
계면활성제는 비누와 세제에서 흔히 발견된다.알코올과 같은 용제는 항균제로 종종 사용된다.그것들은 화장품, 잉크, 그리고 액체 염료 레이저에서 발견됩니다.그것들은 식품 산업, 식물성 [4]기름의 추출과 같은 과정에서 사용된다.
액체는 기체보다 열전도율이 더 좋은 경향이 있으며, 흐르는 능력은 액체를 기계 부품에서 과도한 열을 제거하는 데 적합합니다.열은 라디에이터와 같은 열 교환기를 통해 액체를 통과시켜 제거할 수 있으며 증발 중에 [5]액체와 함께 열을 제거할 수 있습니다.물이나 글리콜 냉각제는 엔진이 [6]과열되는 것을 막기 위해 사용됩니다.원자로에 사용되는 냉각제에는 물이나 나트륨이나 비스무트와 [7]같은 액체 금속이 포함된다.액체 추진제 필름은 [8]로켓의 추력 챔버를 냉각하는 데 사용됩니다.가공 시 물과 오일을 사용하여 발생하는 과도한 열을 제거하며, 이는 공작물과 공구 모두를 빠르게 파괴할 수 있습니다.땀을 흘리는 동안, 땀은 증발함으로써 인체의 열을 제거한다.난방, 환기, 공기조절 산업(HVAC)에서는 물과 같은 액체를 사용하여 한 영역에서 [9]다른 영역으로 열을 전달합니다.
마찬가지로, 액체는 더 나은 열 전달 특성을 위해 요리에 종종 사용됩니다.전도성이 향상될 뿐만 아니라, 따뜻한 유체는 팽창하고 상승하는 반면 차가운 유체는 수축하고 가라앉기 때문에 운동학적 점도가 낮은 액체는 상당히 일정한 온도에서 대류를 통해 열을 전달하는 경향이 있어 데치거나 끓이거나 튀기기에 적합합니다.기체를 액체로 응축함으로써 더 높은 열 전달 속도를 달성할 수 있습니다.액체의 비등점에서는 모든 열에너지가 온도 상승 없이 액체에서 기체로 상변화를 일으키기 위해 사용되며 화학적 위치 에너지로 저장된다.기체가 액체로 다시 응축될 때 이 과도한 열에너지는 일정한 온도에서 방출됩니다.이 현상은 찜질 등의 공정에서 사용됩니다.액체는 종종 끓는점이 다르기 때문에 액체나 기체의 혼합물이나 용액은 일반적으로 증류, 열, 냉, 진공, 압력 또는 다른 방법으로 분리될 수 있습니다.증류는 알코올 음료의 생산에서 정유 공장, 아르곤, 산소, 질소, 네온 또는 제논과 같은 가스의 극저온 증류(개별 끓는점 [10]이하로 냉각)에 이르기까지 모든 분야에서 찾아볼 수 있습니다.
액체는 파스칼의 법칙을 이용하여 유체 동력을 제공하는 유압 시스템의 주요 구성요소입니다.펌프나 물레방아 같은 장치는 고대부터 액체의 움직임을 기계적인 작업으로 바꾸기 위해 사용되어 왔다.오일은 유압 펌프를 통해 강제되며, 유압 펌프는 이 힘을 유압 실린더로 전달합니다.유압 장치는 자동차 브레이크와 변속기, 중장비, 비행기 제어 시스템과 같은 많은 애플리케이션에서 찾을 수 있습니다.다양한 유압 프레스는 수리 및 제조, 리프팅, 프레스, 클램프 및 [11]성형에 광범위하게 사용됩니다.
측정 장치에 액체가 사용되기도 합니다.온도계는 종종 수은과 같은 액체의 열팽창과 온도를 나타내기 위한 유동 능력을 조합하여 사용합니다.압력계는 기압을 [12]나타내기 위해 액체의 무게를 사용합니다.
기계적 특성
용량
액체의 양은 부피 단위로 측정됩니다.여기에는 SI 단위 입방 미터(m3)와 그 눈금, 특히 일반적으로 리터라고3 불리는 입방 데시미터(1dm = 1L = 0.001m3)와 밀리리터라고도 불리는 입방 센티미터(1cm−6 =[13] 1mL3 = 0.001L = 10m3)가 포함됩니다.
액체의 양은 그 온도와 압력에 의해 결정된다.액체는 일반적으로 열을 가하면 팽창하고 식으면 수축합니다.0°C에서 4°C 사이의 물은 눈에 띄는 [14]예외입니다.
반면 액체는 압축성이 거의 없다.예를 들어 물은 기압(bar)[15]이 증가할 때마다 46.4ppm만 압축됩니다.실온에서 약 4000bar(400메가파스칼 또는 58,000psi)의 압력에서 물의 부피는 [16]11%밖에 감소하지 않습니다.비압축성은 액체의 한 지점에서의 압력 변화가 액체의 모든 다른 부분으로 줄어들지 않고 전달되고 [17]압축의 형태로 에너지가 거의 손실되지 않기 때문에 액체를 수력 전달에 적합하게 만듭니다.
그러나 무시할 수 있는 압축성은 다른 현상으로 이어집니다.워터 해머라고 불리는 파이프의 쾅하는 소리는 밸브가 갑자기 닫힐 때 발생하며, 밸브에서 거대한 압력 스파이크를 만들어 음속 바로 아래의 속도로 시스템을 통해 역진합니다.액체의 비압축성으로 인한 또 다른 현상은 캐비테이션이다.액체는 탄성이 거의 없기 때문에 보트 프로펠러의 끝부분이나 파이프의 날카로운 모서리와 같이 난기류가 높거나 방향이 크게 바뀌는 영역에서 말 그대로 분리될 수 있습니다.저압(진공) 영역에 있는 액체가 증발하여 기포를 형성하고 고압 영역에 진입하면 기포가 붕괴됩니다.이로 인해 기포가 남긴 구멍에 엄청난 국소적인 힘으로 액체가 채워져 인접한 고체 표면이 [18]침식됩니다.
압력 및 부력
중력장에서 액체는 용기 옆면뿐만 아니라 액체 안에 있는 모든 것에 압력을 가한다.이 압력은 모든 방향으로 전달되며 깊이에 따라 증가합니다.액체가 균일한 중력장에 정지해 있는 경우 z에서의 p pz는 다음과[19] 같습니다.
여기서:
- 0은 표면의 압력입니다.
- \rho )는 액체의 농도이며 깊이가 균일하다고 합니다.
- g는 중력 가속도입니다.
공기 중에 개방된 수역의 경우 0이 대기압이 됩니다.
균일한 중력장의 정적 액체도 액체에 담근 물체가 깊이에 따른 압력 변화에 의해 순력을 경험하는 부력 현상을 보인다.힘의 크기는 물체에 의해 변위된 액체의 무게와 동일하며 힘의 방향은 물에 잠긴 물체의 평균 밀도에 따라 달라집니다.밀도가 액체의 밀도보다 작을 경우 부력은 위쪽으로 향하고 물체는 떠 있는 반면 밀도가 클 경우 부력은 아래쪽으로 향하고 물체는 가라앉는다.이것은 아르키메데스의 [20]원리라고 알려져 있다.
표면

액체의 부피가 용기의 부피와 정확히 일치하지 않는 한, 하나 이상의 표면이 관찰됩니다.표면의 존재는 벌크 액체에 존재하지 않는 새로운 현상을 일으킨다.이것은 표면의 분자가 표면의 안쪽에서만 다른 액체 분자와 결합을 가지고 있기 때문인데, 이것은 표면 분자를 안으로 끌어당기는 순 힘을 의미합니다.마찬가지로, 이 힘은 에너지의 관점에서 설명될 수 있습니다. 즉, 주어진 영역의 표면을 형성하는 것과 관련된 고정된 양의 에너지가 있습니다.이 양은 단위 면적당 에너지 단위(SI 단위: J/m2)로 표면 장력이라고 불리는 물질 특성입니다.분자간 힘이 강한 액체는 표면 [21]장력이 큰 경향이 있다.
표면 장력의 실제적인 의미는 액체가 표면적을 최소화하는 경향이 있으며, 다른 제약 조건이 존재하지 않는 한 구형 물방울과 기포를 형성한다는 것입니다.표면 장력은 표면파, 모세관 작용, 습윤 및 파문을 포함한 다양한 다른 현상에도 영향을 미칩니다.나노스케일 제한하의 액체에서는, 거시적인 액체 샘플에 비해 훨씬 더 많은 분자가 표면 근처에 있기 때문에, 표면 효과는 지배적인 역할을 할 수 있다.
액체의 표면 장력은 습도에 직접적인 영향을 미친다.대부분의 일반적인 액체는 수십 mJ/m의2 장력을 가지고 있기 때문에 기름, 물 또는 접착제의 물방울이 쉽게 결합되어 다른 표면에 부착될 수 있는 반면, 수은과 같은 액체 금속은 수백 mJ2/m의 장력을 가질 수 있습니다. 따라서 물방울은 쉽게 결합되지 않고 특정 조건에서만 표면이 젖을 수 있습니다.
일반적인 액체의 표면 장력은 온도와 같은 변화하는 조건에 노출될 때 상대적으로 좁은 범위의 값을 차지하는데,[22] 이는 점도와 같은 다른 기계적 특성에서 볼 수 있는 엄청난 변화와 강하게 대비된다.
흐름

액체의 흐름을 특징짓는 중요한 물리적 특성은 점도이다.직관적으로 점도는 액체가 흐르는 저항을 나타냅니다.
좀 더 엄밀히 말하면, 점도는 액체가 한정된 [23]속도로 전단될 때와 같이 주어진 속도로 변형에 대한 저항력을 측정합니다.구체적인 예로는 파이프를 통과하는 액체가 있습니다.이 경우 액체는 중심 부근보다 파이프 벽 부근에서 더 느리게 흐르기 때문에 전단 변형을 겪습니다.그 결과, 흐름에 대한 점성 저항을 나타낸다.유량을 유지하기 위해서는 파이프 단부 사이의 압력차 등 외력을 가해야 한다.
액체의 점도는 [24][25]온도가 올라가면 낮아진다.
점도의 정확한 제어는 많은 용도, 특히 윤활 산업에서 중요합니다.이러한 제어를 달성하는 한 가지 방법은 점도가 다른 두 개 이상의 액체를 정확한 [26]비율로 혼합하는 것입니다.또한 윤활유의 점도의 온도 의존성을 조절할 수 있는 다양한 첨가제가 존재합니다.기계는 종종 일정한 온도에서 작동하기 때문에 이 기능은 중요합니다(점도 [27]지수 참조).
액체의 점성 거동은 뉴턴식일 수도 있고 뉴턴식이 아닐 수도 있다.뉴턴 액체는 선형 변형률/응력 곡선을 나타내며, 이는 점도가 시간, 전단 속도 또는 전단 속도 이력과 무관함을 의미합니다.뉴턴 액체의 예로는 물, 글리세린, 모터 오일, 꿀, 수은 등이 있다.비뉴턴 액체는 점도가 이들 인자와 무관하지 않고 전단하에서 증점(점도의 증가) 또는 틴(점도의 감소)되는 액체를 말한다.뉴턴이 아닌 액체의 예로는 케첩, 마요네즈, 헤어젤, 플레이도 또는 녹말 [28]용액이 있습니다.
구속 중의 탄력성
밀폐된 액체는 부피 액체와 비교하여 다른 기계적 특성을 보일 수 있습니다.예를 들어, (예를 들어 강체 벽 사이의 간격에서) 밀리미터 이하의 구속 하의 액체는 고체 상태의 기계적 반응을 나타내며, 구속 [29]길이의 역입방정도에 따라 스케일링되는 놀랄 만큼 큰 저주파 탄성 전단 계수를 가지고 있다.
음전파
액체의 음속은 c / { c { K / \} ( K / \ K} ) \ displaystyle \ ) 。서는 액체의 부피 계수이고 밀도는 \\rho}입니다.예를 들어, 물의 부피 계수는 약 2.2 GPa이고 밀도는 1000 kg/m이며3, 이는 c = 1.5 km/[30]s이다.
열역학
상전이
끓는점 이하의 온도에서 액체 형태의 물질은 증기의 응축의 역방향 과정과 평형에 도달할 때까지 증발합니다.이 시점에서 증기는 액체가 증발하는 것과 같은 속도로 응축됩니다.따라서 증발된 액체가 지속적으로 [31]제거되면 액체가 영구적으로 존재할 수 없습니다.끓는점 이상의 액체는 일반적으로 끓는다. 그러나 과열로 인해 특정 상황에서는 이를 방지할 수 있다.
응고점 이하의 온도에서는 액체가 결정화되어 고체 형태로 변하는 경향이 있습니다.기체로의 이행과는 달리, 일정한 [citation needed]압력 아래에서는 평형이 없기 때문에 과냉각이 일어나지 않는 한 액체는 결국 완전히 결정화된다.단, 이는 (예를 들어) 밀폐된 강한 용기의 물과 얼음이 두 상이 공존하는 평형에 도달할 수 있도록 일정한 압력 하에서만 해당된다.고체에서 액체로의 전환에 대해서는 용융을 참조하십시오.
우주에 있는 액체
위상 다이어그램은 우주나 다른 진공에 액체가 존재하지 않는 이유를 설명합니다.압력이 0이기 때문에(행성과 달의 표면이나 내부에서는 제외) 물과 우주에 노출된 다른 액체는 온도에 따라 즉시 끓거나 얼게 됩니다.지구 근처 우주 지역에서는 태양이 직접 비추지 않으면 물이 얼고 햇빛을 받으면 바로 증발한다.만약 물이 달에서 얼음으로 존재한다면, 그것은 태양이 결코 빛나지 않고 주변의 바위가 그것을 너무 뜨겁게 달구지 않는 그늘진 구멍에서만 존재할 수 있다.토성 궤도 근처의 어느 지점에서, 태양으로부터의 빛이 너무 희미해서 얼음을 수증기에 승화시킬 수 없다.이것은 토성의 [32]고리를 구성하는 얼음의 수명으로부터 명백하다.
솔루션
액체는 기체, 고체, 그리고 다른 액체와 용액을 형성할 수 있다.
두 액체는 어떤 비율로든 용액을 형성할 수 있다면 혼합할 수 있고, 그렇지 않으면 불용성이라고 한다.예를 들어 물과 에탄올(음용 알코올)은 혼합할 수 있는 반면 물과 휘발유는 혼합할 [33]수 없습니다.경우에 따라서는 불용성 액체의 혼합물을 안정화시켜 에멀젼을 형성할 수 있으며, 여기서 한 액체는 다른 액체를 통해 현미경 물방울로 분산된다.일반적으로 이것은 물방울을 안정시키기 위해 계면활성제의 존재를 필요로 한다.에멀젼의 친숙한 예는 마요네즈인데, 마요네즈는 물과 달걀 [34]노른자에서 발견되는 물질인 레시틴에 의해 안정화된 기름의 혼합물로 구성되어 있습니다.
현미경적 설명
액체를 구성하는 분자는 무질서하고 강하게 상호작용하며, 이것은 액체를 분자 수준에서 엄격하게 묘사하는 것을 어렵게 만든다.이것은 물질의 다른 두 가지 공통상인 가스와 고체와 대조적입니다.가스는 무질서하지만, 충분히 희석되어 다체 상호작용은 무시될 수 있으며, 대신 잘 정의된 이원 충돌 사건의 관점에서 분자 상호작용을 모델링할 수 있습니다.반대로 고체는 밀도가 높고 강하게 상호작용하지만 분자 수준에서 규칙적인 구조(예: 결정 격자)는 상당한 이론적 단순화를 가능하게 한다.이러한 이유로, 액체의 미시적 이론은 기체와 [35]고체의 이론보다 덜 발전되었다.
정적 구조 계수
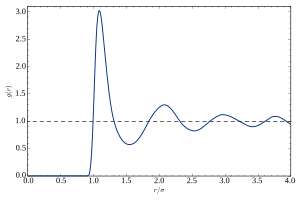
액체에서 원자는 결정 격자를 형성하지 않으며 다른 형태의 장기 질서도 보이지 않습니다.이는 X선과 중성자 회절에서 브래그 피크가 없는 것으로 입증된다.정상 조건 하에서 회절 패턴은 원형의 대칭을 가지며 액체의 등방성을 나타낸다.반경방향에서는 회절강도가 부드럽게 진동한다.이는 보통 정적구조인자 S(q)에 의해 설명되며, 파장 q=(4µ/sin) sin θ는 탐침의 파장 θ와 Bragg 각도 θ에 의해 주어진다.S(q)의 진동은 액체의 가까운 순서, 즉 원자와 가장 가까운 이웃, 두 번째로 가까운 이웃의 몇 개의 껍질 사이의 상관관계를 나타냅니다.
이러한 상관관계에 대한 보다 직관적인 설명은 기본적으로 S(q)의 푸리에 변환인 방사 분포 함수 g(r)에 의해 주어진다.그것은 액체에서 쌍 상관 관계의 시간 스냅샷의 공간 평균을 나타낸다.
음향 분산 및 구조 완화
위의 c / { c={ 식에는 벌크 계수 K가 포함되어 있다.K가 주파수에 의존하지 않는 경우, 액체는 선형 매체로 동작하므로 소리가 소산되지 않고 모드 커플링 없이 전파됩니다.실제로 액체는 어느 정도 분산되어 있습니다.주파수가 증가함에 따라 K는 저주파수 액체상 K 0 K_에서 고주파 고체상 K{\(\ 로 넘어갑니다.일반 액체는 대부분 GHz와 THz 사이의 주파수에서 발생합니다.하이퍼사운드라고 불리는 imes.
GHz 미만의 주파수에서 일반 액체는 전단파를 견딜 수 없습니다. 전단률의 0 주파수 한계는 G G_}=입니다.이것은 때때로 [36][37]액체의 결정적인 특성으로 보여진다.단, 벌크계수 K와 마찬가지로 전단계수 G는 주파수에 의존하며, 초음파 주파수에서는 액체상 G0(\ G_에서 고체상 G G_로 같은 크로스오버를 보인다.
Kramers-Kronig 관계에 따라 음속의 분산(K 또는 G의 실제 부분에 의해 주어짐)은 감음(K 또는 G의 허수 부분에 의해 주어짐)의 최대치에 따른다.선형 반응 이론에 따르면, K 또는 G의 푸리에 변환은 시스템이 외부 섭동 후에 평형으로 돌아오는 방법을 기술합니다. 이러한 이유로, GHz에서 THz 영역으로의 분산 단계를 완화라고도 합니다.변동-분산 정리에 따르면 평형으로의 이완은 평형 변동과 밀접하게 관련되어 있다.음파와 관련된 밀도 변동은 Brilouin 산란으로 실험적으로 관찰할 수 있다.
액체를 유리 천이를 향해 과냉각할 때, 액체와 같은 반응에서 고체와 같은 반응으로 교차하는 것은 GHz에서 MHz, kHz, Hz 등으로 이동한다.; 등가적으로, 구조적 완화의 특성 시간은 ns에서 µs, ms, s, ...로 증가한다.이것은 위에서 언급한 유리 형성 액체의 점탄성 거동에 대한 미시적 설명입니다.
연관성 효과
고체에서의 원자/분자 확산(또는 입자 이동) 메커니즘은 액체 물질의 점성 흐름 및 응고 메커니즘과 밀접하게 관련되어 있습니다.액체[38] 내 분자 "자유 공간"의 관점에서 점도의 설명은 필요에 따라 수정되어 분자가 상온에서 액체 상태에서 "관련된" 것으로 알려진 액체를 설명하였다.다양한 분자가 결합되어 연관된 분자를 형성할 때, 그들은 이동 분자를 위한 자유 공간으로 사용 가능했던 일정량의 공간을 반강체 시스템 내에 둘러쌉니다.따라서 대부분의 물질이 [39]냉각과 관련되는 경향에 따라 냉각 시 점도가 증가한다.
점도에 대한 압력의 영향을 설명하기 위해 유사한 주장을 사용할 수 있으며, 점도는 주로 압축성이 유한한 액체에 대한 부피의 함수라고 가정할 수 있다.따라서 압력 상승에 따른 점도의 증가가 예상된다.또한 부피가 열로 팽창하지만 압력으로 다시 감소해도 점도는 변하지 않는다.
작은 그룹에 있는 분자의 방향성에 대한 국소적인 경향은 액체에 일정 수준의 연관성을 부여한다.이러한 연관성은 액체 내에서 상당한 "내압"을 발생시키는데, 이는 거의 전적으로 일시적인 저속 때문에 (맥스웰 분포에 따라) 다른 분자와 합쳐진 분자 때문이다.이러한 여러 분자 사이의 내부 압력은 고체 형태의 분자 그룹 간의 압력과 일치할 수 있습니다.
로. 부터 | 단단한 | 액체. | 가스 | 플라즈마 |
|---|---|---|---|---|
| 단단한 | 녹는 | 승화 | ||
| 액체. | 냉동 | 기화 | ||
| 가스 | 퇴적 | 응축 | 이온화 | |
| 플라즈마 | 재결합 |
레퍼런스
- ^ The Elements, The Todore Gray:우주의 알려진 모든 원자의 시각적 탐구 뉴욕: 워크맨 출판사, 2009 페이지 127 ISBN1-57912-814-9
- ^ Silberberg, Martin S. (2009), Chemistry: The Molecular Nature of Matter and Change, McGraw-Hill Higher Education, pp. 448–449, ISBN 978-0-07-304859-8
- ^ Theo Mang, Wilfried Dressel '윤활제와 윤활', Wiley-VCH 2007 ISBN 3-527-31497-0
- ^ George Wypych "용제 핸드북" William Andrew 출판사 2001 페이지 847-881 ISBN 1-895198-24-0
- ^ N. B. Vargaftik "액체와 가스의 열전도율 핸드북" CRC Press 1994 ISBN 0-8493-9345-0
- ^ Jack Erjavec "자동차 테크놀로지: 시스템 접근" Dellmar Learning 2000 페이지 309 ISBN 1-4018-4831-1
- ^ 제럴드 웬트 "원자력과 기술의 전망" D.반 노스트랜드 컴퍼니 1957년 266쪽
- ^ 디터 K의 "액체 추진 로켓 엔진 설계를 위한 현대 공학"휴젤, 데이비드 H.Huang – 미국항공우주학회 1992년 페이지 99 ISBN 1-56347-013-6
- ^ 토마스 멀HVAC 원리 및 응용 매뉴얼' McGraw-Hill 1997 ISBN 0-07-044451-X
- ^ R. L. Earle의 식품 가공 단위 운영 -- Pergamon Press 1983 56-62, 138-141페이지
- ^ R. 키스 모블리 유체 동력학 버터워스-하이네만 2000 페이지 vii ISBN 0-7506-7174-2
- ^ Bela G. Liptak "계기 엔지니어 핸드북: 프로세스 제어" CRC Press 1999 페이지 807 ISBN 0-8493-1081-4
- ^ Knight, Randall D. (2008), Physics for Scientists and Engineers: A Strategic Approach (With Modern Physics), Addison-Wesley, p. 443, ISBN 978-0-8053-2736-6
- ^ Silberberg, Martin S. (2009), Chemistry: The Molecular Nature of Matter and Change, McGraw-Hill Higher Education, p. 461, ISBN 978-0-07-304859-8
- ^ "Compressibility of Liquids". hyperphysics.phy-astr.gsu.edu. Archived from the original on 7 December 2017. Retrieved 8 May 2018.
- ^ 인텔리전트 에너지 필드 제조: Wenwu Zhang에 의한 학문 간 프로세스 혁신 -- CRC Press 2011 페이지 144
- ^ 기사(2008) 페이지 454
- ^ S. C. 굽타의 유체 기계와 유압 기계 -- Dorling-Kindersley 2006 85 페이지
- ^ 기사(2008) 페이지 448
- ^ 기사(2008) 페이지 455-459
- ^ Silberberg, Martin S. (2009), Chemistry: The Molecular Nature of Matter and Change, McGraw-Hill Higher Education, p. 457, ISBN 978-0-07-304859-8
- ^ Edward Yu. Bormashenko (5 November 2018). Wetting of Real Surfaces. De Gruyter. pp. 3–5. ISBN 978-3-11-058314-4.
- ^ Landau, L.D.; Lifshitz, E.M. (1987), Fluid Mechanics (2nd ed.), Pergamon Press, pp. 44–45, ISBN 978-0-08-033933-7
- ^ Bird, R. Byron; Stewart, Warren E.; Lightfoot, Edwin N. (2007), Transport Phenomena (2nd ed.), John Wiley & Sons, Inc., p. 21, ISBN 978-0-470-11539-8
- ^ Krausser, J.; Samwer, K.; Zaccone, A. (2015). "Interatomic repulsion softness directly controls the fragility of supercooled metallic melts". Proceedings of the National Academy of Sciences of the USA. 112 (45): 13762–13767. arXiv:1510.08117. Bibcode:2015PNAS..11213762K. doi:10.1073/pnas.1503741112. PMC 4653154. PMID 26504208.
- ^ Zhmud, Boris (2014), "Viscosity Blending Equations" (PDF), Lube-Tech, 93
- ^ "Viscosity Index". UK: Anton Paar. Archived from the original on March 9, 2020. Retrieved 29 August 2018.
- ^ Laid Boukraa의 전통과 현대 의학의 꿀 - CRC Press 2014 페이지 22-24
- ^ Zaccone, A.; Trachenko, K. (2020). "Explaining the low-frequency shear elasticity of confined liquids". Proceedings of the National Academy of Sciences of the USA. 117 (33): 19653–19655. arXiv:2007.11916. Bibcode:2020PNAS..11719653Z. doi:10.1073/pnas.2010787117. PMC 7443959. PMID 32747540.
- ^ Taylor, John R. (2005), Classical Mechanics, University Science Books, pp. 727–729, ISBN 978-1-891389-22-1
- ^ March, N.H.; Tosi, M.P. (2002), Introduction to Liquid State Physics, World Scientific, p. 7, Bibcode:2002ilsp.book.....M, doi:10.1142/4717, ISBN 978-981-3102-53-8
- ^ Siegel, Ethan (2014-12-11). "Does water freeze or boil in space?". Starts With A Bang!. Retrieved 2022-02-10.
- ^ Silberberg, 188페이지 및 502
- ^ Miodownik, Mark (2019), Liquid rules: The Delightful and Dangerous Substances that Flow Through Our Lives, Houghton Mifflin Harcourt, p. 124, ISBN 978-0-544-85019-4
- ^ Fisher, I.Z. (1964), Statistical Theory of Liquids, The University of Chicago Press, pp. 1–11
- ^ Born, Max (1940). "On the stability of crystal lattices". Mathematical Proceedings. Cambridge Philosophical Society. 36 (2): 160–172. Bibcode:1940PCPS...36..160B. doi:10.1017/S0305004100017138.
- ^ Born, Max (1939). "Thermodynamics of Crystals and Melting". Journal of Chemical Physics. 7 (8): 591–604. Bibcode:1939JChPh...7..591B. doi:10.1063/1.1750497. Archived from the original on 2016-05-15.
- ^ D.B. Macleod (1923). "On a relation between the viscosity of a liquid and its coefficient of expansion". Trans. Faraday Soc. 19: 6. doi:10.1039/tf9231900006.
- ^ G.W. Stewart (1930). "The Cybotactic (Molecular Group) Condition in Liquids; the Association of Molecules". Phys. Rev. 35 (7): 726. Bibcode:1930PhRv...35..726S. doi:10.1103/PhysRev.35.726.





 표면의 압력입니다.
표면의 압력입니다. 액체의 농도이며 깊이가 균일하다고
액체의 농도이며 깊이가 균일하다고 


 액체의
액체의 

 고주파 고체상
고주파 고체상 

 고체상
고체상 



