요오드산칼륨
Potassium iodate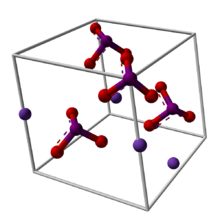 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 요오드산칼륨 | |
| 기타 이름 요오드산, 칼륨염 | |
| 식별자 | |
| |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.028.938 |
| EC 번호 |
|
| E 넘버 | E917 (유리제, ...) |
펍켐 CID | |
| RTECS 번호 |
|
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| 키오3 | |
| 어금질량 | 214.001 g/190 |
| 외관 | 백색 결정 가루 |
| 냄새 | 무취의 |
| 밀도 | 3.89 g/cm3 |
| 녹는점 | 560°C(1,040°F, 833K) (손상) |
| 4.74 g/100 mL(0°C) 9.16 g/100 mL(25 °C) 32.3 g/100 mL (100 °C) | |
| 용해성 | KI 용액에 녹는 알코올, 액체 암모니아, 질산 등에서 불용성인 |
자기 감수성(magnetic susibility) | -63.1·10cm−63/190cm |
| 위험 | |
| GHS 라벨 표시: | |
   | |
| H272, H302, H318 | |
| P210, P280, P301+P312+P330, P305+P351+P338+P310 | |
| NFPA 704(화재 다이아몬드) | |
| 플래시 포인트 | 불연성 |
| 관련 화합물 | |
기타 음이온 | 염소산칼륨 브롬산칼륨 |
기타 양이온 | 요오드산나트륨 |
관련 화합물 | 요오드화칼륨 치주산칼륨 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
요오드산칼륨(KIO3)은 K+ 이온과 IO3− 이온으로 구성된 이온 화합물이다.
준비 및 특성
요오드산칼륨은 산화제로 가연성 물질이나 환원제와 접촉할 경우 화재를 일으킬 수 있다. 수산화칼륨과 같은 칼륨 함유 염기서열을 요오드산과 반응시켜 다음과 같은 방법으로 준비할 수 있다.
또한 수산화칼륨의 뜨겁고 농축된 용액에 요오드를 첨가하여 준비할 수 있다.
또는 요오드화칼륨과 염소산칼륨, 브롬산염 또는 과염소산염을 혼합하여 용액을 추출하고 요오드산칼륨을 결정화하여 용액에서 격리한다.[1]
- KI + KClO3 → KIO3 + KCl
피해야 할 조건/보조물: 열, 충격, 마찰, 가연성 물질, 환원 물질, 알루미늄, 유기 화합물, 탄소, 과산화수소 및 황화물이 포함된다.
적용들
요오드산칼륨은 때때로 요오드결핍을 예방하기 위해 식탁용 소금의 요오드화에 사용된다. 요오드화물은 습윤 상태에서 분자 산소에 의해 요오드로 산화될 수 있기 때문에 미국 회사들은 요오드화칼륨에 티오황산염이나 다른 산화방지제를 첨가한다. 다른 나라에서는 요오드산칼륨이 식이 요오드의 공급원으로 사용된다. 그것은 또한 어떤 아기 분유 우유에 들어있는 성분이다.
브롬산칼륨처럼 요오드산칼륨은 제빵에 숙성제로 쓰이기도 한다.
방사선방호
요오드산칼륨은 노출 전에 요오드의 안정적인 공급원으로 몸을 포화시켜 갑상선에 방사성 요오드가 축적되지 않도록 보호하는 데 사용될 수 있다.[2] 세계보건기구(WHO)의 방사선방호 승인을 받은 요오드산칼륨(KIO3)은 덥고 습한 기후에서 유통기한이 낮은 요오드산칼륨(KI)의 대체품이다.[3] 영국 싱가포르 아랍에미리트(UAE) 미국 아이다호주 유타주 등은 요오드산 칼륨을 태블릿 형태로 비축하는 것으로 알려졌다[by whom?].[citation needed] 아일랜드 정부도 9.11 테러 이후 모든 가정에 요오드산칼륨 알약을 발행했다.[4][failed verification][5] 미국 식품의약국(FDA)의 갑상선 차단제 사용 승인을 받지 않았으며, FDA는 이 사용을 촉진하는 미국의 웹사이트에 대해 조치를 취했다.[6][7]
| 나이 | KI(mg) | KIO3(mg) |
|---|---|---|
| 12살 이상 | 130 | 170 |
| 3살 – 12세 | 65 | 85 |
| 생후 1~36개월 | 32 | 42 |
| < 생후 1개월. | 16 | 21 |
참조
이 글은 검증을 위해 인용구가 추가로 필요하다.– · · 책· · (2009년 1월)(이 |
- ^ 프라디오트 파트나이크. 무기 화학 약품 안내서. 맥그로힐, 2002년 ISBN0-07-049439-8
- ^ Astbury, John; Horsley, Stephen; Gent, Nick (1999), "Evaluation of a scheme for the pre-distribution of stable iodine (potassium iodate) to the civilian population residing within the immediate countermeasures zone of a nuclear submarine construction facility", Journal of Public Health, 21 (4): 2008–10, doi:10.1093/pubmed/21.4.412, PMID 11469363, archived from the original on 2008-09-05
- ^ Pahuja, D.N.; Rajan, M.G.; Borkar, A.V.; Samuel, A.M. (Nov 2008), "Potassium iodate and its comparison to potassium iodide as a blocker of 131I uptake by the thyroid in rats", Health Physics, 65 (5): 545–9, doi:10.1097/00004032-199311000-00014, PMID 8225995
- ^ "Archived copy". Archived from the original on 2013-10-17. Retrieved 2013-04-08.CS1 maint: 제목으로 보관된 복사본(링크)
- ^ a b c "Archived copy". Archived from the original on 2013-10-18. Retrieved 2013-05-22.CS1 maint: 제목으로 보관된 복사본(링크)
- ^ "Potassium iodide vs potassium iodate. Which one works?".
- ^ http://www.nukepills.com/docs/Potassium%20Iodate%20warning%20letter.pdf
- ^ "Archived copy". Archived from the original on 2013-10-17. Retrieved 2013-04-08.CS1 maint: 제목으로 보관된 복사본(링크)
- ^ Guidelines for Iodine Prophylaxis following Nuclear Accidents (PDF), Geneva: World Health Organization, 1999




