사마륨()II) 요오드화합물
Samarium(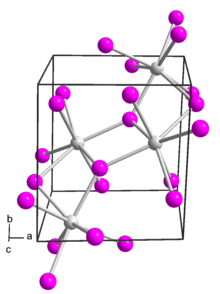 | |
| 이름 | |
|---|---|
| IUPAC 이름 사마륨II) 요오드화합물 | |
| 기타 이름 사마륨 디오다이오드 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| 스미2 | |
| 어금질량 | 404.16 g/190 |
| 외관 | 녹색 고체 |
| 녹는점 | 520°C(968°F, 793K) |
| 위험 | |
| 플래시 포인트 | 불연성 |
| 관련 화합물 | |
기타 음이온 | 사마륨()II) 염화물 사마륨()II) 브로마이드 |
기타 양이온 | 사마륨(III) 요오드화합물 에우로피움(Europium)II) 요오드화합물 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
사마륨()II) 요오드화물은 SmI라는2 공식을 가진 무기 화합물이다.유기합성 용액으로 채용할 때 카간의 시약으로 알려져 있다.smI는2 녹색 고형이며 솔루션도 녹색이다.유기합성에 쓰이는 강력한 1전자 환원제다.
구조
인 사마륨()II) 요오드화합물, 금속 중심은 얼굴형 팔면 기하학으로 7개 조정된다.[1]
사마륨은 에테르 5개와 요오드화합물 2개로 헵타코르딘으로 남아있다.[2]
준비
요오드화 사마륨은 사마륨 금속과 디오도메탄 또는 1,2-다이오도에탄의 거의 정량적인 수확량으로 쉽게 준비된다.[3]이렇게 준비했을 때, 그것의 용액은 무기 시약을 정화하지 않고 가장 자주 사용된다.
-
()
사마륨(III) 요오드화합물(SMI3)의 고온 분해에 의해 고체, 용매 없는 SmI가2 형성된다.[4][5][6]
반응
사마륨()II) 요오드화물은 강력한 환원제로, 예를 들어 물을 수소로 빠르게 감소시킨다.[1]THF에서 진한 청색 0.1M 용액으로 시중에서 구입할 수 있다.일반적으로 초계량계에 사용되지만 촉매적 용도는 설명되어 있다.[7]
유기 화학
사마륨()II) 요오드화물은 탄소-탄소 결합 형성을 위한 시약으로, 예를 들어 케톤과 알킬 요오드화합물 사이의 바비어 반응(그리기 반응과 유사함)에서 3차 알코올을 형성한다.[8]
- R1I + R2COR3 → R1R2C(OH)R3
일반적인 반응 조건에서는 촉매 NiI가2 존재하는 경우 THF의 SmI를2 사용한다.
에스테르도 비슷하게 반응하지만(두 개의 R그룹을 추가), 알데히드는 부산물을 준다.반응이 매우 빠른 경우가 많다는 점에서 편리하다(추위에 5분 이하).비록 사마륨이 있다.II) 요오드화물은 강력한 단일 전자 환원제로 간주되며, 기능 그룹 사이에서 뛰어난 화학적 강인성을 보인다.예를 들어, 다양한 카보닐 함유 기능성(에스테르, 케톤, 아미드, 알데히드 등)이 있는 경우, 황산염과 황산화물을 해당 황화물로 줄일 수 있다.이것은 아마도 황산염과 황산화물에 비해 카보닐에 대한 반응이 상당히 느리기 때문일 것이다.또한 해당 탄화수소 화합물에 대한 할로겐화 탄화수소의 탈산화도 사마륨을 사용하여 달성할 수 있다(II) 요오드화합물또한 THF에서 SmI의2 진한 파란색은 일단 반응이 일어나면 옅은 노란색으로 방출되면서 발생하는 색 변화에 의해 모니터링할 수 있다.사진은 바비어 반응 혼합물과 접촉하는 즉시 어두운 색이 사라지는 것을 보여준다.
작업물은 묽은 염산으로, 사마륨은 수성 Sm으로3+ 제거된다.
카보닐 화합물은 단순한 연골과 결합하여 5개, 6개 또는 8개의 멤브레인 링을 형성할 수도 있다.[9]
Tosyl 그룹은 증류수 및 애니메이션 베이스와 함께2 SmI를 사용하여 거의 즉각적으로 N-to-sylamides에서 제거할 수 있다.이 반응은 아지리딘과 같은 민감한 기질들의 감방에 효과적이다.[10]
마코-람 디옥시겐화에서, 알코올은 SmI가2 있는 곳에서 그들의 톨루산 에스테르를 줄임으로써 거의 즉각적으로 디옥시겐화 될 수 있다.
SMI의2 신청은 검토되었다.[11][12][13]2009년 출간된 사마륨 디오다이드를 이용한 유기합성 책에는 smI가2 매개한 반응에 대한 상세한 개요가 담겨 있다.[14]
참조
- ^ a b Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ William J. Evans; Tammy S. Gummersheimer & Joseph W. Ziller (1995). "Coordination Chemistry of Samarium Diiodide with Ethers Including the Crystal Structure of Tetrahydrofuran-Solvated Samarium Diiodide, SmI2(THF)5". J. Am. Chem. Soc. 117 (35): 8999–9002. doi:10.1021/ja00140a016.
- ^ P. Girard, J. L. Namy and H. B. Kagan (1980). "Divalent Lanthanide Derivatives in Organic Synthesis. 1. Mild Preparation of SmI2 and YbI2 and Their Use as Reducing or Coupling Agents". J. Am. Chem. Soc. 102 (8): 2693–2698. doi:10.1021/ja00528a029.
- ^ G. 얀치, N. 스칼라 : "주르 켄트니스 데르 할로겐니데 데르 셀테넨 에르덴.IV. – 우베르 사마륨()II)jodid und den den thermischen Abbau des Samarium()III)jodids", Zeitschrift für Allgemeine und Anorganische Chemie, 1930, 193, 391–405; doi:10.1002/zaac.19301930303030132.
- ^ G. Jantsch: "Thermischer Abbau von seltenen Erd (III)halogeniden", Die Naturwissenschaften, 1930, 18 (7), 155–155; doi:10.1007/BF01501667.
- ^ Gmelins Handbuch der anorgischen Chemie, System Nr. 39, Band C 6, 페이지 192–194.
- ^ Huang, Huan-Ming; McDouall, Joseph J. W.; Procter, David J. (2019). "SmI2-catalysed cyclization cascades by radical relay". Nature Catalysis. 2 (3): 211–218. doi:10.1038/s41929-018-0219-x. S2CID 104423773.
- ^ Machrouhi, Fouzia; Hamann, Béatrice; Namy, Jean-Louis; Kagan, Henri B. (1996). "Improved Reactivity of Diiodosamarium by Catalysis with Transition Metal Salts". Synlett. 1996 (7): 633–634. doi:10.1055/s-1996-5547.
- ^ Molander, G. A.; McKiie, J. A. (1992). "Samarium(II) iodide-induced reductive cyclization of unactivated olefinic ketones. Sequential radical cyclization/intermolecular nucleophilic addition and substitution reactions". J. Org. Chem. 57 (11): 3132–3139. doi:10.1021/jo00037a033.
- ^ Ankner, Tobias; Göran Hilmersson (2009). "Instantaneous Deprotection of Tosylamides and Esters with SmI2/Amine/Water". Organic Letters. American Chemical Society. 11 (3): 503–506. doi:10.1021/ol802243d. PMID 19123840.
- ^ Patrick G. Steel (2001). "Recent developments in lanthanide mediated organic synthesis". J. Chem. Soc., Perkin Trans. 1 (21): 2727–2751. doi:10.1039/a908189e.
- ^ Molander, G. A.; Harris, C. R. (1996). "Sequencing Reactions with Samarium(II) Iodide". Chem. Rev. 96 (1): 307–338. doi:10.1021/cr950019y. PMID 11848755.
- ^ K. C. Nicolaou; Shelby P. Ellery; Jason S. Chen (2009). "Samarium Diiodide Mediated Reactions in Total Synthesis". Angew. Chem. Int. Ed. 48 (39): 7140–7165. doi:10.1002/anie.200902151. PMC 2771673. PMID 19714695.
- ^ Procter, David J.; Flowers,II, Robert A.; Skydstrup, Troels (2009). Organic Synthesis Using Samarium Diiodide. Royal Society of Chemistry. ISBN 978-1-84755-110-8.

![{\displaystyle {\begin{array}{cl}{}\\{\ce {{Sm}+ ICH2I ->[{\ce {THF}}] SmI2}}+0.5{\ce {H2C=CH2}}\\{\ce {{Sm}+ I(CH2)2I ->[{\ce {THF}}] {SmI2}+ H2C=CH2}}\\{}\end{array}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/97016669936673b8c455d5ddaaef4bb5c8ff5667)