수두대상포진바이러스
Varicella zoster virus| 인간알파헤르페스바이러스3 | |
|---|---|
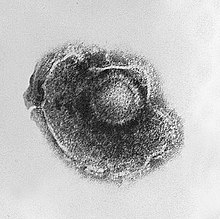 | |
| 인간 알파헤르페스 바이러스 3바이온의 전자 현미경 사진 | |
| 바이러스 분류 | |
| (순위 미지정): | 바이러스 |
| 영역: | 듀플로드나바이러스 |
| 왕국: | 흥공비래 |
| 문: | 페플로비리코타 |
| 클래스: | 헤르비비리케테스 |
| 주문: | 헤르페스바이랄레스 |
| 패밀리: | 헤르페스바이러스과 |
| 속: | 바리셀로바이러스 |
| 종류: | 인간알파헤르페스바이러스3 |
| 동의어 | |
인간 헤르페스 바이러스 3 (HHV-3, HHV3) 또는 인간 알파 헤르페스 바이러스 3 (택소노믹스적으로)라고도 알려진 수두 대상 바이러스 (VZV)는 인간을 감염시킬 수 있는 9개의 알려진 헤르페스 바이러스 중 하나이다.그것은 보통 어린이와 청소년에게 수두(수두)와 대상포진(대상포진)을 유발하지만 어린이에게는 드물게 발생한다.VZV 감염은 인간에 고유한 종이지만, 바이러스는 외부 환경에서 [3]몇 시간 동안 생존할 수 있다.
VZV는 폐에서 증식하여 다양한 증상을 일으킨다.1차 감염 후 바이러스는 뇌신경절, 배근신경절, 자율신경절 등 신경에 잠복한다.수두에서 회복된 지 몇 년이 지난 후, VZV는 신경학적 [4]상태를 일으키기 위해 다시 활성화될 수 있다.
역학
1차 수두 대상 바이러스 감염은 뇌염, 폐렴(직접 바이러스성 폐렴 또는 2차 세균성 폐렴) 또는 기관지염(바이러스성 기관지염 또는 2차 세균성 기관지염)을 포함한 합병증을 초래할 수 있다.수두의 임상 증상이 해결된 경우에도 VZV는 감염된 사람의 신경계(바이러스 잠복기), 삼차 및 배근 신경절에 [5]휴면 상태로 남아 있다.VZV는 호흡기를 통해 들어갑니다.10~21일의 잠복기를 가지며, 평균 14일이다.피부와 말초신경을 대상으로 한 질병 기간은 3~4일입니다.발진이 나타나기 1~2일 전에 이 바이러스가 가장 전염성이 높은 때이다.증상이나 증상에는 고름, 파열, 딱지가 차서 낫는 소포가 포함된다.병변은 얼굴, 목, 허리, 가슴, [6]어깨에서 가장 흔하게 발생한다.
약 1/3의 경우,[7] VZV는 나중에 다시 활성화되어 대상포진 또는 대상포진이라고 알려진 질병을 일으킨다.
대상포진 발병의 개인 평생 위험은 20-30% 또는 약 4명 중 1명꼴로 생각됩니다.그러나 85세 이상의 개인은 이 위험이 [8]2명 중 1명으로 증가한다.닐슨 외 연구진(2015)이 스웨덴에서 실시한 연구에 따르면 대상포진 감염의 연간 발생률은 모든 연령에서 인구 10만 명당 총 315명, 50세 [9]이상 인구 10만 명당 577명으로 추정된다.VZV는 또한 중추신경계를 감염시킬 수 있으며, 2013년 기사에 따르면 스위스의 인구 10만명당 1.02명의 발병률과 스웨덴의 [10]인구 10만명당 연간 발병률이 1.8명의 발병률을 보고한다.
대상포진 병변과 종종 화상으로 묘사되는 관련 통증은 거의 항상 신체의 한쪽에만 있는 하나 또는 두 개의 인접한 감각 신경에 의해 신경화된 피부에 발생하는 경향이 있습니다.피부 병변은 보통 몇 주 동안 가라앉는 반면, 통증은 종종 더 오래 지속된다.10~15%의 경우, 만성적이고 종종 헤르페스 후 신경통으로 알려진 장애인 3개월 이상 통증이 지속된다.수두 대상포진 감염의 다른 심각한 합병증에는 Mollaret의 수막염, 대상포진 다중포진, 그리고 뇌졸중,[11] 골수염, 안과 헤르페스, 또는 대상포진으로 이어지는 뇌 동맥의 염증이 포함됩니다.Ramsay Hunt 증후군에서는 VZV가 얼굴 신경의 특정 분기에 따라 병변을 일으키는 유전체 신경절에 영향을 미친다.증상에는 한쪽 얼굴의 약함과 청력 손실과 함께 혀와 귀에 고통스러운 물집이 생길 수 있다.임신 초기 단계에서 감염되면 태아에게 심각한 손상이 발생할 수 있습니다.레이 증후군은 초기 감염 후에 발생할 수 있으며, 지속적인 구토와 극심한 졸음이나 전투적인 행동과 같은 뇌 기능 부전의 징후를 일으킨다.어떤 경우에는 죽음이나 혼수가 뒤따를 수 있다.레이 증후군은 주로 어린이와 청소년들에게 영향을 미치는데, 감염 중에 아스피린을 사용하는 것은 이러한 [6]위험을 증가시킬 수 있다.
형태학
VZV는 많은 게놈 호몰로지를 공유하는 단순 헤르페스 바이러스(HSV)와 밀접하게 관련되어 있습니다.알려진 엔벨로프 당단백질(gB, gC, gE, gH, gI, gK, gL)은 HSV의 당단백질과 일치하지만 HSV gD와 동등한 것은 없다.또한 VZV는 HSV 지연(단순 헤르페스 바이러스)[12] 확립에 중요한 역할을 하는 LAT(레이텐시 관련 스크립트)를 생성하지 못합니다.VZV 비리온은 구형이며 직경은 180~200 nm입니다.그들의 지질 외피는 20면체 형태로 배열된 162개의 육중합체와 5중합체의 100nm 핵캡시드를 둘러싸고 있다.그것의 DNA는 125,000nt 길이의 단일 선형 이중사슬 분자이다.캡시드는 총칭하여 테그먼트라고 알려진 느슨하게 연관된 단백질에 의해 둘러싸여 있습니다; 이 단백질들 중 많은 것들이 감염된 세포에서 바이러스 번식의 과정을 시작하는데 중요한 역할을 합니다.테그먼트는 각각 약 8nm [13]길이의 비리온 외부에 표시되는 당단백질이 박힌 지질 엔벨로프로 덮여 있습니다.
게놈
이 섹션에서는 HSV와 마찬가지로 주석 ORF에 대한 정보가 누락되어 있습니다.(혹은 적어도 흥미로운 부분은 HSV와의 차이점) PMID20225013이 편리합니다.(2021년 11월) |
그 게놈은 [14]1986년에 처음으로 배열되었다.이것은 선형 이중 DNA 분자이며, 실험실 변종은 124,884개의 염기쌍을 가지고 있습니다.게놈은 S 세그먼트의 방향에 따라 P(프로토타입)와S I(반전 S)라는 2개의 주요 이성질체를 가지고 있으며, 이들은 총 90~95%의 동일한 빈도로 존재한다.L 세그먼트는 반전되어 총 4개의 선형 이성질체(IL 및LS I)가 생성될 수도 있습니다.이것은 HSV의 적합 분포와는 구별되며, 차별적 메커니즘은 알려져 있지 않다.고립된 분자의 소수는 원형 게놈이며, 알려진 것은 거의 없다. (HSV는 감염에 따라 순환하는 것으로 알려져 있다.)게놈에는 적어도 70개의 열린 판독 프레임이 있다.
진화
HSV1 및 HSV2와의 공통성은 공통의 조상을 나타낸다; 5개의 유전자(약 70개 중)는 대응하는 HSV 유전자를 가지고 있지 않다.다른 인간 헤르페스 바이러스와의 관계는 덜 강하지만, 많은 호몰로지와 보존된 유전자 블록이 여전히 발견됩니다.
이 [15]바이러스는 적어도 5군데가 있다.분지 1 및 3은 유럽/북미 균주를 포함하고, 분지 2는 아시아 균주, 특히 일본에서 온 균주이며, 분지 5는 인도를 거점으로 하는 것으로 보인다.Clade 4는 유럽에서 온 균주를 포함하고 있지만, 그 지리적 기원은 더 명확히 할 필요가 있다.또한 이러한 [16]분류군에 맞지 않는 4가지 유전자형이 있다.전체 바이러스 게놈의 필요한 염기서열을 복제하기 위한 VZV 균주의 할당.실질적으로 글로벌 VZV 균주 분포에 관한 모든 분자 역학 데이터는 선택된 영역의 표적 시퀀싱에 의해 얻어진다.
VZV 게놈 배열의 계통학적 분석은 야생형 균주를 9개의 유전자형(E1, E2, J, M1, M2, M3, M4, VII 및 [17][18]IX)으로 분해한다.M3 및 M4 균주에 대한 완전한 배열을 이용할 수 없지만, 대표 균주의 표적 분석에 따르면 균주는 안정적이고 순환하는 VZV 유전자형입니다.VZV 분리물의 시퀀스 분석은 모든 유전자형에 대해 공유 마커와 특정 마커를 모두 식별했으며 통합된 VZV 유전자형 전략을 검증했다.높은 유전자형 다양성에도 불구하고 유전자형 내 재조합의 증거는 관찰되지 않았다.7개의 VZV 유전자형 중 5개는 ORF22에 존재하는 4개의 단일 뉴클레오티드 다형(SNP)만을 사용하여 신뢰성 있게 식별되었으며, E1 및 E2 유전자형은 ORF21, ORF22 또는 ORF50에 위치한 SNP를 사용하여 분해되었다.유럽 18개국의 342개 임상 수두 및 대상 검체의 시퀀스 분석 결과, VZV 유전자형의 분포는 E1, 221(65%), E2, 87(25%), M1, 20(6%), M2, 3(1%), M4, 11(3%)이었다.M3 또는 J 균주는 [17]관찰되지 않았다.이 접근방식을 사용하여 호주와 뉴질랜드의 임상 수두 및 대상 격리체 165개 중, 동부 호주 격리체 127개 중 67개, E2, 16개, J, 10개, M2, 4개였다. 뉴질랜드 격리체 38개 중 25개는 E1, 8개는 E2,[19] 5개는 M1이었다.
헤르페스 바이러스 사이의 동의어 및 비익명 돌연변이율에 대한 돌연변이율은 고도로 보존된 gB [20]유전자를 바탕으로 각각 1 × 10−7 및 2.7 × 10−8 돌연변이/사이트/년 단위로 추정되었다.
치료
인체 내에서는 수두용 아시클로비르, 팜시클로비르, 대상포진용 발라시클로비르, 대상면역글로불린(ZIG) 및 비다라빈을 [21]포함한 많은 약물과 치료제에 의해 치료될 수 있다.애시클로버는 1차 VZV 감염에서 선택된 약물로 자주 사용되며, 조기에 투여를 시작하면 모든 증상의 지속 기간을 크게 단축할 수 있습니다.그러나 효과적인 혈청 농도의 아시클로빌에 도달하려면 정맥 내 투여가 필요하며,[22] 병원 밖에서 사용하는 것이 더 어렵습니다.
예방 접종
활성 감쇠 VZV Oka/Merck 균주 백신을 사용할 수 있으며, 미국에서 Varivax라는 상표명으로 판매되고 있습니다.1980년대 Merck, Sharp, Dohme가 1970년대 다카하시 미치아키와 동료들에 의해 분리·감쇠된 오카 변종 바이러스로부터 개발했다.1990년 미국 식품의약국에 승인을 요청했고 1995년에 승인되었다.그 이후로, 그것은 호주, 미국, 그리고 많은 다른 나라들의 어린이들에게 권장되는 백신 접종 일정에 추가되었다.수두 예방접종은 백신에 의해 유발되는 면역력이 평생이 아닐 수 있다는 우려를 불러일으켰고, 어린 시절 예방접종에 대한 면역력이 떨어짐에 따라 성인들이 더 심각한 질병에 취약해질 수 있다.백신 접종을 권장하는 인구에서 미국의 백신 커버리지가 90%에 육박하고 있으며, VZV로 [citation needed]인한 수두 발병률 및 입원 및 사망률 감소가 동반되고 있다.지금까지 임상 데이터는 백신이 건강한 사람의 수두 감염을 예방하는 데 10년 이상 효과가 있다는 것을 증명했으며 획기적인 감염이 발생했을 때 질병은 일반적으로 경미하다.[23]2006년 CDC의 예방접종실천자문위원회(ACIP)는 높은 수준의 [24]수두면역을 유지하기 위해 입학 전에 두 번째 백신 접종을 권고했다.
2006년 미국 식품의약국은 대상포진 예방을 위해 조스타박스를 승인했다.조스타박스는 나이가 들수록 VZV에 대한 면역력이 떨어지는 노년층에서 면역 반응을 유도하기 위해 고안된 보다 농축된 Varivax 백신이다.Cochrane Library의 체계적인 검토에 따르면 Zostavax는 대상포진의 발생률을 거의 50%[25]까지 감소시킵니다.
신트릭스는 GlaxoSmithKline이 개발한 V. 대상 서브유닛 백신(당단백질 E)으로 2017년 [26]10월 FDA에 의해 미국에서 승인되었다.ACIP는 이미 조스타박스를 접종한 사람들을 포함하여 50세 이상의 성인들에게 신트릭스를 추천했다.위원회는 3단계 임상 데이터가 대상포진에 대해 90% 이상의 백신 효과를 나타냈을 뿐만 아니라 4년간의 후속 조치 동안 지속적인 효과를 나타냈기 때문에 대상포진 및 관련 합병증 예방을 위해 Singrix가 Zostavax보다 더 낫다고 투표했다.1회 주사제로 투여되는 조스타박스와 달리 신트릭스는 2개월에서 6개월 간격으로 [27]근육 내 투여된다.이 백신은 인간 면역 결핍 [28]바이러스에 감염된 성인들에게 면역 유발적이고 안전한 것으로 나타났다.
역사
수두와 유사한 발진은 고대 문명에 의해 인식되고 기술되었다;[29] 대상과 수두 사이의 관계는 1888년까지 실현되지 않았다.1943년 대상포진의 병변에서 분리된 바이러스 입자와 수두에서 분리된 바이러스 입자의 유사성이 발견되었다.[30]1974년에 최초의 수두 백신이 [31]도입되었다.어원: "헤르페스바이러스과의 일원인 수두대상포진바이러스(VZV)는 그것이 일으키는 두 가지 주요 질병(치킨두와 헤르페스대상포진)의 이름을 따서 명명되었다.수두는 천연두의 가벼운 형태로 여겨졌기 때문에 "바리솔라"의 작은 형태일 수 있다."바리올라"는 1764년 루돌프 아우구스틴 보겔에 의해 만들어졌으며 라틴어 바루스("pimple") 또는 바리투스("spickle")에서 유래한 것으로 보인다.대상포진은 그리스어로 헤르페인과 대상포진에서 유래했다.20세기가 되어서야 VZV가 이 [32]두 질병의 원인으로 인식되었습니다."
「 」를 참조해 주세요.
레퍼런스
- ^ "ICTV 9th Report (2011) Herpesviridae". International Committee on Taxonomy of Viruses (ICTV). Retrieved 9 January 2019.
Human herpesvirus 3 Human herpesvirus 3 [X04370=NC_001348] (HHV-3) (Varicella-zoster virus)
- ^ "ICTV Taxonomy history: Human alphaherpesvirus 3". International Committee on Taxonomy of Viruses (ICTV). Retrieved 9 January 2019.
- ^ "Pathogen Safety Data Sheets: Infectious Substances – Varicella-zoster virus". canada.ca. Pathogen Regulation Directorate, Public Health Agency of Canada. 2012-04-30. Retrieved 2017-10-10.
- ^ Nagel MA, Gilden DH (July 2007). "The protean neurologic manifestations of varicella-zoster virus infection". Cleveland Clinic Journal of Medicine. 74 (7): 489–94, 496, 498–9 passim. doi:10.3949/ccjm.74.7.489. PMID 17682626.
- ^ Steiner I, Kennedy PG, Pachner AR (November 2007). "The neurotropic herpes viruses: herpes simplex and varicella-zoster". The Lancet. Neurology. 6 (11): 1015–28. doi:10.1016/S1474-4422(07)70267-3. PMID 17945155. S2CID 6691444.
- ^ a b Tortora G. Microbiology: An Introduction. Pearson. pp. 601–602.
- ^ Harpaz, R; Ortega-Sanchez, IR; Seward, JF (6 June 2008). "Prevention of herpes zoster: recommendations of the Advisory Committee on Immunization Practices (ACIP)". Morbidity and Mortality Weekly Report (MMWR). 57 (RR-5): 1–30, quiz CE2-4. PMID 18528318.
- ^ Pinchinat, Sybil; Cebrián-Cuenca, Ana M; Bricout, Hélène; Johnson, Robert W (December 2013). "Similar herpes zoster incidence across Europe: results from a systematic literature review". BMC Infectious Diseases. 13 (1): 170. doi:10.1186/1471-2334-13-170. PMC 3637114. PMID 23574765.
- ^ Nilsson, Jonas; Cassel, Tobias; Lindquist, Lars (22 May 2015). "Burden of herpes zoster and post-herpetic neuralgia in Sweden". BMC Infectious Diseases. 15: 215. doi:10.1186/s12879-015-0951-7. PMC 4493830. PMID 26002038.
- ^ Becerra JC, Sieber R, Martinetti G, Costa ST, Meylan P, Bernasconi E (July 2013). "Infection of the central nervous system caused by varicella zoster virus reactivation: a retrospective case series study". International Journal of Infectious Diseases. 17 (7): e529-34. doi:10.1016/j.ijid.2013.01.031. PMID 23566589.
- ^ Nagel MA, Cohrs RJ, Mahalingam R, Wellish MC, Forghani B, Schiller A, et al. (March 2008). "The varicella zoster virus vasculopathies: clinical, CSF, imaging, and virologic features". Neurology. 70 (11): 853–60. doi:10.1212/01.wnl.0000304747.38502.e8. PMC 2938740. PMID 18332343.
- ^ Arvin AM (July 1996). "Varicella-zoster virus". Clinical Microbiology Reviews. 9 (3): 361–81. doi:10.1128/CMR.9.3.361. PMC 172899. PMID 8809466.
- ^ Han DH (25 October 2017). "General Characteristics and Epidemiology of varicella-zoster virus (VZV)". The Lecturio Medical Concept Library. Medical Professionals Reference (MPR). Retrieved 2021-06-14.
- ^ Davison AJ, Scott JE (September 1986). "The complete DNA sequence of varicella-zoster virus". The Journal of General Virology. 67 ( Pt 9) (9): 1759–816. doi:10.1099/0022-1317-67-9-1759. PMID 3018124.
- ^ Chow VT, Tipples GA, Grose C (August 2013). "Bioinformatics of varicella-zoster virus: single nucleotide polymorphisms define clades and attenuated vaccine genotypes". Infection, Genetics and Evolution. 18: 351–6. doi:10.1016/j.meegid.2012.11.008. PMC 3594394. PMID 23183312.
- ^ Grose C (September 2012). "Pangaea and the Out-of-Africa Model of Varicella-Zoster Virus Evolution and Phylogeography". Journal of Virology. 86 (18): 9558–65. doi:10.1128/JVI.00357-12. PMC 3446551. PMID 22761371.
- ^ a b Loparev VN, Rubtcova EN, Bostik V, Tzaneva V, Sauerbrei A, Robo A, et al. (January 2009). "Distribution of varicella-zoster virus (VZV) wild-type genotypes in northern and southern Europe: evidence for high conservation of circulating genotypes". Virology. 383 (2): 216–25. doi:10.1016/j.virol.2008.10.026. PMID 19019403.
- ^ Zell R, Taudien S, Pfaff F, Wutzler P, Platzer M, Sauerbrei A (February 2012). "Sequencing of 21 varicella-zoster virus genomes reveals two novel genotypes and evidence of recombination". Journal of Virology. 86 (3): 1608–22. doi:10.1128/JVI.06233-11. PMC 3264370. PMID 22130537.
- ^ Loparev VN, Rubtcova EN, Bostik V, Govil D, Birch CJ, Druce JD, et al. (December 2007). "Identification of five major and two minor genotypes of varicella-zoster virus strains: a practical two-amplicon approach used to genotype clinical isolates in Australia and New Zealand". Journal of Virology. 81 (23): 12758–65. doi:10.1128/JVI.01145-07. PMC 2169114. PMID 17898056.
- ^ McGeoch DJ, Cook S (April 1994). "Molecular phylogeny of the alphaherpesvirinae subfamily and a proposed evolutionary timescale". Journal of Molecular Biology. 238 (1): 9–22. doi:10.1006/jmbi.1994.1264. PMID 8145260.
- ^ Centers for Disease Control Prevention (CDC) (March 2012). "FDA approval of an extended period for administering VariZIG for postexposure prophylaxis of varicella" (PDF). MMWR. Morbidity and Mortality Weekly Report. 61 (12): 212. PMID 22456121.
- ^ Cornelissen CN (2013). Lippincott's illustrated reviews: Microbiology (3rd ed.). Philadelphia: Lippincott Williams & Wilkins Health. pp. 255–272.
- ^ "Prevention of varicella: Recommendations of the Advisory Committee on Immunization Practices (ACIP). Centers for Disease Control and Prevention". MMWR. Recommendations and Reports. 45 (RR-11): 1–36. July 1996. PMID 8668119.
- ^ Marin M, Güris D, Chaves SS, Schmid S, Seward JF (June 2007). "Prevention of varicella: recommendations of the Advisory Committee on Immunization Practices (ACIP)". MMWR. Recommendations and Reports. 56 (RR-4): 1–40. PMID 17585291.
- ^ Gagliardi AM, Andriolo BN, Torloni MR, Soares BG, de Oliveira Gomes J, Andriolo RB, Canteiro Cruz E (November 2019). "Vaccines for preventing herpes zoster in older adults". The Cochrane Database of Systematic Reviews. 2019 (11). doi:10.1002/14651858.CD008858.pub4. PMC 6836378. PMID 31696946.
- ^ Gruber MF (20 October 2017). "Biologics License Application (BLA) for Zoster Vaccine Recombinant, Adjuvant" (PDF). Office of Vaccines Research and Review, Center for Biologics Evaluation and Research, US Food and Drug Administration. Retrieved 16 November 2018.
- ^ Han HD (25 October 2017). "ACIP: New Vaccine Recommendations for Shingles Prevention". Medical Professionals Reference (MPR). Retrieved October 30, 2017.
- ^ Berkowitz EM, Moyle G, Stellbrink HJ, Schürmann D, Kegg S, Stoll M, et al. (April 2015). "Safety and immunogenicity of an adjuvanted herpes zoster subunit candidate vaccine in HIV-infected adults: a phase 1/2a randomized, placebo-controlled study". The Journal of Infectious Diseases. 211 (8): 1279–87. doi:10.1093/infdis/jiu606. PMC 4371767. PMID 25371534.
- ^ Wood MJ (October 2000). "History of Varicella Zoster Virus". Herpes: The Journal of the IHMF. 7 (3): 60–65. PMID 11867004.
- ^ Ruska H (1943). "Über das Virus der Varicellen und des Zoster". Klin Wochenschr. 22 (46–47): 703–704. doi:10.1007/bf01768631. S2CID 11118674.
- ^ Takahashi M, Otsuka T, Okuno Y, Asano Y, Yazaki T (November 1974). "Live vaccine used to prevent the spread of varicella in children in hospital". Lancet. 2 (7892): 1288–90. doi:10.1016/s0140-6736(74)90144-5. PMID 4139526.
- ^ "Etymologia: Varicella Zoster Virus". Emerging Infectious Diseases. 21 (4): 698. 2015. doi:10.3201/eid2104.ET2104. PMC 4378502.
외부 링크
- "Varicella (Chickenpox) Vaccination". Centers for Disease Control and Prevention (CDC). 2017-07-07.


