UGT2B7
UGT2B7| UGT2B7 | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
| |||||||||||||
| 식별자 | |||||||||||||
| 별칭 | UGT2B7, UDPGT 2B9, UDPGT2B7, UDPGTH2, UGT2B9, UDP 글루코노실전달효소 패밀리 2 멤버 B7, UDPGT 2B7, UDPGTh-2 | ||||||||||||
| 외부 ID | OMIM: 600068 MGI: 3576103 HomoloGene: 128251 GeneCard: UGT2B7 | ||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| 직교체 | |||||||||||||
| 종 | 인간 | 마우스 | |||||||||||
| 엔트레스 | |||||||||||||
| 앙상블 | |||||||||||||
| 유니프로트 |
| ||||||||||||
| RefSeq(mRNA) | |||||||||||||
| RefSeq(단백질) |
| ||||||||||||
| 위치(UCSC) | Chr 4: 69.05 – 69.11Mb | n/a | |||||||||||
| PubMed 검색 | [2] | [3] | |||||||||||
| 위키다타 | |||||||||||||
| |||||||||||||
UGT2B7(UDP-Glucuronosyl transferase-2B7)은 하부 위장의 간, 신장, 상피세포에서 활성 상태인 것으로 발견된 2상 대사 이소엔자임이며 뇌에서도 보고된 바 있다. 인간에서 UDP-Glucuronosyl transferase-2B7은 UGT2B7 유전자에 의해 암호화된다.[4][5]
함수
UGT는 잠재적으로 독성이 있는 유전생균제와 내생성 화합물의 결합과 후속 제거에 중요한 역할을 한다. UGT2B7은 3,4-카테콜 에스트로겐과 에스트리올에 대한 독특한 특수성을 가지고 있어, 이 강력한 에스트로겐 대사물의 수준과 활동을 조절하는 데 중요한 역할을 할 수 있음을 시사한다.
이 효소는 세포의 내소성 망막과 핵막에 위치한다. 그 기능은 우리딘 디프인산 글루쿠로닉산을 사용하여 글루쿠로닉산과 다양한 종류의 지방질 아글리콘 기판의 결합을 촉진하는 것이다.
UGT2B4와 함께 UGT2B7은 간에 있는 효소 효소 효소균산 글루코시딩이 가능하지만, 2B4 이소형과 달리 2B7은 다양한 스테로이드 호르몬(안드로스테론, 에피스토스테론)과 지방산도 글루코시딩이 가능하다.[6][7] 또한 진통제(몰핀), 카르복실성 비스테로이드성 항염증제(케토프로펜), 안티카르시노균제(올트랜티노산) 등 주요 등급의 약물을 혼합할 수 있다.[7] UGT2B7은 모르핀, 코딘, 노르코딘 등의 대사 작용을 담당하는 주요 효소 이소폼과 이에 상응하는 3-글루쿠로니드 및 6-글루쿠로니드 아편물의 다른 아편이다. 예를 들어 모르핀 신진대사는 진통 효과가 없는 모르핀-3-글루쿠로니드(M3G)와 진통 효과가 모르핀보다 더 강한 모르핀-6-글루쿠로니드(M6G)를 생산한다.[8][9] 그 결과 UGT2B7의 변화된 활성도는 모르핀의 효과와 부작용뿐만 아니라 일부 관련 아편제에도 크게 영향을 미칠 수 있다.[10][11][12][13][14]
구조
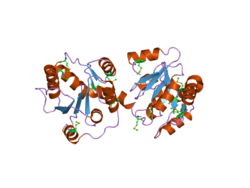
완전한 인간 UGT 효소의 구조는 아직 결정되지 않았지만, Miley 외 연구진은 복합체에서 Rossman과 같은 접힌 두 개의 조광 도메인을 보여주는 C-단자 부분의 부분 UGT2B7 구조를 해결했다.[15][16] Rossman 폴드는 일반적으로 뉴클레오티드 기판을 결합하는데, 이 경우 UGT2B7에 의한 글루쿠론화 작업에 관여하는 UDP-글루쿠론산 공동 인자. 일반적으로 UGT 효소의 C-terminus는 보존도가 높아 UDP-글루쿠론산 코팩터를 결합하는 반면, N-terminus(이 구조에서 분해되지 않음)는 기질 결합을 담당한다.[17] 이 첫 번째 분해된 구조는 두 번째 다이머의 UDP-글루쿠론산 결합 부지에 투영된 두 다이머 중 하나의 C-단자(C-terminus)를 나타내므로 두 번째 다이머는 비효과적인 것으로 나타났다.
추가 연구에서는 UGT 효소 다형성의 조광화를 연구했으며 호모디머와 이성애자(UGT2B7의 유전자 다형성 또는 UGT1A1과 같은 다른 UGT 효소) 형성이 모두 가능하다는 것을 발견했으며, 일부 조합은 효소 활성도에 영향을 미친다.[18]
유전적 다형성
UGT2B7은 다형성 유전자로 간주된다.[18] 다양한 연구 노력은 이러한 다형성 변종이 UGT2B7의 글루쿠로니드화 활동에 미치는 잠재적 영향과 특히 항암 치료를 포함한 투여된 약물의 통관에 대해 연구해왔다. 유전자변형 UGT2B7에 의한 글루쿠로니화 활성 감소는 환자의 장기 특히 간에서 잔류하는 약물의 수치가 증가하거나 축적되어 독성이 증가될 수 있는 반면, 활성도가 증가하면 신체 내 기대치보다 낮아져 투여 요법의 효능이 저하될 수 있다.
한 연구에서는 벤지딘에 노출된 한족 염색산업 종사자들이 UGT2B7 단일 뉴클레오티드 다형성(SNP) C802T로 His268Tyr를 부호화하면 방광암 발병 위험이 더 높은 것으로 나타났다.[19] 잔류물 268에서 히스티딘 대 티로신 돌연변이는 UGT2B7의 N-터미널 부분에 위치하며, UDP-글루쿠론산을 결합하는 C-terminus와는 반대로 이질적인 생물학적 기질을 결합한다. 이러한 암 위험 증가에 대한 추측 메커니즘은 돌연변이 UGT2B7에 의한 벤지딘의 글루쿠로니딘의 글루쿠로니드화 증가와 함께 소변 pH 수준에서 글루쿠론화 벤지딘의 갈라짐으로 인해 방광에 더 높은 농도의 벤지딘이 방출되었다. 또 다른 연구에서는 대장암의 위험이 있는 변종 UGT2B7 G900A와 유사한 연관성을 찾았지만 유의미한 연관성은 발견되지 않았다.[20]
비소세포 폐암 환자의 홍반 간극 연구는 UGT2B7의 홍반 억제에서 알로티닙을 잠재적으로 대사하는 UGT2B7의 SNP에 대해 통계적 유의성을 보이지 않았다.[21] 심각한 약물유발성 간 손상을 일으킬 수 있는 비스테로이드성 항염증제(NSAID) 디클로페낙의 간극을 조사한 결과, C802T SNP를 가진 돌연변이 UGT2B7의 간극이 야생형 UGT27B보다 6배 낮아서 이 돌연변이를 가진 환자의 간 독성 증대에 기여할 가능성이 있는 것으로 나타났다.[22] 결핵성 약물유발성 간손상(ATLI)에서 UGT2B7의 유전자 다형성 분석 결과, 연구 대상 모집단에서 UGT2B7 돌연변이와 ATLI의 돌연변이는 아무런 연관성도 발견되지 않았다.[23]
UGT2B7도 글루쿠로니데이션(glukuronidation)을 통한 오피오이드의 신진대사에 관여하는 것으로 알려져 있으며, 부프레노핀의 진통 효능에 대한 다형성(polymorphism)의 영향을 조사한 결과 돌연변이 C802T가 흉부 수술 후 부프레노핀에 대한 진통반응을 특히 긴 시간(48시간)으로 악화시켰다.e 이 오래 지속되는 오피오이드는 효과를 유지하도록 의도되었다.[24] 이와 동일한 변종이 간질 환자에게 투여되는 발프로산의 혈장 농도에 유의미한 영향을 미치는 것으로 별도로 발견되었으며, 이는 이 협치열 창 치료로 보이는 개별적 변동성의 일부를 설명할 수 있다.[25] 이 두 경우 모두 C802T 다형성 UGT2B7의 글루쿠로니화 활성 증가 때문에 약물 화합물 농도가 감소했음을 나타낸다.
UGT2B7은 많은 유전생물성분들의 글루쿠로니화에 관여하고 있으며 UGT2B7의 다형성이 약리학적 관련성분들의 간극에 미치는 잠재적 영향에 대한 연구는 다양한 연구에서 보여지듯이 종종 관심의 대상이 된다. 예를 들어, UGT2B7 C802T 다형성은 아시아에서 73%의 유병률과 백인에서 46%의 유병률로 주목되어 왔으며, 따라서 이러한 다형성의 영향은 인구의 많은 부분에 영향을 미칠 수 있다.[26] 그러나, 모든 연구가 이러한 유전적 다형성 때문에 간극에서 유의미한 변화를 발견하는 것은 아니다. 이것이 UGT2B7의 효소 활성도에 영향을 미치지 않는 특정 다형성 때문인지, 또는 UGT2B7 활성의 변화에 따른 차이를 가릴 수 있는 다양한 경로에 의해 관심 화합물이 대사되기 때문인지는 항상 명확하지 않다.
참조
- ^ Jump up to: a b c GRCh38: 앙상블 릴리스 89: ENSG00000171234 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Ritter JK, Sheen YY, Owens IS (May 1990). "Cloning and expression of human liver UDP-glucuronosyltransferase in COS-1 cells. 3,4-catechol estrogens and estriol as primary substrates". The Journal of Biological Chemistry. 265 (14): 7900–6. doi:10.1016/S0021-9258(19)39016-7. PMID 2159463.
- ^ Monaghan G, Clarke DJ, Povey S, See CG, Boxer M, Burchell B (September 1994). "Isolation of a human YAC contig encompassing a cluster of UGT2 genes and its regional localization to chromosome 4q13". Genomics. 23 (2): 496–9. doi:10.1006/geno.1994.1531. PMID 7835904.
- ^ Mackenzie P, Little JM, Radominska-Pandya A (February 2003). "Glucosidation of hyodeoxycholic acid by UDP-glucuronosyltransferase 2B7". Biochemical Pharmacology. 65 (3): 417–21. doi:10.1016/S0006-2952(02)01522-8. PMID 12527334.
- ^ Jump up to: a b Barre L, Fournel-Gigleux S, Finel M, Netter P, Magdalou J, Ouzzine M (March 2007). "Substrate specificity of the human UDP-glucuronosyltransferase UGT2B4 and UGT2B7. Identification of a critical aromatic amino acid residue at position 33". The FEBS Journal. 274 (5): 1256–64. doi:10.1111/j.1742-4658.2007.05670.x. PMID 17263731. S2CID 27151203.
- ^ Coffman BL, Rios GR, King CD, Tephly TR (January 1997). "Human UGT2B7 catalyzes morphine glucuronidation". Drug Metabolism and Disposition. 25 (1): 1–4. PMID 9010622.
- ^ van Dorp EL, Romberg R, Sarton E, Bovill JG, Dahan A (June 2006). "Morphine-6-glucuronide: morphine's successor for postoperative pain relief?". Anesthesia and Analgesia. 102 (6): 1789–97. doi:10.1213/01.ane.0000217197.96784.c3. PMID 16717327. S2CID 18890026.
- ^ Coller JK, Christrup LL, Somogyi AA (February 2009). "Role of active metabolites in the use of opioids". European Journal of Clinical Pharmacology. 65 (2): 121–39. doi:10.1007/s00228-008-0570-y. PMID 18958460. S2CID 9977741.
- ^ Fujita K, Ando Y, Yamamoto W, Miya T, Endo H, Sunakawa Y, Araki K, Kodama K, Nagashima F, Ichikawa W, Narabayashi M, Akiyama Y, Kawara K, Shiomi M, Ogata H, Iwasa H, Okazaki Y, Hirose T, Sasaki Y (January 2010). "Association of UGT2B7 and ABCB1 genotypes with morphine-induced adverse drug reactions in Japanese patients with cancer". Cancer Chemotherapy and Pharmacology. 65 (2): 251–8. doi:10.1007/s00280-009-1029-2. PMID 19466410. S2CID 2712957.
- ^ Abildskov K, Weldy P, Garland M (April 2010). "Molecular cloning of the baboon UDP-glucuronosyltransferase 2B gene family and their activity in conjugating morphine". Drug Metabolism and Disposition. 38 (4): 545–53. doi:10.1124/dmd.109.030635. PMC 2845934. PMID 20071451.
- ^ Pergolizzi JV, Raffa RB, Gould E (September 2009). "Considerations on the use of oxymorphone in geriatric patients". Expert Opinion on Drug Safety. 8 (5): 603–13. doi:10.1517/14740330903153854. PMID 19614559. S2CID 12446624.
- ^ Rouguieg K, Picard N, Sauvage FL, Gaulier JM, Marquet P (January 2010). "Contribution of the different UDP-glucuronosyltransferase (UGT) isoforms to buprenorphine and norbuprenorphine metabolism and relationship with the main UGT polymorphisms in a bank of human liver microsomes". Drug Metabolism and Disposition. 38 (1): 40–5. doi:10.1124/dmd.109.029546. PMID 19841060. S2CID 17826299.
- ^ Lampe JN (2017). "Advances in the Understanding of Protein-Protein Interactions in Drug Metabolizing Enzymes through the Use of Biophysical Techniques". Frontiers in Pharmacology. 8: 521. doi:10.3389/fphar.2017.00521. PMC 5550701. PMID 28848438.
- ^ Miley MJ, Zielinska AK, Keenan JE, Bratton SM, Radominska-Pandya A, Redinbo MR (June 2007). "Crystal structure of the cofactor-binding domain of the human phase II drug-metabolism enzyme UDP-glucuronosyltransferase 2B7". Journal of Molecular Biology. 369 (2): 498–511. doi:10.1016/j.jmb.2007.03.066. PMC 1976284. PMID 17442341.
- ^ Yuan L, Qian S, Xiao Y, Sun H, Zeng S (May 2015). "Homo- and hetero-dimerization of human UDP-glucuronosyltransferase 2B7 (UGT2B7) wild type and its allelic variants affect zidovudine glucuronidation activity". Biochemical Pharmacology. 95 (1): 58–70. doi:10.1016/j.bcp.2015.03.002. PMID 25770680.
- ^ Jump up to: a b Yuan LM, Gao ZZ, Sun HY, Qian SN, Xiao YS, Sun LL, Zeng S (November 2016). "Inter-isoform Hetero-dimerization of Human UDP-Glucuronosyltransferases (UGTs) 1A1, 1A9, and 2B7 and Impacts on Glucuronidation Activity". Scientific Reports. 6: 34450. Bibcode:2016NatSR...634450Y. doi:10.1038/srep34450. PMC 5114717. PMID 27857056.
- ^ Lin GF, Guo WC, Chen JG, Qin YQ, Golka K, Xiang CQ, Ma QW, Lu DR, Shen JH (May 2005). "An association of UDP-glucuronosyltransferase 2B7 C802T (His268Tyr) polymorphism with bladder cancer in benzidine-exposed workers in China". Toxicological Sciences. 85 (1): 502–6. doi:10.1093/toxsci/kfi068. PMID 15615884.
- ^ Falkowski S, Woillard JB, Postil D, Tubiana-Mathieu N, Terrebonne E, Pariente A, Smith D, Guimbaud R, Thalamas C, Rouguieg-Malki K, Marquet P, Picard N (December 2017). "Common variants in glucuronidation enzymes and membrane transporters as potential risk factors for colorectal cancer: a case control study". BMC Cancer. 17 (1): 901. doi:10.1186/s12885-017-3728-0. PMC 5745594. PMID 29282011.
- ^ Endo-Tsukude C, Sasaki JI, Saeki S, Iwamoto N, Inaba M, Ushijima S, Kishi H, Fujii S, Semba H, Kashiwabara K, Tsubata Y, Hayashi M, Kai Y, Saito H, Isobe T, Kohrogi H, Hamada A (2018-01-01). "Population Pharmacokinetics and Adverse Events of Erlotinib in Japanese Patients with Non-small-cell Lung Cancer: Impact of Genetic Polymorphisms in Metabolizing Enzymes and Transporters". Biological & Pharmaceutical Bulletin. 41 (1): 47–56. doi:10.1248/bpb.b17-00521. PMID 29311482.
- ^ Lazarska KE, Dekker SJ, Vermeulen NP, Commandeur JN (March 2018). "Effect of UGT2B7*2 and CYP2C8*4 polymorphisms on diclofenac metabolism". Toxicology Letters. 284: 70–78. doi:10.1016/j.toxlet.2017.11.038. PMID 29203276.
- ^ Chen G, Wu SQ, Feng M, Wang Y, Wu JC, Ji GY, Zhang MM, Liu QQ, He JQ (December 2017). "Association of UGT2B7 polymorphisms with risk of induced liver injury by anti-tuberculosis drugs in Chinese Han". International Journal of Immunopathology and Pharmacology. 30 (4): 434–438. doi:10.1177/0394632017733638. PMC 5806809. PMID 28934901.
- ^ Sastre JA, Varela G, López M, Muriel C, González-Sarmiento R (January 2015). "Influence of uridine diphosphate-glucuronyltransferase 2B7 (UGT2B7) variants on postoperative buprenorphine analgesia". Pain Practice. 15 (1): 22–30. doi:10.1111/papr.12152. PMID 24256307. S2CID 33996517.
- ^ Sun YX, Zhuo WY, Lin H, Peng ZK, Wang HM, Huang HW, Luo YH, Tang FQ (August 2015). "The influence of UGT2B7 genotype on valproic acid pharmacokinetics in Chinese epilepsy patients". Epilepsy Research. 114: 78–80. doi:10.1016/j.eplepsyres.2015.04.015. PMID 26088889. S2CID 39744204.
- ^ Lampe JW, Bigler J, Bush AC, Potter JD (March 2000). "Prevalence of polymorphisms in the human UDP-glucuronosyltransferase 2B family: UGT2B4(D458E), UGT2B7(H268Y), and UGT2B15(D85Y)". Cancer Epidemiology, Biomarkers & Prevention. 9 (3): 329–33. PMID 10750673.
추가 읽기
- Kwara A, Lartey M, Boamah I, Rezk NL, Oliver-Commey J, Kenu E, Kashuba AD, Court MH (September 2009). "Interindividual variability in pharmacokinetics of generic nucleoside reverse transcriptase inhibitors in TB/HIV-coinfected Ghanaian patients: UGT2B7*1c is associated with faster zidovudine clearance and glucuronidation". Journal of Clinical Pharmacology. 49 (9): 1079–90. doi:10.1177/0091270009338482. PMC 2749505. PMID 19628728.
- Hwang MS, Lee SJ, Jeong HE, Lee S, Yoo MA, Shin JG (2010). "Genetic variations in UDP-glucuronosyltransferase 2B7 gene (UGT2B7) in a Korean population". Drug Metabolism and Pharmacokinetics. 25 (4): 398–402. doi:10.2133/dmpk.DMPK-10-SC-021. PMID 20814162.
- Rose JE, Behm FM, Drgon T, Johnson C, Uhl GR (2010). "Personalized smoking cessation: interactions between nicotine dose, dependence and quit-success genotype score". Molecular Medicine. 16 (7–8): 247–53. doi:10.2119/molmed.2009.00159. PMC 2896464. PMID 20379614.
- Holmes MV, Shah T, Vickery C, Smeeth L, Hingorani AD, Casas JP (December 2009). "Fulfilling the promise of personalized medicine? Systematic review and field synopsis of pharmacogenetic studies". PLOS ONE. 4 (12): e7960. Bibcode:2009PLoSO...4.7960H. doi:10.1371/journal.pone.0007960. PMC 2778625. PMID 19956635.
- Kwara A, Lartey M, Sagoe KW, Kenu E, Court MH (October 2009). "CYP2B6, CYP2A6 and UGT2B7 genetic polymorphisms are predictors of efavirenz mid-dose concentration in HIV-infected patients". AIDS. 23 (16): 2101–6. doi:10.1097/QAD.0b013e3283319908. PMC 2875867. PMID 19779319.
- Setlur SR, Chen CX, Hossain RR, Ha JS, Van Doren VE, Stenzel B, Steiner E, Oldridge D, Kitabayashi N, Banerjee S, Chen JY, Schäfer G, Horninger W, Lee C, Rubin MA, Klocker H, Demichelis F (January 2010). "Genetic variation of genes involved in dihydrotestosterone metabolism and the risk of prostate cancer" (PDF). Cancer Epidemiology, Biomarkers & Prevention. 19 (1): 229–39. doi:10.1158/1055-9965.EPI-09-1018. PMID 20056642. S2CID 11725521.
- Sánchez MB, Herranz JL, Leno C, Arteaga R, Oterino A, Valdizán EM, Nicolás JM, Adín J, Armijo JA (March 2010). "Genetic factors associated with drug-resistance of epilepsy: relevance of stratification by patient age and aetiology of epilepsy". Seizure. 19 (2): 93–101. doi:10.1016/j.seizure.2009.12.004. PMID 20064729. S2CID 17525536.
- Chen M, LeDuc B, Kerr S, Howe D, Williams DA (March 2010). "Identification of human UGT2B7 as the major isoform involved in the O-glucuronidation of chloramphenicol". Drug Metabolism and Disposition. 38 (3): 368–75. doi:10.1124/dmd.109.029900. PMID 20008037. S2CID 10438280.
- Ross CJ, Katzov-Eckert H, Dubé MP, Brooks B, Rassekh SR, Barhdadi A, Feroz-Zada Y, Visscher H, Brown AM, Rieder MJ, Rogers PC, Phillips MS, Carleton BC, Hayden MR (December 2009). "Genetic variants in TPMT and COMT are associated with hearing loss in children receiving cisplatin chemotherapy". Nature Genetics. 41 (12): 1345–9. doi:10.1038/ng.478. PMID 19898482. S2CID 21293339.
- Tang L, Ye L, Singh R, Wu B, Lv C, Zhao J, Liu Z, Hu M (June 2010). "Use of glucuronidation fingerprinting to describe and predict mono- and dihydroxyflavone metabolism by recombinant UGT isoforms and human intestinal and liver microsomes". Molecular Pharmaceutics. 7 (3): 664–79. doi:10.1021/mp900223c. PMC 2941766. PMID 20297805.
- Woillard JB, Rerolle JP, Picard N, Rousseau A, Drouet M, Munteanu E, Essig M, Marquet P, Le Meur Y (June 2010). "Risk of diarrhoea in a long-term cohort of renal transplant patients given mycophenolate mofetil: the significant role of the UGT1A8 2 variant allele". British Journal of Clinical Pharmacology. 69 (6): 675–83. doi:10.1111/j.1365-2125.2010.03625.x. PMC 2883760. PMID 20565459.
- Yu L, Qian M, Liu Y, Yao T, Zeng S (May 2010). "Stereoselective metabolism of propranolol glucuronidation by human UDP-glucuronosyltransferases 2B7 and 1A9". Chirality. 22 (4): 456–61. doi:10.1002/chir.20765. PMID 19644937.
- Yang JW, Lee PH, Hutchinson IV, Pravica V, Shah T, Min DI (October 2009). "Genetic polymorphisms of MRP2 and UGT2B7 and gastrointestinal symptoms in renal transplant recipients taking mycophenolic acid". Therapeutic Drug Monitoring. 31 (5): 542–8. doi:10.1097/FTD.0b013e3181b1dd5e. PMID 19730281. S2CID 6454841.
- Ahn J, Schumacher FR, Berndt SI, Pfeiffer R, Albanes D, Andriole GL, Ardanaz E, Boeing H, Bueno-de-Mesquita B, Chanock SJ, Clavel-Chapelon F, Diver WR, Feigelson HS, Gaziano JM, Giovannucci E, Haiman CA, Henderson BE, Hoover RN, Kolonel LN, Kraft P, Ma J, Le Marchand L, Overvad K, Palli D, Stattin P, Stampfer M, Stram DO, Thomas G, Thun MJ, Travis RC, Trichopoulos D, Virtamo J, Weinstein SJ, Yeager M, Kaaks R, Hunter DJ, Hayes RB (October 2009). "Quantitative trait loci predicting circulating sex steroid hormones in men from the NCI-Breast and Prostate Cancer Cohort Consortium (BPC3)". Human Molecular Genetics. 18 (19): 3749–57. doi:10.1093/hmg/ddp302. PMC 2742399. PMID 19574343.
- Hu M, Lui SS, Mak VW, Chu TT, Lee VW, Poon EW, Tsui TK, Ko GT, Baum L, Tam LS, Li EK, Tomlinson B (October 2010). "Pharmacogenetic analysis of lipid responses to rosuvastatin in Chinese patients". Pharmacogenetics and Genomics. 20 (10): 634–7. doi:10.1097/FPC.0b013e32833de489. PMID 20679960. S2CID 3475599.
- Zhao W, Fakhoury M, Deschênes G, Roussey G, Brochard K, Niaudet P, Tsimaratos M, André JL, Cloarec S, Cochat P, Bensman A, Azougagh S, Jacqz-Aigrain E (November 2010). "Population pharmacokinetics and pharmacogenetics of mycophenolic acid following administration of mycophenolate mofetil in de novo pediatric renal-transplant patients". Journal of Clinical Pharmacology. 50 (11): 1280–91. doi:10.1177/0091270009357429. PMID 20147615. S2CID 22875166.
- Blanca Sánchez M, Herranz JL, Leno C, Arteaga R, Oterino A, Valdizán EM, Nicolas JM, Adín J, Shushtarian M, Armijo JA (April 2010). "UGT2B7_-161C>T polymorphism is associated with lamotrigine concentration-to-dose ratio in a multivariate study". Therapeutic Drug Monitoring. 32 (2): 177–84. doi:10.1097/FTD.0b013e3181ceecc6. hdl:10261/49808. PMID 20216122. S2CID 44807993.
- Yong M, Schwartz SM, Atkinson C, Makar KW, Thomas SS, Newton KM, Aiello Bowles EJ, Holt VL, Leisenring WM, Lampe JW (February 2010). "Associations between polymorphisms in glucuronidation and sulfation enzymes and mammographic breast density in premenopausal women in the United States". Cancer Epidemiology, Biomarkers & Prevention. 19 (2): 537–46. doi:10.1158/1055-9965.EPI-09-0898. PMC 2820123. PMID 20142249.
- Joy MS, Boyette T, Hu Y, Wang J, La M, Hogan SL, Stewart PW, Falk RJ, Dooley MA, Smith PC (November 2010). "Effects of uridine diphosphate glucuronosyltransferase 2B7 and 1A7 pharmacogenomics and patient clinical parameters on steady-state mycophenolic acid pharmacokinetics in glomerulonephritis". European Journal of Clinical Pharmacology. 66 (11): 1119–30. doi:10.1007/s00228-010-0846-x. PMC 3739695. PMID 20567810.






