페노피브레이트
Fenofibrate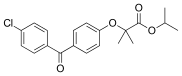 | |
| 임상자료 | |
|---|---|
| 상명 | 페노글라이드, 리포펜 등 |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인플러스 | a601052 |
| 라이센스 데이터 | |
| 임신 범주 |
|
| 경로: 행정 | 입으로 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 | |
| 약동학 데이터 | |
| 단백질 결합 | 99% |
| 신진대사 | 글루쿠로니화 |
| 제거 반감기 | 20시간 |
| 배설 | 소변(60%), 대변(25%) |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| IUPHAR/BPS | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.051.234 |
| 화학 및 물리적 데이터 | |
| 공식 | C20H21CLO4 |
| 어금질량 | 360.83 g·190−1 |
| 3D 모델(JSmol) | |
| 녹는점 | 80~81°C(176~178°F) |
| |
| |
| (iii) | |
페노피브레이트(Tricor, Fenobrat 등 상표명으로 판매)는 비정상적인 혈중 지질수치를 치료하는 데 사용되는 섬유종류의 경구용 약물이다.[2] 스타틴 약은 심장병이나 사망의 위험을 감소시키는 것으로 보이지 않기 때문에 덜 선호된다.[2][3] 이것의 사용은 식습관 변화와 함께 권장된다.[2]
일반적인 부작용으로는 간 질환, 호흡 장애, 복통, 근육 질환, 메스꺼움 등이 있다.[2] 심각한 부작용으로는 독성 표피 네크로리시스, 횡문근리시스, 담석, 췌장염 등이 있을 수 있다.[2] 임신과 모유 수유 중에는 사용하지 않는 것이 좋다.[3][4] 그것은 여러 메커니즘에 의해 작동된다.[2]
1969년에 특허를 받았으며, 1975년에 의학적으로 사용되었다.[5] 그것은 일반적인 약으로 이용할 수 있다.[3] 2019년에는 미국에서 8백만 개 이상의 처방전을 받아 87번째로 가장 많이 처방된 약이었다.[6][7]
의학적 용법
페노피브레이트(fenofibrate)는 주로 1차 고콜레스테롤혈증이나 혼합 이상지질혈증에 사용된다. 페노피브레이트(fenofibrate)는 제2형 당뇨병 환자의 당뇨병성 망막병증의 위험과 진행을 감소시킨다.[8] 처음에는 호주에서 제2형 당뇨병과 당뇨망막병증 환자의 당뇨망막병증에 대해 언급되었다.[9] 대규모 국제 FEART 및 ACC-Eye 실험 결과, 페노피브레이트 치료는 당뇨병성 망막병증에 필요한 레이저 치료를 31% 감소시켰으며, 4년 동안 진행률을 3.7% 감소시킨 것으로 나타났다.[10][8] 이러한 시험에서 통계적으로 유의한 심혈관 위험 편익이 확인되지 않았지만, 현재 스타틴 약물을 복용하고 있는 높은 중성지방 이상지질혈증 환자에게 치료 효과를 더할 수 있다.[11][12]
페노피브레이트(fenofibrate)는 미세혈관 질환이 없는 제2형 당뇨병 환자의 발목 아래 절단 위험을 줄이는 것으로 보인다.[13] FEART 연구에서는 매일 200mg의 용량에서 페노피브레이트가 글리코믹 제어, 이상지질혈증의 유무 및 지질하강 작용 메커니즘과 무관하게 모든 절단 위험을 37% 감소시켰다고 보고했다.[13][14] 그러나, 절단 수술을 받은 참가자들의 코호트는 이전의 심혈관 질환(예: 협심증, 심근경색)을 가지고 있었을 가능성이 더 높았고, 당뇨병의 지속 기간이 더 길었으며, 기저 신경증을 가지고 있었다.[13][14]
Fenofibrate는 통풍에 걸린 사람들의 높은 혈중 요산 수치를 추가 치료하는 라벨 밖의 사용이 있다.[15]
높아진 저밀도 지단백질 콜레스테롤(LDL), 총콜레스테롤, 트리글리세리드(TG), 아폴리포프로테이트 B(apo B)를 줄이고, 1차 고콜레스테롤혈증이나 이상지질혈증이 있는 성인의 고밀도 지단백질콜레스테롤(HDL)을 증가시키는 데 식이요법 외에 사용된다.[16]
중증 하이퍼트리글리세리혈증 유형 IV 또는 V
그것은 심각한 고트리거성혈증을 가진 성인의 치료를 위해 식이요법과 함께 사용된다. 단식 치로미크론혈증을 보이는 당뇨병 환자의 혈당 조절을 개선하면 대개 약리학적 개입의 필요성이 줄어든다.[16]
스타틴은 혈중 콜레스테롤 치료의 첫 번째 선으로 남아 있다. 2013년부터 시행된 AHA 지침은 추가 의약품의 일상적 사용에 대한 증거를 찾지 못했다.[17]
이와 함께 FDA는 2016년 나이아신확장배출제 및 페노피브산 지연배출캡슐의 응용분야에서 스타틴과 공동행정에 관련된 적응증 승인 철회서를 제출했다. 트리글리세리드 수치의 감소 및/또는 스타틴 치료 환자의 HDL 콜레스테롤 수치의 증가는 심혈관 질환의 위험을 감소시킨다. 이러한 결론과 일관되게 FDA는 스타틴과의 공동 관리를 위한 니아신 ER 정제 및 페노피브산 DR 캡슐의 이점이 더 이상 위험을 초과하지 않으며, 이 적응증의 승인은 철회되어야 한다고 결정했다."[18]
COVID-19
2021년 8월 영국과 이탈리아 연구진은 페노피브레이트(fenofibrate)가 체외에서 사스-CoV-2 감염을 현저하게 줄일 수 있다는 실험실 결과를 보고했다.[19][20]
콘트라인커뮤니케이션
Fenofibrate는 다음과 같이 제한된다.[16]
- 투석(노출량 2.7배 증가, 글루머 여과율 추정치가 30 mL/min 미만인 환자)을 포함한 중증 신장장애 환자
- 1차 담도 간경변증, 설명할 수 없는 지속성 간 기능 검사 등 간질환이 있는 환자
- 기존 담낭질환 환자
- 수유하는 어머니들
- 갑상선기능저하증
- 페노피브레이트 또는 페노피브릭산에 대한 과민성이 알려진 환자
역효과
가장 일반적인 부작용(>3%의 공동 관리 스타틴 환자)은 다음과[21] 같다.
주의사항
페노피브레이트와 스타틴을 결합요법으로 투여할 때는 아침에 페노피브레이트를, 밤에는 스타틴을 투여해 피크 복용량이 겹치지 않도록 하는 것이 좋다.[22]
근골격계
간독성
네프로독성
담도
응고/출혈
- 경구 Coumadin 항응고제(예: 와파린)를 사용한 동반 치료 시 주의하십시오. Coumadin의 복용량을 조절하여 프로트롬빈 시간/INR을 원하는 수준으로 유지하여 출혈 합병증을 예방한다.[21]
과다 복용
"페노피브릭산 지연배출 캡슐을 과다복용하는 구체적인 치료법은 없다. 활력징후 모니터링 및 임상 상태 관찰을 포함한 일반적인 지원 관리가 제시된다." 또한, 혈장 투석은 혈장 단백질에 심하게 결합되어 있고 투석 상태가 좋지 않기 때문에 약물 과다복용 치료 옵션으로 간주되어서는 안 된다.[21]
상호작용
이러한 페노피브레이트와의 약물 상호작용은 중대한 것으로 간주되며 치료 수정이 필요할 수 있다.
- 담즙산 격리제(예: 콜레스토피프라민, 콜레스티폴 등): 함께 섭취하면 담즙산 레진이 페노피브레이트(fenofibrate)에 결합되어 페노피브레이트 흡수가 감소할 수 있다. 흡수를 극대화하려면 담즙산분리제를 복용하기 전 1시간 이상, 복용 후 4시간~6시간 정도 투여를 분리해야 한다.[21][23]
- 면역억제제(예: ciclosporin 또는 tacrolimus): 면역억제제와 페노피브레이트를 병행 사용함으로써 신장기능장애의 위험성이 증가한다. 신장 기능을 저하시키는 추가 약물을 공동 투여할 때는 주의하여 접근하십시오.[24]
- 비타민 K 적대제(예: 와파린): 앞서 언급했듯이, 페노피브레이트는 출혈 위험을 증가시키기 위해 쿠마딘 항응고제와 상호작용을 한다. 비타민 K 길항제 투여량 조절이 필요할 수 있다.[21]
- 스타틴: 스타틴과 페노피브레이트의 조합은 횡문근융해증이나 근병증의 위험을 증가시킬 수 있다.[25]
작용기전
요약하면 트리글리세리드가 풍부한 입자의 강화된 카타볼리즘과 VLDL의 분비가 섬유종의 저농축세리빈혈증 효과를 밑바탕으로 하는 반면 HDL 대사에 미치는 영향은 HDL 아폴리포프로틴 표현식의 변화와 관련이 있다.[26]
페노피브레이트(Fenofibrate)는 섬유산 유도체로, 이소프로필 에스테르와 연결된 페노피브산(Fenofibric acid)으로 구성된 프로드약이다. 과록시솜 증식기 활성수용체 알파(PPARα)[26]를 활성화해 지질 수치를 낮추고, PPARα는 지질단백질 지질효소를 활성화하며 아포프로테이트 CIII를 감소시켜 혈장 내 중성지방분해와 중성지방이 풍부한 입자를 제거한다.
또한 PPARα는 아포프로테이트 AI와 AII를 증가시키고, VLD-와 LDL 함유 아포프로테이트 B를 감소시키며, HDL 함유 아포프로테이트 AI와 AII를 증가시킨다.
공식화
Fenofibrate는 몇 가지 공식으로 제공되며 다음과 같은 몇 가지 브랜드 이름으로 판매된다.
- 트리코르 바이 압비
- 리포펜 바이 코와 제약 아메리카
- 로피브라 바이 테바
- 애벗 연구소의 리판틸, 리피딜, 리판틸 마이크로, 수프랄립
- 프레노코르-67(오르데인 건강 관리 기준)
- 피브랙틱스 105/35 코웬트릭스 파마(인도)
- Fenogal by SMB 연구소
- 안타라 바이 오시엔트 제약
- 트리체크 바이 자이두스 (CND)
- 아토르바 TG by 자이두스 메디카
- 골지USA의 골립
- 란박시(인도)의 스탠립
약동학적 특성, 특히 생물학적 가용성의 측면에서 제형이 다를 수 있다. 어떤 것은 식사와 함께 섭취해야 하는 반면, 어떤 것은 음식과 무관하게 섭취할 수 있다.[27]
활성 형태인 페노파이브산(fenofibrate, fenofibric acid)은 미국에서 판매되며 트릴리픽스로 판매된다. 페노피브릭산은 식사와 관계없이 복용할 수 있다.[21][28]
환경 존재
페노피브릭산은 캘리포니아의 12개 폐수처리장에서 채취한 슬러지 샘플에서 확인된 12개 화합물 중 하나로 체외 에스트로겐 활성과 관련이 있었다. [29]
역사
페노피브레이트(Fenofibrate)는 클로피브레이트(clofibrate)의 파생상품으로 1974년에 처음 합성되었으며, 초기에는 프랑스에서 제공되었다. 처음에는 프로세토펜으로 알려졌으며, 후에 세계보건기구(WHO) 국제비수용성명 가이드라인을 준수하기 위해 '페노피브레이트'로 이름이 바뀌었다.[30]
Fenofibrate는 프랑스의 Groofe Fournier SA에 의해 개발되었다.
미국에서 트리코르는 2005년에 개혁되었다. 이러한 개혁은 논란이 되었고, 일반적 등가물과의 경쟁을 억제하기 위한 시도로 보여졌으며,[31] 테바의 독점금지 소송의 대상이 되었다.[31]
참조
- ^ "Fenofibrate 267mg Capsules - Summary of Product Characteristics (SmPC)". (emc). 12 February 2020. Retrieved 13 April 2020.
- ^ a b c d e f "Fenofibric Acid/Fenofibrate Monograph for Professionals". Drugs.com. American Society of Health-System Pharmacists. Retrieved 3 March 2019.
- ^ a b c British national formulary : BNF 76 (76 ed.). Pharmaceutical Press. 2018. p. 198. ISBN 9780857113382.
- ^ "Fenofibrate Pregnancy and Breastfeeding Warnings". Drugs.com. Retrieved 3 March 2019.
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. p. 474. ISBN 9783527607495.
- ^ "The Top 300 of 2019". ClinCalc. Retrieved 16 October 2021.
- ^ "Fenofibrate - Drug Usage Statistics". ClinCalc. Retrieved 16 October 2021.
- ^ a b Wong TY, Simó R, Mitchell P (July 2012). "Fenofibrate - a potential systemic treatment for diabetic retinopathy?". American Journal of Ophthalmology. 154 (1): 6–12. doi:10.1016/j.ajo.2012.03.013. PMID 22709833.
- ^ "Australian Public Assessment Report for fenofibrate". TGA. TGA. Retrieved 27 June 2015.
- ^ Fazio S (June 2009). "More clinical lessons from the FIELD study". Cardiovascular Drugs and Therapy. 23 (3): 235–41. doi:10.1007/s10557-008-6160-5. PMID 19160032. S2CID 7987660.
- ^ Elam MB, Ginsberg HN, Lovato LC, Corson M, Largay J, Leiter LA, et al. (April 2017). "Association of Fenofibrate Therapy With Long-term Cardiovascular Risk in Statin-Treated Patients With Type 2 Diabetes". JAMA Cardiology. 2 (4): 370–380. doi:10.1001/jamacardio.2016.4828. PMC 5470410. PMID 28030716.
- ^ Kim NH, Han KH, Choi J, Lee J, Kim SG (September 2019). "Use of fenofibrate on cardiovascular outcomes in statin users with metabolic syndrome: propensity matched cohort study". BMJ. 366: l5125. doi:10.1136/bmj.l5125. PMC 6763755. PMID 31562117.
- ^ a b c Rajamani K, Colman PG, Li LP, Best JD, Voysey M, D'Emden MC, et al. (May 2009). "Effect of fenofibrate on amputation events in people with type 2 diabetes mellitus (FIELD study): a prespecified analysis of a randomised controlled trial". Lancet. 373 (9677): 1780–8. doi:10.1016/S0140-6736(09)60698-X. PMC 2687887. PMID 19465233.
- ^ a b Steiner G (October 2009). "How can we improve the management of vascular risk in type 2 diabetes: insights from FIELD". Cardiovascular Drugs and Therapy. 23 (5): 403–8. doi:10.1007/s10557-009-6190-7. PMID 19757004. S2CID 12747599.
- ^ Khanna D, Fitzgerald JD, Khanna PP, Bae S, Singh MK, Neogi T, et al. (October 2012). "2012 American College of Rheumatology guidelines for management of gout. Part 1: systematic nonpharmacologic and pharmacologic therapeutic approaches to hyperuricemia". Arthritis Care & Research. 64 (10): 1431–46. doi:10.1002/acr.21772. PMC 3683400. PMID 23024028.
- ^ a b c "TRICOR (fenofibrate) Package Insert" (PDF). Abbot Laboratories. October 2010.
- ^ Stone NJ, Robinson JG, Lichtenstein AH, Bairey Merz CN, Blum CB, Eckel RH, et al. (June 2014). "2013 ACC/AHA guideline on the treatment of blood cholesterol to reduce atherosclerotic cardiovascular risk in adults: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines". Circulation. 129 (25 Suppl 2): S1-45. doi:10.1161/01.cir.0000437738.63853.7a. PMID 24222016.
- ^ "AbbVie Inc. et al; Withdrawal of Approval of Indications Related to the Coadministration With Statins in Applications for Niacin Extended-Release Tablets and Fenofibric Acid Delayed- Release Capsules" (PDF). Food and Drug Administration. 18 April 2016.
- ^ Davies, Scott P.; Mycroft-West, Courtney J.; Pagani, Isabel; Hill, Harriet J.; Chen, Yen-Hsi; Karlsson, Richard; Bagdonaite, Ieva; Guimond, Scott E.; Stamataki, Zania; De Lima, Marcelo Andrade; Turnbull, Jeremy E.; Yang, Zhang; Vicenzi, Elisa; Skidmore, Mark A.; Khanim, Farhat L.; Richardson, Alan (6 August 2021). "The Hyperlipidaemic Drug Fenofibrate Significantly Reduces Infection by SARS-CoV-2 in Cell Culture Models". Frontiers in Pharmacology. 12: 660490. doi:10.3389/fphar.2021.660490. PMC 8377159. PMID 34421587.
- ^ "Licensed drug could reduce SARS-CoV-2 infection by up to 70 per cent, reveals study". University of Birmingham and Keele University in the UK and the San Raffaele Scientific Institute in Italy. 6 August 2021.
- ^ a b c d e f g h i j 페노피브릭산 FDA 라벨 처방 정보"FDA Label Information" (PDF). FDA.
- ^ Wierzbicki AS, Mikhailidis DP, Wray R, Schacter M, Cramb R, Simpson WG, Byrne CB (2003). "Statin-fibrate combination: therapy for hyperlipidemia: a review". Current Medical Research and Opinion. 19 (3): 155–68. doi:10.1185/030079903125001668. PMID 12814127. S2CID 35948128.
- ^ 제품 정보: TriCor(TM), Fenofibrate. 1998년 일리노이주 노스시카고 애벗 연구소
- ^ 제품 정보: 산딤문(R) 구강 캡슐, 구강 용액, 정맥 주사, 사이클로스포린 구강 캡슐, 구강 용액, 정맥 주사. NJ, East Hanover, Novartis Pharmical Corporation, 2010.
- ^ 제품 정보: TRICOR(R) 구강 알약, 페노피브레이트 구강 알약. 2007년, 일리노이 주 노스 시카고 애벗 연구소
- ^ a b Staels B, Dallongeville J, Auwerx J, Schoonjans K, Leitersdorf E, Fruchart JC (November 1998). "Mechanism of action of fibrates on lipid and lipoprotein metabolism". Circulation. 98 (19): 2088–93. CiteSeerX 10.1.1.1004.321. doi:10.1161/01.cir.98.19.2088. PMID 9808609.
- ^ Ling H, Luoma JT, Hilleman D (April 2013). "A Review of Currently Available Fenofibrate and Fenofibric Acid Formulations". Cardiology Research. 4 (2): 47–55. doi:10.4021/cr270w. PMC 5358213. PMID 28352420.
- ^ Alagona P (May 2010). "Fenofibric acid: a new fibrate approved for use in combination with statin for the treatment of mixed dyslipidemia". Vascular Health and Risk Management. 6: 351–62. doi:10.2147/vhrm.s6714. PMC 2879297. PMID 20531954.
- ^ Gabrielle P. Black (2021). "Using Estrogenic Activity and Nontargeted Chemical Analysis to Identify Contaminants in Sewage Sludge". Environmental Science & Technology. 55 (10): 6729–6739. Bibcode:2021EnST...55.6729B. doi:10.1021/acs.est.0c07846. PMC 8378343. PMID 33909413.
- ^ Lalloyer F, Staels B (May 2010). "Fibrates, glitazones, and peroxisome proliferator-activated receptors". Arteriosclerosis, Thrombosis, and Vascular Biology. 30 (5): 894–9. doi:10.1161/ATVBAHA.108.179689. PMC 2997800. PMID 20393155.
- ^ a b "Abbott's request to dismiss the antitrust charge over Tricor was rejected". FDANews, Drug Daily Bulletin. 1 June 2006.
외부 링크
- "Fenofibrate". Drug Information Portal. U.S. National Library of Medicine.


