메발론산 경로
Mevalonate pathway이소프레노이드 경로 또는 HMG-CoA 환원효소 경로로도 알려진 메발론산 경로는 진핵생물, 고세균 및 일부 [1]박테리아에 존재하는 필수 대사 경로이다.이 경로는 콜레스테롤, 비타민 K, 코엔자임 Q10, 그리고 모든 스테로이드 [2]호르몬과 같은 30,000개 이상의 생체 분자의 다양한 클래스인 이소프레노이드를 만드는데 사용되는 아이소펜테닐 피로인산염과 디메틸알릴 피로인산염이라고 불리는 두 개의 5개의 탄소 구성 요소를 생산합니다.
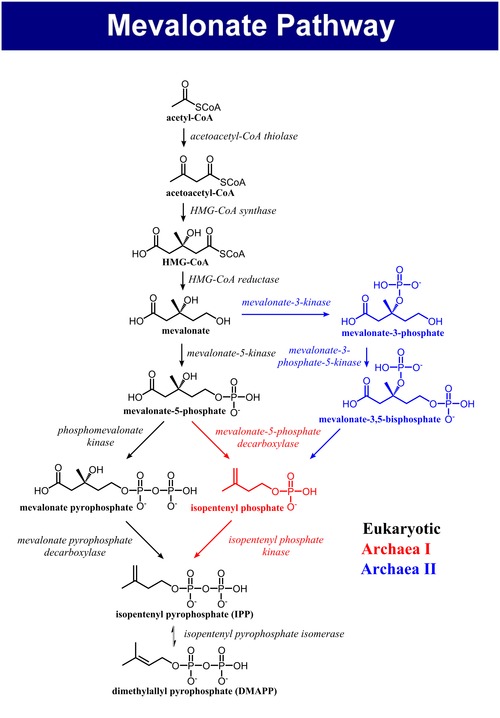
메발론산 경로는 아세틸-CoA에서 시작하여 IPP와 DMAPP의 [3]생성으로 끝납니다.그것은 콜레스테롤을 낮추는 약의 일종인 스타틴의 표적으로 가장 잘 알려져 있다.스타틴은 메발론산 경로 내에서 HMG-CoA 환원효소를 억제한다.
상부 메발론산 경로
진핵생물, 고세균, 그리고 유박테리아의 메발론산 경로는 모두 같은 방식으로 시작된다.경로의 유일한 탄소 공급 원료는 아세틸-CoA이다.첫 번째 단계는 두 개의 아세틸-CoA 분자를 응축하여 아세토아세틸-CoA를 생성한다.이어서 두 번째 응축으로 HMG-CoA(3-히드록시-3-메틸-글루타릴-CoA)를 형성한다.HMG-CoA 수율(R)-메발론산염 감소.이 처음 세 가지 효소 단계는 상부 메발론산 [4]경로라고 불립니다.
하부 메발론산 경로
(R)-메발론산을 IPP 및 DMAPP로 변환하는 하위 메발론산 경로에는 3가지 변형이 있다.진핵생물에서 메발론산염은 5-OH 위치에서 두 번 인산화된 후 탈탄산화되어 IPP를 [4]생성한다.할로페락스 화산(Haloferax volcanii)과 같은 일부 고고학에서는 메발론산염이 5-OH 위치에서 한 번 인산화되어 인산 이소펜테닐(IP)을 생성하고, 마지막으로 다시 인산화되어 IPP(Archaeal Mevalonate Pathway I)[5]를 생성한다.Hotosyasma acidophilum에서 발견된 세 번째 메발론산 경로 변이체는 3-OH 위치에서 메발론산을 인산화한 후 5-OH 위치에서 인산화한다.생성된 대사물인 메발론산-3,5-이인산염은 IP로 탈탄산화되고, 마지막으로 인산화되어 IPP(Archaeal Mevalonate Pathway II)[6][7]를 생성한다.
규제 및 피드백
SREBP(스테롤 조절 요소 결합 단백질-1 및 -2) 활성화에 대한 DNA 전사 조절을 통해 몇 가지 핵심 효소가 활성화될 수 있다.이 세포내 센서는 낮은 콜레스테롤 수치를 검출하여 HMG-CoA 환원효소 경로에 의한 내인생 생산을 촉진하고 LDL 수용체를 상향 조절하여 리포단백질 흡수를 증가시킨다.이 경로의 조절은 mRNA의 번역 속도, 환원효소 분해 및 인산화를 [1]제어함으로써 달성된다.
약리학
많은 약물이 메발론산 경로를 대상으로 한다.
- 스타틴(콜레스테롤 수치를 낮추기 위해 사용)
- 비스포스포네이트(각종 골변성 질환 치료에 사용)
질병.
메발론산염 경로에 영향을 미치는 질병은 다음과 같습니다.
- 메발론산인산화효소결핍증
- 메발론산뇨
- HIDS(Hyperimun Globulinemia D Syndrome)
대체 경로
식물, 대부분의 박테리아, 그리고 말라리아 기생충과 같은 일부 원생동물들은 메틸에리톨인산염([8]MEP) 또는 비메발론산염 경로라고 불리는 대체 경로를 사용하여 이소프레노이드를 생성하는 능력을 가지고 있다.메발론산 경로와 MEP 경로의 출력은 IPP와 DMAPP로 동일하지만, 아세틸-CoA를 IPP로 변환하는 효소 반응은 완전히 다르다.두 대사 경로 간의 상호작용은 C-포도당 아이소토포머를 [9]사용하여 연구할 수 있다.고등 식물에서 MEP 경로는 플라스티드에서 작동하며, 메발론산 경로는 세포질에서 [8]작동한다.MEP 경로를 포함하는 박테리아의 예로는 대장균과 결핵균과 같은 병원균이 있다.
효소 반응
| 효소 | 반응 | 묘사 |
| 아세토아세틸CoA티올라아제 | 아세틸-CoA(아세틸-CoA)는 아세틸-CoA 분자와 축합하여 아세토아세틸-CoA를 형성한다. | |
| HMG-CoA합성효소 | 아세토아세틸-CoA는 다른 아세틸-CoA 분자와 응축하여 3-히드록시-3-메틸글루타릴-CoA(HMG-CoA)를 형성한다. | |
| HMG-CoA 환원효소 | HMG-CoA는 NADPH에 의해 메발론산염으로 환원된다.이것은 콜레스테롤 합성의 속도 제한 단계이며, 이것이 이 효소가 의약품의 좋은 표적이 되는 이유입니다. | |
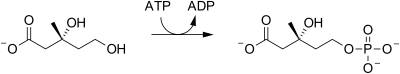
| 메발론산염-5-프로세서 | 메발론산은 5-OH 위치에서 인산화되어 메발론산-5-인산(일명 포스포메발론산)을 생성한다. | |
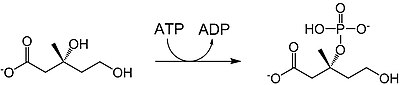
| 메발론산염-3-매개성 | 메발론산은 3-OH 위치에서 인산화되어 메발론산-3-인산을 생성하며, 1 ATP가 소비된다. | |
| 메발론산-3-인산-5-염 | 메발론산-3-인산은 5-OH 위치에서 인산화되어 메발론산-5-인산(일명 포스포메발론산)을 생성한다.1ATP가 소비됩니다. | |
| 포스포메발론산인산화효소 | 메발론산염-5-인산은 인산화되어 메발론산-5-피로인산을 생성한다. 1 ATP가 소비된다. | |
| 메발론산-5-피로인산탈카르복실화효소 | 메발론산-5-피로인산염을 탈탄산화하여 이소펜테닐피로인산(IPP)을 생성하며, 1ATP를 소비한다. | |
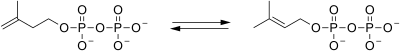
| 이소펜테닐피로인산 이성질화효소 | 이소펜테닐피로인산은 디메틸알릴피로인산으로 이성화된다. |
레퍼런스
- ^ a b Buhaescu I, Izedine H (2007) 메발론산 경로: 임상 및 치료적 의미에 대한 관점.ClinBichem 40:575–584.
- ^ Holstein, S. A. 및 Hol, R. J. (2004) 이소프레노이드:형태와 기능의 현저한 다양성.지질 39, 293-309
- ^ Goldstein, J. L. 및 Brown, S. B. (1990) 메발론산 경로의 규제.네이처 343, 425-430
- ^ a b Miziorko H (2011) 이소프레노이드 생합성 메발론산 경로의 효소.아치 생화학 바이오피스 505:131-143.
- ^ Dellas, N., Thomas, S. T., Manning, G. 및 Noel, J. P.(2013) 기존의 메발론산 경로의 대사 대체 발견.eLife 2, e00672
- ^ Vinokur JM, Korman TP, Cao Z, Bowie JU (2014) 고고학에서 새로운 메발론산염 경로의 증거.생화학 53:4161~4168.
- ^ 아자미Y, 핫토리A, 니시무라H, 카와이데H, 요시무라T, 헤미H(2014)(R)-메발론산-3-인산은 열가소성아시드필럼의 메발론산 경로의 중간체이다.J Biol Chem 289:15957–15967.
- ^ a b Banerjee A, Sharkey TD. (2014) 메틸에리트리톨 4-인산(MEP) 경로 대사 조절.NAT Prod 담당자 31:10431055
- ^ Orsi E, Beekwilder J, Peek S, Eggink G, Kengen SW, Weusthuis RA (2020). "Metabolic flux ratio analysis by parallel 13C labeling of isoprenoid biosynthesis in Rhodobacter sphaeroides". Metabolic Engineering. 57: 228–238. doi:10.1016/j.ymben.2019.12.004. PMID 31843486.
외부 링크
- Rensselaer Polytechnical Institute의 콜레스테롤 합성 페이지(규제 포함)