요소 사이클
Urea cycle요소 주기(ornithine cycle이라고도 함)는 암모니아(NH3)로부터 요소(NH2)2CO를 생성하는 생화학적 반응의 순환이다. 이 순환은 요소 유기체에서 일어난다. 요소 순환은 배설을 위해 매우 독성이 강한 암모니아를 요소로 변환시킨다.[1] 이 사이클은 TCA 사이클이 발견되기 5년 전인 최초의 대사 사이클(Hans Krebs와 Kurt Henseleit, 1932년)이었다. 이 주기는 나중에 래트너와 코헨에 의해 더 자세히 설명되었다. 요소 순환은 주로 간에서 발생하며, 보다 적은 정도는 신장에서 일어난다.
함수
아미노산 카타볼리즘은 폐암모니아를 낳는다. 모든 동물들은 이 제품을 배설할 방법이 필요하다. 대부분의 수생생물, 즉 암모니아성 유기체는 암모니아를 변형시키지 않고 배설한다.[1] 암모니아처럼 질소를 쉽고 안전하게 제거할 수 없는 유기체는 주로 간에서 발생하는 요소 순환을 통해 요소 등 독성이 덜한 물질로 전환한다. 간에서 생성된 요소들은 혈류로 방출되고, 그곳에서 신장으로 이동하며 궁극적으로 소변으로 배설된다. 만약 질소나 암모니아를 유기체에서 제거하지 않으면 매우 해로울 수 있기 때문에 요소 순환은 이 유기체들에게 필수적이다.[2] 새와 대부분의 곤충을 포함한 종에서는 암모니아를 요산이나 요산염으로 바꾸어 고체 형태로 배설한다.
반응
전체 공정은+
4 NH와 아스파리트에서 각각 1개의 아미노 그룹과 HCO에서−
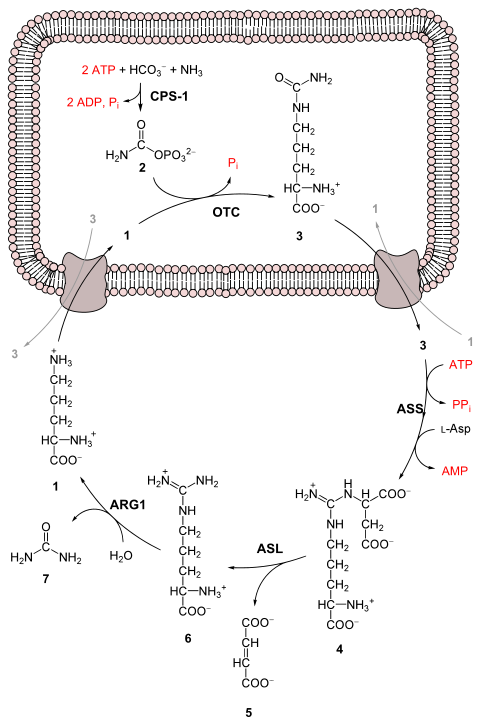
3 1개의 탄소 원자를 상대적으로 무독성 배설물 제품 요소로 변환한다.[3] 이는 4개의 "고에너지" 인산염 결합(3 ATP를 ADP 2개와 1AMP로 가수 분해)의 비용으로 발생한다. 암모니아에서 요소로의 전환은 5가지 주요 단계로 이루어진다. 첫 번째는 암모니아를 사이클로 진입시키기 위해 필요하며 다음의 네 가지는 사이클 자체의 일부분이다. 이 사이클에 들어가기 위해 암모니아는 카바모일 인산염으로 변환된다. 요소 순환은 4가지 효소 반응으로 구성된다: 1개의 미토콘드리아와 3개의 세포질이다.[1][4] 이것은 6개의 효소를 사용한다.[3][4][5]
- 요소 순환의 반응
1 L-오르니틴
카바모일 인산염 2개
3 L-시끌린
아르기니노수치네이트
후마레이트 5
6 L-arginine
7 요소
L-아스프 L-아스파테이트
CPS-1 카바모일 인산염 합성효소 I
OTC Ornithine transcarbamoylase
ASS 아르기니노수치신합성효소
ASL 아르기니노수치네이트 리아제
ARG1 arginase 1
첫 번째 반응: 요소 주기 입력
요소 주기가 시작되기 전에 암모니아는 카바모일 인산염으로 변환된다. 반응은 카바모일 인산염 합성효소 I에 의해 촉매되며 두 개의 ATP 분자를 사용해야 한다.[1] 카바모일 인산염은 그 후 요소 사이클로 들어간다.
요소 사이클의 단계
- 카바모일 인산염은 시스루린으로 변환된다. 오르니틴 트랜스 카르바모일라아제에 의한 카탈루션으로 카바모일 인산염 그룹은 오르니틴에 기증되어 인산염 그룹을 방출한다.[1]
- 아스파르테이트의 아미노 그룹과 아르기니노수치네이트를 형성하기 위한 시트룰린의 카르보닐 그룹 사이에 응축 반응이 일어난다. 이 반응은 ATP에 의존하며 아르기니노수치신합성효소에 의해 촉매된다.[1]
- 아르기니노수치네이트는 아르기닌과 후마린을 형성하기 위해 아르기니노수치나아제로 갈라진다.[1]
- 아르기닌은 아르기나아제에 의해 분해되어 요소와 오르니틴을 형성한다. 그런 다음 오르니틴은 다시 미토콘드리아로 운반되어 요소 순환을 다시 시작한다.[1][4]
전체반응 방정식
첫 번째 반응에서 NH+
4 + HCO는−
3 NH3 + CO2 + HO와2 동일하다.
따라서 요소 주기의 전체 방정식은 다음과 같다.
후마레이트(fumarate)는 아스파리트(반응 3과 4를 이용하여)와3 PP + HO2 → 2 P에서ii NH를 제거함으로써 얻을 수 있으므로 다음과 같이 방정식을 단순화할 수 있다.
요소 사이클과 관련된 반응도 2 NADH의 생성을 유발하므로 전체적인 반응은 소모되는 에너지보다 약간 더 많은 에너지를 방출한다는 점에 유의한다. NADH는 두 가지 방법으로 생산된다.
- 하나의 NADH 분자는 글루탐산염을 암모늄과 α-케토글루타산염으로 변환하는 효소 글루탐산염 탈수소효소에 의해 생성된다. 글루탐산염은 아민 집단의 무독성 운반체다. 이것은 카바모일 인산염의 초기 합성에 사용되는 암모늄 이온을 제공한다.
- 시토솔에 방출된 후마레이트는 시토솔릭 후마라아제에 의해 말라리아에 수분이 공급된다. 그리고 나서 이 말산은 세포성 말산염 탈수소효소에 의해 옥살로아세테이트로 산화되어, 세포솔에서 NADH를 감소시킨다. 옥살로아세테이트(Oxaloacetate)는 트랜스아미노산이 선호하는 케토산 중 하나여서 아스파테이트에 재활용돼 질소의 흐름을 요소 사이클로 유지한다.
우리는 다음과 같은 반응을 종합하여 이것을 요약할 수 있다.
- CO2 + 글루탐산염 + 아스파르타이트 + 3 ATP + 2 NAD++ 32 HO → 요소 + α-케토글루타레이트 + 옥살로아세타레이트 + ADPi + ADP + PPi + 2 NADH
생산된 2개의 NADH는 5 ATP 형성을 위한 에너지를 제공할 수 있다(사이토솔릭 NADH는 인간 간세포의 악성-아스파테이트 셔틀과 함께 2.5 ATP를 제공한다), 요소 사이클을 위한 2개의 고에너지 인산염 결합의 순생산이다. 단, cytosol에서 글루코네제네시스(gluconeogenesis)가 진행 중인 경우, 후자의 환원 등가물이 ATP를 생성하는 대신 GAPDH 단계의 역전을 추진하는 데 사용된다.
옥살로아세테이트의 운명은 트랜스마션을 통해 아스파테이트를 생산하거나 글루코네제네시스 기질인 인산에노폴피루베이트로 변환하는 것이다.
요소 사이클의 생산물
위에 언급된 바와 같이 많은 척추동물들은 암모늄으로 요인을 만들어 암모늄이 몸에 손상을 입히지 않도록 하기 위해 요소 주기를 이용한다. 이것이 도움이 되긴 하지만, 요소 순환의 다른 영향들이 있다. 예를 들어, 두 ATP의 소비, 요소 생산, H+의 생성, HCO3-와 NH4+의 결합을 재생이 가능한 형태로 하고, 마지막으로 NH4+[6]의 소비로 한다.
규정
N-아세틸글루탐산
카바모일 인산염과 요소 주기의 합성은 N-아세틸글루탐산(NAcGlu)의 유무에 따라 달라지며, 이 산물은 모두 CPS1을 활성화한다. NAcGlu는 카바모일 인산염 합성효소의 필수 활성제다.[7] N-acetylgutamate synthase(NAGS)에 의한 NAcGlu 합성 NACS는 NAGGlu를 NAGS의 알로스테릭 자극기인 Arg와 Transamination reaction에 있는 제품인 Glu에 의해 자극되며, 이 두 제품 모두 자유 아미노산이 상승할 때 상승한다. 그래서 글루는 NAGS의 기질일 뿐만 아니라 요소 사이클의 활성제 역할을 한다.
기질 농도
사이클의 나머지 효소는 기판의 농도에 의해 제어된다. 따라서 ARG1 이외의 사이클 효소의 유전적 결핍은 요소 생성에 큰 감소를 초래하지 않는다(만약 어떤 사이클 효소가 완전히 없어진다면, 사망은 출생 직후에 발생한다). 오히려 결핍된 효소의 기질이 쌓이면서 결핍 반응의 비율이 정상으로 높아진다.
그러나 변칙적인 기질 증가는 비용이 없는 것은 아니다. 기질 농도는 사이클을 다시+
4 NH로 상승시켜 고암모니아혈증(이열 [NH+
4])P이 발생한다.
NH+
4 독성의 근본원인은 완전히 이해되지 않지만 [NH+
4]가 높으면 NH 클리어링+
4 시스템에 엄청난 부담이 되며, 특히 뇌에서(요인 순환 효소 결핍의 증상은 지적 장애와 무기력증을 포함한다)가 나타난다. 이 클리어 시스템에는 GLUD1과 GLUL이 적용되어 2-옥소글루타레이트(2OG)와 글루풀을 감소시킨다. 뇌는 이 수영장의 고갈에 가장 민감하다. 2OG의 고갈은 TCAC의 비율을 감소시키는 반면, Glu는 신경전달물질이자 또 다른 신경전달물질인 GABA의 전구체다. [1](p.734)
구연산 사이클과 연결
요소 사이클과 구연산 사이클은 독립 사이클이지만 연계되어 있다. 요소 주기의 질소 원자 중 하나는 옥살로아세테이트의 분열을 통해 아스파테이트로 얻는다.[8] 3단계에서 생성되는 후마레이트도 구연산 사이클의 중간이고 그 사이클로 되돌아간다.[8]
요소 주기 장애
요소 주기 장애는 드물고 미국에서 약 35,000명 중 한 명에게 영향을 미친다.[9] 주기에 관여하는 효소의 유전적 결함이 발생할 수 있는데, 이는 보통 출생 후 며칠 안에 발현된다.[2] 최근에 태어난 아이는 전형적으로 다양한 구토와 무기력증을 경험하게 될 것이다.[2] 궁극적으로, 아기는 혼수상태에 빠져 뇌 손상을 입을 수 있다.[2] UCD를 소지한 신생아는 때아닌 검사와 오진 등으로 합병증이나 사망 위험이 훨씬 높다. 가장 흔한 오진은 신생아 패혈증이다. UCD의 징후는 생후 2~3일 안에 나타날 수 있지만, 현재 테스트 결과를 통해 확인을 받는 방법은 시간이 너무 오래 걸릴 수 있다.[10] 이것은 잠재적으로 혼수상태나 죽음과 같은 합병증을 일으킬 수 있다.[10]
요소 주기 장애는 성인에서도 진단할 수 있으며, 망상증, 무기력증, 뇌졸중과 유사한 증상이 나타날 수 있다.[11] 이러한 증상들 외에도 간에서 요소 순환이 오작동하기 시작하면 간경변증이 생길 수도 있다.[12] 이것은 또한 석관증(근육량 손실)을 초래할 수 있다.[12] 돌연변이는 요소 순환에 관여하는 각종 효소와 전달체의 결함으로 이어져 요소 순환 장애를 일으킨다.[1] 사이클에 사용되는 6개의 효소 중 어느 하나에 결함이 있는 개인이 최소 일일 요건에 필요한 이상으로 아미노산을 섭취하면 생산되는 암모니아는 요소로서 전환될 수 없게 된다. 이러한 개인은 고암모니아혈증, 즉 주기 중간기간의 축적을 경험할 수 있다.
개인 장애
- N-Acetyllutamate synthase(NAGS) 결핍
- CPS(Carbamoyl phosphate synthetase) 결핍
- OTC(Ornithine transcarbamoylase) 결핍증
- 시트라울린혈증 제1종(아르기니노수친산신화효소 결핍증)
- 아르기니노수친산뇨증(아르기니노수친산리아제의 결핍증)
- 아르기닌혈증(아르기나아제 결핍증)
- 고로니틴혈증, 고암모니아혈증, 호모시트리올린루리아(HHH)증후군(미토콘드리아 오니틴 트랜스포터의 결함)[5][13]
OTC 결핍을 제외한 모든 요소 주기 결함은 자동 열성 방식으로 상속된다. 일부 여성들은 증상을 보일 수 있지만, OTC 결핍은 X 연계 열성 장애로 유전된다. 대부분의 요소 주기 장애는 고암모니아혈증과 관련이 있지만 아르기닌혈증과 일부 형태의 아르기니노수신산뇨증은 암모니아 증가와 관련이 없다.
추가 이미지
참조
- ^ Jump up to: a b c d e f g h i Cox, Michael (2013-01-01). Lehninger Principles of Biochemistry. Freeman. ISBN 9781429234146. OCLC 901647690.
- ^ Jump up to: a b c d Tymoczko, John L.; Berg, Jeremy M.; Stryer, Lubert (2013). BIOCHEMISTRY A Short Course. W.H. Freeman and Company, New York. p. 529. ISBN 978-1-4292-8360-1.
- ^ Jump up to: a b Mew, Nicholas Ah; Pappa, Maria Belen; Gropman, Andrea L. (2015-01-01), Rosenberg, Roger N.; Pascual, Juan M. (eds.), "Chapter 57 - Urea Cycle Disorders", Rosenberg's Molecular and Genetic Basis of Neurological and Psychiatric Disease (Fifth Edition), Boston: Academic Press, pp. 633–647, doi:10.1016/b978-0-12-410529-4.00057-7, ISBN 978-0-12-410529-4, retrieved 2020-11-10
- ^ Jump up to: a b c Walker, Valerie (2014-01-01), Makowski, Gregory S. (ed.), "Chapter Three - Ammonia Metabolism and Hyperammonemic Disorders", Advances in Clinical Chemistry, Elsevier, 67: 73–150, doi:10.1016/bs.acc.2014.09.002, retrieved 2020-11-10
- ^ Jump up to: a b Pearl, Phillip L. (2017-01-01), Swaiman, Kenneth F.; Ashwal, Stephen; Ferriero, Donna M.; Schor, Nina F. (eds.), "76 - Inherited Metabolic Epilepsies", Swaiman's Pediatric Neurology (Sixth Edition), Elsevier, pp. 594–599, doi:10.1016/b978-0-323-37101-8.00076-x, ISBN 978-0-323-37101-8, retrieved 2020-11-10
- ^ Atkinson, Daniel (September 20, 1991). "Functional Roles of Urea in Vertebrates". Physiological Zoology (2 ed.). Los Angeles: The University of Chicago Press. 65 (2): 243–267. doi:10.1086/physzool.65.2.30158252. JSTOR 30158252. S2CID 87121092.
- ^ Kaplan Medical USMLE Step 1 Step 생화학 및 의료 유전학 강의 노트 2010, 261페이지
- ^ Jump up to: a b Shambaugh, G. E. (1977-12-01). "Urea biosynthesis I. The urea cycle and relationships to the citric acid cycle". The American Journal of Clinical Nutrition. 30 (12): 2083–2087. doi:10.1093/ajcn/30.12.2083. ISSN 0002-9165. PMID 337792.
- ^ Summar, Marshall L.; Koelker, Stefan; Freedenberg, Debra; Le Mons, Cynthia; Haberle, Johannes; Lee, Hye-Seung; Kirmse, Brian (2013). "The incidence of urea cycle disorders". Molecular Genetics and Metabolism. 110 (1–2): 179–180. doi:10.1016/j.ymgme.2013.07.008. ISSN 1096-7192. PMC 4364413. PMID 23972786.
- ^ Jump up to: a b 메리트, J. L., 브로디, L., 피노, G., & 리날도, P. (2018) 근위부 요소 주기 장애에 대한 신생아 선별: 신생아 선별을 위한 권고사항을 뒷받침하는 현재 증거 분자 유전학 및 대사, 124(2), 109–113. doi: 10.1016/j.ymgme.2018.04.006
- ^ Judd, Sandra (2010). Genetic Disorders Sourcebook. Omnigraphics. p. 225. ISBN 978-0-7808-1076-1.
- ^ Jump up to: a b Qiu, JIa (July 9, 2013). "Hyperammonemia in cirrhosis induces transcriptional regulation of myostatin by an NF-κB–mediated mechanism". Proceedings of the National Academy of Sciences of the United States of America. National Academy of Sciences. 110 (45): 18162–18167. Bibcode:2013PNAS..11018162Q. doi:10.1073/pnas.1317049110. JSTOR 23754730. PMC 3831479. PMID 24145431.
- ^ Smith, L. D.; Garg, U. (2017-01-01), Garg, Uttam; Smith, Laurie D. (eds.), "Chapter 5 - Urea cycle and other disorders of hyperammonemia", Biomarkers in Inborn Errors of Metabolism, San Diego: Elsevier, pp. 103–123, doi:10.1016/b978-0-12-802896-4.00004-3, ISBN 978-0-12-802896-4, retrieved 2020-11-10
외부 링크
- 요소 사이클 뒤의 화학적 논리
- 기초 신경화학 - 아미노산 장애