황달
Jaundice| 황달 | |
|---|---|
| 기타 이름 | 이케루스[1] |
 | |
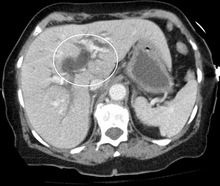
| 췌장암으로 인한 피부 황달 | |
| 발음 |
|
| 전문 | 소화기내과, 간과, 일반외과 |
| 증상 | 피부와 강막의 누런 빛깔[2][3], 가려움증 |
| 원인들 | 높은 빌리루빈 수치[3] |
| 위험요소 | 췌장암, 췌장염, 간질환, 특정 감염 |
| 진단 방법 | 혈중 빌리루빈, 간판넬[3] |
| 차동 진단 | 카로틴혈증, 리팜핀[4] 복용 |
| 치료 | 근본[5] 원인에 의거하여 |
황달은 높은 빌리루빈 [3][6]수치로 인해 피부와 강막의 황색 또는 녹색을 띤 색소 침착이다.성인의 황달은 전형적으로 비정상적인 헴 대사, 간 기능 장애 또는 담도-트럭션 [7]폐색을 포함한 근본적인 질병의 존재를 나타내는 신호이다.성인의 황달 유병률은 드문 반면, 아기의 황달은 생후 [8]첫 주에 80%가 영향을 받는 흔한 일이다.황달의 가장 흔한 증상은 가려움증,[2] 창백한 대변, 어두운 [4]소변이다.
혈중 빌리루빈의 정상 수치는 1.0mg/dl(17μmol/L) 미만이며, 2~3mg/dl(34~51μmol/L)을 초과하면 [4][9]황달이 발생한다.고혈중 빌리루빈은 비결합 빌리루빈과 복합 빌리루빈의 [10]두 가지 유형으로 나뉜다.
황달의 원인은 비교적 양성에서 [10]치명적일 수 있는 것까지 다양하다.높은 비결합 빌리루빈은 과도한 적혈구 파괴, 큰 멍, 길버트 증후군과 같은 유전적 조건, 장기간 먹지 않음, 신생아 황달 또는 갑상선 [4][10]문제 때문일 수 있다.높은 복합 빌리루빈은 간경변이나 간염,[4] 감염, 약물 또는 담석, 암 또는 췌장염을 포함한 인자로 인한 담관의 [4]막힘과 같은 간질환에 의한 것일 수 있다.카로틴이 함유된 많은 양의 음식이나 리팜핀과 [4]같은 약물을 섭취함으로써 생길 수 있는 카로틴 혈증을 포함한 다른 질환들도 황달은 아닙니다.
황달의 치료는 일반적으로 근본적인 [5]원인에 의해 결정된다.담관이 막힌 경우 일반적으로 수술이 필요하며, 그렇지 않은 경우 관리는 [5]의료입니다.의료 관리는 감염 원인 치료와 [5]황달의 원인이 될 수 있는 약물 복용을 중단하는 것을 포함할 수 있습니다.신생아 황달은 빌리루빈이 4~21mg/dl(68~360μmol/L)[9] 이상일 때 연령과 미숙기에 따라 광선요법으로 치료하거나 교환 수혈할 수 있다.가려움증은 담낭, 우르소데옥시콜산 또는 [2]나르토렉손과 같은 오피오이드 길항제들을 배출함으로써 도움을 받을 수 있다."황달"이라는 단어는 "황색병"[11][12]을 뜻하는 프랑스 자니스에서 유래했다.
징후 및 증상

성인의 황달의 가장 흔한 징후는 눈의 흰 부분(스크레라)과[13] 혈청 빌리루빈이 최소 3mg/[14]dl임을 나타내는 강직성 홍반과 함께 피부가 누렇게 변색되는 것이다.다른 일반적인 징후로는 어두운 소변(빌리루빈뇨)과 창백한 지방 대변(스테이터르헤아)[15]이 있다.빌리루빈은 피부 자극성이기 때문에 황달은 일반적으로 심한 [16][17]가려움과 관련이 있습니다.
안결막은 높은 엘라스틴 함량으로 인해 빌리루빈 증착에 대한 친화력이 특히 높다.따라서 혈청 빌리루빈의 약간의 증가는 공막의 황색을 관찰함으로써 조기에 검출할 수 있다.전통적으로 공막 홍반이라고 불리는 이 용어는 사실 잘못된 명칭입니다. 왜냐하면 빌리루빈 퇴적은 기술적으로 무혈관 공막 위에 있는 결막에서 발생하기 때문입니다.따라서 눈의 흰자색을 나타내는 적절한 용어는 결막성 홍반이다.[18]
특히 어린 시절에 황달의 훨씬 덜 흔한 징후는 노란색이나 녹색을 띤 치아이다.성장기 아동의 경우 고빌리루빈혈증은 치아 [19]석회화 과정에서 빌리루빈 침착으로 인해 치아의 노란색 또는 녹색 변색을 일으킬 수 있다.이는 고빌리루빈혈증이 있는 어린이에게 발생할 수 있지만, 고빌리루빈혈증으로 인한 치아 변색은 성인 간 질환을 가진 개인에게 관찰되지 않는다.초기 발달 중 복합 빌리루빈의 혈청 수치 상승과 관련된 질환도 치아 [20]저형성증을 일으킬 수 있다.
원인들
황달은 빌리루빈 대사 이상, 간 기능 장애, 담도-트럭트 폐색 등과 관련된 기초 질환의 존재를 나타내는 징후이다.일반적으로 황달은 빌리루빈의 혈중 수치가 3mg/dl을 [14]초과할 때 나타난다.황달은 병리학적 메커니즘의 어느 부분에 영향을 주느냐에 따라 세 가지 범주로 분류된다.다음의 3개의 카테고리가 있습니다.
| 카테고리 | 정의. |
|---|---|
| 용혈 전/용혈 전 | 간 대사 전에 적혈구 파열의 내인성 원인 또는 적혈구 파열의 외인성 원인 중 하나로 인해 병리가 발생한다. |
| 간/간세포 | 그 병리는 실질 간세포의 손상 때문이다. |
| 간 후/콜레스타틱 | 간에서 빌리루빈 접합 후 담도 폐색 및/또는 빌리루빈 [21]배설 감소로 인해 병리가 발생한다. |
간전 원인
간전 황달은 가장 일반적으로 적혈구 용혈의 병리학적 증가율에 의해 발생한다.적혈구 분해 증가 → 비결합 혈청 빌리루빈 증가 → 비결합 빌리루빈의 점막 [22]조직으로의 침착 증가.이러한 질병은 증가된 적혈구 [23]용혈로 인해 황달을 유발할 수 있습니다.
간 원인
간 황달은 빌리루빈의 [27]간 대사 이상에 의해 발생한다.간 황달의 주요 원인은 전염성, 약물/약물 유발, 자가면역 병인 또는 유전성 [28]유전 질환으로 인한 간세포의 심각한 손상이다.다음은 황달의 [citation needed]간 원인 중 일부를 나열한 것입니다.
- 급성 간염
- 만성 간염
- 간독성
- 간경화
- 약물성 간염
- 알코올성 간질환
- 길버트 증후군(인구의 약 5%에서 발견, 가벼운 황달 유발)
- 크리글러-나자르 증후군, I형
- 크리글러-나자르 증후군, II형
- 렙토스피라증
간 후 원인(폐색성 황달)
간 후 황달(장애성 황달)은 배설을 [29]위해 결합 빌리루빈을 포함한 담즙을 간 밖으로 운반하는 담관이 막혀서 발생합니다.간 후 황달을 일으킬 수 있는 상태를 다음에 나타냅니다.
- 담석증(일반 담관 담석증).그것은 폐색성 황달의 가장 흔한 원인이다.
- 췌두암
- 담도 협착
- 담도폐쇄증
- 원발성 담관염
- 임신의 담즙저하
- 급성 췌장염
- 만성 췌장염
- 췌장가성낭종
- 미리치 증후군
- 기생동물(오피스토르키과와 파시올리과의 [30]간 플룩스)
병태생리학
황달은 일반적으로 헴 대사의 정상적인 생리 경로를 따라 어떤 지점에서 발생하는 근본적인 병리학적 과정에 의해 발생한다.간 전, 간 및 간 후 범주의 중요성을 인식하기 위해서는 정상적인 헴 대사의 해부학적 흐름을 더 깊이 이해하는 것이 필수적이다.따라서, 헴 대사에 대한 해부학적 접근은 [citation needed]황달의 병태생리학에 대한 논의에 선행한다.
정상 헴 대사
간전대사
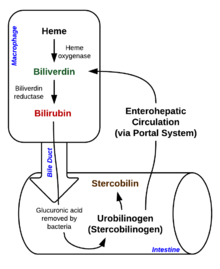
적혈구가 120일 정도 수명을 다하거나 손상되면 망상내피계를 통과하면서 파열돼 헤모글로빈을 포함한 세포 성분이 순환한다.대식세포는 식모세포 유리 헤모글로빈을 형성하고 그것을 헴과 글로빈으로 나눈다.그런 다음 헴 분자와 함께 두 가지 반응이 일어난다.첫 번째 산화 반응은 마이크로솜 효소인 헴 산소화효소에 의해 촉매되어 빌리베르딘(녹색 색소), 철, 일산화탄소를 생성한다.다음 단계는 빌리베르딘을 세포질 효소 빌리베르딘 환원효소에 의해 빌리루빈이라고 불리는 노란색 테트라피롤 색소로 환원시키는 것입니다.이 빌리루빈은 "비결합", "자유" 또는 "간접" 빌리루빈입니다.혈액 kg당 약 4mg의 빌리루빈이 [31]매일 생성됩니다.이 빌리루빈의 대부분은 방금 설명한 과정에서 만료된 적혈구로부터 헴이 분해되면서 발생합니다.그러나 약 20%는 비효율적인 적혈구 및 근육 미오글로빈 및 시토크롬과 [31]같은 다른 헴 함유 단백질의 분해를 포함한 다른 헴 소스로부터 온다.그리고 나서 비결합 빌리루빈은 혈류를 통해 간으로 이동한다.이 빌리루빈은 용해성이 없기 때문에 혈청 알부민에 [citation needed]결합된 혈액을 통해 운반된다.
간대사
비결합 빌리루빈이 간에 도달하면 간 효소 UDP-글루쿠로닐 전달효소가 빌리루빈 + 글루쿠론산 → 빌리루빈 디글루쿠로니드(환원 빌리루빈)를 결합시킨다.간에 결합된 빌리루빈은 수용성으로 담낭으로 [citation needed]배출된다.
간 후 대사
빌리루빈은 담즙을 통해 장으로 들어간다.장내에서는 빌리루빈이 공생장세균에 의해 우로빌리노겐으로 변환된다.대부분의 우로빌리노겐은 스테르코빌리노겐으로 변환되고 스테르코빌린으로 산화된다.스테르코빌린은 대변을 통해 배설되며, 대변의 특징적인 [32]갈색을 띤다.우로빌리노겐의 소량이 위장 세포로 재흡수된다.대부분의 재흡수 우로빌리노겐은 간담도 재순환을 거친다.재흡수된 우로빌리노겐의 적은 부분이 신장에 여과된다.소변에서 우로빌리노겐은 우로빌린으로 변환되어 소변의 특징적인 노란색을 [32]갖게 됩니다.
헴 대사 및 배설 이상
황달 병태 생리를 이해하는 한 가지 방법은 황달을 빌리루빈 생산 증가(이상 헴 대사) 또는 빌리루빈 배설 감소(이상 헴 배설)[citation needed]를 일으키는 질환으로 구성하는 것입니다.
간전병태생리학
간전 황달은 빌리루빈 생산의 병리적인 증가에서 비롯된다: 적혈구 용혈의 증가 속도는 빌리루빈 생산의 증가를 야기하고 점막 조직에서 빌리루빈의 침적을 증가시키고 노란색 [citation needed]색조가 나타난다.
간병태생리학
간성 황달(간세포 황달)은 간세포 사망 및 괴사 및 간세포 간 빌리루빈 수송 장애를 초래하는 간 기능의 현저한 장애에 기인한다.비결합 빌리루빈의 간세포 흡수와 복합 빌리루빈의 담낭으로의 간세포 운반 사이에 간세포를 통한 빌리루빈 수송이 어느 지점에서나 저해될 수 있다.또한 염증으로 인한 후속 세포부종은 간내 담도의 기계적 폐색을 일으킨다.가장 일반적으로, 빌리루빈 대사의 세 가지 주요 단계인 흡수, 결합, 배설에 대한 간섭은 보통 간세포 황달에서 발생한다.따라서 비결합 빌리루빈과 켤레 빌리루빈의 비정상적인 상승이 나타난다.배설(환율 제한 단계)이 가장 크게 손상되기 때문에 복합 고빌리루빈혈증이 우세하다.[33]
비결합 빌리루빈은 여전히 간세포로 들어가 일반적인 방식으로 결합된다.이 복합 빌리루빈은 아마도 충혈된 담관 파열과 간에서 나오는 림프로 담즙이 직접 배출됨으로써 혈액으로 돌아간다.따라서 혈장 중 빌리루빈의 대부분은 비결합형이 아닌 복합형이 되고, 장으로 가서 우로빌리노겐이 되지 않은 이 복합 빌리루빈은 소변을 어두운 색으로 [34][clarification needed]만든다.
간 후병태생리학
폐색성 황달이라고도 불리는 간 후 황달은 담도의 담즙 배설이 막혀 복합 빌리루빈과 담즙염이 증가하기 때문입니다.담관의 완전 폐색 시 복합 빌리루빈은 장에 접근할 수 없어 빌리루빈을 우로빌리노겐으로 전환하는 것을 방해하므로 스테르코빌린 또는 우로빌린은 생성되지 않는다.폐색성 황달에서는 과잉 복합 빌리루빈이 우로빌리노겐 없이 소변에 여과된다.소변(빌리루빈뇨)의 복합 빌리루빈은 소변을 비정상적으로 짙은 갈색으로 만듭니다.따라서 옅은 변(분뇨에 없는 스테코빌린)과 진한 소변(뇨중에 존재하는 복합 빌리루빈)의 존재는 황달의 폐색 원인을 시사한다.이러한 관련 징후는 많은 간 황달 조건에서도 양성이기 때문에 폐색성 대 간세포성 [35]황달의 원인을 구별할 수 있는 신뢰할 수 있는 임상적 특징이 될 수 없습니다.
진단.
황달 증세를 보이는 대부분의 사람들은 유의한 차이가 존재하지만 다양한 예측 가능한 간 패널 이상 패턴을 가지고 있다.전형적인 간 패널에는 아미노전달효소(ALT, AST), 알칼리인산가수분해효소(ALP), 빌리루빈(황달을 일으키는) 등 주로 간에서 발견되는 효소의 혈중 수치와 단백질 수치, 특히 총 단백질과 알부민이 포함됩니다.간 기능에 대한 다른 주요 실험실 검사로는 감마 글루타밀 트랜스펩티드가수분해효소(GGT)와 프로트롬빈 시간(PT)[36]이 있다.어떤 검사도 황달의 다양한 분류를 구별할 수 없다.진단에 도달하기 위해서는 간 기능 검사와 다른 신체 검사 결과를 조합하는 것이 필수적이다.[37]
실험실 테스트
| 간전 황달 | 간황달 | 간 후 황달 | |
|---|---|---|---|
| 총 혈청 빌리루빈 | 정상/증가 | 증가된 | 증가된 |
| 켤레 빌리루빈 | 보통의 | 증가된 | 증가된 |
| 비결합 빌리루빈 | 정상/증가 | 증가된 | 보통의 |
| 우로빌리노겐 | 정상/증가 | 감소. | 감소/음수 |
| 소변색 | 보통[38] | 다크(우로빌리노겐, 복합 빌리루빈) | 다크(공역 빌리루빈) |
| 변색 | 갈색 | 약간 창백하다 | 창백, 흰색 |
| 알칼리성 포스파타아제 농도 | 보통의 | 증가된 | 대폭 증가 |
| 알라닌전달효소 및 아스파르트산전달효소 농도 | 대폭 증가 | 증가된 | |
| 소변 중 켤레 빌리루빈 | 존재하지 않는다 | 현재의. | 현재의. |
일부 뼈와 심장 질환은 ALP와 아미노기전달효소의 증가를 초래할 수 있기 때문에, 이것들을 간 질환과 구별하는 첫 번째 단계는 간 특이적 조건에서만 상승하는 GGT의 수치를 비교하는 것이다.두 번째 단계는 황달과 변경된 실험실 결과의 담도(콜레스타틱) 또는 간 원인과 구별하는 것입니다.ALP 및 GGT 수치는 일반적으로 하나의 패턴으로 상승하는 반면 아스파르트산아미노전달효소(AST) 및 알라닌아미노전달효소(ALT)는 별도의 패턴으로 상승한다.ALP(10~45 IU/l) 및 GGT(18~85 IU/l) 수치가 AST(12~38 IU/l) 및 ALT(10~45 IU/l) 수치만큼 비례적으로 상승하는 경우 이는 콜레스테롤 문제가 있음을 의미한다.그러나 AST 및 ALT 상승이 ALP 및 GGT 상승보다 유의하게 높으면 간에 문제가 있음을 나타냅니다.마지막으로, 황달의 간 원인을 구별하는 것은 AST와 ALT의 수치를 비교하는 것이 유용할 수 있다.AST 레벨은 일반적으로 ALT보다 높습니다.이는 간염(바이러스 또는 간독성)을 제외한 대부분의 간 질환에서 여전히 해당된다.알코올성 간 손상은 상당히 정상적인 ALT 수치를 가질 수 있으며, AST는 ALT보다 10배 더 높습니다.그러나 ALT가 AST보다 높으면 간염임을 나타냅니다.ALT와 AST의 수치는 매우 높은 수치에서 급격한 감소는 심각한 괴사를 나타낼 수 있지만 간 손상의 정도와는 관련이 없다.알부민 수치가 낮은 것은 만성적인 상태를 나타내는 경향이 있는 반면, 간염과 콜레스트증은 [citation needed]정상입니다.
간 패널에 대한 실험실 결과는 순수가 아닌 차이의 크기 및 비율에 따라 자주 비교된다.AST:ALT 비율은 이 질환이 알코올성 간 손상(10 이상), 다른 형태의 간 손상(1 이상) 또는 간염(1 미만)인지 여부를 나타내는 좋은 지표가 될 수 있습니다.빌리루빈 수치가 정상치의 10배 이상일 경우 종양성 또는 간내 콜레스테롤을 나타낼 수 있습니다.이보다 낮은 수치는 간세포의 원인을 나타내는 경향이 있다.정상치의 15배 이상의 AST 수치는 급성 간세포 손상을 나타내는 경향이 있다.이것보다 작으면 폐색 원인을 나타내는 경향이 있습니다.정상치의 5배 이상의 ALP 수치는 폐색을 나타내는 경향이 있는 반면, 정상치의 10배 이상의 수치는 약물(독신) 유도 콜레스테롤 간염 또는 사이토메갈로바이러스 감염을 나타낼 수 있습니다.이 두 조건 모두 ALT와 AST가 정상의 20배 이상일 수 있습니다.GGT 수치가 정상치의 10배를 넘으면 일반적으로 담즙저하증이 나타납니다.레벨 5~10은 바이러스성 간염을 나타내는 경향이 있다.정상치의 5배 미만은 약물 독성을 나타내는 경향이 있다.급성 간염은 일반적으로 ALT와 AST 수치가 정상의 20-30배(1000배 이상) 상승하며, 몇 주 동안 현저하게 상승할 수 있다.아세트아미노펜 독성은 ALT 및 AST 수치가 [citation needed]정상보다 50배 이상 높아질 수 있습니다.
검사 결과는 황달의 원인에 따라 달라집니다.
- 소변: 복합 빌리루빈 존재, 우로빌리노겐 > 2 단위이지만 가변적(어린이 제외)
- 혈장 단백질은 특징적인 변화를 보인다.
- 혈장 알부민 수치는 낮지만 항체 형성이 증가하여 혈장 글로불린이 상승한다.
비결합 빌리루빈은 소수성이기 때문에 소변으로 배설할 수 없다.따라서 소변에 빌리루빈이 없는 상태에서 소변에서 우로빌리노겐이 증가했다는 사실은 용혈성 황달을 기초 질환 [39]과정으로 시사한다.Urobilinogen은 용혈성 빈혈이 헴 대사를 증가시키기 때문에 2단위 이상일 것이다. 단, 장내 균이 발달하지 않은 유아의 경우는 예외이다.)반대로 켤레빌리루빈은 친수성이므로 [40]소변에 없는 비결합빌리루빈과 대조적으로 소변에 존재하는 빌리루빈으로 검출될 수 있다.
이미징
초음파, CT 스캔, HIDA 스캔 등의 의료 영상은 담도 폐색을 [40]검출하는 데 유용합니다.
차동 진단
피부, 특히 손바닥과 발바닥의 노란색 변색은 종종 경동맥혈증(무해한 상태)[41]에 기인한다.
치료
황달의 치료는 근본적인 [5]원인에 따라 다르다.담관이 막힌 경우 일반적으로 수술이 필요하며, 그렇지 않은 경우 관리는 [5][42][43][44]의료입니다.
합병증
고빌리루빈혈증은, 보다 정확하게는 비접합 분획으로 인한 고빌리루빈혈증으로 인해 빌리루빈이 중추신경계의 회백질에 축적되어 돌이킬 수 없는 신경학적 손상을 일으킬 수 있으며, 이는 kernfuldus로 알려진 상태를 초래할 수 있다.노출의 정도에 따라 눈에 띄지 않는 것에서부터 심각한 뇌 손상, 심지어 사망에 이르기까지 그 영향은 다양하다.신생아는 고빌리루빈혈증으로 인한 신경학적 손상에 특히 취약하므로 혈청 빌리루빈 [citation needed]수치 변화를 주의 깊게 관찰해야 합니다.
지혈이 손상된 실질성 간질환자는 출혈에 [45]문제가 생길 수 있다.
역학
성인의 황달은 드물다.[46][47][48]영국에서 5년간 DISCOVERY 프로그램에 따르면 45세 이상 개인 1000명당 연간 황달 발생률은 0.74명이었다. 그러나 [49]이 비율은 프로그램의 주요 목표 수집 및 분석으로 인해 약간 부풀려질 수 있다.황달은 ICU에서 [48]황달을 경험하는 집중 치료가 필요한 환자의 최대 40%의 발병률로 질병의 심각성과 관련이 있다.중환자실 환경에서 황달의 원인은 ICU 체류의 주된 이유로서 황달에 기인하거나 기초 질환(예: 패혈증)[48]에 대한 이환률에 기인한다.
선진국에서 황달의 가장 흔한 원인은 담관폐색이나 약물유발이다.개발도상국에서 황달의 가장 흔한 원인은 바이러스성 간염, 렙토스피라증, 주혈흡충증, [4]말라리아와 같은 전염병이다.
위험요소
높은 혈청 빌리루빈 수치와 관련된 위험 요소에는 남성 성별, 백인 인종, 적극적 [50]흡연이 포함됩니다.성인의 평균 혈청 총 빌리루빈 수치는 남성(0.72±0.004mg/dl)이 여성(0.52±0.003mg/dl)[50]보다 높은 것으로 나타났다.성인에서 높은 빌리루빈 수치는 비히스패닉계 백인 인구(0.63 ± 0.004mg/dl)와 멕시코계 미국인 인구(0.61 ± 0.005mg/dl)에서도 확인되며, 비히스패닉계 흑인 인구(0.55 ± 0.005mg/dl)[50]에서는 낮다.빌리루빈 수치는 활발한 [50]흡연자에게서 더 높다.
특수 모집단
신생아 황달
증상
유아의 황달은 피부가 누렇게 변하고 황달과 황달성 강막을 일으킨다.신생아 황달은 얼굴과 목에 영향을 미치는 두부 패턴으로 [51]퍼지며, 더 심각한 경우 몸통, 하지로 퍼집니다.다른 증상으로는 졸음, 영양 부족 등이 있을 수 있으며, 심각한 경우 비결합 빌리루빈이 혈액-뇌 장벽을 넘어 영구적인 신경학적 손상(커널황달)을 일으킬 수 있다.
원인들
유아에게 황달의 가장 흔한 원인은 정상적인 생리적 황달이다.신생아 황달의 병리학적 원인은 다음과 같다.
- 조제 황달[52]
- 유전성 구상세포증
- 포도당6-인산탈수소효소결핍증
- 피루브산인산화효소결핍증
- ABO/Rh형 자가항체
- 알파1-항이트립신결핍증
- 알라길 증후군(간내 담관 저형성을 초래하는 유전적 결함)
- 진행성 가족성 간내 담즙혈증
- 화농세포증(비타민 결핍으로 인한)
- 크레틴증(공중 갑상선 기능 저하증)
- 패혈증 및 기타 감염 원인
병태생리학
일시적 신생아 황달은 출생 [53]첫 주에 80% 이상이 황달을 경험하는 신생아(28일 미만 어린이)에게 발생하는 가장 흔한 질환 중 하나이다.유아의 황달은 성인과 마찬가지로 빌리루빈 수치가 증가하는 것이 특징이다(유아: 총 혈청 빌리루빈 5mg/dL 이상).
정상적인 생리적 신생아 황달은 빌리루빈 대사와 관련된 간 효소의 미성숙, 미숙한 내장 미생물 및 태아 헤모글로빈(HbF)[54]의 분해 증가로 인해 발생합니다.모유 황달은 모유의 β-글루쿠로니다아제 농도 증가에 의해 발생하며, 이는 빌리루빈 탈결합 및 빌리루빈 재흡수를 증가시켜 비결합성 고빌리루빈혈증과 함께 생리학적 황달의 지속성을 초래한다.모유 황달의 시작은 생후 2주 이내이며 4-13주 [citation needed]동안 지속된다.
신생아 황달의 대부분의 경우는 해롭지 않지만 빌리루빈 수치가 매우 높을 경우 뇌 손상(커널 황달)이 발생하여 심각한 [56]장애를 초래할 수 있습니다[55][8].Kern 황달은 증가된 비결합 빌리루빈(알부민에 의해 운반되지 않는 빌리루빈)과 관련이 있다.신생아는 특히 태아 헤모글로빈의 분해와 장내 식물군의 미성숙과 동시에 비결합 빌리루빈의 증가와 함께 발생하는 혈액-뇌 장벽의 투과성 증가로 인해 이러한 손상에 취약하다.이 상태는 최근 몇 년 동안 증가하고 있다. 아기들이 햇빛을 [citation needed]쬐는 시간이 줄어들면서.
치료
신생아의 황달은 보통 일시적이며 의학적 개입 없이 사라진다.혈청 빌리루빈 수치가 4–21mg/dl(68–360μmol/l) 이상일 경우, 신생아의 나이와 미숙아 [9]상태에 따라 광선 치료 또는 교환 수혈을 받을 수 있다.담즙등은 종종 아기를 집중적인 광선 [57]치료에 노출시키는 것으로 구성된 조기 치료에 사용되는 도구입니다.2014년 체계적 검토에서는 병원 기반 [58]치료와 가정 치료의 결과가 다른지 여부를 나타내는 증거가 발견되지 않았다.2021년 코크란의 체계적 검토 결과, 과열과 [59]피부 손상을 방지하기 위해 주의를 기울이는 한 햇빛을 광선 치료를 보충하는 데 사용할 수 있는 것으로 나타났습니다.햇빛 자체가 효과적인 [59]치료제라고 결론지을 만한 충분한 증거가 없었다.빌리루빈 수치는 배설(배변 및 배뇨)을 통해서도 감소하기 때문에 [60]유아의 황달을 줄이기 위해 빈번하고 효과적인 영양섭취가 필수적입니다.
어원학
황달은 노란색을 뜻하는 프랑스 자운에서 유래했고, 황달은 "노란 질병"을 뜻하는 자운스입니다.그것의 의학용어는 그리스어 이케로스([61]ikteros)에서 유래한 ilcterus이다.황달이라는 말의 [62]유래는 황달을 보면 낫는다는 고대 믿음에서 유래한 기이한 말이다.황달이라는 용어는 때때로 공막 특유의 [61][63]황달을 지칭하는 데 잘못 쓰이기도 한다.
레퍼런스
- ^ Torre DM, Lamb GC, Ruiswyk JV, Schapira RM (2009). Kochar's Clinical Medicine for Students. Lippincott Williams & Wilkins. p. 101. ISBN 9780781766999.
- ^ a b c Bassari R, Koea JB (February 2015). "Jaundice associated pruritis: a review of pathophysiology and treatment". World Journal of Gastroenterology. 21 (5): 1404–13. doi:10.3748/wjg.v21.i5.1404. PMC 4316083. PMID 25663760.
- ^ a b c d Jaundice. MedlinePlus. Archived from the original on 27 August 2016. Retrieved 13 August 2016.
- ^ a b c d e f g h Jones R (2004). Oxford Textbook of Primary Medical Care. Oxford University Press. p. 758. ISBN 9780198567820. Archived from the original on 8 September 2017.
- ^ a b c d e f Ferri FF (2014). Ferri's Clinical Advisor 2015: 5 Books in 1. Elsevier Health Sciences. p. 672. ISBN 9780323084307. Archived from the original on 8 September 2017.
- ^ Buttaro TM, Trybulski J, Polgar-Bailey P, Sandberg-Cook J (2012). Primary Care: A Collaborative Practice (4 ed.). Elsevier Health Sciences. p. 690. ISBN 978-0323075855. Archived from the original on 8 September 2017.
- ^ Al-Tubaikh, Jarrah Ali (2017). Internal Medicine. doi:10.1007/978-3-319-39747-4. ISBN 978-3-319-39746-7.
- ^ a b Kaplan M, Hammerman C (2017). "Hereditary Contribution to Neonatal Hyperbilirubinemia". Fetal and Neonatal Physiology. Elsevier: 933–942.e3. doi:10.1016/b978-0-323-35214-7.00097-4. ISBN 978-0-323-35214-7.
- ^ a b c Maisels MJ (March 2015). "Managing the jaundiced newborn: a persistent challenge". CMAJ. 187 (5): 335–43. doi:10.1503/cmaj.122117. PMC 4361106. PMID 25384650.
- ^ a b c Winger J, Michelfelder A (September 2011). "Diagnostic approach to the patient with jaundice". Primary Care. 38 (3): 469–82, viii. doi:10.1016/j.pop.2011.05.004. PMID 21872092.
- ^ Dr. Chase's Family Physician, Farrier, Bee-keeper, and Second Receipt Book,: Being an Entirely New and Complete Treatise ... Chase Publishing Company. 1873. p. 542. Archived from the original on 8 September 2017.
- ^ Sullivan KM, Gourley GR (2011). Jaundice. Pediatric Gastrointestinal and Liver Disease. Elsevier. pp. 176–186.e3. doi:10.1016/b978-1-4377-0774-8.10017-x. ISBN 978-1-4377-0774-8.
- ^ Gondal B, Aronsohn A (December 2016). "A Systematic Approach to Patients with Jaundice". Seminars in Interventional Radiology. 33 (4): 253–258. doi:10.1055/s-0036-1592331. PMC 5088098. PMID 27904243.
- ^ a b Reuben A (2012). "Jaundice". Textbook of Clinical Gastroenterology and Hepatology. John Wiley & Sons, Ltd. pp. 84–92. doi:10.1002/9781118321386.ch15. ISBN 978-1-118-32138-6.
- ^ Goroll AH (2009). Primary care medicine : office evaluation and management of the adult patient (6th ed.). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. p. 496. ISBN 9780781775137. Archived from the original on 8 September 2017.
- ^ James, William D. (2006). Andrews' diseases of the skin : clinical dermatology. Berger, Timothy G., Elston, Dirk M., Odom, Richard B., 1937– (10th ed.). Philadelphia: Saunders Elsevier. ISBN 0-7216-2921-0. OCLC 62736861.
- ^ Bassari, Ramez (2015). "Jaundice associated pruritis: A review of pathophysiology and treatment". World Journal of Gastroenterology. 21 (5): 1404–1413. doi:10.3748/wjg.v21.i5.1404. ISSN 1007-9327. PMC 4316083. PMID 25663760.
- ^ McGee, Steven R. (2018). "Jaundice". Evidence-Based Physical Diagnosis (4th ed.). Philadelphia, PA: Elsevier. pp. 59–68. ISBN 978-0-323392761.
- ^ Neville BW (2012). Oral and Maxillofacial Pathology (3rd ed.). Singapore: Elsevier. p. 798. ISBN 9789814371070.
- ^ Amin SB, Karp JM, Benzley LP (May 2010). "Unconjugated hyperbilirubinemia and early childhood caries in a diverse group of neonates". American Journal of Perinatology. 27 (5): 393–7. doi:10.1055/s-0029-1243314. PMC 3264945. PMID 20013583.
- ^ Chatterjea MN, Shinde R (2012). Textbook of medical biochemistry (8th ed.). New Delhi: Jaypee Brothers Medical Publications (P) Ltd. p. 672. ISBN 978-93-5025-484-4.
- ^ Joseph, Abel; Samant, Hrishikesh (2022), "Jaundice", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 31334972, retrieved 23 April 2022
- ^ "What causes jaundice in hemolytic anemia?". www.medscape.com. Retrieved 26 April 2022.
- ^ "What Is Sickle Cell Disease?". National Heart, Lung, and Blood Institute. 12 June 2015. Archived from the original on 6 March 2016. Retrieved 8 March 2016.
- ^ Robert S. Hillman; Kenneth A. Ault; Henry M. Rinder (2005). Hematology in clinical practice: a guide to diagnosis and management. McGraw-Hill Professional. pp. 146–. ISBN 978-0-07-144035-6. Retrieved 15 November 2010.
- ^ "Thalassemia". The Lecturio Medical Concept Library. Retrieved 27 July 2021.
- ^ Kalakonda, Aditya; Jenkins, Bianca A.; John, Savio (2022), "Physiology, Bilirubin", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 29261920, retrieved 23 April 2022
- ^ Tripathi, Nishant; Jialal, Ishwarlal (2022), "Conjugated Hyperbilirubinemia", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 32965843, retrieved 23 April 2022
- ^ "Bilirubin Metabolism – an overview ScienceDirect Topics". www.sciencedirect.com. Retrieved 23 April 2022.
- ^ "CDC – Liver Flukes". www.cdc.gov. 18 April 2019. Retrieved 5 June 2020.
- ^ a b Pashankar D, Schreiber RA (July 2001). "Jaundice in older children and adolescents". Pediatrics in Review. 22 (7): 219–26. doi:10.1542/pir.22-7-219. PMID 11435623. S2CID 11100275.
- ^ a b Berthelot, P.; Duvaldestin, Ph.; Fevery, J. (18 January 2018), "Physiology and Disorders of Human Bilirubin Metabolism", Bilirubin, CRC Press, pp. 173–214, doi:10.1201/9781351070119-6, ISBN 978-1-351-07011-9
- ^ Mathew KG (2008). Medicine: Prep Manual for Undergraduates (3rd ed.). Elsevier India. pp. 296–297. ISBN 978-8131211540.
- ^ Hall JE, Guyton AC (2011). Textbook of Medical Physiology. Saunders/Elsevier. p. 841. ISBN 978-1416045748.
- ^ Beckingham IJ, Ryder SD (January 2001). "ABC of diseases of liver, pancreas, and biliary system. Investigation of liver and biliary disease". BMJ. 322 (7277): 33–6. doi:10.1136/bmj.322.7277.33. PMC 1119305. PMID 11141153.
- ^ "Liver Function Tests". MedlinePlus. US National Library of Medicine. Retrieved 16 January 2021.
- ^ Roche SP, Kobos R (2004). "Jaundice in the Adult Patient". American Family Physician. 69 (2): 299–304. PMID 14765767. Retrieved 22 September 2020.
- ^ Llewelyn H, Ang HA, Lewis K, Al-Abdullah A (2014). Oxford Handbook of Clinical Diagnosis. Oxford University Press. p. 18. ISBN 9780199679867. Archived from the original on 8 September 2017.
- ^ Cadogen M (21 April 2019). "Bilirubin and Jaundice". Life in the Fast Lane. Retrieved 19 November 2019.
- ^ a b Roche SP, Kobos R (January 2004). "Jaundice in the adult patient". American Family Physician. 69 (2): 299–304. PMID 14765767.
- ^ eMedicine에서의 경동맥혈증
- ^ Wang, Long; Yu, Wei-Feng (March 2014). "Obstructive jaundice and perioperative management". Acta Anaesthesiologica Taiwanica. 52 (1): 22–29. doi:10.1016/j.aat.2014.03.002. ISSN 1875-4597. PMID 24999215.
- ^ Dixon, Elijah; Vollmer, Charles M.; May, Gary R., eds. (2015). Management of Benign Biliary Stenosis and Injury. doi:10.1007/978-3-319-22273-8. ISBN 978-3-319-22272-1.
- ^ Lorenz, Jonathan (31 October 2016). "Management of Malignant Biliary Obstruction". Seminars in Interventional Radiology. 33 (4): 259–267. doi:10.1055/s-0036-1592330. ISSN 0739-9529. PMC 5088103. PMID 27904244.
- ^ Neville BW (2012). Oral and Maxillofacial Pathology (3rd ed.). Singapore: Elsevier. p. 798. ISBN 9789814371070.
- ^ Ahmad J, Friedman SL, Dancygier H (2014). Mount Sinai Expert Guides: Hepatology. John Wiley & Sons. ISBN 9781118742525. Archived from the original on 8 September 2017.
- ^ Björnsson, Einar; Gustafsson, Jonas; Borkman, Jakob; Kilander, Anders (2008). "Fate of patients with obstructive jaundice". Journal of Hospital Medicine. 3 (2): 117–123. doi:10.1002/jhm.272. ISSN 1553-5592. PMID 18438808.
- ^ a b c Bansal, Vishal; Schuchert, Vaishali Dixit (December 2006). "Jaundice in the Intensive Care Unit". Surgical Clinics of North America. 86 (6): 1495–1502. doi:10.1016/j.suc.2006.09.007. ISSN 0039-6109. PMID 17116459.
- ^ Taylor, Anna; Stapley, Sally; Hamilton, William (1 August 2012). "Jaundice in primary care: a cohort study of adults aged >45 years using electronic medical records". Family Practice. 29 (4): 416–420. doi:10.1093/fampra/cmr118. ISSN 0263-2136. PMID 22247287.
- ^ a b c d Zucker, Stephen D.; Horn, Paul S.; Sherman, Kenneth E. (October 2004). "Serum bilirubin levels in the U.S. Population: Gender effect and inverse correlation with colorectal cancer". Hepatology. 40 (4): 827–835. doi:10.1002/hep.1840400412. PMID 15382174. S2CID 25854541.
- ^ Telega, Grzegorz W. (2018). "Jaundice". Nelson Pediatric Symptom-Based Diagnosis. Elsevier. pp. 255–274.e1. doi:10.1016/b978-0-323-39956-2.00015-7. ISBN 978-0-323-39956-2.
- ^ Bertini G, Dani C, Tronchin M, Rubaltelli FF (March 2001). "Is breastfeeding really favoring early neonatal jaundice?". Pediatrics. 107 (3): E41. doi:10.1542/peds.107.3.e41. PMID 11230622.
- ^ Maisels, M. Jeffrey (17 March 2015). "Managing the jaundiced newborn: a persistent challenge". Canadian Medical Association Journal. 187 (5): 335–343. doi:10.1503/cmaj.122117. ISSN 0820-3946. PMC 4361106. PMID 25384650.
- ^ Collier J, Longore M, Turmezei T, Mafi AR (2010). "Neonatal jaundice". Oxford Handbook of Clinical Specialties. Oxford University Press. ISBN 978-0-19-922888-1.[페이지 필요]
- ^ "Facts about Jaundice and Kernicterus". CDC. 23 February 2015. Archived from the original on 8 August 2016. Retrieved 13 August 2016.
- ^ Click R, Dahl-Smith J, Fowler L, DuBose J, Deneau-Saxton M, Herbert J (2013). "An osteopathic approach to reduction of readmissions for neonatal jaundice". Osteopathic Family Physician. 5 (1): 17–23. doi:10.1016/j.osfp.2012.09.005.
- ^ "Bili Lights for Jaundice: Effectiveness for Neonatal and Adults Heliotherapy Research Institute". Retrieved 24 July 2022.
- ^ Malwade, Ujjwala S; Jardine, Luke A (2014). "Home- versus hospital-based phototherapy for the treatment of non-haemolytic jaundice in infants at more than 37 weeks' gestation". Cochrane Database of Systematic Reviews (6): CD010212. doi:10.1002/14651858.cd010212.pub2. ISSN 1465-1858. PMID 24913724.
- ^ a b Horn, Delia; Ehret, Danielle; Gautham, Kanekal S; Soll, Roger (6 July 2021). Cochrane Neonatal Group (ed.). "Sunlight for the prevention and treatment of hyperbilirubinemia in term and late preterm neonates". Cochrane Database of Systematic Reviews. 2021. doi:10.1002/14651858.CD013277.pub2. PMC 8259558. PMID 34228352.
- ^ O'Keefe L (May 2001). "Increased vigilance needed to prevent kernicterus in newborns". American Academy of Pediatrics. 18 (5): 231. Archived from the original on 27 September 2007.
- ^ a b "Definition of Icterus". MedicineNet.com. 2011. Archived from the original on 7 August 2012. Retrieved 3 February 2013.
- ^ "Questions and Answers". JAMA: The Journal of the American Medical Association. 186 (6): 615. 9 November 1963. doi:10.1001/jama.1963.03710060101048. ISSN 0098-7484.
- ^ ICTerus Define ICTerus Dictionary.com 2010-12-31 Wayback Machine 아카이브 완료Dictionary.reference.com 를 참조해 주세요.2013-12-23에 취득.