금속 이산화탄소 복합체
Metal carbon dioxide complex금속 이산화탄소 복합체는 이산화탄소 리간드를 함유한 조정 복합체다. 단순 분자의 조정 화학에 대한 근본적인 관심과는 별개로, 이 분야의 연구는 전환 금속이 CO의2 유용한 변환을 촉진할 수 있다는 가능성에 의해 동기 부여된다. 이 연구는 유기적 합성 및 석유 기반 연료의 사용을 피할 수 있는 "태양 연료"의 생산과 관련이 있다.[1]
구조 경향
 변환 금속 이산화탄소 복합체의 예시 구조: 왼쪽부터 Ni(--CO22)(PCy3),2 Rh(--CO1212)Cl4(L4 = (diars),2 Metalacarboxylic ester CpFe(CO1)((:(-2CO)Re(5CO) 및 다른 디메탈라-ester.
변환 금속 이산화탄소 복합체의 예시 구조: 왼쪽부터 Ni(--CO22)(PCy3),2 Rh(--CO1212)Cl4(L4 = (diars),2 Metalacarboxylic ester CpFe(CO1)((:(-2CO)Re(5CO) 및 다른 디메탈라-ester.
이산화탄소는 단지 몇 가지 방법으로 금속과 결합한다. 본딩 모드는 금속 중심부의 전기영역성 및 기본성에 따라 달라진다.[2] 가장2.[3][4] 흔한 것은 아레스타의 콤플렉스인 니(CO2)(PCY3)에서 도해한 η-CO22 조정 모드로서,2 CO의 첫 번째 콤플렉스로 보고된 이 사각 평면 화합물은 CO2 리간드를 줄인 니(II)의 파생물이다. 드문 경우지만 CO는2 산소센터를 통해 루이스 기지로 금속과 결합하지만, 그러한 유도체는 약하고 주로 이론적 관심사가 있다. 다양한 다핵 복합체는 루이스 베이직과 루이스 산성 금속(예: 메탈리카복실산염(CH52)Fe(CO))2을 포함하는 경우도 종종 알려져 있다.COK2−+. 다핵 사례(금속이 둘 이상 포함된 복합체)에서는 더 복잡하고 더 다양한 조정 기하학적 형상이 관찰된다. 한 예로 네 개의 레늄 중심, [(5CO2)ReCORe(42[citation needed]CO)]를 포함하는 비대칭 화합물이 있다. 이산화탄소는 또한 하이드록시 리간드를 카보나토 리간드로 변환시킴으로써 금속 복합체(금속과 동일)의 리간드에 결합할 수 있다.[citation needed]
반응
전이 금속 이산화탄소 복합체는 다양한 반응을 겪는다. 메탈리카르복실산은 산소에서 양성되어 결국 금속 카보닐 복합체로 전환된다.
- [LMCOn2]− + 2H+ → [LMCOn]+ + HO2
이 반응은 CO에서2 연료로의 잠재적 촉매변환과 관련이 있다.[5]
금속-탄소 결합의 탄산화
Cu-C 본드에 삽입
N-heterocyclic carbene (NHC)은 CuI 콤플렉스가 유기농 에스테르의 탄복제를 촉진하도록 지원했다.[6] 이 촉매는 NHC 리간드인 CuCl과 KOBu에서t 형성된다. 구리 테르트-부토산화물은 유기농 에스테르와 함께 투과하여 Cu-CI 결합을 생성할 수 있으며, 중간은 CO에2 부드럽게 삽입되어 각각의 카르복시산을 얻을 수 있다. 코부(KOBut)가 함유된 염기전환은 제품을 방출하고 촉매(Scheme 2)를 재생한다.
투과 외에 Cu-C 결합을 형성하는 다른 접근법이 있다. C-H 기능화는 직설적이고 원자적인 경제 방식이다. 베이스는 산성 C-H 양성자를 감압시키고 Cu-C 결합을 형성하는 데 도움을 줄 수 있다. [(페난트로라인)[7]Cu(PR3))] CsCO와23 함께 단자 알키네스에 대한 촉매 효과 C-H 카르복실화. NHC-Cu-H 종은 단자 알키네스의 탄복제를 유발하기 위해 산성 양성자를 감압한다.[8] Cu-H 종은 Cu-F와 유기체로부터 생성되었다. 카복실산물은 실릴 에테르를 얻기 위해 실릴 플루오르에 의해 갇혔다. 비산성 C-H 본드의 경우, BuAl3(TMP)Li와의 유도 금속화가 채택된 후 구리로 투과하여 Cu-C 본드를 얻는다. Alilic C-H 본드와 페닐 C-H 본드는 Hou와 동료들에 의해 다음과 같은 접근법으로 탄복시화되었다.[9][10]
오르가노진크와 오르가노민크 시약을 사용한 알키네스와 알렌에 대한 카르보메탈레이션에 이어 구리로의 투과도 카르복시화를 개시하는 전략이다. 트리메틸알루미늄은 에테르 디렉팅 그룹이 연출한 싱 패션으로 편중되지 않은 알키네스에 삽입할 수 있다. 비닐 구리 콤플렉스는 투과로 형성되고, 비슷한 경로로 탄복실화가 실현되어 사분해성 알리파틱 비닐 카르복실산이 나온다.[11] 이 경우 섭생성은 6mb(memb) 알루미늄 링 형성의 호의에 의해 제어된다. 또한, 유사한 접근법을 통해 반응성이 낮은 디메틸 아연을 사용하여 이나미드와 알라나미드에 카르복실화를 달성할 수 있다.[12][13]
Pd-C 본드에 삽입
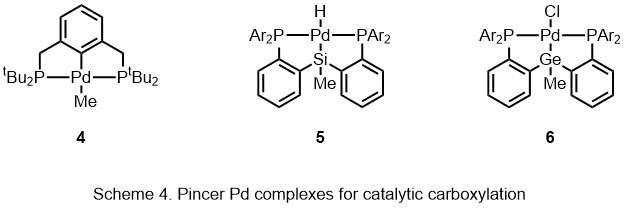
CO2 1-30 bar 미만의 팔라듐 아세테이트가 존재하는 경우, 단순한 방향성 화합물이 방향성 카르복실산으로 변환된다.[14][15][16][17][18] PSiP-핀서 리간드(5)는 사전 기능화된 기판을 사용하지 않고 알렌의 카르복시화를 촉진한다.[19] 팔라듐으로 투과하기3 위해 촉매 재생, EtAl이 추가되었다. 다음과 같은 β-H 제거에 의해 촉매가 재생된다. 말단 알렌과는 별도로 일부 내부 알렌도 이러한 반응에서 용인되어 수율이 54%~95%인 아릴 카복실산을 생성한다. 이 시스템은 1,3-다이엔에도 적용되어 카복실산을 1,2 추가 방식으로 발생시켰다.[20] 이와사와 외 연구진은 2015년 게르마늄 아날로그(6)를 보고하고 CO2 선원과 하이드라이드 선원을 결합해 염류를 형성했다.[21]
팔라듐은 C-H 기능화를 촉진하는 막강한 힘을 보였다. C-H 활성화로 인해 카르복실화 반응의 Pd-C 중간값이 발생하는 경우, 그러한 방법론은 금속 촉매 카르복실화를 훨씬 더 높은 효용 수준으로 촉진해야 한다. 이와사와와 동료들은 쿠마린 유도체를 생성하는 스타일레닐 C-H 활성화에 의한 직접적인 탄복제 효과를 보고했다.[22] 다른 전자적 특성을 가진 벤젠 링과 일부 이질적 링은 50%에서 90%까지 수율과 함께 이러한 반응에서 허용된다. C-H 활성화는 결정학 연구에 의해 입증되었다.
Rh-C 본드에 의한 삽입
위에서 언급한 Cu(I) 화학처럼 Rh(I) 복합체도 아릴보론 에스테르와 함께 투과하여 아릴로듐 중간체를 얻을 수 있으며, 여기에 CO가2 삽입되어 카복실산을 제공할 수 있다.[23] 이후 이와사와 외에서는 C-H 카르복시화 전략을 설명했다. Rh(I)는 아릴 C-H 결합에 산화성 첨가 후 알킬 알루미늄 종과의 투과성을 겪는다. 아르-Rh(I)는 메탄을 방출하는 환원 제거에 의해 재생된다. 아르-Rh(I) 공격 CO는2 아릴 보론산으로 투과하여 제품의 보론산을 방출하여 가수분해에 의한 최종 카르복실산을 제공한다. 지시된 버전과 지시되지 않은 버전이 모두 달성된다.[24][25][26]
이와사와의 동료들은 Rh(I)가 비닐라렌에 Rh-H 삽입에 의해 촉발된 탄산화 반응을 촉진시켰다. CO에2 핵동위원소를 추가한 후 반응성 Rh-H를 재생하기 위해 광촉매 양성자 결합 전자전달 접근법을 채택하였다.[27] 이 시스템에서, 과도한 양의 디에틸프로필틸틸아민(Deethylpyltylamine)은 희생 전자 공여자로 작용한다(Scheme 5).
Ni-C 결합에 의한 삽입
벤질 할로겐화물의 카르복시화가 보고되었다.[28] 반응 메커니즘은 니(0)에 염화 벤질(benzyl)을 산화 첨가하는 것을 제안한다. 니(II) 벤질 콤플렉스는 예를 들어 아연에 의해 니(I)로 감소하고, 아연은 니켈 카르복실산을 전달하는 CO를2 삽입한다. Ni(I) 카복시산물을 Ni(0)로 감소시키면 아연 카복시산염(Scheme 6)이 배출된다. 이와 유사하게, 아릴과 벤질 피발레이트,[29] 알킬 할리드,[30][31] 아릴 에스테르에서도 그러한 카르복시화가 이루어졌다.[32]
참조
- ^ 미슐레 아레스타가 편집한 "화학 공급원으로서의 이산화탄소" Wiley-VCH, Weinheim, 2010. ISBN978-3-527-32475-0
- ^ Gibson, Dorothy H. (1996). "The Organometallic Chemistry Carbon Dioxide". Chem. Rev. 96 (6): 2063–2095. doi:10.1021/cr940212c. PMID 11848822.
- ^ Aresta, Michele; Gobetto, Roberto; Quaranta, Eugenio; Tommasi, Immacolata (October 1992). "A bonding-reactivity relationship for (carbon dioxide)bis(tricyclohexylphosphine)nickel: a comparative solid-state-solution nuclear magnetic resonance study (phosphorus-31, carbon-13) as a diagnostic tool to determine the mode of bonding of carbon dioxide to a metal center". Inorganic Chemistry. 31 (21): 4286–4290. doi:10.1021/ic00047a015.
- ^ Yeung, Charles S.; Dong, Vy M. (June 2008). "Beyond Aresta's Complex: Ni- and Pd-Catalyzed Organozinc Coupling with CO". Journal of the American Chemical Society. 130 (25): 7826–7827. doi:10.1021/ja803435w. PMID 18510323.
- ^ Benson, Eric E.; Kubiak, Clifford P.; Sathrum, Aaron J.; Smieja, Jonathan M. (2009). "Electrocatalytic and homogeneous approaches to conversion of CO2 to liquid fuels". Chem. Soc. Rev. 38 (1): 89–99. doi:10.1039/b804323j. PMID 19088968.
- ^ Ohishi, Takeshi; Nishiura, Masayoshi; Hou, Zhaomin (21 July 2008). "Carboxylation of Organoboronic Esters Catalyzed by N‐Heterocyclic Carbene Copper(I) Complexes". Angewandte Chemie International Edition. 47 (31): 5792–5795. doi:10.1002/anie.200801857. PMID 18576463.
- ^ Gooßen, Lukas J.; Rodríguez, Nuria; Manjolinho, Filipe; Lange, Paul P. (22 November 2010). "Synthesis of Propiolic Acids via Copper-Catalyzed Insertion of Carbon Dioxide into the C-H Bond of Terminal Alkynes". Advanced Synthesis & Catalysis. 352 (17): 2913–2917. doi:10.1002/adsc.201000564.
- ^ Fujihara, Tetsuaki; Xu, Tinghua; Semba, Kazuhiko; Terao, Jun; Tsuji, Yasushi (10 January 2011). "Copper-Catalyzed Hydrocarboxylation of Alkynes Using Carbon Dioxide and Hydrosilanes". Angewandte Chemie International Edition. 50 (2): 523–527. doi:10.1002/anie.201006292. PMID 21157832.
- ^ Ueno, Atsushi; Takimoto, Masanori; O, Wylie W. N.; Nishiura, Masayoshi; Ikariya, Takao; Hou, Zhaomin (April 2015). "Copper-Catalyzed Formal C-H Carboxylation of Aromatic Compounds with Carbon Dioxide through Arylaluminum Intermediates". Chemistry: An Asian Journal. 10 (4): 1010–1016. doi:10.1002/asia.201403247. PMID 25491488.
- ^ Ueno, Atsushi; Takimoto, Masanori; Hou, Zhaomin (2017). "Synthesis of 2-aryloxy butenoates by copper-catalysed allylic C–H carboxylation of allyl aryl ethers with carbon dioxide". Org. Biomol. Chem. 15 (11): 2370–2375. doi:10.1039/C7OB00341B. PMID 28244535.
- ^ Takimoto, Masanori; Hou, Zhaomin (19 August 2013). "Cu-Catalyzed Formal Methylative and Hydrogenative Carboxylation of Alkynes with Carbon Dioxide: Efficient Synthesis of α,β-Unsaturated Carboxylic Acids". Chemistry - A European Journal. 19 (34): 11439–11445. doi:10.1002/chem.201301456. PMID 23852827.
- ^ Gholap, Sandeep Suryabhan; Takimoto, Masanori; Hou, Zhaomin (13 June 2016). "Regioselective Alkylative Carboxylation of Allenamides with Carbon Dioxide and Dialkylzinc Reagents Catalyzed by an N-Heterocyclic Carbene-Copper Complex". Chemistry - A European Journal. 22 (25): 8547–8552. doi:10.1002/chem.201601162. PMID 27167688.
- ^ Takimoto, Masanori; Gholap, Sandeep Suryabhan; Hou, Zhaomin (19 October 2015). "Cu-Catalyzed Alkylative Carboxylation of Ynamides with Dialkylzinc Reagents and Carbon Dioxide". Chemistry - A European Journal. 21 (43): 15218–15223. doi:10.1002/chem.201502774. PMID 26346513.
- ^ Sugimoto, Hiroshi; Kawata, Itaru; Taniguchi, Hiroshi; Fujiwara, Yuzo (May 1984). "Preliminary communication: Palladium-Catalyzed Carboxylation of Aromatic-Compounds with Carbon-Dioxide". Journal of Organometallic Chemistry. 266 (3): c44–c46. doi:10.1016/0022-328X(84)80150-3.
- ^ Shi, Min; Nicholas, Kenneth M. (May 1997). "Palladium-Catalyzed Carboxylation of Allyl Stannanes". Journal of the American Chemical Society. 119 (21): 5057–5058. doi:10.1021/ja9639832.
- ^ Johansson, Roger; Jarenmark, Martin; Wendt, Ola F. (September 2005). "Insertion of Carbon Dioxide into (PCP)Pd-II-Me bonds". Organometallics. 24 (19): 4500–4502. doi:10.1021/om0505561.
- ^ Johansson, Roger; Wendt, Ola F. (2007). "Insertion of CO2 into a palladium allyl bond and a Pd(II) catalysed carboxylation of allyl stannanes". Dalton Trans. (4): 488–492. doi:10.1039/B614037H. PMID 17213935.
- ^ Johnson, Magnus T.; Johansson, Roger; Kondrashov, Mikhail V.; Steyl, Gideon; Ahlquist, Mårten S. G.; Roodt, Andreas; Wendt, Ola F. (23 August 2010). "=Mechanisms of the CO2 Insertion into (PCP) Palladium Allyl and Methyl sigma-Bonds. A Kinetic and Computational Study". Organometallics. 29 (16): 3521–3529. doi:10.1021/om100325v.
- ^ Takaya, Jun; Iwasawa, Nobuharu (19 November 2008). "Hydrocarboxylation of Allenes with CO2 Catalyzed by Silyl Pincer-Type Palladium Complex". Journal of the American Chemical Society. 130 (46): 15254–15255. doi:10.1021/ja806677w. PMID 18942785.
- ^ Takaya, Jun; Sasano, Kota; Iwasawa, Nobuharu (April 2011). "Efficient One-to-One Coupling of Easily Available 1,3-Dienes with Carbon Dioxide". Organic Letters. 13 (7): 1698–1701. doi:10.1021/ol2002094. PMID 21370864.
- ^ Zhu, Chuan; Takaya, Jun; Iwasawa, Nobuharu (3 April 2015). "Use of formate salts as a hydride and a co2 source in PGeP-palladium complex-catalyzed hydrocarboxylation of allenes". Organic Letters. 17 (7): 1814–1817. doi:10.1021/acs.orglett.5b00692. PMID 25794110.
- ^ Sasano, Kota; Takaya, Jun; Iwasawa, Nobuharu (31 July 2013). "Palladium(II)-Catalyzed Direct Carboxylation of Alkenyl C–H Bonds with CO2". Journal of the American Chemical Society. 135 (30): 10954–10957. doi:10.1021/ja405503y. PMID 23865901.
- ^ Ukai, Kazutoshi; Aoki, Masao; Takaya, Jun; Iwasawa, Nobuharu (2006-07-01). "Rhodium(I)-Catalyzed Carboxylation of Aryl- and Alkenylboronic Esters with CO2". Journal of the American Chemical Society. 128 (27): 8706–8707. doi:10.1021/ja061232m. ISSN 0002-7863. PMID 16819845.
- ^ Mizuno, Hajime; Takaya, Jun; Iwasawa, Nobuharu (2011-02-09). "Rhodium(I)-Catalyzed Direct Carboxylation of Arenes with CO2 via Chelation-Assisted C−H Bond Activation". Journal of the American Chemical Society. 133 (5): 1251–1253. doi:10.1021/ja109097z. ISSN 0002-7863. PMID 21192682.
- ^ Suga, Takuya; Mizuno, Hajime; Takaya, Jun; Iwasawa, Nobuharu (2014-10-23). "Direct carboxylation of simple arenes with CO2 through a rhodium-catalyzed C–H bond activation". Chemical Communications. 50 (92): 14360–14363. doi:10.1039/C4CC06188H. ISSN 1364-548X. PMID 25296263.
- ^ Suga, Takuya; Saitou, Takanobu; Takaya, Jun; Iwasawa, Nobuharu (2017-01-30). "Mechanistic study of the rhodium-catalyzed carboxylation of simple aromatic compounds with carbon dioxide". Chemical Science. 8 (2): 1454–1462. doi:10.1039/C6SC03838G. ISSN 2041-6539. PMC 5460598. PMID 28616144.
- ^ Murata, Kei; Numasawa, Nobutsugu; Shimomaki, Katsuya; Takaya, Jun; Iwasawa, Nobuharu (2017-03-09). "Construction of a visible light-driven hydrocarboxylation cycle of alkenes by the combined use of Rh(I) and photoredox catalysts". Chemical Communications. 53 (21): 3098–3101. doi:10.1039/C7CC00678K. ISSN 1364-548X. PMID 28243662.
- ^ León, Thierry; Correa, Arkaitz; Martin, Ruben (2013-01-30). "Ni-Catalyzed Direct Carboxylation of Benzyl Halides with CO2". Journal of the American Chemical Society. 135 (4): 1221–1224. doi:10.1021/ja311045f. ISSN 0002-7863. PMID 23301781.
- ^ Correa, Arkaitz; León, Thierry; Martin, Ruben (2014-01-22). "Ni-Catalyzed Carboxylation of C(sp2)– and C(sp3)–O Bonds with CO2". Journal of the American Chemical Society. 136 (3): 1062–1069. doi:10.1021/ja410883p. hdl:2072/305833. ISSN 0002-7863. PMID 24377699.
- ^ Liu, Yu; Cornella, Josep; Martin, Ruben (2014-08-13). "Ni-Catalyzed Carboxylation of Unactivated Primary Alkyl Bromides and Sulfonates with CO2" (PDF). Journal of the American Chemical Society. 136 (32): 11212–11215. doi:10.1021/ja5064586. hdl:2072/305831. ISSN 0002-7863. PMID 25068174.
- ^ Börjesson, Marino; Moragas, Toni; Martin, Ruben (2016-06-22). "Ni-Catalyzed Carboxylation of Unactivated Alkyl Chlorides with CO2". Journal of the American Chemical Society. 138 (24): 7504–7507. doi:10.1021/jacs.6b04088. hdl:2072/305936. ISSN 0002-7863. PMID 27269443.
- ^ Moragas, Toni; Cornella, Josep; Martin, Ruben (2014-12-24). "Ligand-Controlled Regiodivergent Ni-Catalyzed Reductive Carboxylation of Allyl Esters with CO2". Journal of the American Chemical Society. 136 (51): 17702–17705. doi:10.1021/ja509077a. hdl:2072/305832. ISSN 0002-7863. PMID 25473825.