바나듐 테트라플루오리드
Vanadium tetrafluoride| | |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름 테트라플루오리드 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 켐스파이더 | |||
| ECHA InfoCard | 100.030.143 | ||
| EC 번호 |
| ||
펍켐 CID | |||
| 유니 | |||
| UN 번호 | UN2923 | ||
CompTox 대시보드 (EPA) | |||
| |||
| |||
| 특성. | |||
| F4V | |||
| 어금질량 | 126.9351 g·2011−1 | ||
| 외관 | 라임 그린 파우더, 저광학[1] | ||
| 냄새 | 무취 | ||
| 밀도 | 3.15 g/cm3(20°C)[1] 2.975 g/cm3(23°C)[2] | ||
| 녹는점 | 325°C(617°F, 598K) 760mmHg 분해[1] 시 | ||
| 비등점 | 서브라임[1] | ||
| 용해성이[1] 매우 좋은 | |||
| 용해성 | 아세톤, 아세트산에 용해성 SOCl22, 알코올, CHCl에3[2] 매우 약간 용해됨 | ||
| 구조 | |||
| 모노클린어, monoclinic | |||
| 14번 P21/c | |||
| 열화학 | |||
성 어금니 엔트로피 (S | 126[3] J/몰·K | ||
의 성 엔탈피 대형화 (ΔfH⦵298) | −1412 kJ/mol[3] | ||
기브스 자유 에너지 (ΔfG˚) | −1312 kJ/mol[3] | ||
| 위험 | |||
| 산업안전보건(OHS/OSH): | |||
눈 위험 | 심각한 피해를 입힌다. | ||
피부 유해성 | 화상의 원인 | ||
| GHS 라벨 표시:[4] | |||
  | |||
| 위험 | |||
| H300, H314, H330 | |||
| P260, P301+P310, P303+P361+P353, P304+P340, P305+P351+P338, P320, P330, P405, P501 | |||
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |||
| Infobox 참조 자료 | |||
바나듐(IV) 플루오르화(VF4)는 바나듐과 플루오린의 무기 화합물이다. 그것은 매우 흡습적인 파라자성 황갈색 고체다.[2] 해당 바나듐 테트라클로라이드와 달리 테트라플루오라이드는 고분자 구조를 채택하기 때문에 휘발성이 없다. 녹기 전에 분해된다.
준비 및 반응
VF는4 VCl을4 HF로 처리하여 준비할 수 있다.
- VCl4 + 4HF → VF4 + 4HCl
처음에는 이런 식으로 준비되었다.[5]
325 °C에서 분해되어 삼불화합물과 오불화합물에 불균형을 겪는다.[2]
- 2 VF4 → VF3 + VF5
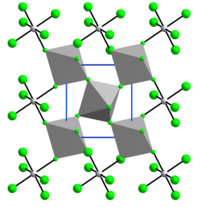
구조
VF의4 구조는 SnF의4 구조와 관련이 있다. 각각의 바나듐 중심은 6개의 불소 리간드로 둘러싸인 팔각형이다. 불소 중심 중 4개는 인접한 바나듐 센터에 연결된다.[6]
참조
- ^ a b c d e Lide, David R., ed. (2009). CRC Handbook of Chemistry and Physics (90th ed.). Boca Raton, Florida: CRC Press. ISBN 978-1-4200-9084-0.
- ^ a b c d Kwasnik, W. (1963). Brauer, Georg (ed.). Handbook of Preparative Inorganic Chemistry (UK ed.). London: Academic Press. pp. 252–253.
- ^ a b c Anatolievich, Kiper Ruslan. "vanadium(IV) fluoride". http://chemister.ru. Retrieved 2014-06-25.
{{cite web}}: 외부 링크 위치website= - ^ "Vanadium(IV) fluoride, 95%". http://www.alfa.com. Alfa Aesar. Retrieved 2014-06-25.
{{cite web}}: 외부 링크 위치website= - ^ 오토 러프, 허버트 릭페트 "Vanadinfuoride" Chemische Berichte 1911, vol. 44, 페이지 2539–2549. doi:10.1002/cber.110440379
- ^ 베커 S, 뮬러 B. G. 바나듐 테트라플루오라이드, 안젤루. 화학. intnl. 에드. 엥글 1990년, 제29권, 406쪽
- WebEles
- Cotton, F. Albert; Wilkinson, Geoffrey; Murillo, Carlos A.; Bochmann, Manfred (1999), Advanced Inorganic Chemistry (6th ed.), New York: Wiley-Interscience, ISBN 0-471-19957-5