치매
Dementia| 치매 | |
|---|---|
| 기타이름 | 노쇠,[1] 노인성 치매 |
 | |
| 1800년대 치매 진단을 받은 남성의 리소그래피 | |
| 전문 | 신경과 정신과 |
| 증상 | 사고력 및 기억력 저하, 정서적 문제, 언어문제, 동기부여[2] 저하 |
| 합병증 | 영양 부족, 폐렴, 자가 관리 업무 수행 불능, 개인 안전 문제.[3] |
| 통상적인 발병 | 점진적[2] |
| 지속 | 장기[2] |
| 원인들 | 알츠하이머병, 혈관병, 루이체병 그리고 전측두엽변성증.[2] |
| 진단방법 | 인지검사(미니멘탈상태검사)[4] |
| 감별진단 | 섬망, 갑상선[5][6] 기능 저하증 |
| 예방 | 조기교육, 고혈압예방, 비만예방, 금연, 사회참여[7] |
| 치료 | 지원적 돌봄[2] |
| 약 | 아세틸콜린에스테라아제 억제제(소이득)[8] |
| 빈도수. | 5500만 (2021년)[2] |
| 데스 | 240만 (2016년)[9] |
치매는 사람의 일상적인 활동 수행 능력에 영향을 미치는 인지 능력의 저하를 통칭합니다.이것은 일반적으로 기억, 사고 그리고 행동의 문제를 포함합니다.기억력 장애와 사고 패턴의 붕괴를 제외하고, 가장 흔한 증상은 감정적인 문제, 언어의 어려움, 그리고 동기 저하를 포함합니다.[2]증상은 여러 단계에 걸쳐 연속체에서 발생하는 것으로 설명될 수 있습니다.[10][a]치매는 궁극적으로 개인, 양육자, 그리고 일반적인 사회적 관계에 중요한 영향을 미칩니다.[2]치매 진단은 사람의 평소 정신 기능의 변화와 정상적인 노화로 인한 것보다 더 큰 인지 저하를 관찰하는 것이 필요합니다.[12]
뇌졸중과 같은 뇌의 여러 질병과 부상은 치매를 일으킬 수 있습니다.하지만 가장 흔한 원인은 신경 퇴행성 질환인 알츠하이머병입니다.[2]정신 질환 진단 및 통계 매뉴얼 제5판(DSM-5)은 치매를 다양한 심각도와 많은 원인이 되는 하위 유형을 가진 경증 또는 주요 신경 인지 질환으로 다시 설명했습니다.국제질병분류(ICD-11)는 또한 치매를 많은 형태나 아류를 가진 신경인지장애(NCD)로 분류하고 있습니다.[13]치매는 후천적 뇌증후군으로, 인지기능 저하가 특징이며, 신경발달장애와 대비됩니다.[14]치매는 또한 파킨슨병 치매에 대해 파킨슨병과 같은 알려진 장애에 기초한 치매의 원인적인 아형을 가진 장애의 스펙트럼으로 설명됩니다.헌팅턴병, 헌팅턴병, 혈관병, 혈관병, HIV 감염,[15] HIV 치매 유발, 전측두엽성 치매, 또는 루이 몸을 가진 치매, 프리온 질환.신경퇴행성 탈멘티아의 하위 유형은 또한 시뉴클레오패스 및 타우오패스와 같은 잘못 접힌 단백질의 근본적인 병리학에 기초할 수 있습니다.[15]함께 존재하는 치매의 한 가지 이상의 유형은 혼합 치매로 알려져 있습니다.[14]
많은 신경인지장애는 뇌종양, 경막하혈종, 갑상선기능저하증, 저혈당증과 같은 내분비계 장애, 티아민, 니아신을 포함한 영양결핍, 감염, 면역장애, 간 또는 신장부전, 쿠프병과 같은 대사장애에 의해 야기될 수 있습니다.e, 그리고 일부 백혈구 감소증, 간질, 다발성 경화증과 같은 신경 질환들.신경 인지 결손 중 일부는 때때로 질병의 치료에 따라 개선을 보일 수도 있습니다.[16]
진단은 대개 질병의 병력과 영상을 통한 인지 검사를 기반으로 합니다.혈액 검사는 갑상선 기능 저하증과 같은 가역적일 수 있는 다른 가능한 원인을 배제하고 치매 아형을 결정하기 위해 시행될 수 있습니다.일반적으로 사용되는 하나의 인지 검사는 미니 정신 상태 검사입니다.치매 발병의 가장 큰 위험 요소는 노화이지만, 치매는 노화의 정상적인 부분이 아닙니다.90세 이상의 많은 사람들은 치매의 징후를 보이지 않습니다.[17]흡연이나 비만과 같은 치매의 여러 위험 요소들은 생활 방식의 변화에 의해 예방할 수 있습니다.일반적인 노년층을 대상으로 그 장애를 선별하는 것은 결과에 영향을 미치지 않는 것으로 보입니다.[18]
치매는 현재 전 세계적으로 7번째로 높은 사망 원인이며 매년 1,000만 건(~3초당 1건)의 신규 환자가 보고되고 있습니다.[2]치매에 대한 알려진 치료법은 없습니다.도네페질과 같은 아세틸콜린에스테라아제 억제제는 종종 사용되며 경도 또는 중등도의 장애에서 도움이 될 수 있습니다.그러나 전체적인 이점은 미미할 수 있습니다.치매환자와 보호자의 삶의 질을 높일 수 있는 방안이 많습니다.인지적 및 행동적 개입은 우울증 관련 증상을 치료하는 데 적절할 수 있습니다.[19]
징후 및 증상


치매의 징후와 증상을 신경정신적 증상, 치매의 행동 및 심리적 증상이라고도 합니다.[20][21]행동 증상에는 동요, 불안정, 부적절한 행동, 성적 억제, 공격성이 포함될 수 있는데, 이는 언어적이거나 신체적일 수 있습니다.[22]이러한 증상은 인지 억제의 장애로 인해 발생할 수 있습니다.[23]심리적 증상에는 우울증, 환각(대부분 시각적),[24] 망상, 무관심, 불안 등이 포함될 수 있습니다.[22][25]가장 일반적으로 영향을 받는 분야는 기억력, 지각과 지향에 영향을 미치는 시공간 기능, 언어, 주의 집중 및 문제 해결입니다.여러 단계에 걸쳐 연속체에서 증상이 발생하는 속도이며, 치매 아형에 따라 증상이 다양합니다.[26][10]치매의 대부분의 유형은 서서히 진행되며, 장애의 징후가 분명해지기 전에 뇌가 잘 형성됩니다.종종 고혈압이나 당뇨와 같은 다른 질환들이 존재하며, 때로는 이러한 동반 질환들 중 4가지 정도가 있을 수 있습니다.[27]
치매에 걸린 사람들은 또한 요실금 문제를 가질 가능성이 더 높습니다: 그들은 비슷한 나이의 사람들에 비해 요실금을 가질 가능성이 3배 더 높고 대변 요실금을 가질 가능성이 4배 더 높습니다.[28][29]
치매 증상은 사람마다 천차만별일 수 있습니다.기억력, 주의력, 의사소통, 추론, 판단력, 문제해결, 시각지각 등에 영향을 미칩니다.치매를 가리키는 징후로는 익숙한 동네에서 길을 잃거나, 특이한 단어를 사용해 익숙한 물건을 지칭하거나, 가까운 가족이나 친구의 이름을 잊어버리거나, 옛 기억을 잊어버리거나, 혼자서 일을 끝내지 못하는 등이 있습니다.[30]
스테이지들
치매의 경과는 종종 점진적인 인지 및 기능 장애의 패턴을 나타내는 4단계로 설명됩니다.그러나 숫자 척도를 사용하면 더 자세한 설명이 가능합니다.이러한 척도에는 일차 퇴행성 치매 평가를 위한 글로벌 악화 척도(GDS 또는 레이스버그 척도), 기능 평가 단계 테스트(FAST) 및 임상 치매 등급(CDR)이 포함됩니다.[31]질병 진행의 각 단계를 보다 정확하게 식별하는 GDS를 사용하여 보다 상세한 과정을 7단계로 설명합니다. 그 중 2단계는 5도와 6도로 더 세분화됩니다.7단계(f)가 마지막 단계입니다.[32][33]
치매전
치매 전 상태는 임상 전 단계와 전구 단계를 포함합니다.전구 단계에는 (1) 경도 인지 장애(MCI), (2) 섬망 발병 및 정신 의학 발병 프레젠테이션이 포함됩니다.[34]
전임상
이 단계는 치매의 첫 번째 임상 징후보다 최대 10년 앞서 감각 기능 장애를 주장합니다.[10]가장 눈에 띄는 것은 후각의 상실입니다.[10][35]후각의 상실은 우울증과 식욕 감퇴가 영양실조로 이어지는 것과 관련이 있습니다.[36]후각 상피가 환경에 노출되기 때문에 이러한 기능 장애가 발생할 수도 있다고 합니다.혈액-뇌 장벽 보호 기능이 없다는 것은 독성 요소가 들어가 화학 센서 네트워크에 손상을 줄 수 있다는 것을 의미합니다.[10]
프로프로말
전구 병변으로 간주되는 치매 전 상태는 경도 인지 장애(MCI)와 경도 행동 장애(MBI)입니다.[37][38][39]
키뉴레닌은 마이크로바이옴 신호전달, 면역세포 반응, 그리고 신경세포 흥분을 조절하는 트립토판의 대사산물입니다.키뉴레닌 경로의 장애는 가벼운 치매에서 신경정신적 증상과 인지 예후와 관련이 있을 수 있습니다.[40][41]
이 단계에서는 징후와 증상이 미묘할 수 있습니다.종종, 뒤를 돌아보면 초기 징후가 분명해집니다.[42]MCI 진단을 받은 사람의 70%는 나중에 치매로 진행됩니다.[12]MCI에서는 사람의 뇌의 변화가 오래 전부터 일어나고 있지만 이제 막 증상이 나타나기 시작했습니다.그러나 이러한 문제는 일상적인 기능에 영향을 미칠 만큼 심각하지는 않습니다.그들이 그렇게 된다면, 그 진단은 치매가 됩니다.그들은 기억력에 문제가 있을 수도 있고 단어를 찾는데 어려움이 있을 수도 있지만, 일상적인 문제를 해결하고 그들의 삶의 일을 능숙하게 처리합니다.[43]이 단계에서는 본인의 의사를 보호하기 위한 사전 관리 계획이 수립되도록 하는 것이 이상적입니다.치매에 특화된 사전 지침이 존재하며,[44] 이는 질병의 진행에 따라 나타나는 영양 공급과 관련된 결정을 해결하는 데 특히 도움이 될 수 있습니다.
가벼운 인지 장애는 DSM-5와 ICD-11에서 주요 신경 인지 장애(치매) 아형의 가벼운 형태인 가벼운 신경 인지 장애로 다시 등록되었습니다.[45]
빠른
치매 초기에는 다른 사람에게 증상이 두드러집니다.또한, 이 증상은 일상 활동에 방해가 되기 시작하며, 최소 정신 상태 검사(MMSE)에 점수를 등록하게 됩니다.MMSE 점수는 정상 인지 등급의 경우 24에서 30으로 설정되며 낮은 점수는 증상의 심각성을 반영합니다.증상은 치매의 종류에 따라 다릅니다.집 주변이나 직장에서 더 복잡한 집안일과 업무는 더 어려워집니다.그 사람은 보통 자신을 돌볼 수 있지만 약을 먹거나 빨래를 하는 것과 같은 것들을 잊어버릴 수도 있고 재촉하거나 상기시키는 것이 필요할 수도 있습니다.[46]
초기 치매의 증상은 보통 기억력의 어려움을 포함하지만 단어 찾기의 문제, 계획과 조직의 실행 기능의 문제를 포함할 수 있습니다.[47]재정 관리가 어려울 수 있습니다.다른 징후들은 새로운 장소에서 길을 잃고, 반복되는 것들, 성격 변화들일 수 있습니다.[48]
루이체 치매, 전측두엽 치매 등 일부 치매 유형에서는 성격 변화와 조직 및 계획의 어려움이 첫 번째 징후일 수 있습니다.[49]
가운데
치매가 진행되면 초기 증상이 악화되는 것이 일반적입니다.감소율은 사람마다 다릅니다.MMSE 점수는 6-17점 사이에서 중간 정도의 치매를 나타냅니다.예를 들어, 적당한 알츠하이머 치매를 가진 사람들은 거의 모든 새로운 정보를 잃습니다.치매에 걸린 사람들은 문제 해결에 심각한 장애가 있을 수 있으며, 그들의 사회적 판단력 또한 대개 손상됩니다.그들은 보통 자신의 집 밖에서 활동할 수 없으며, 일반적으로 혼자 두어서는 안됩니다.그들은 집 주변에서 간단한 집안일은 할 수 있지만 다른 일은 할 수 없을 것이고, 단순한 주의 사항을 넘어서는 개인적인 보살핌과 위생을 위한 도움이 필요하기 시작합니다.[12]그 상태를 가지고 있는 것에 대한 통찰력의 부족이 명백해질 것입니다.[50][51]
늦게.
말기 치매 환자들은 일반적으로 점점 더 안쪽으로 몸을 돌리며 개인적인 치료의 대부분 또는 전부에 대한 도움이 필요합니다.치매 말기 환자들은 보통 24시간 감시를 통해 신변 안전을 확보하고 기본적인 욕구를 충족시켜야 합니다.감독을 받지 않은 상태로 놔두면 어슬렁거리거나 넘어지거나, 뜨거운 난로와 같은 일반적인 위험을 인식하지 못하거나, 화장실을 사용해야 한다는 것을 깨닫지 못하고 실금을 할 수도 있습니다.[43]그들은 침대에서 일어나기를 원치 않거나, 침대에서 일어나는데 도움이 필요할 수도 있습니다.일반적으로, 그 사람은 더 이상 익숙한 얼굴을 인식하지 못합니다.그들은 수면 습관에 상당한 변화가 있거나 아예 잠을 자지 못할 수도 있습니다.[12]
먹는 것에 변화가 자주 일어납니다.식사와 삼킴에 대한 인지적 인식이 필요하고, 점진적인 인지능력 저하로 인해 식사와 삼킴에 어려움이 발생합니다.이로 인해 음식이 거부되거나 목이 메게 될 수 있으며, 종종 음식 공급에 대한 도움이 필요합니다.[52]음식을 먹기 쉽게 하기 위해, 음식은 두꺼운 퓨레로 액체화 될 수 있습니다.그들은 특히 알츠하이머병을 앓고 있는 사람들 사이에서 걷기가 힘들 수도 있습니다.[53][54][55]죽음 직전에 예상치 못한 정신적 명료함의 회복이 나타나는 역설적인 자각이 있는 경우도 있습니다.[56]
원인들
치매의 많은 원인들은 신경퇴행성이며, 단백질 미스폴딩은 이것들의 주요 특징입니다.[57]다른 일반적인 원인으로는 혈관성 치매, 루이체 치매, 전측두엽성 치매, 혼합 치매 등이 있습니다.[2][b][61]덜 흔한 원인으로는 상압성 수두증, 파킨슨병 치매, 매독, HIV, 크로이츠펠트 야콥병 등이 있습니다.[62]
알츠하이머병

알츠하이머병은 전세계 치매 환자의 60-70%를 차지합니다.알츠하이머병의 가장 흔한 증상은 단기 기억력 감퇴와 단어 찾기의 어려움입니다.공간적 기능의 문제(자주 길을 잃음), 추론, 판단 및 통찰력이 실패합니다.통찰력은 사람이 기억력에 문제가 있다는 것을 깨닫는지 여부를 말합니다.
알츠하이머에 가장 영향을 받는 뇌의 부분은 해마입니다.위축(수축)을 보이는 다른 부분에는 측두엽과 두정엽이 있습니다.이러한 뇌 수축의 패턴은 알츠하이머를 시사하지만, 그것은 가변적이고 뇌 스캔은 진단에 불충분합니다.
알츠하이머병을 일으키는 동안에 일어나고 실제로 일어나는 사건들에 대해서는 거의 알려져 있지 않습니다.이는 이 병을 앓고 있는 환자들의 뇌 조직이 그 사람이 죽은 후에야 연구될 수 있기 때문입니다.하지만, 이 질병의 첫 번째 측면 중 하나는 아밀로이드를 생산하는 유전자의 기능 장애인 것으로 알려져 있습니다.AD의 두 가지 잘 확립된 병리학적 특징은 베타-아밀로이드(Aβ) 펩타이드 및 과인산화 타우 단백질에 의해 형성된 세포 내 신경섬유상 엉킴(NFT)으로 구성된 세포 외 노인성 플라크(SP)입니다.[63]아밀로이드는 뇌의 노인반 주위에 염증을 일으키고, 이 염증이 지나치게 쌓이면 조절이 불가능한 뇌의 변화가 생겨 알츠하이머 증상이 나타납니다.[64]
특히 노인에서 전신마취와 알츠하이머 사이의 가능한 관계(알츠하이머병의 주요 원인 또는 악화)에 대해 여러 기사가 발표되었습니다.[65]
혈관
혈관성 치매는 치매 환자의 최소 20%를 차지해 두 번째로 흔한 유형입니다.[66]그것은 일반적으로 일련의 미니 스트로크를 수반하는 뇌에 혈액 공급에 영향을 미치는 질병이나 부상에 의해 발생합니다.이 치매의 증상은 뇌의 어디에서 뇌졸중이 발생했는지, 영향을 받는 혈관이 큰지 작은지에 따라 달라집니다.[12]반복적인 부상은 시간이 지남에 따라 진행성 치매를 유발할 수 있는 반면 해마, 즉 시상과 같은 인지에 중요한 부위에 위치한 단일 부상은 갑작스러운 인지 저하로 이어질 수 있습니다.[66]혈관성 치매의 요소는 다른 모든 형태의 치매에 존재할 수 있습니다.[67]
뇌 스캔은 다양한 위치에서 크기가 다른 여러 뇌졸중의 증거를 보여줄 수 있습니다.혈관성 치매를 앓고 있는 사람들은 담배 사용, 고혈압, 심방세동, 고콜레스테롤, 당뇨병과 같은 혈관 질환의 위험인자 또는 이전의 심장마비나 협심증과 같은 다른 징후를 가지고 있는 경향이 있습니다.[68]
루이체
Lewy body (DLB)를 동반한 치매의 전구 증상으로는 경도 인지 장애, 섬망 발생 등이 있습니다.[69]DLB의 증상은 다른 치매 아형에 비해 더 빈번하고, 더 심하며, 더 일찍 나타납니다.[70]Lewy 몸을 가진 치매는 인지, 경계 또는 주의를 요동치는 주요 증상; 렘 수면 행동 장애(RBD); 약물이나 뇌졸중으로 인한 것이 아닌 파킨슨병의 주요 특징 중 하나 이상; 그리고 반복적인 시각적 환각을 갖습니다.[71]DLB의 시각적 환각은 일반적으로 사람이나 동물의 생생한 환각이며, 누군가가 잠들려고 할 때나 깨어날 때 종종 발생합니다.다른 눈에 띄는 증상으로는 계획(실행 기능)의 문제와 시공간 기능의 어려움,[12] 자율적인 신체 기능의 장애 등이 있습니다.[72]비정상적인 수면 행동은 인지 저하가 관찰되기 전에 시작될 수 있으며 DLB의 핵심 특징입니다.[71] RBD는 수면 연구 기록 또는 수면 연구를 수행할 수 없는 경우 병력 및 검증된 설문지에 의해 진단됩니다.[71]
파킨슨병
파킨슨병(Parkinson's disease)은 루이(Lewy) 신체 질환으로, 치매가 없는 파킨슨병 시기 이후 종종 파킨슨병 치매로 진행됩니다.[73]
전면측두
전두엽성 치매(FTD)는 급격한 성격 변화와 언어적 어려움을 특징으로 합니다.모든 FTD에서, 사람은 비교적 일찍 사회적으로 물러나고 통찰력이 일찍 부족합니다.메모리 문제는 주요 기능이 아닙니다.[12][74]FTD에는 크게 6가지 유형이 있습니다.첫번째는 성격과 행동에 큰 증상이 있습니다.이를 행동 변형 FTD(bv-FTD)라고 하며 가장 일반적입니다.bv-FTD의 특징은 충동적인 행동이며, 이는 치매 전 상태에서 발견될 수 있습니다.[39]bv-FTD에서 개인 위생에 변화를 보이고, 사고가 경직되며, 문제를 거의 인식하지 못합니다. 사회적으로 위축되고, 식욕이 급격하게 증가하는 경우가 많습니다.그들은 사회적으로 부적절해질 수 있습니다.예를 들어 부적절한 성적 발언을 하거나 음란물을 공개적으로 사용하기 시작할 수도 있습니다.가장 흔한 징후 중 하나는 무관심하거나, 어떤 것에도 신경 쓰지 않는 것입니다.그러나 무관심은 많은 치매에서 흔한 증상입니다.[12]
두 가지 유형의 FTD는 실어증(언어 문제)을 주요 증상으로 합니다.한 가지 유형은 의미 변이 일차 진행성 실어증(SV-PPA)이라고 불립니다.이것의 가장 큰 특징은 단어의 의미가 사라진다는 것입니다.이름을 짓는데 어려움에서 시작할 수도 있습니다.그 사람은 결국 사물의 의미를 잃을 수도 있습니다.예를 들어, FTD를 가진 사람의 새, 개, 비행기 그림은 모두 거의 똑같이 보일 수 있습니다.[12]이것을 위한 고전적인 테스트에서, 환자는 피라미드의 그림을 보여주고 그 아래에는 야자수와 소나무의 그림을 보여줍니다.그 사람은 어떤 것이 피라미드와 가장 잘 어울리는지를 말하도록 요구 받습니다.SV-PPA에서는 해당 질문에 답변할 수 없습니다.다른 유형은 비유동 문법 변이 일차 진행성 실어증(NFA-PPA)이라고 합니다.이것은 주로 연설을 만드는 문제입니다.그들은 적절한 단어를 찾는데 어려움을 겪지만, 대부분 그들이 말하는 데 필요한 근육을 조정하는데 어려움을 겪습니다.결국, NFA-PPA를 사용하는 사람은 한 음절의 단어만 사용하거나 완전히 벙어리가 될 수 있습니다.
(FTD-ALS)로 알려진 근위축성 측삭 경화증 (ALS)과 관련된 전방측삭 치매는 근위축성 측삭 경화증 (운동 뉴런의 손실)과 동시에 발생하는 FTD (행동, 언어 및 움직임 문제)의 증상을 포함합니다.진행성 초핵성마비([75][76]Parkinson-plus syndrome)와 피질염기변성증(corticobasal degeneration)[12]은 두 가지 FTD 관련 질환입니다.이 장애들은 타우와 연관되어 있습니다.
헌팅턴병
헌팅턴병은 주석 단백질을 암호화하는 단일 유전자 HTT의 돌연변이에 의해 발생하는 신경퇴행성 질환입니다.증상은 인지 장애를 포함하고 이것은 보통 치매로 더 떨어집니다.[77]
헌팅턴병의 첫 번째 주요 증상은 다음과 같습니다.
- 집중력이 떨어짐
- 기억이 흐르다
- 우울증 - 이것은 낮은 기분, 사물에 대한 흥미 부족 또는 단지 비정상적인 절망감을 포함할 수 있습니다.
- 평범하지 않은 비틀거리고 어설픈 것.
- 사소한 것에[78] 대한 짜증이나 공격적인 행동과 같은 기분 변화
HIV를
HIV 관련 치매는 HIV 감염의 후기 단계로 발생하며, 대부분 젊은 사람들에게 영향을 미칩니다.[79]HIV와 관련된 치매의 본질적인 특징은 운동 기능 장애, 언어 문제, 행동 변화를 동반한 인지 장애를 무력화하는 것입니다.[79]인지 장애는 정신적으로 느림, 기억력 문제, 집중력 저하가 특징입니다.운동 증상으로는 미세한 운동 조절 기능의 상실로 인해 어설프게 되고 균형이 떨어지고 떨림이 나타납니다.행동 변화에는 무관심, 무기력, 감정 반응의 감소와 자발성이 포함될 수 있습니다.조직병리학적으로, 중추신경계(CNS)로의 단세포와 대식세포의 침투, 교모세포증, 미엘린 외피의 창백, 수지상 과정의 이상 및 신경세포 소실에 의해 확인됩니다.[80]
크로이츠펠트 야콥병
크로이츠펠트 야콥병은 치매를 몇 주에서 몇 달에 걸쳐 악화시키는 급속한 진행성 프리온 질환입니다.프리온은 비정상적인 단백질로부터 생성된 질병을 유발하는 병원체입니다.[81]
알코올 중독
알코올성 뇌 손상이라고도 불리는 알코올성 치매는 특히 약물 남용 장애로서 알코올의 과다 사용으로 인해 발생합니다.티아민 결핍과 나이의 취약성을 포함한 다양한 요인들이 이 발달에 관련될 수 있습니다.[82][83]알코올 사용 장애가 있는 사람들의 70% 이상이 뇌 손상 정도를 보입니다.영향을 받는 뇌 부위는 노화와 알츠하이머병의 영향을 받는 부위와 비슷합니다.부피 손실을 보이는 부위는 전두엽, 측두엽, 두정엽과 소뇌, 시상, 해마 등입니다.[83]이러한 손실은 65세 이상의 사람들에게서 더 큰 인지 장애가 나타나면서 더욱 두드러질 수 있습니다.[83]
혼합치매
치매 환자의 약 10%에서 혼합 치매로 알려진 치매의 한 가지 이상의 유형이 함께 존재할 수 있습니다.[2]혼합 치매의 가장 흔한 유형은 알츠하이머병과 혈관성 치매입니다.[84]이 혼합 치매의 주요 발병 원인은 노화, 고혈압, 그리고 뇌의 혈관 손상의 혼합입니다.[14]
혼합 치매의 진단은 종종 한 가지 유형만 우세하기 때문에 어려울 수 있습니다.이것은 많은 사람들이 잠재적으로 도움이 되는 치료법을 놓치면서, 혼합 치매를 가진 사람들의 치료를 흔하지 않게 만듭니다.혼합 치매는 증상이 더 일찍 시작되고 뇌의 더 많은 부분이 영향을 받기 때문에 더 빨리 악화되는 것을 의미할 수 있습니다.[14]
다른.
뇌와 인지에 영향을 미칠 수 있는 만성 염증성 질환에는 베체트병, 다발성 경화증, 녹농균증, 쇼그렌 증후군, 루푸스, 셀리악병, 비셀리악 글루텐 감수성 등이 있습니다.[85][86]이런 종류의 치매는 빠르게 진행될 수 있지만, 보통 초기 치료에 좋은 반응을 보입니다.이것은 면역 조절제 또는 스테로이드 투여, 또는 특정한 경우에는 원인 물질의 제거로 구성됩니다.[86]2019년 리뷰는 전반적으로 셀리악병과 치매 사이의 연관성은 발견하지 못했지만 혈관성 치매와의 연관성은 발견했습니다.[87]2018년 리뷰는 셀리악병 또는 셀리악이 아닌 글루텐 민감성과 인지 장애 사이의 연관성을 발견했으며 셀리악병이 알츠하이머병, 혈관성 치매, 전측두엽성 치매와 관련이 있을 수 있다고 밝혔습니다.[88]글루텐이 없는 엄격한 식단은 글루텐 관련 질환과 관련된 치매를 예방할 수 있습니다.[87][88]
쉽게 가역적인 치매의 예로는 갑상선기능저하증, 비타민B12 결핍증, 라임병, 신경매독 등이 있습니다.라임병과 신경매독의 경우 위험인자가 있으면 검사를 해야 합니다.치매가 의심되는 경우에는 물론 신경매독, 라임병 등의 검사도 위험인자를 판단하기 어려운 경우가 많기 때문입니다.[12]: 31–32
다른 많은 의학적, 신경학적 질환들은 치매를 병의 말기에만 포함합니다.예를 들어, 파킨슨병 환자의 비율이 치매에 걸렸지만, 이 비율에 대해서는 매우 다양한 수치가 인용되고 있습니다.[89]파킨슨병에서 치매가 발생했을 때, 근본적인 원인은 루이 몸을 가진 치매일 수도 있고 알츠하이머병일 수도 있고, 또는 둘 다일 수도 있습니다.[90]인지 장애는 진행성 초핵성마비와 피질기저변성의 파킨슨 플러스 증후군에서도 발생합니다. (그리고 같은 근본적인 병리 현상이 전측두엽성 퇴행의 임상 증후군을 일으킬 수 있습니다.)비록 급성 포피리아가 혼란과 정신적인 장애를 일으킬지 모르지만, 치매는 이러한 희귀한 질병의 드문 특징입니다.변연계성 연령관련성 TDP-43뇌증(LATE)은 80대나 90대에 주로 영향을 미치며 TDP-43 단백질이 뇌의 변연계에 침착하는 치매의 한 종류입니다.[91]
치매를 유발할 수 있는 유전성 질환에는 리소좀 저장 장애, 백혈구 감소증, 척추 소뇌 마비와 같은 일부 대사 장애가 포함됩니다.
진단.
치매 유형별로 증상이 비슷하고 증상만으로는 진단이 어렵습니다.진단은 뇌 스캔 기술에 의해 도움을 받을 수 있습니다.많은 경우 뇌 조직 검사를 통해 최종 진단을 받아야 하지만, 부검을 수행할 수는 있지만 이를 권장하는 경우는 거의 없습니다.연령이 증가하는 사람들에게서 인지검사를 이용한 인지장애의 일반적인 선별이나 치매의 조기진단은 결과를 향상시키지 못하는 것으로 나타났습니다.[18][92]그러나 선별검사는 65명 이상의 기억장애인들에게 유용합니다.[12]
일반적으로 진단을 뒷받침하기 위해서는 최소 6개월 이상 증상이 있어야 합니다.[93]더 짧은 기간의 인지기능 장애는 섬망이라고 불립니다.섬망은 유사한 증상으로 인해 치매와 혼동되기 쉽습니다.섬망은 갑자기 시작되고 요동치는 과정, 짧은 기간(종종 몇 시간에서 몇 주까지 지속됨)을 특징으로 하며, 주로 체성(또는 의학적) 교란과 관련이 있습니다.이에 비해 치매는 일반적으로 길고 느린 발병(뇌졸중이나 외상의 경우 제외), 느린 정신 기능 저하, 더 긴 궤도(수개월에서 수년까지)를 가지고 있습니다.[94]
우울증과 정신병을 포함한 몇몇 정신 질환들은 섬망과 치매 둘 다와 구별되어야 하는 증상들을 일으킬지도 모릅니다.[95]이것들은 가성 치매로 다르게 진단되며, 모든 치매 평가는 신경정신의학적 인벤토리 또는 노인 우울 척도와 같은 우울증 선별을 포함할 필요가 있습니다.[96][12]의사들은 기억 장애가 있는 사람들이 치매가 아닌 우울증을 가지고 있다고 생각하곤 했습니다. (그들은 치매가 있는 사람들이 일반적으로 그들의 기억 문제를 알지 못한다고 생각했기 때문입니다.)하지만, 연구원들은 기억 장애가 있는 많은 노인들이 사실 치매의 초기 단계인 가벼운 인지 장애를 가지고 있다는 것을 깨달았습니다.그러나 기억력 장애가 있는 노인의 경우 우울증은 항상 가능성의 목록에서 높은 상태를 유지해야 합니다.사고, 청각, 시각의 변화는 정상적인 노화와 관련이 있으며 치매 진단 시 유사성으로 인해 문제를 일으킬 수 있습니다.[97]치매 발병을 예측하고 치매 진단 임상 의사 결정을 내리는 어려운 특성을 감안할 때 머신러닝과 인공지능이 뒷받침하는 임상 의사 결정 보조는 임상 실습을 강화할 수 있는 가능성이 있습니다.[98]
인지검사
| 시험 | 감수성 | 특이성 | 언급 |
| MMSE | 71–92% | 56–96% | [99] |
| 3MS | 83–93% | 85–90% | [100] |
| AMTS | 73–100% | 71–100% | [100] |
다양한 간단한 인지 테스트(5-15분)는 치매를 선별하는 데 합리적인 신뢰성을 가지고 있지만 연령, 교육 및 민족성과 같은 요인에 의해 영향을 받을 수 있습니다.[101]치매 진단에는 나이와 학력이 큰 영향을 미칩니다.예를 들어, 교육 수준이 낮은 사람들은 교육을 받은 사람들보다 치매 진단을 받을 가능성이 더 높습니다.[102]많은 테스트가 연구되었지만,[103][104][105] 현재는 최소 정신 상태 검사(MMSE)가 가장 잘 연구되고 가장 일반적으로 사용되고 있습니다.MMSE는 사람의 성격, 일상생활 활동 수행 능력, 행동에 대한 평가와 함께 결과가 해석될 경우 치매 진단에 도움을 주는 유용한 도구입니다.[4]다른 인지 테스트에는 축약된 정신 테스트 점수(AMTS), 수정된 미니 정신 상태 검사(3MS),[106] 인지 능력 선별 도구(CASI),[107] 트레일 만들기 테스트,[108] 시계 그리기 테스트 등이 있습니다.[31]MoCA(Montreal Cognitive Assessment)는 신뢰할 수 있는 선별 테스트이며 35개의 다른 언어로 온라인에서 무료로 제공됩니다.[12]MoCA는 MMSE보다 경도 인지 장애를 다소 더 잘 감지하는 것으로 나타났습니다.[109][38] 치매와 함께 흔히 발생하는 청력 손실이 있는 사람들은 MoCA 테스트에서 점수가 더 나빠지고, 이는 치매의 잘못된 진단으로 이어질 수 있습니다.연구원들은 정확하고 신뢰할 수 있으며 사람들이 질문을 듣고 응답할 필요가 없는 MoCA 테스트의 번안 버전을 개발했습니다.[110][111]인지 저하와 관련된 기능의 변화를 평가하기 위해 사용되는 선별 설문지인 AD-8은 잠재적으로 유용하지만 진단적이지 않고 가변적이며 편향의 위험이 있습니다.[112]통합 인지 평가(CognICA)는 치매 초기 단계에 매우 민감한 5분간의 테스트로, 아이패드에 전달할 수 있는 애플리케이션을 사용합니다.[113][114]이전에 영국에서 사용된 2021년 CognICA는 의료기기로서의 상업적 사용에 대해 FDA 승인을 받았습니다.[114]
치매 검진의 또 다른 방법은 정보원(친척 또는 다른 후원자)에게 그 사람의 일상적인 인지 기능에 대한 질문서를 작성하도록 요청하는 것입니다.제보자 질문지는 간단한 인지 검사에 보완적인 정보를 제공합니다.아마도 이런 종류의 가장 잘 알려진 설문지는 노인 인지 저하에 관한 제보자 설문지(IQCODE)일 것입니다.[115]IQCODE가 치매를 진단하거나 예측하는 데 얼마나 정확한지를 판단하기에는 증거가 부족합니다.[116]알츠하이머병 간병인 설문지도 또 다른 도구입니다.간병인에 의해 알츠하이머에 대한 정확도는 약 90%입니다.[12]General Practician Assessment Of Cognition은 환자 평가와 정보 제공자 인터뷰를 모두 결합합니다.1차 진료 환경에서 사용할 수 있도록 특별히 설계되었습니다.
임상 신경 심리학자들은 다양한 종류의 치매와 관련된 기능적인 감소 패턴을 결정하기 위해 종종 몇 시간 동안 지속되는 인지 검사의 전체 배터리를 투여한 후 진단 상담을 제공합니다.기억력, 실행 기능, 처리 속도, 주의력 및 언어 능력에 대한 테스트와 감정 및 심리적 조정 테스트가 관련되어 있습니다.이러한 테스트는 다른 질병을 배제하고 시간이 지남에 따라 또는 이전 인지 능력의 추정치로부터 상대적 인지 저하를 결정하는 데 도움이 됩니다.[117]
실험실 테스트
정기적인 혈액 검사는 치료 가능한 원인을 배제하기 위해 보통 시행됩니다.여기에는 비타민 B12, 엽산, 갑상선 자극 호르몬(TSH), C-반응 단백질, 전혈수, 전해질, 칼슘, 신기능, 간 효소에 대한 검사가 포함됩니다.이상은 노인들에게 흔히 혼란이나 방향감각 상실을 일으키는 비타민 결핍, 감염, 또는 다른 문제들을 시사할 수 있습니다.[118]
이미징
CT 스캔 또는 MRI 스캔은 일반적으로 정상 압력 수두증, 잠재적으로 가역적인 치매 원인 또는 연결된 종양을 발견하기 위해 수행됩니다.스캔을 통해 혈관성 치매를 가리키는 경색(뇌졸중)과 같은 다른 치매 유형과 관련된 정보도 얻을 수 있습니다.이러한 검사는 신경학적 검사에서 심각한 신경학적 문제(마비나 쇠약 등)를 보이지 않는 사람에게서 치매와 관련된 확산성 대사 변화를 감지하지 못합니다.[119]
SPECT와 PET의 기능적 신경 영상 양식은 치매를 임상 검사와 인지 검사로 진단할 수 있는 유사한 능력을 보여주었기 때문에 오랜 인지 기능 장애를 평가하는 데 더 유용합니다.[120]혈관성 치매와 알츠하이머병을 구별하는 SPECT의 능력은 임상시험에 의한 구별보다 우수한 것으로 보입니다.[121]
Pittsburgh compound B (PiB)를 방사선 트레이서로 사용하는 PiB-PET 이미징의 가치는 예측 진단, 특히 알츠하이머병에서 입증되었습니다.[122]
예방
위험요인
2020년 리뷰는 치매와 관련된 위험 요소의 수를 증가시켰습니다.[7] 알코올 과몰입, 외상성 뇌 손상 및 대기 오염의 위험은 낮은 수준의 교육, 고혈압, 청력 손실, 흡연, 비만, 우울증, 비활동, 당뇨병 및 낮은 사회적 접촉에 추가되었습니다.[7]낮은 수준의 교육, 흡연, 신체적 비활동 및 당뇨병을 포함하여 확인된 이러한 위험 요소들 중 많은 것들이 수정 가능합니다.[123]2022년 검토에서는 빈혈과 수면을 수정 가능한 위험 요소에 추가했습니다.[124]그룹 중 몇 가지는 줄이거나 제거할 수 있는 혈관 위험 인자로 알려져 있습니다.[125]이러한 위험 요소를 관리하면 중년 후반 또는 그 이상의 연령에 있는 개인의 치매 위험을 줄일 수 있습니다.이러한 위험 요소의 감소는 긍정적인 결과를 가져올 수 있습니다.[126]건강한 생활 방식을 채택함으로써 얻을 수 있는 위험 감소는 유전적 위험이 높은 사람들에게서도 나타납니다.[127]
이상의 위험요인 외에도 메타분석을 통해 성격(높은 신경증, 낮은 양심성), 낮은 삶의 목적, 높은 외로움 등 다른 심리적 특성이 알츠하이머병 및 이와 관련된 치매의 위험요인이라는 강력한 증거가 있음을 알 수 있습니다.[128][129][130]예를 들어, 영국 노화 종단 연구(ELSA)에 근거하여, 노인들의 외로움이 치매 위험을 1/3 증가시킨다는 연구 결과가 나왔습니다.배우자가 없는 것은 치매의 위험을 두 배로 증가시켰습니다.하지만, 두세 명의 더 가까운 관계를 갖는 것은 위험을 3/5로 줄였습니다.[131][132]
치매의 가장 수정 가능한 두 가지 위험 요소는 신체적인 활동 불능과 인지 자극의 부족입니다.[133]신체 활동, 특히 유산소 운동은 나이와 관련된 뇌 조직 손실의 감소와 관련이 있으며, 신경 독성 요인이 뇌의 부피와 신경세포의 완전성을 유지합니다.인지 활동은 신경 가소성을 강화하고 함께 인지 예비력을 지원하는 데 도움을 줍니다.이러한 위험 요소를 무시하면 이러한 예비력이 줄어듭니다.[133]
연구에 따르면 시각과 청각의 감각 장애는 치매의 수정 가능한 위험 요소라고 합니다.[134]이러한 장애는 예를 들어 수년에 걸쳐 알츠하이머병의 인지적 증상보다 먼저 나타날 수 있습니다.[135]청력 손실은 인지에 부정적인 영향을 미치는 사회적 고립을 초래할 수 있습니다.[136]사회적 고립도 수정 가능한 위험 요소로 파악됩니다.[135]중년기의 나이와 관련된 청력 손실은 후기 인지 장애와 관련이 있으며, 알츠하이머병과 치매 발병의 위험 요소로 여겨집니다.이러한 청력 손실은 배경 소음에 대한 말의 이해를 어렵게 하는 중추 청각 처리 장애에 의해 발생할 수 있습니다.나이와 관련된 청력 손실은 청각 정보의 중앙 처리가 느려지는 것을 특징으로 합니다.[135][137]전 세계적으로, 중년의 청력 손실은 치매 환자의 약 9%를 차지할 수 있습니다.[138]
증거는 허약함이 인지기능 저하와 치매의 위험을 증가시킬 수 있다는 것과 반대로 인지기능 장애가 허약의 위험을 증가시킨다는 것을 보여줍니다.허약의 예방은 인지기능 저하를 예방하는 데 도움이 될 수 있습니다.[135]
그러나 2018년 리뷰에서는 혈압약을 포함한 어떤 약도 예방 효과에 대한 좋은 증거를 가지고 있지 않다고 결론 내렸습니다.[139]2020년 리뷰에 따르면 혈압 강하제를 사용하면 치매나 인지 문제의 위험이 7.5%에서 7.0%로 감소했습니다.[140]
경제적 불이익은 치매 유병률 증가와 강한 연관성을 가지고 있는 것으로 나타났는데,[141] 이는 다른 위험 요인들에 의해서도 아직 충분히 설명될 수 없습니다.
치아건강
제한된 증거는 구강 건강의 악화를 인지 저하와 연관 짓습니다.하지만 칫솔질 실패와 치은염은 치매 위험 예측 요인으로 활용될 수 있습니다.[142]
구강세균
알츠하이머와 잇몸 질환의 연관성은 구강 세균입니다.[143]구강 내 세균종으로는 P. gingivalis, F. nucleatum, P. intermedia, T. 개나리 등이 있습니다.알츠하이머 환자의 뇌에서 6개의 경구 트레포네마 스피로셰트가 검사되었습니다.[144]스피로셰트는 신경 조직을 파괴하고 염증을 일으키는 작용을 하는 본질적으로 신경성입니다.염증성 병원균은 알츠하이머병의 지표로 알츠하이머병 환자의 뇌에서 잇몸 질환과 관련된 박테리아가 발견됐습니다.[144]이 박테리아는 뇌의 신경 조직을 침범하여 혈액 뇌 장벽의 투과성을 증가시키고 알츠하이머의 발병을 촉진시킵니다.과도한 치석을 가진 사람들은 인지기능이 저하될 위험이 있습니다.[145]구강 위생 상태가 나쁘면 언어와 영양에 악영향을 미쳐 일반적이고 인지적인 건강을 해칠 수 있습니다.
구강 바이러스
50세 이상 노인의 70% 이상에게서 단순포진 바이러스(HSV)가 발견됐습니다.HSV는 말초 신경계에 지속되며 스트레스, 질병 또는 피로에 의해 유발될 수 있습니다.[144]아밀로이드반 또는 신경섬유성 엉킴(NFT)에서 바이러스 관련 단백질의 높은 비율은 알츠하이머병 병리학에서 HSV-1의 관여를 확인합니다.NFT는 알츠하이머병의 주요 표식으로 알려져 있습니다.HSV-1은 NFT의 주요 부품을 생산합니다.[146]
다이어트
식이요법은 치매 발병의 수정 가능한 위험 요소로 여겨집니다.티아민 결핍은 성인에서 알츠하이머병의 위험을 증가시키는 것으로 확인됩니다.[147]뇌 생리학에서 티아민의 역할은 독특하고 노인들의 정상적인 인지 기능에 필수적입니다.[148]글루텐 프리 제품의 높은 섭취를 포함한 노인 인구의 많은 식이 선택은 이러한 제품들이 티아민으로 강화되지 않기 때문에 티아민의 섭취를 손상시킵니다.[149]
지중해식과 DASH식은 둘 다 인지기능 저하와 관련이 있습니다.다른 접근법은 이 두 다이어트의 요소를 MIND 다이어트라고 알려진 것에 포함시키는 것이었습니다.[150]이러한 식단은 일반적으로 포화지방이 적은 반면, 탄수화물의 좋은 공급원, 주로 혈당과 인슐린 수준을 안정시키는 데 도움을 주는 것을 제공합니다.[151]혈당 수치가 장기간에 걸쳐 높아지면 신경을 손상시키고 관리하지 않으면 기억력에 문제가 생길 수 있습니다.[152]치매 위험을 줄이기 위해 제안된 식단과 관련된 영양적인 요소들은 불포화 지방산, 비타민 E, 비타민 C, 플라보노이드, 비타민 B, 그리고 비타민 D를 포함합니다.[153][154]영국의 엑세터 대학에서 시행된 한 연구는 과일, 채소, 통곡물, 그리고 건강한 지방이 치매의 위험을 약 25%[155] 줄이는데 도움을 줄 수 있는 최적의 식단을 만드는 것으로 이러한 결과를 확인한 것으로 보입니다.
MIND 식단이 더 보호적일 수 있지만 더 많은 연구가 필요합니다.지중해식이 DASH보다 알츠하이머를 더 예방하는 것 같지만 일반적으로 치매에 대한 일관된 발견은 없습니다.올리브 오일의 역할은 인지기능 저하와 치매의 위험을 줄이는 데 가장 중요한 요소 중 하나일 수 있기 때문에 더 많은 연구가 필요합니다.[150][156]
셀리악병이나 셀리악 글루텐 과민증이 있는 사람들에게, 글루텐이 없는 엄격한 식단은 가벼운 인지 장애가 주어지면 증상을 완화시킬 수 있습니다.[87][88]일단 치매가 진행되면 글루텐이 없는 식단이 유용하다는 증거는 없습니다.[87]
오메가-3 지방산 보충제는 경미하거나 중등도의 증상을 가진 사람들에게 도움이 되거나 해를 끼치지 않는 것으로 보입니다.[157]그러나 식단에 오메가3를 포함시키는 것이 흔한 증상이자 [158]잠재적으로 치매의 수정 가능한 위험 요소인 우울증을 치료하는 데 도움이 된다는 좋은 증거가 있습니다.[7]
관리
치매를 치료하는 방법은 제한적이며, 대부분의 접근법은 개인의 증상을 관리하거나 줄이는 데 초점을 맞추고 있습니다.치매 발병을 지연시킬 수 있는 치료 방법은 없습니다.[159]아세틸콜린에스테라아제 억제제는 종종 장애 과정 초기에 사용되지만, 일반적으로 이점은 적습니다.[8][160]치매에 걸린 사람의 절반 이상은 동요, 수면 문제, 공격성 및/또는 정신병을 포함한 심리적 또는 행동적 증상을 경험할 수 있습니다.이러한 증상에 대한 치료는 그 사람의 고통을 줄이고 그 사람을 안전하게 유지하는 것을 목적으로 합니다.동요나 공격성에는 약물 이외의 치료가 더 좋은 것 같습니다.[161]인지적 및 행동적 개입이 적절할 수 있습니다.치매 환자는 물론 간병인과 가족에 대한 교육과 지원이 성과를 높인다는 증거도 있습니다.[162]완화의료 개입은 죽음에 대한 편안함을 향상시킬 수 있을지 모르지만, 그 증거는 낮습니다.[163]운동 프로그램은 일상 생활 활동에 도움이 되며 치매를 개선할 수 있습니다.[164]
치료법의 효과는 예를 들어 코헨-맨스필드 교반 재고(CMAI)를 사용하여 동요를 평가하거나, 메노라 공원 참여 척도(MPES)[165]를 사용하여 기분과 참여를 평가하거나, 관찰된 감정 등급 척도(OERS)를 사용하여 우울증 지표를 평가하거나, 코넬 치매 우울증 척도([166]C)를 사용하여 우울증 지표를 평가함으로써 평가할 수 있습니다.SDD)[167] 또는 이를 단순화한 버전.[168]
치매를 치료하고 관리하는 데 있어 종종 간과되는 것은 간병인의 역할과 그들이 다양한 개입을 어떻게 지원할 수 있는지에 대해 알려진 것입니다.2021년 문헌을 체계적으로 검토한 결과 요양원에서 치매에 걸린 사람을 돌보는 사람은 약물 사용과 함께 치매의 행동 및 심리적 증상(BPSD)에 대한 충분한 도구나 임상 지침을 가지고 있지 않습니다.[169]관심사에 대해 사람들에게 말하는 것과 같은 간단한 조치는 치매를 앓고 있는 요양원 거주자들의 삶의 질을 향상시킬 수 있습니다.한 프로그램은 그러한 간단한 조치들이 주민들의 동요와 우울증을 감소시켰다는 것을 보여주었습니다.그들은 또한 GP 방문과 병원 입원이 더 적게 필요했고, 이는 이 프로그램이 비용을 절감한다는 것을 의미하기도 했습니다.[170][171]
심리·심리사회적 치료법
치매에 대한 심리적 치료에는 회상 치료에 대한 일부 제한된 증거(즉, 삶의 질, 인지, 의사소통 및 기분 영역에서 일부 긍정적인 효과 – 특히 요양원 환경에서 첫 세 가지),[172] 간병인의 인지 재구성에 대한 일부 이점,[173] 검증[174] 치료에 대한 명확하지 않은 증거 및 잠정적인 것이 포함됩니다.경도에서 중등도의 치매를 가진 사람들을 위한 인지 자극 프로그램과 같은 정신 운동에 대한 증거.[175]개인 맞춤형 활동을 제공하는 것은 도전적인 행동을 줄이고 삶의 질을 향상시킬 수 있습니다.[176]개인 맞춤형 활동이 돌봄자의 삶의 질에 영향을 미치거나 개선하는 데 영향을 미치는지는 명확하지 않습니다.[176]
요양원 내 특수요양시설은 물론 성인어린이집에서도 치매환자에 대한 전문적인 돌봄을 제공하는 경우가 많습니다.어린이집은 참가자들에게 관리, 레크리에이션, 식사, 제한된 건강관리를 제공하며, 보호자들에게 휴식을 제공합니다.또한 가정 간호는 가정 내에서 일대일 지원과 돌봄을 제공할 수 있어 장애가 진행됨에 따라 필요한 보다 개별화된 관심을 받을 수 있습니다.정신과 간호사는 사람들의 정신 건강에 뚜렷한 기여를 할 수 있습니다.[177]
치매는 계획을 세우고 문제를 해결하는 능력뿐만 아니라 수용적이고 표현적인 언어의 변화로 정상적인 의사소통을 저해하기 때문에 동요행동은 치매환자에게 의사소통의 한 형태가 되는 경우가 많습니다.통증, 신체적 질병 또는 과도한 자극과 같은 잠재적인 원인을 적극적으로 찾는 것이 동요를 줄이는데 도움이 될 수 있습니다.[178]또한 '행동분석(ABC analysis of behavior)'을 통해 치매환자의 행동을 파악하는데 유용한 도구가 될 수 있습니다.사건과 관련된 선행(A), 행동(B), 결과(C)를 살펴보는 것으로 문제를 정의하고 당사자의 요구를 오해할 경우 발생할 수 있는 추가 사건을 방지하는 데 도움이 됩니다.[179]치매의 변화된 행동의 관리를 위한 비약물학적 치료의 가장 강력한 증거는 그러한 접근법을 사용하는 것입니다.[180]낮은 품질의 증거는 정기적인 (최소 5회의) 음악 치료가 제도화된 거주자들에게 도움이 될지도 모른다는 것을 암시합니다.우울증 증상을 줄이고 전반적인 행동을 개선할 수 있습니다.그것은 또한 정서적인 행복과 삶의 질에 유익한 효과를 제공할 뿐만 아니라 불안을 줄일 수 있습니다.[181]2003년, 알츠하이머 협회는 시범 연구를 바탕으로 한 프로젝트인 'Sing for the Brain'을 설립했는데, 이 프로젝트는 참여를 장려하고 새로운 노래를 배울 수 있게 해준다고 제안했습니다.그 세션들은 회상 치료의 측면과 음악을 결합합니다.[182]음악적, 대인관계적 연결은 그 사람의 가치를 강조하고 삶의 질을 향상시킬 수 있습니다.[183]
일부 런던 병원들은 색깔, 디자인, 사진, 불빛을 사용하는 것이 치매에 걸린 사람들이 병원에 있는 것에 적응하는 데 도움이 된다는 것을 발견했습니다.이러한 병원의 치매 날개 배치에 대한 이러한 조정은 혼란을 방지함으로써 환자를 돕습니다.[184]
회상 치료의 일환으로 인생 이야기 작업을 수행하며, 비디오 전기는 다양한 방법으로 고객과 보호자의 요구를 해결하는 것으로 밝혀졌으며, 고객에게 유산을 남기고 인격을 향상시킬 수 있는 기회를 제공하며, 또한 그러한 작업에 참여하는 청소년들에게 혜택을 줍니다.그러한 개입은 치매의 비교적 초기 단계에서 이루어질 때 더 유익할 수 있습니다.과거 경험을[183] 처리하는 데 어려움을 겪는 사람들에게서도 문제가 될 수 있습니다.
동물을 이용한 치료가 도움이 된다는 것이 밝혀졌습니다.돌봄 환경에서 공동 공간에서 애완동물을 항상 환영하지는 않는다는 단점이 있을 수 있습니다.동물은 거주자에게 위험을 초래할 수도 있고 위험하다고 인식될 수도 있습니다.어떤 문화 집단에서는 어떤 동물들이 "깨끗하지 않다"거나 "위험하다"고 여겨질 수도 있습니다.[183]
또한 작업치료는 일상적인 작업수행능력과 간병인의 역량 향상을 통해 치매환자의 심리적, 심리사회적 욕구를 해결합니다.[185]보상적 개입 전략이 그들의 일상에 추가되면, 성과 수준은 향상되고 그들의 간병인들에게 공통적으로 가해지는 부담은 줄어듭니다.[185]작업 치료사는 다른 분야와 협력하여 고객 중심의 개입을 만들 수도 있습니다.[186]인지장애를 관리하고 치매의 행동 및 심리적 증상에 대처하기 위해 직업 및 행동 치료를 결합하면 치매 환자를 더욱 지원할 수 있습니다.[186]
인지훈련
인지 훈련이 파킨슨병, 치매, 또는 경도 인지 장애가 있는 사람들에게 도움이 된다는 강력한 증거는 없습니다.[187]
개인 맞춤형 활동
장기 요양원에서 치매 환자에게 개인 맞춤형 활동 시간을 제공하면 어려운 행동을 약간 줄일 수 있습니다.[188]
약물

치매를 예방하거나 치료할 수 있는 어떠한 약물도 제시되지 않았습니다.[189]약물은 행동 및 인지 증상을 치료하는 데 사용될 수 있지만 근본적인 질병 과정에는 영향을 미치지 않습니다.[12][190]
도네페질과 같은 아세틸콜린에스테라아제 억제제는 알츠하이머병,[191] 파킨슨병 치매, DLB 또는 혈관성 치매에 유용할 수 있습니다.[190]증거의 질이 떨어지고[192] 이익이 적습니다.[8]이 가족의 요원들 사이에 차이는 보이지 않습니다.[193]소수의 사람들에게는 느린 심박수와 실신을 포함한 부작용이 있습니다.[194]리바스티그민은 파킨슨병 치매의 증상을 치료하는데 권장됩니다.[61]
2021년에 발표된 체계적인 리뷰에 따르면, 항콜린제 효과가 있는 약물은 치매 환자의 모든 원인 사망률을 증가시키지만, 이러한 약물이 인지 기능에 미치는 영향은 여전히 불확실합니다.[195]
노인에게 항정신병 약물을 처방하기 전에 행동의 근본적인 원인에 대한 평가가 필요합니다.[196]심각하고 생명을 위협하는 반응은 DLB를 가진 사람들의 거의 절반에서 일어나며,[72][197] 한 번 복용하면 치명적일 수 있습니다.[198]신경병증을 앓는 루이성 치매 환자들은 생명을 위협하는 질병인 신경병증 악성 증후군에 걸릴 위험이 있습니다.[199]DLB 환자들은 항정신병 약물에 민감하기 때문에 항정신병 약물을 사용할 때는 극도의 주의가 필요합니다.[71]항정신병 약물은 비약물요법이 효과가 없을 경우에만 치매 치료에 사용되며, 그 사람의 행동은 자신이나 다른 사람을 위협합니다.[200][201][202][203]공격적인 행동 변화는 때때로 다른 해결 가능한 문제들의 결과인데, 이것은 항정신병 치료를 불필요하게 만들 수 있습니다.[200]치매에 걸린 사람들은 공격적일 수 있고, 치료에 저항력이 있으며, 그렇지 않으면 파괴적일 수 있기 때문에, 때때로 항정신병 약물은 대응하는 치료법으로 간주됩니다.[200]이러한 약물은 뇌졸중과 사망 가능성을 높이는 것을 포함하여 위험한 부작용을 가지고 있습니다.[200]이러한 부작용과 작은 유익성 항정신병약은 가능하면 언제든지 사용하지 않습니다.[180]일반적으로 치매 환자에게 항정신병약을 중단하는 것은 오랜 기간 복용한 사람에게도 문제가 되지 않습니다.[204]
메만틴과 같은 NMDA(N-methyl-D-aspartate) 수용체 차단제가 도움이 될 수 있지만 AChEIs보다 증거가 덜 확실합니다.[191]작용기전이 다르기 때문에 메만틴과 아세틸콜린에스테라아제 억제제를 병용할 수 있지만 이점은 미미합니다.[205][206]
EGb 761은 은행나무 빌로바 추출물로 경증에서 중등도의 치매 및 기타 신경정신질환 치료에 널리 사용되고 있습니다.[207]유럽 전역에서 사용이 승인되었습니다.[208]세계생물정신의학협회 지침에는 아세틸콜린에스테라아제 억제제와 메멘틴에 동일한 증거 무게(레벨 B)를 부여한 EGb 761이 기재되어 있습니다.EGB 761은 AD와 혈관성 치매 모두에서 증상 개선을 보인 유일한 환자입니다.EGB 761은 특히 다른 치료법들이 효과가 없다고 증명되었을 때 그 자체로 또는 부가적인 역할을 할 수 있는 것으로 여겨집니다.[207]EGb 761은 자유 라디칼 소거제이며, 미토콘드리아 기능을 향상시키고 세로토닌 및 도파민 수준을 조절하는 신경 보호제로 간주됩니다.경도에서 중등도 치매에서의 그것의 사용에 대한 많은 연구들은 그것이 인지 기능, 일상 생활의 활동, 신경 정신적 증상 그리고 삶의 질을 크게 향상시킨다는 것을 보여주었습니다.[207][209]하지만, 그것의 사용이 치매의 진행을 막지는 못하는 것으로 나타났습니다.[207]
우울증은 종종 치매와 관련이 있지만 선택적 세로토닌 재흡수 억제제(SSRI)와 같은 항우울제의 사용은 결과에 영향을 미치지 않는 것으로 보입니다.[210][211]그러나 SSRIs sertraline과 citalopram은 위약에 비해 동요 증상을 감소시키는 것으로 입증되었습니다.[212]
어떤 확실한 증거도 엽산이나 비타민 B가12 인지 문제가 있는 사람들의 결과를 개선시킨다는 것을 나타내지 않습니다.[213]스타틴은 치매에 효과가 없습니다.[214]치매 진단을 받은 사람의 경우 다른 건강 상태에 대한 약물을 다르게 관리해야 할 수도 있습니다.혈압약과 치매가 연관이 있는지는 불분명합니다.이러한 약들이 철회되면 사람들은 심혈관 관련 사건들이 증가할 수 있습니다.[215]
MATCH-D(Medication Officiency Tool for Combord Health Conditions in Dementia) 기준은 치매 진단이 다른 건강 상태의 약물 관리를 변경하는 방법을 식별하는 데 도움이 될 수 있습니다.[216]이러한 기준은 치매 환자들이 평균 5가지의 다른 만성질환을 가지고 살기 때문에 개발된 것으로, 이들 질병은 종종 약물과 함께 관리됩니다.기준을 알려주는 체계적 검토는 2018년에 후속적으로 발표되고 2022년에 업데이트되었습니다.[217]
수면장애
치매 환자의 40% 이상이 수면 문제를 보고하고 있습니다.이러한 수면 문제를 치료하기 위한 접근법으로는 약물과 비약물학적 접근이 있습니다.[218]치매 환자들이 흔히 겪는 수면장애를 완화하기 위한 약물의 사용은 일반적으로 처방되는 약물에 대해서도 잘 연구되지 않고 있습니다.[219]2012년 미국 노인병 학회는 치매 환자들에게 디아제팜과 같은 벤조디아제핀과 비벤조디아제핀 최면술을 피하라고 권고했는데, 이는 인지 장애와 낙상의 위험이 증가하기 때문입니다.[220]벤조디아제핀 또한 섬망을 촉진하는 것으로 알려져 있습니다.[221]또한, 벤조디아제핀의 효과를 입증하는 증거는 거의 없습니다.[219][222]알츠하이머로 인해 치매에 걸린 사람들의 수면이 개선된다는 명확한 증거는 없지만,[219] 루이 몸으로 치매에서 렘수면행동장애를 치료하는 데 사용됩니다.[72]적은 양의 트라조돈이 수면을 개선시킬 수 있다는 제한된 증거가 있지만, 더 많은 연구가 필요합니다.[219]
치매 환자의 수면 문제를 치료하기 위한 비약물학적 접근법이 제안되었지만, 특히 요양원이나 장기 요양원과 같은 제도화된 환경에서 살고 있는 사람들에 대한 다양한 유형의 개입의 효과에 대한 강력한 증거나 확실한 결론은 없습니다.[218]
통증
사람들은 나이가 들수록 더 많은 건강 문제를 경험하게 되고, 노화와 관련된 대부분의 건강 문제는 상당한 고통을 수반하기 때문에 노인의 25%에서 50%가 지속적인 고통을 경험하게 됩니다.치매가 있는 노인은 치매가 없는 노인과 같은 고통을 유발할 가능성이 있는 질환의 유병률을 경험합니다.[223]노인들의 경우 통증을 간과하는 경우가 많으며, 검진을 받을 때, 다른 사람들에게 통증을 알릴 수 없기 때문에 특히 치매 환자들 사이에서 종종 좋지 않은 평가를 받습니다.[223][224]인간적인 보살핌의 문제를 넘어, 해소되지 않은 고통은 기능적인 의미를 갖습니다.노인의 낙상 요인은 지속적인 통증으로 인한 보행장애, 우울한 기분, 수면장애, 식욕부진, 인지장애[224] 및 통증 관련 활동방해의 악화로 이어질 수 있습니다.[223][225]
치매 환자의 지속적인 통증은 의사소통, 진단, 치료가 어렵지만, 지속적인 통증을 해결하지 못하면 이 취약계층에게 심각한 기능적, 심리적, 삶의 질에 영향을 미칩니다.보건 전문가들은 종종 기술이 부족하고 보통 치매 환자들의 고통을 인식하고 정확하게 평가하고 적절하게 감시하는 데 필요한 시간이 부족합니다.[223][226]가족과 친구들은 치매 환자의 고통을 인식하고 평가하는 법을 배우면 치매 환자의 치료에 귀중한 기여를 할 수 있습니다.교육 자원과 관찰 평가 도구를 이용할 수 있습니다.[223][227][228]
섭식장애
치매가 있는 사람은 먹는 것에 어려움을 겪을 수 있습니다.선택 사항으로 이용 가능할 때마다, 식사 문제에 대한 권장되는 대응 방법은 관리인이 그들을 돕도록 하는 것입니다.[200]효과적으로 삼킬 수 없는 사람들을 위한 2차적인 선택은 영양을 주는 방법으로 위루관을 배치하는 것을 고려하는 것입니다.그러나 흡인성 폐렴과 사망의 위험을 줄이면서 편안함을 가져오고 기능 상태를 유지하는 데 있어 경구 공급의 도움은 적어도 튜브 공급만큼 좋습니다.[200][229]튜브 공급은 동요, 물리적, 화학적 구속 장치의 증가, 그리고 악화되는 압력 궤양과 관련이 있습니다.튜브 공급은 수액 과다, 설사, 복통, 국소 합병증을 유발할 수 있으며 인체 상호 작용이 적으며 흡인 위험이 높아질 수 있습니다.[230][231]
진행성 치매를 가진 사람들의 이점은 아직 나타나지 않았습니다.[232]튜브 공급을 사용할 경우 위험에는 동요, 사람에 의한 거부(튜브를 빼내거나 그렇지 않으면 물리적 또는 화학적으로 움직이지 못하도록 함), 또는 압력 궤양이 발생합니다.[200]이 시술은 치명률[233] 1%와 주요 합병증률 3%와 직접적인 관련이 있습니다.[234]미국에서는 2000년 12%였던 치매 말기 환자의 영양공급관 사용률이 2014년 현재 6%로 떨어졌습니다.[235][236]
치매 환자의 삼킴 곤란을 위한 수액의 두께를 조절하는 즉각적이고 장기적인 효과는 잘 알려져 있지 않습니다.[237]수분을 두껍게 하는 것이 삼킴과 구강 섭취 개선에 즉각적인 긍정적인 영향을 줄 수 있지만, 치매 환자의 건강에 대한 장기적인 영향도 고려해야 합니다.[237]
운동
운동 프로그램은 치매 환자들의 일상 활동 수행 능력을 향상시킬 수도 있지만, 최상의 운동 유형은 여전히 불분명합니다.[238]운동을 더 많이 하면 치매와 같은 인지 문제의 발생을 늦출 수 있어 알츠하이머병의 위험을 약 50% 감소시키는 것으로 증명됩니다.근력운동, 근육이 뇌로 피를 뿜어내는 것을 도와주는 밸런스 운동, 그리고 나이 든 사람들에게는 밸런스 운동이 권장됩니다.제안된 양은 약 3.0 정도입니다.주당 2+1⁄ 2시간은 낙상과 같은 다른 건강상의 위험뿐만 아니라 인지적 부패의 위험을 줄일 수 있습니다.
보조기술
보조 기술이 치매 환자의 기억력 문제를 효과적으로 관리할 수 있는지를 판단할 수 있는 양질의 증거가 부족합니다.[240]오늘날 치매에 도움이 되는 몇 가지 특정한 것들은 시계, 통신 보조 장치, 전기 기구 사용 모니터링, GPS 위치/추적 장치, 홈케어 로봇, 가정 내 카메라, 약물 관리 등입니다.[241]
대체의학
아로마 요법과 마사지의 치료적 가치에 대한 증거는 불분명합니다.[242][243]칸나비노이드가 치매에 걸린 사람들에게 해로운지 혹은 효과적인지는 확실하지 않습니다.[244]
완화의료
치매의 점진적이고 말기적인 특성을 고려할 때, 완화의료는 장애를 가진 사람들과 그들의 간병인들이 무엇을 기대해야 하는지를 이해하고, 신체적, 정신적 능력의 상실에 대처하고, 대리적 의사결정을 포함한 그 사람의 희망과 목표를 지원함으로써 환자와 그들의 간병인들에게 도움이 될 수 있습니다.심폐소생술과 생명유지장치에 대한 찬성 또는 반대의 뜻을 논의합니다.[245][246]감소 속도가 빠를 수 있고, 대부분의 사람들이 치매 환자가 스스로 결정할 수 있도록 하는 것을 선호하기 때문에, 치매 말기 이전에 완화의료 참여를 권장합니다.[247][248]적절한 완화의료 개입과 그것들이 치매 진행자들에게 얼마나 잘 도움이 되는지를 결정하기 위해서는 추가적인 연구가 필요합니다.[163]
사람 중심의 돌봄은 치매 환자의 존엄성을 유지하는 데 도움이 됩니다.[249]
간병인을 위해 원격으로 정보를 전달
지원, 교육 및 정보를 포함한 원격으로 제공되는 개입은 비공식 간병인의 부담을 줄이고 우울 증상을 개선할 수 있습니다.[250]그들이 건강과 관련된 삶의 질을 향상시킨다는 확실한 증거는 없습니다.[250]
일본의 몇몇 지역에서는 치매 환자가 길을 잃고 실종되기 쉬운 경우 가족 구성원이 디지털 감시를 이용할 수 있습니다.[251]
역학
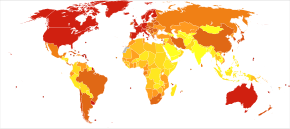

<100 100–120 120–140 140–160 160–180 180–200 | 200–220 220–240 240–260 260–280 280–300 >300 |
2021년 전 세계 치매 환자 수는 5,500만 명으로 추산되며, 매년 1,000만 명에 육박하는 신규 환자가 발생하고 있습니다.[2]2050년까지, 치매에 걸린 사람들의 수는 전세계적으로 1억 5천만 명 이상이 될 것으로 추정됩니다.[252]65세 이상 노인의 약 7%가 치매에 걸렸고, 기대수명이 상대적으로 높은 곳에서는 약간 높은 비율(65세 이상 노인의 최대 10%)을 보였습니다.[253]치매에 걸린 사람들의 약 58%가 저소득 국가와 중산층 국가에 살고 있습니다.[254][255]치매의 유병률은 중부 유럽의 4.7%에서 북아프리카/중동의 8.7%에 이르는 세계 지역마다 차이가 있으며, 다른 지역의 유병률은 5.6~7.6%[254]로 추정됩니다.치매에 걸린 사람들의 수는 20년마다 두 배로 늘어날 것으로 추정됩니다.2016년 치매로 인해 약 240만명이 사망했는데,[9] 이는 1990년의 80만명에서 증가한 수치입니다.[256]치매장애의 유전적, 환경적 위험요인은 민족별로 차이가 있습니다.[257][258]예를 들어, 히스패닉계/라틴계 및 아프리카계 미국인 피험자 중 알츠하이머병은 비 히스패닉계 백인 피험자보다 아폴리포단백질 E 유전자의 유전자 변화와 관련된 위험성이 낮은 것으로 나타났습니다.[citation needed]
치매 진단의 연간 발생률은 전 세계적으로 천만 명에 육박합니다.[163]신규 치매 환자의 거의 절반은 아시아에서 발생하며, 유럽(25%), 미주(18%), 아프리카(8%)가 그 뒤를 이룹니다.치매 발병률은 나이가 들수록 기하급수적으로 증가하며, 나이가 6.3세 증가할 때마다 두 배씩 증가합니다.[254]치매는 65세 이상 인구의 5%와 85세 이상 인구의 20~40%에 영향을 미칩니다.[259]65세 이상에서는 남성보다 여성의 비율이 약간 높습니다.[259]60-69세 진단을 받은 사람의 경우 6.7세에서 90세 이상 진단을 받은 사람의 경우 1.9세까지 질병의 궤적은 다양하며 진단 시 사망까지의 평균 시간은 진단 시 연령에 따라 크게 달라집니다.[163]
치매는 치매에 걸린 개인뿐만 아니라 보호자와 사회 전반에 영향을 미칩니다.2010년 세계질병부담지수(GBD)에 따르면, 60세 이상의 사람들 중 치매는 9번째로 부담스러운 질환으로 꼽혔습니다.전 세계 치매 비용은 2015년 약 8,180억 달러로 2010년 6,040억 달러에 비해 35.4% 증가했습니다.[254]
환부연령
65세에서 74세 사이의 사람들 중 약 3%가 치매에 걸렸고, 75세에서 84세 사이의 사람들 중 19%가 치매에 걸렸고, 85세 이상의 사람들 중 거의 절반이 치매에 걸렸습니다.더 많은 사람들이 장수하면서 치매는 점점 더 보편화되고 있습니다.[260]그러나 특정 연령대의 사람들에게는 더 큰 재정적 및 교육적 자원에 의해 가능해진 수정 가능한 위험 요소의 감소로 인해 선진국에서 빈도가 낮아지고 있을 수 있습니다.노인들 사이에서 가장 흔한 장애 원인 중 하나이지만, 조기발병성 치매나 전노인성 치매로 알려진 65세 이전에 발병할 수 있습니다.[261][262]알츠하이머병을 앓고 있는 사람들의 1% 미만은 초기 발병 알츠하이머병으로 알려진 45세 전후로 훨씬 더 이른 발병을 일으키는 유전자 돌연변이를 가지고 있습니다.[263]알츠하이머병 환자의 95% 이상이 산발적인 형태(발병 후기, 80~90세)를 가지고 있습니다.[263]2015년 치매 비용은 전 세계적으로 8,180억 달러에 달했습니다.치매에 걸린 사람들은 필요 이상으로 신체적 또는 화학적으로 제약을 받는 경우가 많아 인권 문제가 제기되고 있습니다.[2][264]사회적 낙인은 질병을 가진 사람들과 그들의 간병인들이 흔히 인식합니다.[92]
역사
이 섹션은 검증을 위해 추가적인 인용이 필요합니다.(2015년 11월)(이 를 및 |
19세기 말까지 치매는 훨씬 더 광범위한 임상적 개념이었습니다.그것은 정신 질환과 가역적인 상태를 포함한 어떤 종류의 심리 사회적인 무력도 포함했습니다.[265]이때의 치매는 단순히 이성능력을 상실한 사람을 지칭하는 것으로 정신병, 뇌를 파괴하는 매독과 같은 '유기적'인 질병, '동맥경화'에 기인하는 노년기 치매에도 동일하게 적용됐습니다.
치매는 고대부터 의학 문헌에서 언급되어 왔습니다.치매에 대한 가장 초기의 알려진 암시들 중 하나는 기원전 7세기 그리스 철학자 피타고라스에 의한 것으로, 그는 인간의 수명을 여섯 단계로 나누었습니다: 0–6세 (유아기), 7–21세 (청소년기), 22–49세 (청소년기), 50–62세 (중년기), 63–79세 (고령기), 그리고 80–사망 (고령기).마지막 두 단계는 정신적, 육체적으로 쇠퇴하는 시기인 "세니움"으로 묘사되었으며, 마지막 단계는 "매우 운 좋게도 인류의 종들 중 거의 도착하지 않는 인간의 존재의 장면이 유아기의 첫 번째 시대의 무능함으로 감소하는 매우 긴 시간 후에 닫히는 것"이라고 설명했습니다.[266]기원전 550년, 아테네의 정치가이자 시인인 솔론은 고령으로 인해 판단력을 잃으면 사람의 의지가 무효가 될 수도 있다고 주장했습니다.중국 의학 문헌에서도 이 병을 암시하고 있으며, "치매"를 뜻하는 문자는 문자 그대로 "바보 노인"으로 번역됩니다.[267]
아테네의 철학자 아리스토텔레스와 플라톤은 노년과 함께 올 수 있는 정신적 쇠퇴에 대해 논의하고 이것이 노년이 되는 모든 사람들에게 영향을 미치고 이러한 쇠퇴가 일어나는 것을 막기 위해 아무것도 할 수 없다고 예측했습니다.플라톤은 구체적으로 어떻게 노인들이 책임감이 필요한 위치에 있어서는 안 되는지에 대해 이야기했는데, 그 이유는 "젊은 시절에 그들을 운반했던 마음의 감각, 사람들이 판단력, 상상력, 추론력, 그리고 기억력이라고 부르는 그러한 특징들은 많지 않습니다.그들은 그들이 점점 악화되어 가는 것을 보고 그들의 기능을 거의 다하지 못합니다."[268]
이에 비해 로마의 정치가 키케로는 노인들에게 정신적 기능의 상실은 필연적인 것이 아니며 "의지가 약한 노인들에게만 영향을 미친다"는 현대 의학적 지혜와 훨씬 더 일치하는 견해를 가지고 있었습니다.그는 정신적으로 활동적이고 새로운 것을 배우려는 열망을 가진 사람들이 치매를 예방할 수 있는 방법에 대해 말했습니다.그러나, 키케로의 노화에 대한 견해는 비록 진보적이기는 하지만, 아리스토텔레스의 의학 저술에 의해 수세기 동안 지배될 세계에서는 대체로 무시되었습니다.갈렌과 셀수스와 같은 로마 제국 시대의 의사들은 의학 지식에 새로운 기여를 거의 하지 않으면서 아리스토텔레스의 믿음을 단순히 반복했습니다.
비잔틴 의사들은 가끔 치매에 대해 썼습니다.수명이 70세를 넘긴 황제 중 최소 7명이 인지기능 저하 증세를 보였다고 기록돼 있습니다.콘스탄티노플에서는 치매나 정신 이상 진단을 받은 사람들이 특수 병원에 입원해 있었지만, 법 위에 있고 건강 상태를 공개적으로 인정할 수 없는 황제들에게는 적용되지 않았습니다.
그렇지 않으면, 거의 1700년 동안 서양 의학 문헌에는 치매에 대해 거의 기록되어 있지 않습니다.13세기 수사 로저 베이컨은 노년을 원죄에 대한 신성한 형벌로 여겼습니다.치매는 피할 수 없다는 기존 아리스토텔레스적인 믿음을 반복했지만, 뇌는 심장이 아닌 기억과 사고의 중심이라는 진보적인 주장을 펼쳤습니다.
시인, 극작가, 그리고 다른 작가들은 노년기의 정신 기능 상실에 대해 자주 암시했습니다.윌리엄 셰익스피어는 햄릿과 리어왕과 같은 연극에서 그것을 언급합니다.
19세기 동안 의사들은 노인 치매가 뇌를 공급하는 주요 동맥의 막힘이나 대뇌 피질의 혈관 내의 작은 뇌졸중 때문이라는 의견들 사이에서 의견이 엇갈렸지만, 일반적으로 노인 치매가 대뇌 죽상경화증의 결과라고 믿게 되었습니다.
1907년 바이에른의 정신과 의사 알로이스 알츠하이머는 51세의 오귀스트 데어의 뇌에서 진행성 치매의 특징을 처음으로 발견하고 기술했습니다.[269]데어는 남편을 간통 혐의로 고발하고, 집안일을 소홀히 하며, 글쓰기와 대화에 어려움을 보이며, 불면증이 고조되고, 방향감각을 상실하는 등 평소답지 않은 행동을 하기 시작했습니다.[270]한때, 데어는 "밖으로 침대 시트를 끌고 나가서 미친 듯이 돌아다녔고, 자정에 몇 시간 동안 울었습니다"[270]라고 보도되었습니다. 1901년 11월 25일, 데어가 프랑크푸르트 정신병원에 입원했을 때, 알츠하이머는 데어를 치료하기 시작했습니다.[270]그녀가 진행 중인 치료 동안, 데어와 그녀의 남편은 의료 비용을 감당하기 위해 고군분투했고, 알츠하이머는 데어의 의료 기록과 사망 시 그녀의 뇌를 기증하는 대가로 그녀의 치료를 계속하기로 동의했습니다.[270]데어는 패혈증과 폐렴에 굴복한 후 1906년 4월 8일 사망했습니다.[270]알츠하이머는 당시 새로운 방법으로 개발된 비엘쇼스키 염색법을 이용하여 뇌 조직 검사를 실시하였고, 노인반, 신경섬유 엉킴, 죽상경화성 변화를 관찰하였습니다.[269]당시 의사들 사이에서는 노인반이 일반적으로 노인 환자에게서 발견된다는 의견이 일치했으며, 신경섬유상 엉킴의 발생은 당시로서는 완전히 새로운 관찰이었습니다.[270]알츠하이머는 1906년 4월 11일 튀빙겐에서 열린 제37차 독일 남서부 정신의학회의에서 그의 연구결과를 발표했지만, 그의 동료들은 그 정보를 제대로 받아들이지 못했습니다.[270]1910년까지 Alois Alzheimer의 선생님인 Emil Kraepelin은 알츠하이머 발견의 중요성을 인정하기 위한 시도로 "알츠하이머병"이라는 용어를 만든 책을 출판했습니다.[269][270]
1960년대까지 신경퇴행성 질환과 나이와 관련된 인지 저하 사이의 관계가 더욱 확립되었습니다.1970년대까지 의료계는 혈관성 치매가 이전에 생각했던 것보다 드물었고 알츠하이머병이 노년기 정신장애의 대부분을 초래했다고 주장했습니다.그러나 최근에는 치매가 종종 복합적인 상태라고 여겨집니다.
1976년 신경학자 로버트 카츠만(Robert Katzmann)은 노인성 치매와 알츠하이머병 사이의 연관성을 제시했습니다.[271]Katzmann은 65세 이후에 발생하는 노인성 치매의 많은 부분이 65세 미만의 사람들에게서 발생하는 알츠하이머병과 병리학적으로 동일하므로 다르게 취급해서는 안 된다고 제안했습니다.[272]따라서 카츠만 박사는 알츠하이머병이 65세 이상에서 발병할 경우 희귀한 질병이 아니라 실제로 흔하며 1976년 사망 진단서에 거의 보고되지 않았음에도 불구하고 사망 원인 4위 또는 5위를 차지했다고 주장했습니다.
알츠하이머병의 발병률이 연령에 따라 증가했음에도 불구하고(75세의 5-10%에서 90세의 40-50%까지), 모든 사람들이 발병한 연령에 따른 한계점은 발견되지 않았다는 것이는 유용한 가지 유용한 발견입니다.이는 상당한 인지 장애를 경험하지 않은 수퍼센타 노인(110세 이상 거주하는 사람)이 보여줍니다.몇몇 증거들은 치매가 80세에서 84세 사이에 발병할 가능성이 가장 높고, 영향을 받지 않고 그 시점을 지난 사람들은 치매에 걸릴 가능성이 더 낮다는 것을 암시합니다.여성이 남성보다 치매 환자의 비율이 더 높지만, 이것은 그들의 전체 수명이 더 길고, 치매가 발생할 가능성이 높은 나이에 도달할 가능성이 더 높기 때문일 수 있습니다.[273]
노화와 관련된 다른 질병들과 마찬가지로, 치매는 20세기 이전에는 비교적 드물었는데, 이는 80세가 넘은 사람들이 거의 없었기 때문입니다.반대로, 매독성 치매는 2차 세계대전 이후 페니실린 사용으로 대부분 퇴치되기 전까지 선진국에서 널리 퍼져 있었습니다.그 후 기대수명이 크게 늘어나면서 65세 이상 인구가 빠르게 증가하기 시작했습니다.1945년 이전에는 노인이 인구의 평균 3-5%를 차지했지만, 2010년까지 많은 국가들이 10-14%에 달했고, 독일과 일본에서는 이 수치가 20%를 넘었습니다.1994년 로널드 레이건 전 미국 대통령이 알츠하이머 진단을 받았다고 발표하면서 알츠하이머에 대한 대중의 인식이 크게 높아졌습니다.
21세기에 다른 종류의 치매는 알츠하이머병과 혈관성 치매(가장 흔한 종류)와 구별되었습니다.이러한 구분은 뇌의 SPECT 및 PET 스캔과 같은 핵의학 영상 검사에서 뇌 조직의 병리학적 검사, 증상학적 검사 및 뇌 대사 활동의 다른 패턴에 기초합니다.다양한 형태는 예후가 다르고 역학적 위험 요인도 다릅니다.알츠하이머병을 포함한 많은 질병들의 주요 원인은 아직도 명확하지 않습니다.[274]
용어.
노인의 치매는 한때 노인성 치매 또는 노쇠라고 불렸고, 노화의 정상적이고 다소 불가피한 측면으로 여겨졌습니다.[275][276]
1913-20년까지 치매 프라에콕스라는 용어는 더 어린 나이에 노인성 치매의 발병을 암시하기 위해 도입되었습니다.결국 두 용어가 융합되어 1952년까지 의사들은 치매 프리옥스(조숙성 치매)와 조현병이라는 용어를 혼용하여 사용했습니다.그 이후로, 과학은 치매와 조현병이 서로 다른 두 가지 질병이라는 것을 밝혀냈습니다.[277]정신 질환에 대한 조숙성 치매라는 용어는 조현병과 같은 정신 질환의 유형(파라노아증 및 인지 능력 저하 포함)이 더 나이가 많은 모든 사람에게 정상적으로 도착할 것으로 예상할 수 있음을 시사했습니다(파라노아증 참조).약 1920년 이후, 치매를 현재 조현병과 노인성 치매로 사용하기 시작한 것은 그 단어의 의미를 "영구적이고 돌이킬 수 없는 정신적 악화"로 제한하는 데 도움이 되었습니다.이것이 그 용어의 나중 사용으로의 변경을 시작했습니다.최근 연구에서 연구자들은 조현병 진단을 받은 사람들과 치매 진단을 받은 환자들 사이의 연관성을 보고 두 질병 사이의 긍정적인 상관관계를 발견했습니다.[278]
치매는 항상 특정 질병 과정의 결과일 수밖에 없다는 견해는 65세 이상에서 '알츠하이머형 노인성 치매'(SDAT) 진단을 제안하는 데까지 한동안 이어졌고, 65세 미만에서 '알츠하이머병' 진단은 같은 병리를 가진 65세 미만에서 이뤄졌습니다.하지만 결국 나이 제한은 인위적인 것이고, 알츠하이머병은 나이에 상관없이 그 특정한 뇌병리를 가진 사람들에게 적합한 용어라는 것에 동의했습니다.
1952년 이후, 조현병을 포함한 정신 질환은 유기 뇌 증후군의 범주에서 제외되었고, 따라서 (정의상) "치매"의 가능한 원인으로부터 제거되었습니다.그러나 동시에 노인성 치매의 전통적인 원인인 "동맥 경화"는 이제 혈관 원인(작은 뇌졸중)의 치매 세트로 돌아왔습니다.이것들은 이제 다중-유아성 치매 또는 혈관성 치매라고 불렸습니다.
사회와 문화

치매로 인한 사회적 비용은 특히 간병인들에게 높습니다.[279]영국에 기반을 둔 한 연구에 따르면 치매 환자의 보호자 3명 중 거의 2명이 외로움을 느낀다고 합니다.연구에 참여한 대부분의 보호자들은 가족이나 친구들이었습니다.[280][281]
2015년[update] 기준, 미국의 알츠하이머 환자 1인당 연간 비용은 약 19,144.36달러였습니다.국가의 총 비용은 약 1,677억 4천만 달러로 추정됩니다.2030년까지 연간 사회경제적 비용은 약 5,070억 달러에 이를 것으로 예상되며, 2050년에는 1조 8,900억 달러에 이를 것으로 예상됩니다.이러한 꾸준한 증가는 미국 내에서 뿐만 아니라 전 세계적으로 나타날 것입니다.치매 비용에 대한 세계적인 추정치는 2015년에 9,575억 6천만 달러였지만 2050년까지 추정되는 세계적인 비용은 9조 1,200억 달러입니다.[282]
많은 국가들은 치매에 걸린 사람들의 돌봄을 국가 우선순위로 간주하고 보건 및 사회 서비스 종사자, 무급 간병인, 친척 및 더 넓은 지역사회의 구성원들에게 더 잘 알리기 위해 자원과 교육에 투자합니다.몇몇 국가들은 국가 계획이나 전략을 작성했습니다.[283][284]이러한 계획들은 적절한 지원과 진단에 대한 적시의 접근이 가능한 한, 사람들이 치매와 함께 수년간 합리적으로 살 수 있다는 것을 인식하고 있습니다.데이비드 캐머런 전 영국 총리는 치매를 "국가적 위기"라고 표현하며 영국 내 80만 명에게 영향을 끼쳤습니다.[285]사실, 치매는 영국 여성들의 주요 사망원인이 되었습니다.[286]
모든 정신 질환과 마찬가지로 치매에 걸린 사람은 자신이나 다른 사람에게 잠재적인 위험이 될 수 있으므로 1983년 정신 건강법에 따라 구금하여 평가, 관리 및 치료를 받을 수 있습니다.이것은 최후의 수단이며, 가족이 있는 사람이나 치료를 확실히 할 수 있는 친구들은 보통 피합니다.
영국의 일부 병원들은 풍부하고 친절한 진료를 제공하기 위해 일하고 있습니다.병원 병동을 더 차분하고 거주자들에게 덜 부담을 주기 위해 직원들은 보통의 간호사 사무실을 접수처와 비슷한 작은 책상들로 대체했습니다.밝은 조명의 접목은 긍정적인 분위기를 증대시키고 거주자들이 보다 쉽게 볼 수 있도록 도와줍니다.[287]
치매 운전은 부상이나 사망으로 이어질 수 있습니다.의사들은 운전을 언제 그만두어야 하는지에 대한 적절한 검사를 조언해야 합니다.[288]영국 DVLA(Driver & Vehicle Licensing Agency)는 특히 단기 기억력이 떨어지거나 방향감각이 떨어지거나 통찰력이나 판단력이 부족한 치매 환자는 운전할 수 없으며, 이러한 경우 DVLA에 알려야 운전면허가 취소될 수 있습니다.이들은 중증도가 낮은 경우와 조기 진단을 받은 경우 운전자가 계속 운전할 수 있도록 허용될 수 있다는 점을 인정하고 있습니다.
치매 환자와 그 가족 및 간병인은 많은 지원 네트워크를 이용할 수 있습니다.자선 단체들은 치매에 걸린 사람들의 권리에 대한 인식을 높이고 캠페인을 하는 것을 목표로 합니다.치매환자의 증언능력 평가에 대한 지원과 지침이 제공됩니다.[289]
2015년, 애틀랜틱 자선단체는 치매를 이해하고 줄이는 것을 목표로 1억 7천 7백만 달러의 선물을 발표했습니다.수상자는 캘리포니아 대학교 샌프란시스코와 트리니티 칼리지 더블린이 공동으로 주도한 프로그램인 글로벌 뇌 건강 연구소였습니다.이 기부금은 애틀랜틱이 지금까지 낸 비자본적 기부금 중 가장 큰 금액이며 아일랜드 역사상 가장 큰 자선 기부금입니다.[290]
2020년 10월, 관리인의 마지막 음원인 'Everywhere at End Time'은 치매의 단계를 묘사하여 틱톡 사용자들에게 인기를 끌었습니다.[291]간병인들은 이 현상에 찬성했습니다; 이 기록을 만든 레이랜드 커비는 젊은 대중들 사이에 공감을 불러일으킬 수 있다고 설명하면서, 이 감정을 반복했습니다.[292]
2020년 11월 2일, 스코틀랜드의 억만장자 톰 헌터 경은 전 치매 음악 교사 폴 하비가 피아노로 작곡한 곡 중 하나를 바이럴 비디오에서 연주하는 것을 본 후 치매 자선 단체에 100만 파운드를 기부했습니다.기부금은 알츠하이머 학회와 치매 음악회가 나누어 낸다고 발표되었습니다.[293]
메모들
- ^ 2020년 현재 루이체를 포함한 섬망발성 치매의 전구 아형이 제안되어 있습니다.[11]
- ^ Kosaka(2017)는 다음과 같이 썼습니다. "루이 몸을 가진 치매(DLB)는 이제 알츠하이머병(AD)에 이어 두 번째로 빈번한 치매로 잘 알려져 있습니다. 모든 유형의 치매 중 AD가 약 50%, DLB가 약 20%, 혈관성 치매(VD)가 약 15%를 차지하는 것으로 알려져 있습니다.따라서 AD, DLB, VD는 현재 3대 치매로 간주되고 있습니다."[58]NINDS(2020)는 루이 체성 치매가 "알츠하이머병과 혈관질환 다음으로 치매의 가장 흔한 원인 중 하나"라고 말합니다.[59]허쉬(2019)는 "DLB는 알츠하이머병과 파킨슨병 다음으로 세 번째로 흔한 신경퇴행성 질환"[60]이라고 말합니다.
참고문헌
- ^ "Dementia". medlineplus.gov. Retrieved 20 January 2022.
- ^ a b c d e f g h i j k l m n "Dementia". www.who.int. Retrieved 26 September 2022.
- ^ "Dementia". mayoclinic.org. Mayo Clinic. Retrieved June 5, 2022.
- ^ a b Creavin ST, Wisniewski S, Noel-Storr AH, et al. (January 2016). "Mini-Mental State Examination (MMSE) for the detection of dementia in clinically unevaluated people aged 65 and over in community and primary care populations" (PDF). The Cochrane Database of Systematic Reviews. 2016 (1): CD011145. doi:10.1002/14651858.CD011145.pub2. hdl:1983/00876aeb-2061-43f5-b7e1-938c666030ab. PMC 8812342. PMID 26760674.
- ^ "Differential diagnosis dementia". NICE. Retrieved 20 January 2022.
- ^ Hales RE (2008). The American Psychiatric Publishing Textbook of Psychiatry. American Psychiatric Pub. p. 311. ISBN 978-1-58562-257-3. Archived from the original on 2017-09-08.
- ^ a b c d Livingston G, Huntley J, Sommerlad A, et al. (August 2020). "Dementia prevention, intervention, and care: 2020 report of the Lancet Commission". Lancet. 396 (10248): 413–446. doi:10.1016/S0140-6736(20)30367-6. PMC 7392084. PMID 32738937.
- ^ a b c Commission de la transparence (June 2012). "Drugs for Alzheimer's disease: best avoided. No therapeutic advantage" [Drugs for Alzheimer's disease: best avoided. No therapeutic advantage]. Prescrire International. 21 (128): 150. PMID 22822592.
- ^ a b Nichols E, Szoeke CE, Vollset SE, Abbasi N, Abd-Allah F, Abdela J, et al. (GBD 2016 Dementia Collaborators) (January 2019). "Global, regional, and national burden of Alzheimer's disease and other dementias, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016". The Lancet. Neurology. 18 (1): 88–106. doi:10.1016/S1474-4422(18)30403-4. PMC 6291454. PMID 30497964.
- ^ a b c d e Bathini P, Brai E, Auber LA (November 2019). "Olfactory dysfunction in the pathophysiological continuum of dementia" (PDF). Ageing Research Reviews. 55: 100956. doi:10.1016/j.arr.2019.100956. PMID 31479764. S2CID 201742825.
- ^ McKeith IG, Ferman TJ, Thomas AJ, et al. (April 2020). "Research criteria for the diagnosis of prodromal dementia with Lewy bodies". Neurology (Review). 94 (17): 743–755. doi:10.1212/WNL.0000000000009323. PMC 7274845. PMID 32241955.
- ^ a b c d e f g h i j k l m n o p Budson A, Solomon P (2011). Memory loss : a practical guide for clinicians. [Edinburgh?]: Elsevier Saunders. ISBN 978-1-4160-3597-8.
- ^ "ICD-11 for Mortality and Morbidity Statistics". icd.who.int. Retrieved 20 January 2022.
- ^ a b c d "What is mixed dementia". Dementia UK. Retrieved 2020-12-13.
- ^ a b Wilson H, Pagano G, Politis M (March 2019). "Dementia spectrum disorders: lessons learnt from decades with PET research". J Neural Transm (Vienna). 126 (3): 233–251. doi:10.1007/s00702-019-01975-4. PMC 6449308. PMID 30762136.
- ^ American Psychiatric Association (2013). Diagnostic and statistical manual of mental disorders : DSM-5 (5th ed.). Washington, DC: American Psychiatric Association. pp. 591–603. ISBN 978-0-89042-554-1.
- ^ "The Dementias: Hope Through Research National Institute of Neurological Disorders and Stroke". www.ninds.nih.gov. Retrieved 9 December 2022.
- ^ a b Lin JS, O'Connor E, Rossom RC, Perdue LA, Eckstrom E (November 2013). "Screening for cognitive impairment in older adults: A systematic review for the U.S. Preventive Services Task Force". Annals of Internal Medicine. 159 (9): 601–612. doi:10.7326/0003-4819-159-9-201311050-00730. PMID 24145578.
- ^ Orgeta V, Leung P, Del-Pino-Casado R, Qazi A, Orrell M, Spector AE, Methley AM (April 2022). "Psychological treatments for depression and anxiety in dementia and mild cognitive impairment". The Cochrane Database of Systematic Reviews. 2022 (4): CD009125. doi:10.1002/14651858.CD009125.pub3. PMC 9035877. PMID 35466396.
- ^ Radue R, Walaszek A, Asthana S (2019). "Chapter 24 – Neuropsychiatric symptoms in dementia". Handbook of Clinical Neurology. Vol. 167. pp. 437–454. doi:10.1016/B978-0-12-804766-8.00024-8. ISBN 978-0128047668. PMID 31753148. S2CID 208230186.
- ^ Kales HC, Gitlin LN, Lyketsos CG (March 2015). "Assessment and management of behavioral and psychological symptoms of dementia". BMJ. 350: h369. doi:10.1136/bmj.h369. PMC 4707529. PMID 25731881.
- ^ a b Şahin Cankurtaran E (December 2014). "Management of Behavioral and Psychological Symptoms of Dementia". Noro Psikiyatri Arsivi. 51 (4): 303–312. doi:10.5152/npa.2014.7405. PMC 5353163. PMID 28360647.
- ^ "Inhibition in Cognition". www.apa.org. Retrieved 7 February 2021.
- ^ "Hallucinations: MedlinePlus Medical Encyclopedia". medlineplus.gov. Retrieved 9 December 2022.
- ^ Shub D, Kunik ME (April 16, 2009). "Psychiatric Comorbidity in Persons With Dementia: Assessment and Treatment Strategies". Psychiatric Times. 26 (4). Archived from the original on April 27, 2009.
- ^ "Dementia – Signs and Symptoms". American Speech Language D Association.
- ^ "Dementia: comorbidities in patients – data briefing". GOV.UK. Retrieved 22 November 2020.
- ^ "Continence, dementia, and care that preserves dignity". NIHR Evidence. 21 June 2022. doi:10.3310/nihrevidence_51255. S2CID 251785991.
- ^ Grant RL, Drennan VM, Rait G, Petersen I, Iliffe S (August 2013). Prince MJ (ed.). "First diagnosis and management of incontinence in older people with and without dementia in primary care: a cohort study using The Health Improvement Network primary care database". PLOS Medicine. 10 (8): e1001505. doi:10.1371/journal.pmed.1001505. PMC 3754889. PMID 24015113.
- ^ "What Is Dementia? CDC". www.cdc.gov. 2019-12-19. Retrieved 2022-10-03.
- ^ a b Sheehan B (November 2012). "Assessment scales in dementia". Ther Adv Neurol Disord. 5 (6): 349–358. doi:10.1177/1756285612455733. PMC 3487532. PMID 23139705.
- ^ "Seven Stages of Dementia Symptoms, Progression & Durations". Retrieved 19 December 2020.
- ^ "Clinical Stages of Alzheimer's". Fisher Center for Alzheimer's Research Foundation. 29 January 2014. Retrieved 19 December 2020.
- ^ "Preclinical, Prodromal, and Dementia Stages of Alzheimer's Disease". Practical Neurology. Retrieved 2022-06-28.
- ^ Bhatia-Dey N, Heinbockel T (June 2021). "The Olfactory System as Marker of Neurodegeneration in Aging, Neurological and Neuropsychiatric Disorders". Int J Environ Res Public Health. 18 (13): 6976. doi:10.3390/ijerph18136976. PMC 8297221. PMID 34209997.
- ^ Boesveldt S, Parma V (January 2021). "The importance of the olfactory system in human well-being, through nutrition and social behavior". Cell Tissue Res. 383 (1): 559–567. doi:10.1007/s00441-020-03367-7. PMC 7802608. PMID 33433688.
- ^ Sherman C, Liu CS, Herrmann N, Lanctôt KL (February 2018). "Prevalence, neurobiology, and treatments for apathy in prodromal dementia". Int Psychogeriatr. 30 (2): 177–184. doi:10.1017/S1041610217000527. PMID 28416030. S2CID 46788701.
- ^ a b Breton A, Casey D, Arnaoutoglou NA (February 2019). "Cognitive tests for the detection of mild cognitive impairment (MCI), the prodromal stage of dementia: Meta-analysis of diagnostic accuracy studies". International Journal of Geriatric Psychiatry. 34 (2): 233–242. doi:10.1002/gps.5016. PMID 30370616. S2CID 53097138.
- ^ a b Bateman DR, Gill S, Hu S, Foster ED, Ruthirakuhan MT, Sellek AF, Mortby ME, Matušková V, Ng KP, Tarawneh RM, Freund-Levi Y, Kumar S, Gauthier S, Rosenberg PB, Ferreira de Oliveira F, Devanand DP, Ballard C, Ismail Z (2020). "Agitation and impulsivity in mid and late life as possible risk markers for incident dementia". Alzheimer's & Dementia: Translational Research & Clinical Interventions. 6 (1): e12016. doi:10.1002/trc2.12016. PMC 7507499. PMID 32995467.
- ^ Cervenka I, Agudelo LZ, Ruas JL (July 2017). "Kynurenines: Tryptophan's metabolites in exercise, inflammation, and mental health". Science. 357 (6349): eaaf9794. doi:10.1126/science.aaf9794. PMID 28751584.
- ^ Solvang SH, Nordrehaug JE, Aarsland D, et al. (2019). "Kynurenines, Neuropsychiatric Symptoms, and Cognitive Prognosis in Patients with Mild Dementia". Int J Tryptophan Res. 12: 1178646919877883. doi:10.1177/1178646919877883. PMC 6769202. PMID 31632053.
- ^ Atri A (March 2019). "The Alzheimer's Disease Clinical Spectrum: Diagnosis and Management". Med Clin North Am. 103 (2): 263–293. doi:10.1016/j.mcna.2018.10.009. PMID 30704681.
- ^ a b Hugo J, Ganguli M (August 2014). "Dementia and cognitive impairment: epidemiology, diagnosis, and treatment". Clinics in Geriatric Medicine. 30 (3): 421–442. doi:10.1016/j.cger.2014.04.001. PMC 4104432. PMID 25037289.
- ^ "Advance Directive for Dementia". Advance Directive for Dementia. Retrieved 2023-01-12.
- ^ American Psychiatric Association (2013). Diagnostic and statistical manual of mental disorders : DSM-5 (5th ed.). Washington, DC: American Psychiatric Association. pp. 591–603. ISBN 978-0-89042-554-1.
- ^ Jenkins C, Ginesi L, Keenan B (2016). Dementia care at a glance. Chichester, West Sussex. ISBN 978-1-118-85998-8. OCLC 905089525.
{{cite book}}: CS1 유지 관리: 위치 누락 게시자(링크) - ^ Rohrer JD, Knight WD, Warren JE, Fox NC, Rossor MN, Warren JD (January 2008). "Word-finding difficulty: a clinical analysis of the progressive aphasias". Brain. 131 (Pt 1): 8–38. doi:10.1093/brain/awm251. PMC 2373641. PMID 17947337.
- ^ Islam M, Mazumder M, Schwabe-Warf D, Stephan Y, Sutin AR, Terracciano A (February 2019). "Personality Changes With Dementia From the Informant Perspective: New Data and Meta-Analysis". Journal of the American Medical Directors Association. 20 (2): 131–137. doi:10.1016/j.jamda.2018.11.004. PMC 6432780. PMID 30630729.
- ^ "Diagnosing Lewy Body Dementia". National Institute on Aging. Retrieved 10 May 2020.
- ^ Wilson RS, Sytsma J, Barnes LL, Boyle PA (September 2016). "Anosognosia in Dementia". Current Neurology and Neuroscience Reports. 16 (9): 77. doi:10.1007/s11910-016-0684-z. PMID 27438597. S2CID 3331009.
- ^ Sunderaraman P, Cosentino S (March 2017). "Integrating the Constructs of Anosognosia and Metacognition: a Review of Recent Findings in Dementia". Current Neurology and Neuroscience Reports. 17 (3): 27. doi:10.1007/s11910-017-0734-1. PMC 5650061. PMID 28283961.
- ^ Payne M, Morley JE (1 May 2018). "Editorial: Dysphagia, Dementia and Frailty". The Journal of Nutrition, Health & Aging. 22 (5): 562–565. doi:10.1007/s12603-018-1033-5. PMID 29717753. S2CID 13753522.
- ^ Della Sala S, Spinnler H, Venneri A (February 2004). "Walking difficulties in patients with Alzheimer's disease might originate from gait apraxia" (PDF). Journal of Neurology, Neurosurgery, and Psychiatry. 75 (2): 196–201. PMC 1738895. PMID 14742586. Archived (PDF) from the original on 2022-10-09.
- ^ Mc Ardle R, Galna B, Donaghy P, Thomas A, Rochester L (October 2019). "Do Alzheimer's and Lewy body disease have discrete pathological signatures of gait?". Alzheimer's & Dementia. 15 (10): 1367–1377. doi:10.1016/j.jalz.2019.06.4953. PMID 31548122.
- ^ "Mental, physical and speech abilities in later stages of dementia". Alzheimer's Society. 29 June 2022. Retrieved 30 July 2022.
- ^ Mashour, George A.; Frank, Lori; Batthyany, Alexander; Kolanowski, Ann Marie; Nahm, Michael; Schulman-Green, Dena; Greyson, Bruce; Pakhomov, Serguei; Karlawish, Jason; Shah, Raj C. (2019-06-19). "Paradoxical lucidity: A potential paradigm shift for the neurobiology and treatment of severe dementias". Alzheimer's & Dementia. 15 (8): 1107–1114. doi:10.1016/j.jalz.2019.04.002. ISSN 1552-5260. PMID 31229433.
- ^ Chung CG, Lee H, Lee SB (September 2018). "Mechanisms of protein toxicity in neurodegenerative diseases". Cell Mol Life Sci. 75 (17): 3159–3180. doi:10.1007/s00018-018-2854-4. PMC 6063327. PMID 29947927.
- ^ Kosaka K, ed. (2017). Dementia with Lewy bodies: clinical and biological aspects (1st ed.). Springer: Japan. doi:10.1007/978-4-431-55948-1. ISBN 978-4-431-55948-1. S2CID 45950966.
- ^ "Lewy body dementia: Hope through research". National Institute of Neurological Disorders and Stroke. US National Institutes of Health. January 10, 2020. Retrieved March 18, 2020.
- ^ Hershey LA, Coleman-Jackson R (April 2019). "Pharmacological management of dementia with Lewy dodies". Drugs Aging (Review). 36 (4): 309–319. doi:10.1007/s40266-018-00636-7. PMC 6435621. PMID 30680679.
- ^ a b Arvanitakis Z, Shah RC, Bennett DA (October 2019). "Diagnosis and Management of Dementia: Review". JAMA. 322 (16): 1589–1599. doi:10.1001/jama.2019.4782. PMC 7462122. PMID 31638686.
- ^ Gauthier S (2006). Clinical diagnosis and management of Alzheimer's disease (3rd ed.). Abingdon, Oxon: Informa Healthcare. pp. 53–54. ISBN 978-0-203-93171-4. Archived from the original on 2016-05-03.
- ^ Abyadeh M, Gupta V, Chitranshi N, Gupta V, Wu Y, Saks D, et al. (April 2021). "Mitochondrial dysfunction in Alzheimer's disease – a proteomics perspective". Expert Review of Proteomics. 18 (4): 295–304. doi:10.1080/14789450.2021.1918550. PMID 33874826. S2CID 233310698.
- ^ Wenk GL (2003). "Neuropathologic changes in Alzheimer's disease". The Journal of Clinical Psychiatry. 64 (Suppl 9): 7–10. PMID 12934968.
- ^ https://pubmed.ncbi.nlm.nih.gov/21344011/
- ^ a b Iadecola C (November 2013). "The pathobiology of vascular dementia". Neuron. 80 (4): 844–66. doi:10.1016/j.neuron.2013.10.008. PMC 3842016. PMID 24267647.
- ^ Baskys A, Cheng JX (November 2012). "Pharmacological prevention and treatment of vascular dementia: approaches and perspectives". Exp Gerontol. 47 (11): 887–91. doi:10.1016/j.exger.2012.07.002. PMID 22796225. S2CID 1153876.
- ^ "Vascular dementia – Symptoms and causes". Mayo Clinic. Retrieved 2021-07-08.
- ^ McKeith IG, Ferman TJ, Thomas AJ, et al. (April 2020). "Research criteria for the diagnosis of prodromal dementia with Lewy bodies". Neurology. 94 (17): 743–755. doi:10.1212/WNL.0000000000009323. PMC 7274845. PMID 32241955.
- ^ Jurek L, Herrmann M, Bonze M, et al. (1 March 2018). "Behavioral and psychological symptoms in Lewy body disease: a review". Gériatrie et Psychologie Neuropsychiatrie du Vieillissement. 16 (1): 87–95. doi:10.1684/pnv.2018.0723. PMID 29569570.
- ^ a b c d McKeith IG, Boeve BF, Dickson DW, et al. (July 2017). "Diagnosis and management of dementia with Lewy bodies: Fourth consensus report of the DLB Consortium". Neurology (Review). 89 (1): 88–100. doi:10.1212/WNL.0000000000004058. PMC 5496518. PMID 28592453.
- ^ a b c Taylor JP, McKeith IG, Burn DJ, et al. (February 2020). "New evidence on the management of Lewy body dementia". Lancet Neurol (Review). 19 (2): 157–69. doi:10.1016/S1474-4422(19)30153-X. PMC 7017451. PMID 31519472. 여기서 구애 링크를 이용할 수 있습니다.
- ^ Gomperts SN (April 2016). "Lewy Body Dementias: Dementia With Lewy Bodies and Parkinson Disease Dementia". Continuum (Minneap Minn) (Review). 22 (2 Dementia): 435–63. doi:10.1212/CON.0000000000000309. PMC 5390937. PMID 27042903.
- ^ Finger EC (April 2016). "Frontotemporal Dementias". Continuum. 22 (2 Dementia): 464–489. doi:10.1212/CON.0000000000000300. PMC 5390934. PMID 27042904.
- ^ "Progressive Supranuclear Palsy Fact Sheet National Institute of Neurological Disorders and Stroke". www.ninds.nih.gov. Retrieved 2021-01-20.
- ^ Lopez G, Bayulkem K, Hallett M (October 2016). "Progressive supranuclear palsy (PSP): Richardson syndrome and other PSP variants". Acta Neurol Scand. 134 (4): 242–9. doi:10.1111/ane.12546. PMC 7292631. PMID 27070344.
- ^ Frank S (January 2014). "Treatment of Huntington's disease". Neurotherapeutics. 11 (1): 153–60. doi:10.1007/s13311-013-0244-z. PMC 3899480. PMID 24366610.
- ^ "Huntington's disease – Symptoms". nhs.uk. 2018-02-16. Retrieved 2022-06-28.
- ^ a b "HIV-Associated Dementia – Neurologic Disorders". MSD Manual Professional Edition.
- ^ Gray F, Adle-Biassette H, Chretien F, Lorin de la Grandmaison G, Force G, Keohane C (2001). "Neuropathology and neurodegeneration in human immunodeficiency virus infection. Pathogenesis of HIV-induced lesions of the brain, correlations with HIV-associated disorders and modifications according to treatments". Clinical Neuropathology. 20 (4): 146–55. PMID 11495003.
- ^ Collinge J (July 2005). "Molecular neurology of prion disease". Journal of Neurology, Neurosurgery, and Psychiatry. 76 (7): 906–919. doi:10.1136/jnnp.2004.048660. PMC 1739714. PMID 15965195.
- ^ Ridley NJ, Draper B, Withall A (2013). "Alcohol-related dementia: an update of the evidence". Alzheimers Res Ther. 5 (1): 3. doi:10.1186/alzrt157. PMC 3580328. PMID 23347747.
- ^ a b c Nunes PT, Kipp BT, Reitz NL, Savage LM (2019). "Aging with alcohol-related brain damage: Critical brain circuits associated with cognitive dysfunction". Late Aging Associated Changes in Alcohol Sensitivity, Neurobehavioral Function, and Neuroinflammation. International Review of Neurobiology. Vol. 148. pp. 101–168. doi:10.1016/bs.irn.2019.09.002. ISBN 9780128175309. PMC 7372724. PMID 31733663.
- ^ "What is mixed dementia?". Alzheimer's Society. Retrieved 2020-12-13.
- ^ Schofield P (2005). "Dementia associated with toxic causes and autoimmune disease". International Psychogeriatrics (Review). 17 (Suppl 1): S129–47. doi:10.1017/s1041610205001997. hdl:1959.13/24647. PMID 16240488. S2CID 11864913.
- ^ a b Rosenbloom MH, Smith S, Akdal G, Geschwind MD (September 2009). "Immunologically mediated dementias". Current Neurology and Neuroscience Reports (Review). 9 (5): 359–67. doi:10.1007/s11910-009-0053-2. PMC 2832614. PMID 19664365.
- ^ a b c d Zis P, Hadjivassiliou M (26 February 2019). "Treatment of Neurological Manifestations of Gluten Sensitivity and Coeliac Disease". Curr Treat Options Neurol (Review). 21 (3): 10. doi:10.1007/s11940-019-0552-7. PMID 30806821.
- ^ a b c Makhlouf S, Messelmani M, Zaouali J, Mrissa R (2018). "Cognitive impairment in celiac disease and non-celiac gluten sensitivity: review of literature on the main cognitive impairments, the imaging and the effect of gluten free diet". Acta Neurol Belg (Review). 118 (1): 21–27. doi:10.1007/s13760-017-0870-z. PMID 29247390. S2CID 3943047.
- ^ Aarsland D, Kurz MW (February 2010). "The epidemiology of dementia associated with Parkinson disease". Journal of the Neurological Sciences (Review). 289 (1–2): 18–22. doi:10.1016/j.jns.2009.08.034. PMID 19733364. S2CID 24541533.
- ^ Galvin JE, Pollack J, Morris JC (November 2006). "Clinical phenotype of Parkinson disease dementia". Neurology. 67 (9): 1605–1611. doi:10.1212/01.wnl.0000242630.52203.8f. PMID 17101891. S2CID 25023606.
- ^ Abbasi J (September 2019). "Debate Sparks Over LATE, a Recently Recognized Dementia". JAMA. 322 (10): 914–916. doi:10.1001/jama.2019.12232. PMID 31433447. S2CID 201118832.
- ^ a b Martin S, Kelly S, Khan A, Cullum S, Dening T, Rait G, Fox C, Katona C, Cosco T, Brayne C, Lafortune L (June 2015). "Attitudes and preferences towards screening for dementia: a systematic review of the literature". BMC Geriatr. 15: 66. doi:10.1186/s12877-015-0064-6. PMC 4469007. PMID 26076729.
- ^ "Dementia definition". MDGuidelines. Reed Group. Archived from the original on 2009-06-29. Retrieved 2009-06-04.
- ^ Caplan JP, Rabinowitz T (November 2010). "An approach to the patient with cognitive impairment: delirium and dementia". The Medical Clinics of North America. 94 (6): 1103–1116, ix. doi:10.1016/j.mcna.2010.08.004. PMID 20951272.
- ^ Gleason OC (March 2003). "Delirium". American Family Physician. 67 (5): 1027–1034. PMID 12643363. Archived from the original on 2007-09-29.
- ^ Lai CK (2014). "The merits and problems of Neuropsychiatric Inventory as an assessment tool in people with dementia and other neurological disorders". Clinical Interventions in Aging. 9: 1051–1061. doi:10.2147/CIA.S63504. PMC 4099101. PMID 25031530.
- ^ Worrall L, Hickson LM (2003). "Implications for theory, practice, and policy". In Worrall LE, Hickson LM (eds.). Communication disability in aging: from prevention to intervention. Clifton Park, NY: Delmar Learning. pp. 297–298. ISBN 978-0-7693-0015-3.
- ^ James C, Ranson JM, Everson R, Llewellyn DJ (December 2021). "Performance of Machine Learning Algorithms for Predicting Progression to Dementia in Memory Clinic Patients". JAMA Network Open. 4 (12): e2136553. doi:10.1001/jamanetworkopen.2021.36553. PMC 8678688. PMID 34913981.
- ^ Boustani M, Peterson B, Hanson L, Harris R, Lohr KN (June 2003). "Screening for dementia in primary care: a summary of the evidence for the U.S. Preventive Services Task Force". Annals of Internal Medicine. 138 (11): 927–937. doi:10.7326/0003-4819-138-11-200306030-00015. PMID 12779304. S2CID 20779164.
- ^ a b Cullen B, O'Neill B, Evans JJ, Coen RF, Lawlor BA (August 2007). "A review of screening tests for cognitive impairment". Journal of Neurology, Neurosurgery, and Psychiatry. 78 (8): 790–799. doi:10.1136/jnnp.2006.095414. PMC 2117747. PMID 17178826.
- ^ Ranson JM, Kuźma E, Hamilton W, Muniz-Terrera G, Langa KM, Llewellyn DJ (April 2019). "Predictors of dementia misclassification when using brief cognitive assessments". Neurology. Clinical Practice. 9 (2): 109–117. doi:10.1212/CPJ.0000000000000566. PMC 6461420. PMID 31041124.
- ^ Contador, I. et al. (2017) "문해력과 다년간의 교육이 치매 진단에 미치는 영향:인구 기반 연구", Journal of Clinical and Experimental Neuropsychology, 39(2), pp. 112-119https://doi.org/10.1080/13803395.2016.1204992 에서 이용할 수 있습니다.
- ^ Sager MA, Hermann BP, La Rue A, Woodard JL (October 2006). "Screening for dementia in community-based memory clinics" (PDF). WMJ. 105 (7): 25–29. PMID 17163083. Archived from the original (PDF) on 2010-06-26.
- ^ Fleisher AS, Sowell BB, Taylor C, Gamst AC, Petersen RC, Thal LJ (May 2007). "Clinical predictors of progression to Alzheimer disease in amnestic mild cognitive impairment". Neurology. 68 (19): 1588–1595. doi:10.1212/01.wnl.0000258542.58725.4c. PMID 17287448. S2CID 9129604.
- ^ Karlawish JH, Clark CM (March 2003). "Diagnostic evaluation of elderly patients with mild memory problems". Annals of Internal Medicine. 138 (5): 411–419. doi:10.7326/0003-4819-138-5-200303040-00011. PMID 12614094. S2CID 43798118.
- ^ Teng EL, Chui HC (August 1987). "The Modified Mini-Mental State (3MS) examination". The Journal of Clinical Psychiatry. 48 (8): 314–318. PMID 3611032.
- ^ Teng EL, Hasegawa K, Homma A, Imai Y, Larson E, Graves A, et al. (1994). "The Cognitive Abilities Screening Instrument (CASI): a practical test for cross-cultural epidemiological studies of dementia". International Psychogeriatrics. 6 (1): 45–58, discussion 62. doi:10.1017/S1041610294001602. PMID 8054493. S2CID 25322040.
- ^ Tombaugh TN (March 2004). "Trail Making Test A and B: normative data stratified by age and education". Archives of Clinical Neuropsychology. 19 (2): 203–214. doi:10.1016/S0887-6177(03)00039-8. PMID 15010086.
- ^ Nasreddine ZS, Phillips NA, Bédirian V, Charbonneau S, Whitehead V, Collin I, Cummings JL, Chertkow H (April 2005). "The Montreal Cognitive Assessment, MoCA: a brief screening tool for mild cognitive impairment". Journal of the American Geriatrics Society. 53 (4): 695–699. doi:10.1111/j.1532-5415.2005.53221.x. PMID 15817019. S2CID 9014589.
- ^ Dawes, Piers; Reeves, David; Yeung, Wai Kent; Holland, Fiona; Charalambous, Anna Pavlina; Côté, Mathieu; David, Renaud; Helmer, Catherine; Laforce, Robert; Martins, Ralph N.; Politis, Antonis; Pye, Annie; Russell, Gregor; Sheikh, Saima; Sirois, Marie‐Josée (2023-05-01). "Development and validation of the Montreal cognitive assessment for people with hearing impairment ( MoCA‐H )". Journal of the American Geriatrics Society. 71 (5): 1485–1494. doi:10.1111/jgs.18241. ISSN 0002-8614. PMID 36722180. S2CID 256457783.
- ^ "How to identify dementia in people with hearing loss". NIHR Evidence. 2023-02-08. doi:10.3310/nihrevidence_59137. S2CID 260465275.
- ^ Hendry K, Green C, McShane R, Noel-Storr AH, Stott DJ, Anwer S, et al. (March 2019). "AD-8 for detection of dementia across a variety of healthcare settings". The Cochrane Database of Systematic Reviews. 3 (3): CD011121. doi:10.1002/14651858.CD011121.pub2. PMC 6398085. PMID 30828783.
- ^ Bee P. "The five-minute test that can tell if you're on the road to dementia". Retrieved 1 January 2022.
- ^ a b "FDA Clears 5-Minute Test for Early Dementia". Medscape. Retrieved 1 January 2022.
- ^ Jorm AF (September 2004). "The Informant Questionnaire on cognitive decline in the elderly (IQCODE): a review". International Psychogeriatrics. 16 (3): 275–293. doi:10.1017/S1041610204000390. PMID 15559753. S2CID 145256616.
- ^ Burton JK, Stott DJ, McShane R, Noel-Storr AH, Swann-Price RS, Quinn TJ (July 2021). "Informant Questionnaire on Cognitive Decline in the Elderly (IQCODE) for the early detection of dementia across a variety of healthcare settings". The Cochrane Database of Systematic Reviews. 2021 (7): CD011333. doi:10.1002/14651858.CD011333.pub3. PMC 8406787. PMID 34275145.
- ^ Jacova, Claudia; Kertesz, Andrew; Blair, Mervin; Fisk, John D.; Feldman, Howard H. (October 2007). "Neuropsychological testing and assessment for dementia". Alzheimer's & Dementia. 3 (4): 299–317. doi:10.1016/j.jalz.2007.07.011. ISSN 1552-5260. PMID 19595951. S2CID 40462470.
- ^ Boise L, Camicioli R, Morgan DL, Rose JH, Congleton L (August 1999). "Diagnosing dementia: perspectives of primary care physicians". The Gerontologist. 39 (4): 457–464. doi:10.1093/geront/39.4.457. PMID 10495584.
- ^ Espino DV, Jules-Bradley AC, Johnston CL, Mouton CP (March 1998). "Diagnostic approach to the confused elderly patient". American Family Physician. 57 (6): 1358–1366. PMID 9531917.
- ^ Bonte FJ, Harris TS, Hynan LS, Bigio EH, White CL (July 2006). "Tc-99m HMPAO SPECT in the differential diagnosis of the dementias with histopathologic confirmation". Clinical Nuclear Medicine. 31 (7): 376–378. doi:10.1097/01.rlu.0000222736.81365.63. PMID 16785801. S2CID 39518497.
- ^ Dougall NJ, Bruggink S, Ebmeier KP (2004). "Systematic review of the diagnostic accuracy of 99mTc-HMPAO-SPECT in dementia" (PDF). The American Journal of Geriatric Psychiatry. 12 (6): 554–570. doi:10.1176/appi.ajgp.12.6.554. PMID 15545324. S2CID 12375536. Archived from the original (PDF) on 2020-07-13.
- ^ Angelopoulou E, Paudel YN, Shaikh MF, Piperi C (March 2020). "Flotillin: A Promising Biomarker for Alzheimer's Disease". J Pers Med. 10 (2): 20. doi:10.3390/jpm10020020. PMC 7354424. PMID 32225073.
- ^ Huntley, Jonathan D.; Corbett, Anne; Wesnes, Keith; Hampshire, Adam; Ballard, Clive (2017). "[P3–563]: Risk Factors for Dementia and Cognitive Function in Healthy Adults". Alzheimer's & Dementia. 13 (7S_Part_24). doi:10.1016/j.jalz.2017.06.1783. S2CID 53255124.
- ^ Zhang YR, Xu W, Zhang W, et al. (October 2022). "Modifiable risk factors for incident dementia and cognitive impairment: An umbrella review of evidence". J Affect Disord. 314: 160–167. doi:10.1016/j.jad.2022.07.008. PMID 35863541.
- ^ "vascular risk factors and brain health" (PDF). Archived (PDF) from the original on 2022-10-09. Retrieved 1 January 2021.
- ^ Ding J, Davis-Plourde KL, Sedaghat S, Tully PJ, Wang W, Phillips C, et al. (January 2020). "Antihypertensive medications and risk for incident dementia and Alzheimer's disease: a meta-analysis of individual participant data from prospective cohort studies". The Lancet. Neurology. 19 (1): 61–70. doi:10.1016/S1474-4422(19)30393-X. PMC 7391421. PMID 31706889.
- ^ Lourida I, Hannon E, Littlejohns TJ, Langa KM, Hyppönen E, Kuzma E, Llewellyn DJ (July 2019). "Association of Lifestyle and Genetic Risk With Incidence of Dementia". JAMA. 322 (5): 430–437. doi:10.1001/jama.2019.9879. PMC 6628594. PMID 31302669.
- ^ Aschwanden D, Strickhouser JE, Luchetti M, Stephan Y, Sutin AR, Terracciano A (May 2021). "Is personality associated with dementia risk? A meta-analytic investigation". Ageing Research Reviews. 67: 101269. doi:10.1016/j.arr.2021.101269. PMC 8005464. PMID 33561581.
- ^ Sutin AR, Aschwanden D, Luchetti M, Stephan Y, Terracciano A (2021). "Sense of Purpose in Life Is Associated with Lower Risk of Incident Dementia: A Meta-Analysis". Journal of Alzheimer's Disease. 83 (1): 249–258. doi:10.3233/JAD-210364. PMC 8887819. PMID 34275900.
- ^ Luchetti M, Terracciano A, Aschwanden D, Lee JH, Stephan Y, Sutin AR (July 2020). "Loneliness is associated with risk of cognitive impairment in the Survey of Health, Ageing and Retirement in Europe". International Journal of Geriatric Psychiatry. 35 (7): 794–801. doi:10.1002/gps.5304. PMC 7755119. PMID 32250480.
- ^ "Loneliness, but not social isolation, predicts development of dementia in older people". NIHR Evidence (Plain English summary). 2020-05-27. doi:10.3310/alert_40330. S2CID 241649845.
- ^ Rafnsson SB, Orrell M, d'Orsi E, Hogervorst E, Steptoe A (January 2020). Carr D (ed.). "Loneliness, Social Integration, and Incident Dementia Over 6 Years: Prospective Findings From the English Longitudinal Study of Ageing". The Journals of Gerontology. Series B, Psychological Sciences and Social Sciences. 75 (1): 114–124. doi:10.1093/geronb/gbx087. PMC 6909434. PMID 28658937.
- ^ a b Cheng ST (September 2016). "Cognitive Reserve and the Prevention of Dementia: the Role of Physical and Cognitive Activities". Current Psychiatry Reports. 18 (9): 85. doi:10.1007/s11920-016-0721-2. PMC 4969323. PMID 27481112.
- ^ Dawes P (March 2019). "Hearing interventions to prevent dementia". HNO. 67 (3): 165–171. doi:10.1007/s00106-019-0617-7. PMC 6399173. PMID 30767054.
- ^ a b c d Panza F, Lozupone M, Sardone R, Battista P, Piccininni M, Dibello V, et al. (2019). "Sensorial frailty: age-related hearing loss and the risk of cognitive impairment and dementia in later life". Therapeutic Advances in Chronic Disease. 10: 2040622318811000. doi:10.1177/2040622318811000. PMC 6700845. PMID 31452865.
- ^ Thomson RS, Auduong P, Miller AT, Gurgel RK (April 2017). "Hearing loss as a risk factor for dementia: A systematic review". Laryngoscope Investigative Otolaryngology. 2 (2): 69–79. doi:10.1002/lio2.65. PMC 5527366. PMID 28894825.
- ^ Hubbard HI, Mamo SK, Hopper T (July 2018). "Dementia and Hearing Loss: Interrelationships and Treatment Considerations". Seminars in Speech and Language. 39 (3): 197–210. doi:10.1055/s-0038-1660779. PMID 29933487. S2CID 49383232.
- ^ Ford AH, Hankey GJ, Yeap BB, Golledge J, Flicker L, Almeida OP (June 2018). "Hearing loss and the risk of dementia in later life". Maturitas. 112: 1–11. doi:10.1016/j.maturitas.2018.03.004. PMID 29704910. S2CID 13998812.
- ^ Fink HA, Jutkowitz E, McCarten JR, Hemmy LS, Butler M, Davila H, et al. (January 2018). "Pharmacologic Interventions to Prevent Cognitive Decline, Mild Cognitive Impairment, and Clinical Alzheimer-Type Dementia: A Systematic Review". Annals of Internal Medicine. 168 (1): 39–51. doi:10.7326/M17-1529. PMID 29255847. S2CID 24193907.
- ^ Hughes D, Judge C, Murphy R, Loughlin E, Costello M, Whiteley W, et al. (May 2020). "Association of Blood Pressure Lowering With Incident Dementia or Cognitive Impairment: A Systematic Review and Meta-analysis". JAMA. 323 (19): 1934–1944. doi:10.1001/jama.2020.4249. PMC 7237983. PMID 32427305.
- ^ Arapakis K, Brunner E, French E, McCauley J (October 2021). "Dementia and disadvantage in the USA and England: population-based comparative study". BMJ Open. 11 (10): e045186. doi:10.1136/bmjopen-2020-045186. PMC 8496387. PMID 34615672.
- ^ Daly B, Thompsell A, Sharpling J, Rooney YM, Hillman L, Wanyonyi KL, White S, Gallagher JE (January 2018). "Evidence summary: the relationship between oral health and dementia" (PDF). British Dental Journal. 223 (11): 846–853. doi:10.1038/sj.bdj.2017.992. PMID 29192686. S2CID 19633523.
- ^ Miklossy J (2015). "Historic evidence to support a causal relationship between spirochetal infections and Alzheimer's disease". Frontiers in Aging Neuroscience. 7: 46. doi:10.3389/fnagi.2015.00046. PMC 4399390. PMID 25932012.
- ^ a b c Olsen I, Singhrao SK (2015-09-17). "Can oral infection be a risk factor for Alzheimer's disease?". Journal of Oral Microbiology. 7: 29143. doi:10.3402/jom.v7.29143. PMC 4575419. PMID 26385886.
- ^ "Can poor oral health lead to dementia?". British Dental Journal. 223 (11): 840. December 2017. doi:10.1038/sj.bdj.2017.1064. PMID 29243693. S2CID 25898592.
- ^ Carter CJ (February 2011). "Alzheimer's disease plaques and tangles: cemeteries of a pyrrhic victory of the immune defence network against herpes simplex infection at the expense of complement and inflammation-mediated neuronal destruction". Neurochemistry International. 58 (3): 301–320. doi:10.1016/j.neuint.2010.12.003. PMID 21167244. S2CID 715832.
- ^ 깁슨, GE, Hirsch, JA, Fonzetti, P, et al. (2016) 비타민 B1 (티아민) 및 치매Ann Y Acad Sci 1367, 21–30
- ^ Butterworth, RF (2003) 티아민 결핍과 뇌 장애Nutr Res Rev 16, 277–284.
- ^ 호프만, R. (2016)서구 식단의 티아민 결핍과 치매 위험.영국 영양학 저널, 116(1), 188–189.
- ^ a b Dominguez LJ, Barbagallo M (June 2018). "Nutritional prevention of cognitive decline and dementia". Acta Biomed. 89 (2): 276–290. doi:10.23750/abm.v89i2.7401. PMC 6179018. PMID 29957766.
- ^ Goodman B. "Diet Affects Markers of Alzheimer's Disease". WebMD. Retrieved 2020-12-13.
- ^ "Memory loss can be caused by a number of factors, from short term causes such as low blood sugar or medication side effects to long term health issues such as dementia". Diabetes. 2019-01-15. Retrieved 2020-12-13.
- ^ Cao L, Tan L, Wang HF, Jiang T, Zhu XC, Lu H, et al. (November 2016). "Dietary Patterns and Risk of Dementia: a Systematic Review and Meta-Analysis of Cohort Studies". Molecular Neurobiology. 53 (9): 6144–6154. doi:10.1007/s12035-015-9516-4. OCLC 6947867710. PMID 26553347. S2CID 8188716.
- ^ Canevelli M, Lucchini F, Quarata F, Bruno G, Cesari M (March 2016). "Nutrition and Dementia: Evidence for Preventive Approaches?". Nutrients. MDPI. 8 (3): 144. doi:10.3390/nu8030144. OCLC 8147564576. PMC 4808873. PMID 26959055.
- ^ Shannon OM, Ranson JM, Gregory S, Macpherson H, Milte C, Lentjes M, Mulligan A, McEvoy C, Griffiths A, Matu J, Hill TR, Adamson A, Siervo M, Minihane AM, Muniz-Tererra G, Ritchie C, Mathers JC, Llewellyn DJ, Stevenson E (March 2023). "Mediterranean diet adherence is associated with lower dementia risk, independent of genetic predisposition: findings from the UK Biobank prospective cohort study". BMC Med. 21 (1): 81. doi:10.1186/s12916-023-02772-3. PMC 10012551. PMID 36915130. S2CID 257499227.
- ^ Omar SH (June 2019). "Mediterranean and MIND Diets Containing Olive Biophenols Reduces the Prevalence of Alzheimer's Disease". Int J Mol Sci. 20 (11): 2797. doi:10.3390/ijms20112797. PMC 6600544. PMID 31181669.
- ^ Burckhardt M, Herke M, Wustmann T, Watzke S, Langer G, Fink A (April 2016). "Omega-3 fatty acids for the treatment of dementia". The Cochrane Database of Systematic Reviews. 2016 (4): CD009002. doi:10.1002/14651858.CD009002.pub3. PMC 7117565. PMID 27063583.
- ^ Firth J, Teasdale SB, Allott K, Siskind D, Marx W, Cotter J, Veronese N, Schuch F, Smith L, Solmi M, Carvalho AF, Vancampfort D, Berk M, Stubbs B, Sarris J (October 2019). "The efficacy and safety of nutrient supplements in the treatment of mental disorders: a meta-review of meta-analyses of randomized controlled trials". World Psychiatry. 18 (3): 308–324. doi:10.1002/wps.20672. PMC 6732706. PMID 31496103.
- ^ Hafdi M, Hoevenaar-Blom MP, Richard E (November 2021). "Multi-domain interventions for the prevention of dementia and cognitive decline". The Cochrane Database of Systematic Reviews. 2021 (11): CD013572. doi:10.1002/14651858.CD013572.pub2. PMC 8574768. PMID 34748207. S2CID 243846602.
- ^ Schneider LS, Mangialasche F, Andreasen N, Feldman H, Giacobini E, Jones R, et al. (March 2014). "Clinical trials and late-stage drug development for Alzheimer's disease: an appraisal from 1984 to 2014". Journal of Internal Medicine. 275 (3): 251–283. doi:10.1111/joim.12191. PMC 3956752. PMID 24605808.
- ^ Watt JA, Goodarzi Z, Veroniki AA, Nincic V, Khan PA, Ghassemi M, et al. (November 2019). "Comparative Efficacy of Interventions for Aggressive and Agitated Behaviors in Dementia: A Systematic Review and Network Meta-analysis". Annals of Internal Medicine. 171 (9): 633–642. doi:10.7326/M19-0993. PMID 31610547. S2CID 204699972.
- ^ Vandepitte S, Van Den Noortgate N, Putman K, Verhaeghe S, Verdonck C, Annemans L (December 2016). "Effectiveness of respite care in supporting informal caregivers of persons with dementia: a systematic review". International Journal of Geriatric Psychiatry. 31 (12): 1277–1288. doi:10.1002/gps.4504. PMID 27245986. S2CID 3464912.
- ^ a b c d Walsh SC, Murphy E, Devane D, Sampson EL, Connolly S, Carney P, O'Shea E (September 2021). "Palliative care interventions in advanced dementia". The Cochrane Database of Systematic Reviews. 2021 (9): CD011513. doi:10.1002/14651858.CD011513.pub3. PMC 8478014. PMID 34582034.
- ^ Forbes D, Forbes SC, Blake CM, Thiessen EJ, Forbes S (April 2015). "Exercise programs for people with dementia". The Cochrane Database of Systematic Reviews (Submitted manuscript). 132 (4): CD006489. doi:10.1002/14651858.CD006489.pub4. PMC 9426996. PMID 25874613.
- ^ Camp CJ (2010). "Origins of Montessori Programming for Dementia". Non-pharmacological Therapies in Dementia. 1 (2): 163–174. PMC 3600589. PMID 23515663.
- ^ Cheong CY, Tan JA, Foong YL, Koh HM, Chen DZ, Tan JJ, Ng CJ, Yap P (2016). "Creative Music Therapy in an Acute Care Setting for Older Patients with Delirium and Dementia". Dementia and Geriatric Cognitive Disorders Extra. 6 (2): 268–275. doi:10.1159/000445883. PMC 4959431. PMID 27489560.
- ^ Jeon YH, Li Z, Low LF, Chenoweth L, O'Connor D, Beattie E, Liu Z, Brodaty H (August 2015). "The clinical utility of the Cornell Scale for Depression in Dementia as a routine assessment in nursing homes". The American Journal of Geriatric Psychiatry. 23 (8): 784–793. doi:10.1016/j.jagp.2014.08.013. PMID 25256214.
- ^ Jeon YH, Liu Z, Li Z, et al. (November 2016). "Development and Validation of a Short Version of the Cornell Scale for Depression in Dementia for Screening Residents in Nursing Homes". The American Journal of Geriatric Psychiatry. 24 (11): 1007–1016. doi:10.1016/j.jagp.2016.05.012. PMID 27538349.
- ^ Harper AE, Rouch S, Leland NE, Turner RL, Mansbach WE, Day CE, Terhorst L (April 2022). "A Systematic Review of Tools Assessing the Perspective of Caregivers of Residents With Dementia". Journal of Applied Gerontology. 41 (4): 1196–1208. doi:10.1177/07334648211028692. PMID 34229505. S2CID 235758241.
- ^ "The WHELD programme for people with dementia helps care home staff deliver person-centred care". NIHR Evidence (Plain English summary). 2020-11-26. doi:10.3310/alert_42713. S2CID 240719455.
- ^ Ballard C, Orrell M, Moniz-Cook E, Woods R, Whitaker R, Corbett A, et al. (July 2020). "Improving mental health and reducing antipsychotic use in people with dementia in care homes: the WHELD research programme including two RCTs". Programme Grants for Applied Research. 8 (6): 1–98. doi:10.3310/pgfar08060. PMID 32721145. S2CID 225489651.
- ^ Woods B, O'Philbin L, Farrell EM, Spector AE, Orrell M (March 2018). "Reminiscence therapy for dementia". The Cochrane Database of Systematic Reviews. 2018 (3): CD001120. doi:10.1002/14651858.CD001120.pub3. PMC 6494367. PMID 29493789.
- ^ Vernooij-Dassen M, Draskovic I, McCleery J, Downs M (November 2011). "Cognitive reframing for carers of people with dementia". The Cochrane Database of Systematic Reviews (11): CD005318. arXiv:0706.4406. doi:10.1002/14651858.CD005318.pub2. hdl:2066/97731. PMID 22071821. S2CID 205178315.
- ^ Neal M, Barton Wright P (2003). "Validation therapy for dementia". The Cochrane Database of Systematic Reviews (3): CD001394. doi:10.1002/14651858.CD001394. PMID 12917907.
- ^ Woods B, Aguirre E, Spector AE, Orrell M (February 2012). "Cognitive stimulation to improve cognitive functioning in people with dementia". The Cochrane Database of Systematic Reviews. 2 (2): CD005562. doi:10.1002/14651858.CD005562.pub2. PMID 22336813. S2CID 7086782.
- ^ a b Möhler R, Renom A, Renom H, Meyer G (August 2020). "Personally tailored activities for improving psychosocial outcomes for people with dementia in community settings". The Cochrane Database of Systematic Reviews. 2020 (8): CD010515. doi:10.1002/14651858.CD010515.pub2. PMC 8094398. PMID 32786083.
- ^ Barker P (2003). Psychiatric and mental health nursing: the craft of caring. London: Arnold. ISBN 978-0-340-81026-2. OCLC 53373798.
- ^ Weitzel T, Robinson S, Barnes MR, et al. (2011). "The special needs of the hospitalized patient with dementia". Medsurg Nursing. 20 (1): 13–18, quiz 19. PMID 21446290.
- ^ Cunningham C (2006). "Understanding challenging behaviour in patients with dementia". Nursing Standard. 20 (47): 42–45. doi:10.7748/ns2006.08.20.47.42.c4477. PMID 16913375.
- ^ a b Dyer SM, Harrison SL, Laver K, Whitehead C, Crotty M (March 2018). "An overview of systematic reviews of pharmacological and non-pharmacological interventions for the treatment of behavioral and psychological symptoms of dementia". International Psychogeriatrics. 30 (3): 295–309. doi:10.1017/S1041610217002344. PMID 29143695.
- ^ van der Steen JT, Smaling HJ, van der Wouden JC, Bruinsma MS, Scholten RJ, Vink AC (July 2018). "Music-based therapeutic interventions for people with dementia". The Cochrane Database of Systematic Reviews. 2018 (7): CD003477. doi:10.1002/14651858.CD003477.pub4. hdl:1874/350441. PMC 6513122. PMID 30033623.
- ^ Osman SE, Tischler V, Schneider J (November 2016). "'Singing for the Brain': A qualitative study exploring the health and well-being benefits of singing for people with dementia and their carers". Dementia. 15 (6): 1326–1339. doi:10.1177/1471301214556291. PMC 5089222. PMID 25425445.
- ^ a b c Johnston B, Narayanasamy M (April 2016). "Exploring psychosocial interventions for people with dementia that enhance personhood and relate to legacy- an integrative review". BMC Geriatrics. 16: 77. doi:10.1186/s12877-016-0250-1. PMC 4820853. PMID 27044417.
- ^ "British hospitals are having a dementia-friendly makeover". The Economist. Retrieved 2018-09-19.
- ^ a b Raj SE, Mackintosh S, Fryer C, Stanley M (2021-01-01). "Home-Based Occupational Therapy for Adults With Dementia and Their Informal Caregivers: A Systematic Review". The American Journal of Occupational Therapy. 75 (1): 7501205060p1–7501205060p27. doi:10.5014/ajot.2020.040782. PMID 33399054. S2CID 230618534.
- ^ a b Frankenstein LL, Jahn G (2020-04-20). "Behavioral and Occupational Therapy for Dementia Patients and Caregivers". GeroPsych. 33 (2): 85–100. doi:10.1024/1662-9647/a000225. ISSN 1662-9647. S2CID 219081899.
- ^ Orgeta V, McDonald KR, Poliakoff E, Hindle JV, Clare L, Leroi I (February 2020). "Cognitive training interventions for dementia and mild cognitive impairment in Parkinson's disease". The Cochrane Database of Systematic Reviews. 2020 (2): CD011961. doi:10.1002/14651858.cd011961.pub2. PMC 7043362. PMID 32101639.
- ^ Möhler, Ralph; Calo, Stella; Renom, Anna; Renom, Helena; Meyer, Gabriele (2023-03-13). "Personally tailored activities for improving psychosocial outcomes for people with dementia in long-term care". The Cochrane Database of Systematic Reviews. 2023 (3): CD009812. doi:10.1002/14651858.CD009812.pub3. ISSN 1469-493X. PMC 10010156. PMID 36930048.
- ^ Rafii MS, Aisen PS (February 2009). "Recent developments in Alzheimer's disease therapeutics". BMC Medicine. 7: 7. doi:10.1186/1741-7015-7-7. PMC 2649159. PMID 19228370.
- ^ a b Lleó A, Greenberg SM, Growdon JH (2006). "Current pharmacotherapy for Alzheimer's disease". Annual Review of Medicine. 57 (1): 513–533. doi:10.1146/annurev.med.57.121304.131442. PMID 16409164.
- ^ a b Bond M, Rogers G, Peters J, Anderson R, Hoyle M, Miners A, et al. (2012). "The effectiveness and cost-effectiveness of donepezil, galantamine, rivastigmine and memantine for the treatment of Alzheimer's disease (review of Technology Appraisal No. 111): a systematic review and economic model". Health Technology Assessment. 16 (21): 1–470. doi:10.3310/hta16210. PMC 4780923. PMID 22541366.
- ^ Rodda J, Morgan S, Walker Z (October 2009). "Are cholinesterase inhibitors effective in the management of the behavioral and psychological symptoms of dementia in Alzheimer's disease? A systematic review of randomized, placebo-controlled trials of donepezil, rivastigmine and galantamine". International Psychogeriatrics. 21 (5): 813–824. doi:10.1017/S1041610209990354. PMID 19538824. S2CID 206299435.
- ^ Birks J (January 2006). Birks JS (ed.). "Cholinesterase inhibitors for Alzheimer's disease". The Cochrane Database of Systematic Reviews. 2016 (1): CD005593. doi:10.1002/14651858.CD005593. PMC 9006343. PMID 16437532.
- ^ Gill SS, Anderson GM, Fischer HD, Bell CM, Li P, Normand SL, Rochon PA (May 2009). "Syncope and its consequences in patients with dementia receiving cholinesterase inhibitors: a population-based cohort study". Archives of Internal Medicine. 169 (9): 867–873. doi:10.1001/archinternmed.2009.43. PMID 19433698.
- ^ Wang K, Alan J, Page AT, Dimopoulos E, Etherton-Beer C (September 2021). "Anticholinergics and clinical outcomes amongst people with pre-existing dementia: A systematic review". Maturitas. Elsevier BV. 151: 1–14. doi:10.1016/j.maturitas.2021.06.004. PMID 34446273.
- ^ AMDA – The Society for Post-Acute and Long-Term Care Medicine (February 2014), "Ten Things Physicians and Patients Should Question", Choosing Wisely: an initiative of the ABIM Foundation, AMDA – The Society for Post-Acute and Long-Term Care Medicine, archived from the original on 12 April 2015, retrieved 20 April 2015
- ^ Walker Z, Possin KL, Boeve BF, Aarsland D (October 2015). "Lewy body dementias". Lancet (Review). 386 (10004): 1683–1697. doi:10.1016/S0140-6736(15)00462-6. PMC 5792067. PMID 26595642.
- ^ Boot BP (2015). "Comprehensive treatment of dementia with Lewy bodies". Alzheimers Res Ther (Review). 7 (1): 45. doi:10.1186/s13195-015-0128-z. PMC 4448151. PMID 26029267.
- ^ Gomperts SN (April 2016). "Lewy body dementias: Dementia with Lewy bodies and Parkinson disease dementia". Continuum (Minneap Minn) (Review). 22 (2 Dementia): 435–463. doi:10.1212/CON.0000000000000309. PMC 5390937. PMID 27042903.
- ^ a b c d e f g American Geriatrics Society. "Five Things Physicians and Patients Should Question". Choosing Wisely: An Initiative of the ABIM Foundation. Archived from the original on September 1, 2013. Retrieved August 1, 2013.
- ^ American Psychiatric Association (September 2013), "Five Things Physicians and Patients Should Question", Choosing Wisely: an initiative of the ABIM Foundation, American Psychiatric Association, archived from the original on 3 December 2013, retrieved 30 December 2013
- ^ "Dementia: assessment, management and support for people living with dementia and their carers Guidance and guidelines NICE". NICE. 20 June 2018. Retrieved 18 December 2018.
- ^ Dyer SM, Laver K, Pond CD, Cumming RG, Whitehead C, Crotty M (December 2016). "Clinical practice guidelines and principles of care for people with dementia in Australia". Australian Family Physician. 45 (12): 884–889. PMID 27903038.
- ^ Declercq T, Petrovic M, Azermai M, Vander Stichele R, De Sutter AI, van Driel ML, Christiaens T (March 2013). "Withdrawal versus continuation of chronic antipsychotic drugs for behavioural and psychological symptoms in older people with dementia" (PDF). The Cochrane Database of Systematic Reviews. 3 (3): CD007726. doi:10.1002/14651858.CD007726.pub2. hdl:1854/LU-3109108. PMID 23543555.
- ^ Raina P, Santaguida P, Ismaila A, Patterson C, Cowan D, Levine M, et al. (March 2008). "Effectiveness of cholinesterase inhibitors and memantine for treating dementia: evidence review for a clinical practice guideline". Annals of Internal Medicine. 148 (5): 379–397. doi:10.7326/0003-4819-148-5-200803040-00009. PMID 18316756.
- ^ Atri A, Shaughnessy LW, Locascio JJ, Growdon JH (2008). "Long-term course and effectiveness of combination therapy in Alzheimer disease". Alzheimer Disease and Associated Disorders. 22 (3): 209–221. doi:10.1097/WAD.0b013e31816653bc. PMC 2718545. PMID 18580597.
- ^ a b c d Kandiah N, Ong PA, Yuda T, Ng LL, Mamun K, Merchant RA, et al. (February 2019). "Treatment of dementia and mild cognitive impairment with or without cerebrovascular disease: Expert consensus on the use of Ginkgo biloba extract, EGb 761®". CNS Neuroscience & Therapeutics. 25 (2): 288–298. doi:10.1111/cns.13095. PMC 6488894. PMID 30648358.
- ^ McKeage K, Lyseng-Williamson KA (2018). "Ginkgo biloba extract EGb 761® in the symptomatic treatment of mild-to-moderate dementia: a profile of its use". Drugs & Therapy Perspectives. 34 (8): 358–366. doi:10.1007/s40267-018-0537-8. PMC 6267544. PMID 30546253.
- ^ Wang M, Peng H, Peng Z, Huang K, Li T, Li L, et al. (September 2020). "Efficacy and safety of ginkgo preparation in patients with vascular dementia: A protocol for systematic review and meta-analysis". Medicine. 99 (37): e22209. doi:10.1097/MD.0000000000022209. PMC 7489658. PMID 32925798.
- ^ Jones HE, Joshi A, Shenkin S, Mead GE (July 2016). "The effect of treatment with selective serotonin reuptake inhibitors in comparison to placebo in the progression of dementia: a systematic review and meta-analysis". Age and Ageing. 45 (4): 448–456. doi:10.1093/ageing/afw053. PMID 27055878.
- ^ Dudas R, Malouf R, McCleery J, Dening T, et al. (Cochrane Dementia and Cognitive Improvement Group) (August 2018). "Antidepressants for treating depression in dementia". The Cochrane Database of Systematic Reviews. 2018 (8): CD003944. doi:10.1002/14651858.CD003944.pub2. PMC 6513376. PMID 30168578.
- ^ Seitz DP, Adunuri N, Gill SS, Gruneir A, Herrmann N, Rochon P (February 2011). "Antidepressants for agitation and psychosis in dementia". The Cochrane Database of Systematic Reviews (2): CD008191. doi:10.1002/14651858.CD008191.pub2. PMID 21328305.
- ^ Malouf R, Grimley Evans J (October 2008). "Folic acid with or without vitamin B12 for the prevention and treatment of healthy elderly and demented people". The Cochrane Database of Systematic Reviews (4): CD004514. doi:10.1002/14651858.CD004514.pub2. PMID 18843658.
- ^ McGuinness B, Craig D, Bullock R, Malouf R, Passmore P (July 2014). "Statins for the treatment of dementia" (PDF). The Cochrane Database of Systematic Reviews. 7 (7): CD007514. doi:10.1002/14651858.CD007514.pub3. PMID 25004278. Archived from the original (PDF) on 2019-09-03. Retrieved 2019-09-03.
- ^ Jongstra S, Harrison JK, Quinn TJ, Richard E (November 2016). "Antihypertensive withdrawal for the prevention of cognitive decline". The Cochrane Database of Systematic Reviews. 2016 (11): CD011971. doi:10.1002/14651858.CD011971.pub2. PMC 6465000. PMID 27802359.
- ^ Page AT, Potter K, Clifford R, McLachlan AJ, Etherton-Beer C (October 2016). "Medication appropriateness tool for co-morbid health conditions in dementia: consensus recommendations from a multidisciplinary expert panel". Internal Medicine Journal. 46 (10): 1189–1197. doi:10.1111/imj.13215. PMC 5129475. PMID 27527376.
- ^ Wang K, Alan J, Page A, Percival M, Etherton-Beer C (2018). "Medication use to manage comorbidities for people with dementia: a systematic review". Journal of Pharmacy Practice and Research. 48 (4): 356–367. doi:10.1002/jppr.1403. ISSN 2055-2335.
- ^ a b Wilfling, Denise; Calo, Stella; Dichter, Martin N.; Meyer, Gabriele; Möhler, Ralph; Köpke, Sascha (2023-01-03). "Non-pharmacological interventions for sleep disturbances in people with dementia". The Cochrane Database of Systematic Reviews. 1 (1): CD011881. doi:10.1002/14651858.CD011881.pub2. ISSN 1469-493X. PMC 9808594. PMID 36594432.
- ^ a b c d McCleery J, Sharpley AL (November 2020). "Pharmacotherapies for sleep disturbances in dementia". The Cochrane Database of Systematic Reviews. 2020 (11): CD009178. doi:10.1002/14651858.CD009178.pub4. PMC 8094738. PMID 33189083.
- ^ American Geriatrics Society 2012 Beers Criteria Update Expert Panel (April 2012). "American Geriatrics Society updated Beers Criteria for potentially inappropriate medication use in older adults". Journal of the American Geriatrics Society. 60 (4): 616–631. doi:10.1111/j.1532-5415.2012.03923.x. PMC 3571677. PMID 22376048.
- ^ Tisher A, Salardini A (April 2019). "A Comprehensive Update on Treatment of Dementia". Semin Neurol. 39 (2): 167–178. doi:10.1055/s-0039-1683408. PMID 30925610. S2CID 88474685.
- ^ Lolk A, Gulmann NC (October 2006). "[Psychopharmacological treatment of behavioral and psychological symptoms in dementia]". Ugeskrift for Laeger (in Danish). 168 (40): 3429–3432. PMID 17032610.
- ^ a b c d e Hadjistavropoulos T, Herr K, Turk DC, Fine PG, Dworkin RH, Helme R, Jackson K, Parmelee PA, Rudy TE, Lynn Beattie B, Chibnall JT, Craig KD, Ferrell B, Ferrell B, Fillingim RB, Gagliese L, Gallagher R, Gibson SJ, Harrison EL, Katz B, Keefe FJ, Lieber SJ, Lussier D, Schmader KE, Tait RC, Weiner DK, Williams J (January 2007). "An interdisciplinary expert consensus statement on assessment of pain in older persons". The Clinical Journal of Pain. 23 (1 Suppl): S1–43. doi:10.1097/AJP.0b013e31802be869. PMID 17179836. S2CID 43777445.
- ^ a b Shega J, Emanuel L, Vargish L, Levine SK, Bursch H, Herr K, Karp JF, Weiner DK (May 2007). "Pain in persons with dementia: complex, common, and challenging". The Journal of Pain. 8 (5): 373–378. doi:10.1016/j.jpain.2007.03.003. PMID 17485039.
- ^ Blyth FM, Cumming R, Mitchell P, Wang JJ (July 2007). "Pain and falls in older people". European Journal of Pain. 11 (5): 564–571. doi:10.1016/j.ejpain.2006.08.001. PMID 17015026. S2CID 27460864.
- ^ Brown C (2009). "Pain, aging and dementia: The crisis is looming, but are we ready?". British Journal of Occupational Therapy. 72 (8): 371–375. doi:10.1177/030802260907200808. S2CID 73245194.
- ^ Herr K, Bjoro K, Decker S (February 2006). "Tools for assessment of pain in nonverbal older adults with dementia: a state-of-the-science review". Journal of Pain and Symptom Management. 31 (2): 170–192. doi:10.1016/j.jpainsymman.2005.07.001. PMID 16488350.
- ^ Stolee P, Hillier LM, Esbaugh J, Bol N, McKellar L, Gauthier N (February 2005). "Instruments for the assessment of pain in older persons with cognitive impairment". Journal of the American Geriatrics Society. 53 (2): 319–326. doi:10.1111/j.1532-5415.2005.53121.x. PMID 15673359. S2CID 21006144.
- ^ AMDA – The Society for Post-Acute and Long-Term Care Medicine (February 2014), "Five Things Physicians and Patients Should Question", Choosing Wisely: an initiative of the ABIM Foundation, AMDA – The Society for Post-Acute and Long-Term Care Medicine, archived from the original on 13 September 2014, retrieved 10 February 2013
- ^ AMDA – The Society for Post-Acute and Long-Term Care Medicine (February 2014), "Five Things Physicians and Patients Should Question", Choosing Wisely: an initiative of the ABIM Foundation, AMDA – The Society for Post-Acute and Long-Term Care Medicine, archived from the original on 13 September 2014, retrieved 10 February 2013AMDA – The Society for Post-Acute and Long-Term Care Medicine (February 2014), "Five Things Physicians and Patients Should Question", Choosing Wisely: an initiative of the ABIM Foundation, AMDA – The Society for Post-Acute and Long-Term Care Medicine, archived from the original on 13 September 2014, retrieved 10 February 2013다음을 언급합니다.
- Teno JM, Gozalo PL, Mitchell SL, Kuo S, Rhodes RL, Bynum JP, Mor V (October 2012). "Does feeding tube insertion and its timing improve survival?". Journal of the American Geriatrics Society. 60 (10): 1918–1921. doi:10.1111/j.1532-5415.2012.04148.x. PMC 3470758. PMID 23002947.
- Palecek EJ, Teno JM, Casarett DJ, Hanson LC, Rhodes RL, Mitchell SL (March 2010). "Comfort feeding only: a proposal to bring clarity to decision-making regarding difficulty with eating for persons with advanced dementia". Journal of the American Geriatrics Society. 58 (3): 580–584. doi:10.1111/j.1532-5415.2010.02740.x. PMC 2872797. PMID 20398123.
- Gillick MR, Volandes AE (June 2008). "The standard of caring: why do we still use feeding tubes in patients with advanced dementia?". Journal of the American Medical Directors Association. 9 (5): 364–367. doi:10.1016/j.jamda.2008.03.011. PMID 18519120.
- ^ Mitchell SL, Kiely DK, Lipsitz LA (February 1997). "The risk factors and impact on survival of feeding tube placement in nursing home residents with severe cognitive impairment". Archives of Internal Medicine. 157 (3): 327–332. doi:10.1001/archinte.1997.00440240091014. PMID 9040301.
- ^ Sampson EL, Candy B, Jones L (April 2009). "Enteral tube feeding for older people with advanced dementia". The Cochrane Database of Systematic Reviews. 2009 (2): CD007209. doi:10.1002/14651858.CD007209.pub2. PMC 7182132. PMID 19370678.
- ^ Lockett MA, Templeton ML, Byrne TK, Norcross ED (February 2002). "Percutaneous endoscopic gastrostomy complications in a tertiary-care center". The American Surgeon. 68 (2): 117–120. doi:10.1177/000313480206800202. PMID 11842953. S2CID 43796062.
- ^ Finocchiaro C, Galletti R, Rovera G, Ferrari A, Todros L, Vuolo A, Balzola F (June 1997). "Percutaneous endoscopic gastrostomy: a long-term follow-up". Nutrition. 13 (6): 520–523. doi:10.1016/S0899-9007(97)00030-0. PMID 9263232.
- ^ Mitchell SL, Mor V, Gozalo PL, Servadio JL, Teno JM (August 2016). "Tube Feeding in US Nursing Home Residents With Advanced Dementia, 2000–2014" (PDF). JAMA. 316 (7): 769–770. doi:10.1001/jama.2016.9374. PMC 4991625. PMID 27533163. Archived (PDF) from the original on 2017-09-21.
- ^ Span P (29 August 2016). "The Decline of Tube Feeding for Dementia Patients". The New York Times. Archived from the original on 3 September 2016. Retrieved 31 August 2016.
- ^ a b Flynn E, Smith CH, Walsh CD, Walshe M (September 2018). "Modifying the consistency of food and fluids for swallowing difficulties in dementia". The Cochrane Database of Systematic Reviews. 2018 (9): CD011077. doi:10.1002/14651858.cd011077.pub2. PMC 6513397. PMID 30251253.
- ^ Forbes D, Forbes SC, Blake CM, Thiessen EJ, Forbes S (April 2015). "Exercise programs for people with dementia". The Cochrane Database of Systematic Reviews. 2015 (4): CD006489. doi:10.1002/14651858.CD006489.pub4. PMC 9426996. PMID 25874613.
- ^ Smith M, Robinson L, Segal J. "Preventing Alzheimer's Disease – HelpGuide.org". HelpGuide.org. Retrieved 2020-12-13.
- ^ Van der Roest HG, Wenborn J, Pastink C, Dröes RM, Orrell M (June 2017). "Assistive technology for memory support in dementia". The Cochrane Database of Systematic Reviews. 2017 (6): CD009627. doi:10.1002/14651858.cd009627.pub2. PMC 6481376. PMID 28602027.
- ^ "7 Technological Innovations for Those With Dementia". Alzheimers.net. Retrieved 2022-06-28.
- ^ Viggo Hansen N, Jørgensen T, Ørtenblad L (October 2006). "Massage and touch for dementia". The Cochrane Database of Systematic Reviews. 2006 (4): CD004989. doi:10.1002/14651858.CD004989.pub2. PMC 6823223. PMID 17054228.
- ^ Ball EL, Owen-Booth B, Gray A, Shenkin SD, Hewitt J, McCleery J (August 2020). "Aromatherapy for dementia". The Cochrane Database of Systematic Reviews. 2020 (8): CD003150. doi:10.1002/14651858.CD003150.pub3. PMC 7437395. PMID 32813272.
- ^ Bosnjak Kuharic D, Markovic D, Brkovic T, Jeric Kegalj M, Rubic Z, Vuica Vukasovic A, et al. (September 2021). "Cannabinoids for the treatment of dementia". The Cochrane Database of Systematic Reviews. 2021 (9): CD012820. doi:10.1002/14651858.CD012820.pub2. PMC 8446835. PMID 34532852.
- ^ Sampson EL, Ritchie CW, Lai R, Raven PW, Blanchard MR (March 2005). "A systematic review of the scientific evidence for the efficacy of a palliative care approach in advanced dementia" (PDF). International Psychogeriatrics. 17 (1): 31–40. doi:10.1017/S1041610205001018. PMID 15945590. S2CID 7861568. Archived from the original (PDF) on 2019-02-24.
- ^ Van den Block L (October 2014). "The need for integrating palliative care in ageing and dementia policies". European Journal of Public Health. 24 (5): 705–706. doi:10.1093/eurpub/cku084. PMID 24997202.
- ^ van der Steen JT, Radbruch L, Hertogh CM, de Boer ME, Hughes JC, Larkin P, et al. (March 2014). "White paper defining optimal palliative care in older people with dementia: a Delphi study and recommendations from the European Association for Palliative Care". Palliative Medicine. 28 (3): 197–209. doi:10.1177/0269216313493685. PMID 23828874.
- ^ Birch D, Draper J (May 2008). "A critical literature review exploring the challenges of delivering effective palliative care to older people with dementia" (PDF). Journal of Clinical Nursing. 17 (9): 1144–1163. doi:10.1111/j.1365-2702.2007.02220.x. PMID 18416791.
- ^ Mitchell G, Agnelli J (October 2015). "Person-centred care for people with dementia: Kitwood reconsidered". Nursing Standard. 30 (7): 46–50. doi:10.7748/ns.30.7.46.s47. PMID 26463810.
- ^ a b González-Fraile E, Ballesteros J, Rueda JR, Santos-Zorrozúa B, Solà I, McCleery J (January 2021). "Remotely delivered information, training and support for informal caregivers of people with dementia". The Cochrane Database of Systematic Reviews. 1 (1): CD006440. doi:10.1002/14651858.cd006440.pub3. PMC 8094510. PMID 33417236.
- ^ Dooley B, Ueno H (2022-02-02). "Where a Thousand Digital Eyes Keep Watch Over the Elderly". The New York Times. ISSN 0362-4331. Retrieved 2022-02-06.
- ^ Nichols E, Steinmetz JD, Vollset SE, Fukutaki K, Chalek J, Abd-Allah F, et al. (GBD 2019 Dementia Forecasting Collaborators) (February 2022). "Estimation of the global prevalence of dementia in 2019 and forecasted prevalence in 2050: an analysis for the Global Burden of Disease Study 2019". The Lancet. Public Health. 7 (2): e105–e125. doi:10.1016/S2468-2667(21)00249-8. PMC 8810394. PMID 34998485.
- ^ Gale SA, Acar D, Daffner KR (October 2018). "Dementia". Am J Med. 131 (10): 1161–1169. doi:10.1016/j.amjmed.2018.01.022. PMID 29425707. S2CID 240122313.
- ^ a b c d Alzheimer's Disease International (Sep 2015). "World Alzheimer Report 2015" (PDF). Archived (PDF) from the original on 2022-10-09. Retrieved 30 October 2018.
- ^ Prince M, Jackson J (2009). "World Alzheimer Report 2009". Alzheimer's Disease International: 38. Archived from the original on 11 March 2012. Retrieved 11 March 2012.
- ^ Wang H, Naghavi M, Allen C, Barber RM, Bhutta ZA, Carter A, et al. (GBD 2015 Mortality and Causes of Death Collaborators) (October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980–2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1459–1544. doi:10.1016/s0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
- ^ Brijnath, Bianca; Croy, Samantha; Sabates, Julieta; Thodis, Antonia; Ellis, Stephanie; de Crespigny, Fleur; Moxey, Annette; Day, Robert; Dobson, Annette; Elliott, Cerise; Etherington, Cathy; Geronimo, Mary Ann; Hlis, Danijela; Lampit, Amit; Low, Lee-Fay (2022). "Including ethnic minorities in dementia research: Recommendations from a scoping review". Alzheimer's & Dementia. 8 (1): e12222. doi:10.1002/trc2.12222. ISSN 2352-8737. PMC 9053375. PMID 35505899.
- ^ Sabayan, Behnam; Wyman-Chick, Kathryn A.; Sedaghat, Sanaz (February 2023). "The Burden of Dementia Spectrum Disorders and Associated Comorbid and Demographic Features". Clinics in Geriatric Medicine. 39 (1): 1–14. doi:10.1016/j.cger.2022.07.001. ISSN 1879-8853. PMID 36404023. S2CID 253068389.
- ^ a b Sadock BJ, Sadock VA (2008). "Delirium, Dementia, and Amnestic and Other Cobnitive Disorders and Mental Disorders Due to a General Medical Condition". Kaplan & Sadock's concise textbook of clinical psychiatry (3rd ed.). Philadelphia: Wolters Kluwer/Lippincott Williams & Wilkins. p. 52. ISBN 978-0-7817-8746-8.
- ^ "What causes young-onset dementia? Alzheimer's Society". www.alzheimers.org.uk. Retrieved 2022-06-28.
- ^ "What causes young-onset dementia? Alzheimer's Society". www.alzheimers.org.uk. Retrieved 10 January 2022.
- ^ Vieira RT, Caixeta L, Machado S, Silva AC, Nardi AE, Arias-Carrión O, Carta MG (2013-06-14). "Epidemiology of early-onset dementia: a review of the literature". Clinical Practice and Epidemiology in Mental Health. 9: 88–95. doi:10.2174/1745017901309010088. PMC 3715758. PMID 23878613.
- ^ a b Masters CL, Bateman R, Blennow K, Rowe CC, Sperling RA, Cummings JL (October 2015). "Alzheimer's disease". Nature Reviews. Disease Primers. 1: 15056. doi:10.1038/nrdp.2015.56. PMID 27188934. S2CID 20844163.
- ^ Jessop T, Peisah C (July 2021). "Human Rights and Empowerment in Aged Care: Restraint, Consent and Dying with Dignity". International Journal of Environmental Research and Public Health. 18 (15): 7899. doi:10.3390/ijerph18157899. PMC 8345762. PMID 34360196.
- ^ Berrios GE (November 1987). "Dementia during the seventeenth and eighteenth centuries: a conceptual history". Psychological Medicine. 17 (4): 829–837. doi:10.1017/S0033291700000623. PMID 3324141. S2CID 8262492.
- ^ Berchtold NC, Cotman CW (1998). "Evolution in the conceptu-alization of dementia and Alzheimer's disease: Greco-Roman period to the 1960s". Neurobiol Aging. 19 (3): 173–189. doi:10.1016/s0197-4580(98)00052-9. PMID 9661992. S2CID 24808582.
- ^ Bergener M, Reisberg B (1989). Diagnosis and treatment of senile dementia. Berlin: Springer-Verlag. ISBN 0-387-50800-7. OCLC 19455117.
- ^ Xihua J (1989). Diagnosis and Treatment of Senile Dementia: Research Methods and Perspective. Madhav Books (P) Limited, a unit of Serials Publications. p. 38. ISBN 9380615345.
- ^ a b c 질카, N. & Novak, M. (2006)알로이스 알츠하이머의 뒤엉킨 이야기.브라티슬라프스케 레카르스켈리, 107(9–10), 343–345.
- ^ a b c d e f g h Yang HD, Kim DH, Lee SB, Young LD (December 2016). "History of Alzheimer's Disease". Dementia and Neurocognitive Disorders. 15 (4): 115–121. doi:10.12779/dnd.2016.15.4.115. PMC 6428020. PMID 30906352.
- ^ Kolata G (June 17, 2010). "Drug Trials Test Bold Plan to Slow Alzheimer's". The New York Times. Archived from the original on April 9, 2012. Retrieved June 17, 2010.
- ^ Katzman R (April 1976). "Editorial: The prevalence and malignancy of Alzheimer disease. A major killer". Archives of Neurology. 33 (4): 217–218. doi:10.1001/archneur.1976.00500040001001. PMID 1259639.
- ^ "Prevalence by gender in the UK". Dementia Statistics Hub. Retrieved 2021-10-04.
- ^ "Alzheimer's disease – Symptoms and causes". Mayo Clinic. Retrieved 2021-10-01.
- ^ "What is dementia?". Alzheimer's Association. Retrieved 6 August 2018.
Dementia is often incorrectly referred to as "senility" or "senile dementia," which reflects the formerly widespread but incorrect belief that serious mental decline is a normal part of aging.
- ^ Taylor DC. "Dementia". MedicineNet. Retrieved 6 August 2018.
Senile dementia ("senility") is a term that was once used to describe all dementias; this term is no longer used as a diagnosis.
- ^ "Healthfully". Healthfully. Retrieved 2020-12-13.
- ^ "The Relationship Between Schizophrenia and Dementia". Psychology Today. Retrieved 2020-12-13.
- ^ Brodaty H, Donkin M (29 April 2017). "Family caregivers of people with dementia". Dialogues in Clinical Neuroscience. 11 (2): 217–228. doi:10.31887/DCNS.2009.11.2/hbrodaty. PMC 3181916. PMID 19585957.
- ^ "Most people caring for relatives with dementia experience loneliness". NIHR Evidence (Plain English summary). 2020-07-22. doi:10.3310/alert_40575. S2CID 243269845.
- ^ Victor CR, Rippon I, Quinn C, Nelis SM, Martyr A, Hart N, et al. (July 2021). "The prevalence and predictors of loneliness in caregivers of people with dementia: findings from the IDEAL programme". Aging & Mental Health. 25 (7): 1232–1238. doi:10.1080/13607863.2020.1753014. PMID 32306759. S2CID 216028843.
- ^ Jia J, Wei C, Chen S, Li F, Tang Y, Qin W, et al. (April 2018). "The cost of Alzheimer's disease in China and re-estimation of costs worldwide". Alzheimer's & Dementia. 14 (4): 483–491. doi:10.1016/j.jalz.2017.12.006. PMID 29433981. S2CID 46762069.
- ^ "National Alzheimer and Dementia Plans Planned Policies and Activities (PDF)" (PDF). London: Alzheimer's Disease International. April 2012. Archived from the original (PDF) on 2012-05-18. Retrieved 2012-12-03.
- ^ "Addressing Alzheimer's and Other Types of Dementia:Israeli National Strategy Summary Document of the Interdisciplinary, Inter-Organizational Group of Experts » Brookdale". Brookdale. Retrieved 2018-06-04.
- ^ Boseley S (26 March 2012). "Dementia research funding to more than double to £66m by 2015". The Guardian. London. ISSN 0261-3077. OCLC 60623878. Archived from the original on 20 October 2013. Retrieved 27 April 2012.
- ^ O'Dowd A (July 2017). "Dementia is now leading cause of death in women in England". BMJ. 358: j3445. doi:10.1136/bmj.j3445. PMID 28710087. S2CID 29011449. ProQuest 1919058612.
- ^ "British hospitals are having a dementia-friendly makeover". The Economist. Retrieved 2018-09-17.
- ^ "Drivers with dementia a growing problem, MDs warn". CBC News, Canada. September 19, 2007. Archived from the original on October 2, 2007.
- ^ Thompson SB (2009). "Testamentary capacity and cognitive rehabilitation: implications for head-injured and neurologically impaired individuals". Journal of Cognitive Rehabilitation. 27: 11–13. 다음에도 게시됨:
- ^ "Tackling dementia". Philanthropy magazine. Winter 2016. Archived from the original on 2016-02-11.
- ^ Garvey M (22 October 2020). "What Happens When TikTok Looks To The Avant-Garde For A Challenge?". NPR. Archived from the original on 22 October 2020. Retrieved 6 April 2021.
- ^ Ezra M (23 October 2020). "Why Are TikTok Teens Listening to an Album About Dementia?". The New York Times. Archived from the original on 23 October 2020. Retrieved 21 April 2021.
- ^ "Paul Harvey: Composer with dementia inspires £1m donation". BBC News. 2 November 2020. Retrieved 2 November 2020.
외부 링크
- 컬리의 치매
- "Result List: PM 32016328: EBSCOhost". web.s.ebscohost.com. Retrieved 2022-10-03.
- 알츠하이머 협회
- 국립노화연구소 – 알츠하이머병


