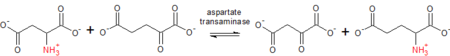트랜스페라아제
Transferase트랜스페라아제는 특정 기능기(예:[2] 메틸기 또는 글리코실기)가 한 분자(공여체라고 함)에서 다른 분자(수용체라고 함)로 전달되는 것을 촉매하는 효소 중 하나이다.그것들은 생물학을 통해 수백 가지의 다른 생화학적 경로에 관여하며, 생명의 가장 중요한 과정 중 일부에 필수적입니다.
트랜스페라아제는 세포 내에서 무수한 반응에 관여한다.이러한 반응의 세 가지 예는 티올에스테르를 [3]전달하는 조효소 A(CoA) 전달효소 활성, 트립토판을 [4]대사하는 경로의 일부인 N-아세틸 전달효소 작용, 피루브산을 아세틸 CoA로 [5]변환하는 피루브산 탈수소효소(PDH) 조절이다.트랜스페라아제는 번역 시에도 사용됩니다.여기서 아미노산사슬은 펩티딜전달효소에 의해 전달되는 관능기이다.전달은 리보솜의 A 부위의 tRNA 분자에서 성장 아미노산 사슬의 제거와 P [6]부위의 tRNA에 부착된 아미노산에 대한 후속 추가를 포함한다.
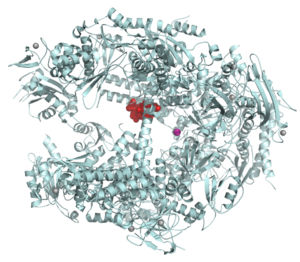
기계적으로, 다음과 같은 반응을 촉매하는 효소는 트랜스페라아제이다.
상기 반응에서는 X가 기증자이고 Y가 [7]수용체이다."그룹"은 전달효소 활성의 결과로 전달되는 기능군이 될 것이다.기증자는 종종 보효소이다.
역사
트랜스페라아제와 관련된 가장 중요한 발견들 중 일부는 1930년대 초에 일어났다.트랜스페라아제 활성의 최초 발견은 베타-갈락토시드가수분해효소, 단백질분해효소, 산/염기 포스파타아제를 포함한 다른 효소 분류에서 일어났다.개별 효소가 그러한 작업을 수행할 수 있다는 것을 깨닫기 전에는, 두 개 이상의 효소가 기능성 기 이동을 [8]수행한다고 믿었다.
아미노산(또는 "트랜스아미나아제"라고도 함)에 의한 아미노산에서 케토산으로의 아민(또는2 NH) 그룹의 전달은 도로시 M에 의해 1930년에 처음 발견되었다. 니덤, 비둘기 가슴 [9]근육에 첨가된 글루탐산이 사라지는 것을 관찰한 후.이 관찰은 나중에 1937년 [10]브라운스타인과 크리츠만이 그것의 반응 메커니즘을 발견함으로써 증명되었다.그들의 분석은 이 가역 반응이 다른 [11]조직에도 적용될 수 있다는 것을 보여주었다.이 주장은 1937년 [12][13]추적기로서 방사성 동위원소를 사용한 루돌프 쇤하이머의 연구에 의해 입증되었다.이것은 차례로 유사한 전달이 아미노산 [14]전달을 통해 대부분의 아미노산을 생산하는 주요 수단이라는 가능성을 열어줄 것이다.
초기 전달효소 연구와 이후 재분류의 또 다른 예는 우리딜 전달효소의 발견을 포함했다.1953년 UDP-포도당 피로인산가수분해효소는 UDP-포도당 및 유기 피로인산으로부터 UTP와 G1P를 가역적으로 생성할 수 있는 것으로 확인되었을 때 전달효소인 [15]것으로 나타났다.
트랜스페라아제와 관련된 역사적 중요성의 또 다른 예는 카테콜-O-메틸 트랜스페라아제에 의한 카테콜아민 분해 메커니즘의 발견이다.이 발견은 Julius Axelrod가 1970년 노벨 생리의학상을 수상한 이유의 큰 부분을 차지했습니다.[16]
전달효소의 분류는 오늘날까지 계속되고 있으며,[17][18] 새로운 것이 자주 발견됩니다.그 예로는 Drosophila의 [19]등측 복부 패턴화에 관여하는 술포전달효소인 Pipe가 있다.처음에 파이프의 정확한 메커니즘은 기판에 [20]대한 정보가 부족하여 알려지지 않았습니다.파이프의 촉매 활성에 대한 연구는 헤파란 [21]황산 글리코사미노글리칸일 가능성을 제거했습니다.추가 연구에 따르면 Pipe는 황화를 [22]위해 난소 구조를 대상으로 한다.현재 파이프는 드로소필라 헤파란 황산염 2-O-술포전달효소이다.[23]
명명법
전달효소의 계통명은 "공여체:수용체 그루프 전달효소"[24]의 형태로 구성됩니다.예를 들어 메틸아민은 다음과 같습니다.L-글루탐산 N-메틸전달효소는 트랜스페라아제 메틸아민-글루탐산 N-메틸전달효소의 표준 명명 규칙이 될 수 있으며, 여기서 메틸아민은 공여체, L-글루탐산염은 수용체, 메틸전달효소는 EC 범주 그룹이다.전달 효소에 의한 이와 같은 작용은 다음과 같이 설명할 수 있습니다.
- 메틸아민+L-글루탐산δ(\ NH3+N-메틸-L-글루탐산[25]
그러나 다른 수용된 이름은 전달 효소에 더 자주 사용되며, 종종 "수용체 그루프 전달 효소" 또는 "도너 그루프 전달 효소"로 형성됩니다.예를 들어 DNA메틸전달효소는 DNA수용체로의 메틸기 전달을 촉매하는 전달효소이다.실제로, 많은 분자가 일반적인 [26]이름 때문에 이 용어를 사용하지 않는다.예를 들어, RNA 중합효소는 이전에 RNA 뉴클레오티딜 전이효소로 알려진 것의 현대적 통칭이다. 이것은 성장하는 RNA 가닥의 3' [27]끝에 뉴클레오티드를 전달하는 뉴클레오티딜 전이효소의 일종이다.EC 분류 체계에서 RNA 중합효소의 수용명은 DNA 지향 RNA 중합효소이다.[28]
분류
전달 효소는 주로 전달되는 생화학 그룹의 유형에 따라 10가지 범주로 나눌 수 있습니다(EC 번호 분류 [29]기준).이러한 범주는 450개 이상의 고유한 [30]효소로 구성됩니다.EC 번호 체계에서 전달 효소는 EC2로 분류되어 있습니다.수소는 전달효소 표적에 관한 한 관능기로 간주되지 않으며, 대신 전자 전달 고려사항으로 인해 [30]산화환원효소 아래에 수소 전달이 포함된다.
| EC 번호 | 예 | 전송된 그룹 |
|---|---|---|
| EC 2.1 | 메틸전달효소 및 포르밀전달효소 | 단탄소군 |
| EC 2.2 | 트랜스케톨라아제 및 트랜스알돌라아제 | 알데히드 또는 케톤기 |
| EC 2.3 | 아실전달효소 | 이동 중에 알킬기가 되는 아실기 또는 그룹 |
| EC 2.4 | 글리코실전달효소, 헥소실전달효소 및 펜토실전달효소 | 글리코실기 및 헥소스와 펜토오스 |
| EC 2.5 | 리보플라빈합성효소 및 클로로필합성효소 | 메틸기 이외의 알킬기 또는 아릴기 |
| EC 2.6 | 트랜스아미나아제 및 옥시미노전달효소 | 질소족 |
| EC 2.7 | 포스포전달효소, 중합효소 및 키나아제 | 인을 포함한 그룹; 아종은 수용체(예를 들어 알코올, 카르복실 등)에 기초한다. |
| EC 2.8 | 황전달효소 및 술포전달효소 | 유황 함유기 |
| EC 2.9 | 셀레노전달효소 | 셀레늄 함유기 |
| EC 2.10 | 몰리브덴전달효소 및 텅스텐전달효소 | 몰리브덴 또는 텅스텐 |
역할.
EC 2.1: 단일 탄소전달효소
EC 2.1은 단일 탄소기를 전달하는 효소를 포함한다.이 범주는 메틸기,[31] 히드록시메틸기, 포밀기, 카르복시기, 카르바모일기 및 아미도기의 전달로 구성됩니다.예를 들어, 카바모일 전달효소는 한 분자에서 다른 [32]분자로 카바모일기를 전달한다.카르바모일기는 NHCO [33]공식에2 따른다.ATCase에서 이러한 전달은 카르바모일 인산염 + L-아스파르트산 L-carbamoyl 아스파르트산 +[34] 인산염으로 표기된다.
EC 2.2: 알데히드 및 케톤전달효소
알데히드 또는 케톤기를 전달하고 EC 2.2에 포함된 효소.이 범주는 다양한 트랜스케톨라아제 [35]및 트랜스알돌라아제들로 구성됩니다.알데히드전달효소의 이름인 트랜스알돌라아제는 펜토오스 인산 [36]경로의 중요한 부분이다.디히드록시아세톤이 글리세린알데히드 3-인산(G3P라고도 함)으로 작용한다.반응은 세도헵툴로오스 7-인산 + 글리세린알데히드 3-인산 { \ 에리트로스 4-인산 +[37] 과당 6-인산이다
EC 2.3: 아실전달효소
전달 과정에서 알킬기가 되는 아실기 또는 아실기의 전달은 EC 2.3의 주요 측면이다.또한 아미노아실기와 비아미노아실기를 구별한다.펩티딜전달효소는 [38]번역 중 펩타이드 결합의 형성을 촉진하는 리보자임이다.아미노아실전달효소로서 펩티딜-tRNA + 아미노아실-tRNAB[39]na { \} tRNA +A 펩티딜 아미노아실-tRNA의 전달을 촉매한다.
EC 2.4: 글리코실, 헥소실 및 펜토실전달효소
EC 2.4는 글리코실기를 전달하는 효소뿐만 아니라 헥소스와 펜토스를 전달하는 효소를 포함한다.글리코실전달효소는 단당류를 다른 [40]분자로 전달하여 이당류와 다당류의 생합성에 관여하는 EC 2.4 전달효소의 하위 범주이다.대표적인 글리코실전달효소는 2개의 단백질 서브유닛을 가진 이합체인 유당합성효소이다.이것의 주요 작용은 포도당과 [41]UDP-갈락토스로부터 유당을 생산하는 것이다.이는 UDP-β-D-갈락토스 + D-포도당δ {} UDP + [42]유당 경로를 통해 발생한다.
EC 2.5: 알킬 및 아릴전달효소
EC 2.5는 알킬기 또는 아릴기를 전달하는 효소와 관련이 있지만 메틸기는 포함하지 않는다.이는 EC 2.3에 포함된 알킬기가 이전될 때 알킬기가 되는 기능군과 대조적이다. EC 2.5는 현재 하위 클래스를 하나만 보유하고 있다.알킬과 아릴전달효소.[43]예를 들어 시스테인 합성효소는 O-아세틸-L-세린3 및 황화수소로부터 아세트산과 시스테인의 형성을 촉매한다: O-아세틸-L-세린3 + HS2 { L-시스테인 + 아세테이트.[44]
EC 2.6: 질소전달효소
질소 그룹의 이동과 일치하는 그룹은 EC 2.6이다.이것은 트랜스아미나아제(아미노기전달효소)와 같은 효소, 그리고 극소수의 옥시미노기전달효소 및 기타 질소기전달효소를 포함한다.EC 2.6은 이전에는 아미디노전달효소([45]amidinotransferase)를 포함하였으나 이후 EC 2.1(단일 탄소전달효소)티로신, 페닐알라닌, 트립토판에 작용 가능한 아스파르트산 트랜스아미나아제에서는 아미노기를 분자 간에 [46]가역적으로 전달한다.
예를 들어, 반응은 L-aspartate +2-oxoglutarate \ oxaloacetate + L-glutamate의 [47]순서로 이루어집니다.
EC 2.7: 인전달효소
EC 2.7은 인 함유기를 전달하는 효소를 포함하지만 뉴클로티딜 전이효소도 포함한다.[48]서브카테고리 포스포트랜스퍼레이스는 전달을 받아들이는 [24]그룹의 종류에 따라 분류된다.인산염 수용체로 분류되는 그룹에는 알코올, 카르복시기, 질소기 [29]및 인산기가 포함됩니다.이 전달효소 서브클래스의 또 다른 구성 요소는 다양한 키나아제이다.대표적인 키나제는 단백질 키나아제 하위군을 구성하는 사이클린 의존성 키나제(또는 CDK)이다.이름에서 알 수 있듯이 CDK는 활성화를 [49]위해 특정 사이클린 분자에 크게 의존합니다.CDK-사이클린 복합체는 결합되면 세포 [50]주기 내에서 기능을 수행할 수 있다.
CDK에 의해 촉매되는 반응은 ATP + 표적 단백질 \ ADP + 인산단백질이다.[51]
EC 2.8: 유황전달효소

황 함유기의 전달은 EC 2.8에서 다루며, 황 전달효소, 술포 전달효소, CoA 전달효소 등의 하위 범주와 알킬티오기를 [53]전달하는 효소로 세분화된다.황산염기 [54]공여체로서 PAPS를 사용하는 것이 술포트전달효소이다.이 소분류는 광범위한 [55]표적화 능력을 가진 알코올 술포전달효소이다.이로 인해 알코올 술포트랜스퍼레이스는 "히드록시스테로이드 술포트랜스퍼레이스", "스테로이드 술포키나아제", "에스트로겐 술포트랜스퍼레이스"[56]를 포함한 여러 다른 이름으로도 알려져 있다.그 활동의 감소는 인간의 [57]간질환과 관련이 있다.이 전달효소는 3'-포스포아데닐 황산염 + 알코올 } 아데노신 3', 5'비스인산염 + 알킬 [58]황산염의 반응을 통해 작용한다.
EC 2.9: 셀레늄전달효소
EC 2.9는 셀레늄 함유기를 [59]전달하는 효소를 포함한다.이 범주는 전달 효소를 두 개만 포함하므로 전달 효소의 가장 작은 범주 중 하나이다.1999년 분류 시스템에 처음 추가된 셀레노시스테인 합성효소는 세릴-tRNA(Sec UCA)를 셀레노시스테일-tRNA(Sec UCA)[60]로 변환한다.
EC 2.10: 금속전달효소
EC 2.10의 범주에는 몰리브덴 또는 텅스텐 함유기를 전달하는 효소가 포함된다.그러나 2011년 현재 몰리브도프테린 [61]몰리브도트랜스퍼라아제라는 한 가지 효소만 추가되었다.이 효소는 [62]대장균의 MoCo 생합성 성분이다.반응의 촉매는 아데닐-몰리브탑테린 + 몰리브덴 \} 몰리브덴 보조인자 + [63]AMP이다.
조직 혈액형에서의 역할
A와 B 전달 효소는 인간 ABO 혈액형 시스템의 기초이다.A와 B 전달효소 모두 글리코실 전달효소이며, 이는 당 분자를 H-항원 [64]물질로 전달한다는 것을 의미한다.이것은 H-항원이 A/B [64]항원으로 알려진 당단백질과 당지질 결합체를 합성할 수 있게 한다.A 전이효소의 전체 이름은 α-1-3-N-아세틸갈락토사미닐전달효소이며[65], 세포 내 기능은 H-항원에 N-아세틸갈락토사민을 첨가하여 A-항원을 [66]: 55 생성하는 것이다.B전달효소의 전체 이름은 알파 1-3-갈락토실전달효소이며,[65] 세포 내 기능은 H-항원에 갈락토오스 분자를 첨가하여 [66]B-항원을 생성하는 것이다.
호모 사피엔스는 네 가지 혈액형 중 하나를 가질 수 있다.A형(A항원 표현), B형(B항원 표현), AB형(A항원과 B항원 모두 표현) 및 O형(A항원과 B항원 [67]모두 표현)입니다.A와 B 전달효소 유전자는 [68]9번 염색체에 있다.이 유전자는 7개의 엑손과 6개의[69] 인트론을 포함하고 있으며 유전자 자체는 [70]18kb가 넘는다.A와 B 전달 효소에 대한 대립 유전자는 매우 유사합니다.결과 효소는 4개의 아미노산 [66]잔류물에서만 차이가 난다.서로 다른 잔류물은 [66]: 82–83 효소의 위치 176, 235, 266 및 268에 있습니다.
결점

.
트랜스페라아제 결핍은 많은 흔한 질병의 근원이다.트랜스페라아제 결핍의 가장 일반적인 결과는 세포 생성물의 축적이다.
SCOT 결핍증
숙시닐-CoA:3-케토산 CoA전달효소 결핍증(또는 SCOT 결핍증)은 케톤의 [71]축적을 일으킨다.케톤은 체내의 지방이 분해되면서 생성되고 중요한 에너지원입니다.[72]케톤을 이용할 수 없는 것은 간헐적인 케토산증을 유발하며,[72] 이는 보통 유아기에 처음 나타난다.질병 환자들은 메스꺼움, 구토, 음식을 먹을 수 없고 호흡곤란을 [72]겪는다.극단적인 경우, 케토산증은 혼수상태와 [72]사망으로 이어질 수 있다.그 결핍은 OXCT1 [73]유전자의 돌연변이에 의해 야기된다.치료는 대부분 환자의 [74]식단 조절에 의존한다.
CPT-II 결핍증
카르니틴 팔미토일전달효소 II 결핍증(CPT-II 결핍증이라고도 함)은 인체가 미토콘드리아로 지방산을 운반하여 연료원으로 [75]처리하는 능력이 부족하기 때문에 과도한 긴 사슬 지방산으로 이어진다.그 병은 유전자 CPT2의 [76]결함으로 인해 발생한다.이 결핍은 치명적인 신생아, 심각한 유아성 심근경련, 근질환의 [76]세 가지 방법 중 하나로 환자에게 나타난다.근병증은 결손의 가장 덜 심각한 형태이며 환자의 [76]수명 중 어느 시점에서나 나타날 수 있다.다른 두 가지 형태는 [76]유아기에 나타난다.치명적인 신생아 형태와 심각한 유아 형태의 일반적인 증상은 간부전, 심장 질환, 발작 및 [76]사망이다.근병증은 격렬한 운동 [76]후 근육통과 쇠약함을 특징으로 한다.치료에는 일반적으로 식이 수정과 카르니틴 [76]보충제가 포함됩니다.
갈락토세미아
갈락토오스혈증은 단순 [77]당인 갈락토스를 처리할 수 없기 때문에 발생한다.이 결핍은 갈락토스-1-인산우리딜전달효소(GALT) 유전자가 돌연변이를 몇 개라도 가지고 있을 때 발생하며,[78][79] GALT의 생성량 부족을 초래한다.갈락토세미아에는 클래식과 두아르테의 [80]두 가지 형태가 있다.두아르테 갈락토오스혈증은 일반적으로 전통적인 갈락토오스혈증보다 덜 심각하며 갈락토키나아제 [81]결핍에 의해 발생한다.갈락토오스혈증은 모유 속의 당분을 처리할 수 없게 만들어 [81]생후 며칠 안에 구토와 거식증을 일으킨다.대부분의 증상은 [81]체내 갈락토오스-1-인산이 축적되어 발생한다.일반적인 증상으로는 간부전,[82] 패혈증, 성장장애, 정신장애 등이 있다.두 번째 독성 물질인 갈락티톨의 축적은 눈의 수정체에서 일어나 [83]백내장을 일으킨다.현재, 이용할 수 있는 유일한 치료법은 조기 진단에 이어 유당이 없는 식단을 고수하고 [84]발병할 수 있는 감염에 항생제를 처방하는 것이다.
콜린아세틸전달효소결핍증
콜린 아세틸전달효소(ChAT 또는 CAT)는 신경전달물질인 아세틸콜린을 생성하는 중요한 [85]효소이다.아세틸콜린은 기억력, 주의력, 수면, [86][87][88]각성과 같은 많은 신경정신 기능에 관여한다.이 효소는 구상이고 단일 아미노산 [89]사슬로 구성되어 있습니다.ChAT는 신경 세포의 시냅스에서 아세틸 조효소 A에서 콜린으로 아세틸기를 전달하는 기능을 하며 용해성과 막 [89]결합의 두 가지 형태로 존재한다.ChAT 유전자는 [90]10번 염색체에 있다.
알츠하이머병
ChAT의 발현 감소는 알츠하이머병의 [91]특징 중 하나이다.알츠하이머 환자는 측두엽, 두정엽,[92] 전두엽을 포함한 뇌의 여러 부위에서 3090%의 활동 감소를 보인다.그러나 ChAT 결핍이 이 [89]질병의 주된 원인이라고는 생각되지 않는다.
근위축성 측삭경화증(ALS 또는 루게릭병)
ALS 환자는 척수와 [93]뇌의 운동 뉴런에서 ChAT 활성의 현저한 감소를 보인다.낮은 수준의 ChAT 활동은 질병의 초기 징후이며 운동 뉴런이 죽기 훨씬 전에 발견될 수 있습니다.이것은 환자가 증상이 [94]나타나기 전에 감지될 수도 있다.
헌팅턴병
헌팅턴병 환자들 또한 ChAT [95]생산량이 현저하게 감소하는 것을 보여준다.생산량 감소의 구체적인 원인은 분명하지 않지만 가시가 있는 수상돌기를 가진 중형 운동 뉴런의 죽음은 ChAT [89]생산의 낮은 수준으로 이어진다고 여겨진다.
정신분열증
정신분열증 환자들은 또한 ChAT의 감소된 수치를 나타내며, 이는 뇌와[96] 핵의 메조폰틴 절단에 [97]국소화되어 있으며, 이는 이러한 [89]환자에 의해 경험되는 인지 기능의 감소와 관련이 있는 것으로 여겨진다.
영아 돌연사 증후군(SIDS)
최근 연구에 따르면 SIDS 유아들은 시상하부와 [89]선조체 모두에서 ChAT 수치가 감소하는 것으로 나타났다.SIDS 유아들은 또한 미주신경계에서 [98]ChAT를 생성할 수 있는 더 적은 뉴런을 보인다.이러한 수질의 결함은 심혈관 및 [98]호흡기와 같은 필수적인 자율 기능을 제어할 수 없게 할 수 있다.
선천성근력증후군(CMS)
CMS는 [99]치명적일 수 있는 무호흡(호흡 불능)이 반복적으로 발생하는 신경근 전달의 결함으로 특징지어지는 질병 패밀리입니다.ChAT 결핍은 전이 문제가 시냅스 [100]전에 발생하는 근육증 증후군에 관련된다.이러한 증후군은 환자가 아세틸콜린을 [100]재동기화할 수 없는 것이 특징이다.
생명공학에서의 사용
단말전송효소
말단 전달효소는 DNA를 표시하거나 플라스미드 [101]벡터를 생성하는 데 사용될 수 있는 전달효소이다.디옥시뉴클레오티드를 기존 DNA 분자의 하류단 또는 3'단에 템플릿 형태로 첨가함으로써 이 두 가지 과제를 모두 달성한다.Terminal transferase는 RNA [101]프라이머 없이 기능할 수 있는 몇 안 되는 DNA 중합효소 중 하나입니다.
글루타치온전달효소
글루타티온 전이효소(GST)의 종류는 매우 다양하기 때문에 많은 생물공학적 목적으로 사용될 수 있다.식물은 세포의 나머지로부터 독성 [102]금속을 분리하는 수단으로 글루타치온 전이효소를 사용한다.이러한 글루타치온 전달효소는 제초제나 [103]살충제와 같은 오염물질을 검출하는 바이오센서를 만드는데 사용될 수 있다.글루타치온 전이효소는 또한 트랜스제닉 식물에서 생체 [103]및 비생물적 스트레스 모두에 대한 저항성을 증가시키기 위해 사용된다.글루타치온 전이효소는 약물 [103]내성에 대한 역할 때문에 항암제의 표적으로 현재 연구되고 있다.또한 글루타치온전달효소 유전자는 산화손상을 방지하는 능력으로 연구되어 트랜스제닉 컬티겐의 [104]내성이 향상되었다.
고무전달효소
현재 천연고무의 상업적 공급원은 헤베아 공장(Hevea Brasiliensis)뿐이다.천연고무는 여러 가지 상업적 [105]용도에서 합성고무보다 우수하다.담배, [106]해바라기 등 천연고무를 합성할 수 있는 트랜스제닉 식물 생산에 힘쓰고 있다.이러한 노력은 이러한 유전자를 다른 [106]식물에 전달하기 위해 고무전달효소 복합체의 서브유닛을 배열하는 데 초점을 맞추고 있다.
막관련전달효소
많은 전달효소는 말초막 단백질로서 생물학적 막과 결합하거나 단일 막 통과 [107]나선을 통해 막에 고정됩니다. 예를 들어 골지 기구의 수많은 글리코실 전달효소입니다.다른 일부는 다경간막 통과 단백질, 예를 들어 특정 올리고사카릴 전이효소 또는 MPEG 계열의 마이크로솜 글루타티온 S 전이효소이다.
레퍼런스
- ^ "EC 2.7.7 Nucleotidyltransferases". Enzyme Nomenclature. Recommendations. Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Retrieved 4 October 2020.
- ^ "Transferase". Genetics Home Reference. National Institute of Health. Retrieved 4 November 2013.
- ^ Moore SA, Jencks WP (Sep 1982). "Model reactions for CoA transferase involving thiol transfer. Anhydride formation from thiol esters and carboxylic acids". The Journal of Biological Chemistry. 257 (18): 10882–92. doi:10.1016/S0021-9258(18)33907-3. PMID 6955307.
- ^ Wishart D. "Tryptophan Metabolism". Small Molecule Pathway Database. Department of Computing Science and Biological Sciences, University of Alberta. Retrieved 4 November 2013.
- ^ Herbst EA, MacPherson RE, LeBlanc PJ, Roy BD, Jeoung NH, Harris RA, Peters SJ (Jan 2014). "Pyruvate dehydrogenase kinase-4 contributes to the recirculation of gluconeogenic precursors during postexercise glycogen recovery". American Journal of Physiology. Regulatory, Integrative and Comparative Physiology. 306 (2): R102–7. doi:10.1152/ajpregu.00150.2013. PMC 3921314. PMID 24305065.
- ^ 왓슨, 제임스 D.유전자의 분자생물학.어퍼 새들 리버, 뉴저지주: 피어슨, 2013.인쇄.
- ^ Boyce S, Tipton KF (2005). "Enzyme Classification and Nomenclature". Encyclopedia of Life Sciences. doi:10.1038/npg.els.0003893. ISBN 978-0470016176.
- ^ Morton RK (Jul 1953). "Transferase activity of hydrolytic enzymes". Nature. 172 (4367): 65–8. Bibcode:1953Natur.172...65M. doi:10.1038/172065a0. PMID 13072573. S2CID 4180213.
- ^ Needham, Dorothy M (1930). "A quantitative study of succinic acid in muscle: Glutamic and aspartic acids as precursors". Biochem J. 24 (1): 208–27. doi:10.1042/bj0240208. PMC 1254374. PMID 16744345.
- ^ Snell EE, Jenkins WT (December 1959). "The mechanism of the transamination reaction". Journal of Cellular and Comparative Physiology. 54 (S1): 161–177. doi:10.1002/jcp.1030540413. PMID 13832270.
- ^ Braunstein AE, Kritzmann MG (1937). "Formation and Breakdown of Amino-acids by Inter-molecular Transfer of the Amino Group". Nature. 140 (3542): 503–504. Bibcode:1937Natur.140R.503B. doi:10.1038/140503b0. S2CID 4009655.
- ^ Schoenheimer R (1949). The Dynamic State of Body Constituents. Hafner Publishing Co Ltd. ISBN 978-0-02-851800-8.
- ^ Guggenheim KY (Nov 1991). "Rudolf Schoenheimer and the concept of the dynamic state of body constituents". The Journal of Nutrition. 121 (11): 1701–4. doi:10.1093/jn/121.11.1701. PMID 1941176.
- ^ Hird FJ, Rowsell EV (Sep 1950). "Additional transaminations by insoluble particle preparations of rat liver". Nature. 166 (4221): 517–8. Bibcode:1950Natur.166..517H. doi:10.1038/166517a0. PMID 14780123. S2CID 4215187.
- ^ Munch-Petersen A, Kalckar HM, Cutolo E, Smith EE (Dec 1953). "Uridyl transferases and the formation of uridine triphosphate; enzymic production of uridine triphosphate: uridine diphosphoglucose pyrophosphorolysis". Nature. 172 (4388): 1036–7. Bibcode:1953Natur.172.1036M. doi:10.1038/1721036a0. PMID 13111246. S2CID 452922.
- ^ "Physiology or Medicine 1970 - Press Release". Nobelprize.org. Nobel Media AB. Retrieved 5 November 2013.
- ^ Lambalot RH, Gehring AM, Flugel RS, Zuber P, LaCelle M, Marahiel MA, Reid R, Khosla C, Walsh CT (Nov 1996). "A new enzyme superfamily - the phosphopantetheinyl transferases". Chemistry & Biology. 3 (11): 923–36. doi:10.1016/S1074-5521(96)90181-7. PMID 8939709.
- ^ Wongtrakul J, Pongjaroenkit S, Leelapat P, Nachaiwieng W, Prapanthadara LA, Ketterman AJ (Mar 2010). "Expression and characterization of three new glutathione transferases, an epsilon (AcGSTE2-2), omega (AcGSTO1-1), and theta (AcGSTT1-1) from Anopheles cracens (Diptera: Culicidae), a major Thai malaria vector". Journal of Medical Entomology. 47 (2): 162–71. doi:10.1603/me09132. PMID 20380296. S2CID 23558834.
- ^ Sen J, Goltz JS, Stevens L, Stein D (Nov 1998). "Spatially restricted expression of pipe in the Drosophila egg chamber defines embryonic dorsal-ventral polarity". Cell. 95 (4): 471–81. doi:10.1016/s0092-8674(00)81615-3. PMID 9827800. S2CID 27722532.
- ^ Moussian B, Roth S (Nov 2005). "Dorsoventral axis formation in the Drosophila embryo--shaping and transducing a morphogen gradient". Current Biology. 15 (21): R887–99. doi:10.1016/j.cub.2005.10.026. PMID 16271864. S2CID 15984116.
- ^ Zhu X, Sen J, Stevens L, Goltz JS, Stein D (Sep 2005). "Drosophila pipe protein activity in the ovary and the embryonic salivary gland does not require heparan sulfate glycosaminoglycans". Development. 132 (17): 3813–22. doi:10.1242/dev.01962. PMID 16049108.
- ^ Zhang Z, Stevens LM, Stein D (Jul 2009). "Sulfation of eggshell components by Pipe defines dorsal-ventral polarity in the Drosophila embryo". Current Biology. 19 (14): 1200–5. doi:10.1016/j.cub.2009.05.050. PMC 2733793. PMID 19540119.
- ^ Xu D, Song D, Pedersen LC, Liu J (Mar 2007). "Mutational study of heparan sulfate 2-O-sulfotransferase and chondroitin sulfate 2-O-sulfotransferase". The Journal of Biological Chemistry. 282 (11): 8356–67. doi:10.1074/jbc.M608062200. PMID 17227754.
- ^ a b "EC 2 Introduction". School of Biological & Chemical Sciences at Queen Mary, University of London. Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Retrieved 5 November 2013.
- ^ Shaw WV, Tsai L, Stadtman ER (Feb 1966). "The enzymatic synthesis of N-methylglutamic acid". The Journal of Biological Chemistry. 241 (4): 935–45. doi:10.1016/S0021-9258(18)96855-9. PMID 5905132.
- ^ Lower S. "Naming Chemical Substances". Chem1 General Chemistry Virtual Textbook. Retrieved 13 November 2013.
- ^ Hausmann R (3 December 2010). To grasp the essence of life: a history of molecular biology. Dordrecht: Springer. pp. 198–199. ISBN 978-90-481-6205-5.
- ^ "EC 2.7.7.6". IUBMB Enzyme Nomenclature. Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Retrieved 12 November 2013.
- ^ a b "EC2 Transferase Nomenclature". School of Biological & Chemical Sciences at Queen Mary, University of London. Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Retrieved 4 November 2013.
- ^ a b "Transferase". Encyclopædia Britannica. Encyclopædia Britannica, Inc. Retrieved 28 July 2016.
- ^ "EC 2.1.3: Carboxy- and Carbamoyltransferases". School of Biological & Chemical Sciences at Queen Mary, University of London. Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Retrieved 25 November 2013.
- ^ "carbamoyltransferase". The Free Dictionary. Farlex, Inc. Retrieved 25 November 2013.
- ^ "carbamoyl group (CHEBI:23004)". ChEBI: The database and ontology of Chemical Entities of Biological Interest. European Molecular Biology Laboratory. Retrieved 25 November 2013.
- ^ Reichard P, Hanshoff G (1956). "Aspartate Carbamyl Transferase from Escherichia coli" (PDF). Acta Chemica Scandinavica. 10: 548–566. doi:10.3891/acta.chem.scand.10-0548.
- ^ "ENZYME class 2.2.1". ExPASy: Bioinformatics Resource Portal. Swiss Institute of Bioinformatics. Retrieved 25 November 2013.
- ^ "Pentose Phosphate Pathway". Molecular Biochemistry II Notes. The Biochemistry and Biophysics Program at Renssalaer Polytechnic Institute. Retrieved 25 November 2013.
- ^ "EC 2.2.1.2 Transaldolase". Enzyme Structures Database. European Molecular Biology Laboratory. Retrieved 25 November 2013.
- ^ Voorhees RM, Weixlbaumer A, Loakes D, Kelley AC, Ramakrishnan V (May 2009). "Insights into substrate stabilization from snapshots of the peptidyl transferase center of the intact 70S ribosome". Nature Structural & Molecular Biology. 16 (5): 528–33. doi:10.1038/nsmb.1577. PMC 2679717. PMID 19363482.
- ^ "ENZYME entry: EC 2.3.2.12". ExPASy: Bioinformatics Resource Portal. Swiss Institute of Bioinformatics. Retrieved 26 November 2013.
- ^ "Keyword Glycosyltransferase". UniProt. UniProt Consortium. Retrieved 26 November 2013.
- ^ Fitzgerald DK, Brodbeck U, Kiyosawa I, Mawal R, Colvin B, Ebner KE (Apr 1970). "Alpha-lactalbumin and the lactose synthetase reaction". The Journal of Biological Chemistry. 245 (8): 2103–8. doi:10.1016/S0021-9258(18)63212-0. PMID 5440844.
- ^ "ENZYME entry: EC 2.4.1.22". ExPASy: Bioinformatics Resource Portal. Swiss Institute of Bioinformatics. Retrieved 26 November 2013.
- ^ "EC 2.5". IntEnz. European Molecular Biology Laboratory. Retrieved 26 November 2013.
- ^ Qabazard B, Ahmed S, Li L, Arlt VM, Moore PK, Stürzenbaum SR (2013). "C. elegans aging is modulated by hydrogen sulfide and the sulfhydrylase/cysteine synthase cysl-2". PLOS ONE. 8 (11): e80135. Bibcode:2013PLoSO...880135Q. doi:10.1371/journal.pone.0080135. PMC 3832670. PMID 24260346.
- ^ "EC 2.6.2". IUBMB Enzyme Nomenclatur. Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Retrieved 28 November 2013.
- ^ Kirsch JF, Eichele G, Ford GC, Vincent MG, Jansonius JN, Gehring H, Christen P (Apr 1984). "Mechanism of action of aspartate aminotransferase proposed on the basis of its spatial structure". Journal of Molecular Biology. 174 (3): 497–525. doi:10.1016/0022-2836(84)90333-4. PMID 6143829.
- ^ "Enzyme entry:2.6.1.1". ExPASy: Bioinformatics Resource Portal. Swiss Institute of Bioinformatics. Retrieved 28 November 2013.
- ^ "EC 2.7". School of Biological & Chemical Sciences at Queen Mary, University of London. Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Retrieved 4 December 2013.
- ^ Yee A, Wu L, Liu L, Kobayashi R, Xiong Y, Hall FL (Jan 1996). "Biochemical characterization of the human cyclin-dependent protein kinase activating kinase. Identification of p35 as a novel regulatory subunit". The Journal of Biological Chemistry. 271 (1): 471–7. doi:10.1074/jbc.271.1.471. PMID 8550604. S2CID 20348897.
- ^ Lewis R (2008). Human genetics : concepts and applications (8th ed.). Boston: McGraw-Hill/Higher Education. p. 32. ISBN 978-0-07-299539-8.
- ^ "ENZYME Entry: EC 2.7.11.22". ExPASy: Bioinformatics Resource Portal. Swiss Institute of Bioinformatics. Retrieved 4 December 2013.
- ^ "1aqy Summary". Protein Data Bank in Europe Bringing Structure to Biology. The European Bioinformatics Institute. Retrieved 11 December 2013.
- ^ "EC 2.8 Transferring Sulfur-Containing Groups". School of Biological & Chemical Sciences at Queen Mary, University of London. Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Retrieved 11 December 2013.
- ^ Negishi M, Pedersen LG, Petrotchenko E, Shevtsov S, Gorokhov A, Kakuta Y, Pedersen LC (Jun 2001). "Structure and function of sulfotransferases". Archives of Biochemistry and Biophysics. 390 (2): 149–57. doi:10.1006/abbi.2001.2368. PMID 11396917.
- ^ "EC 2.8 Transferring Sulfur-Containing Groups". School of Biological & Chemical Sciences at Queen Mary, University of London. Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Retrieved 11 December 2013.
- ^ "Enzyme 2.8.2.2". Kegg: DBGET. Kyoto University Bioinformatics Center. Retrieved 11 December 2013.
- ^ Ou Z, Shi X, Gilroy RK, Kirisci L, Romkes M, Lynch C, Wang H, Xu M, Jiang M, Ren S, Gramignoli R, Strom SC, Huang M, Xie W (Jan 2013). "Regulation of the human hydroxysteroid sulfotransferase (SULT2A1) by RORα and RORγ and its potential relevance to human liver diseases". Molecular Endocrinology. 27 (1): 106–15. doi:10.1210/me.2012-1145. PMC 3545217. PMID 23211525.
- ^ Sekura RD, Marcus CJ, Lyon ES, Jakoby WB (May 1979). "Assay of sulfotransferases". Analytical Biochemistry. 95 (1): 82–6. doi:10.1016/0003-2697(79)90188-x. PMID 495970.
- ^ "EC 2.9.1". School of Biological & Chemical Sciences at Queen Mary, University of London. Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Retrieved 11 December 2013.
- ^ Forchhammer K, Böck A (Apr 1991). "Selenocysteine synthase from Escherichia coli. Analysis of the reaction sequence". The Journal of Biological Chemistry. 266 (10): 6324–8. doi:10.1016/S0021-9258(18)38121-3. PMID 2007585.
- ^ "EC 2.10.1". School of Biological & Chemical Sciences at Queen Mary, University of London. Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Retrieved 11 December 2013.
- ^ Nichols JD, Xiang S, Schindelin H, Rajagopalan KV (Jan 2007). "Mutational analysis of Escherichia coli MoeA: two functional activities map to the active site cleft". Biochemistry. 46 (1): 78–86. doi:10.1021/bi061551q. PMC 1868504. PMID 17198377.
- ^ Wünschiers R, Jahn M, Jahn D, Schomburg I, Peifer S, Heinzle E, Burtscher H, Garbe J, Steen A, Schobert M, Oesterhelt D, Wachtveitl J, Chang A (2010). "Chapter 3: Metabolism". In Michal G, Schomburg D (eds.). Biochemical Pathways: an Atlas of Biochemistry and Molecular Biology (2nd ed.). Oxford: Wiley-Blackwell. p. 140. doi:10.1002/9781118657072.ch3. ISBN 9780470146842.
- ^ a b Nishida C, Tomita T, Nishiyama M, Suzuki R, Hara M, Itoh Y, Ogawa H, Okumura K, Nishiyama C (2011). "B-transferase with a Pro234Ser substitution acquires AB-transferase activity". Bioscience, Biotechnology, and Biochemistry. 75 (8): 1570–5. doi:10.1271/bbb.110276. PMID 21821934.
- ^ a b "ABO ABO blood group (transferase A, alpha 1-3-N-acetylgalactosaminyltransferase; transferase B, alpha 1-3-galactosyltransferase) [ Homo sapiens (human) ]". NCBI. Retrieved 2 December 2013.
- ^ a b c d Datta SP, Smith GH, Campbell PN (2000). Oxford Dictionary of Biochemistry and Molecular Biology (Rev. ed.). Oxford: Oxford Univ. Press. ISBN 978-0-19-850673-7.
- ^ O'Neil D. "ABO Blood Groups". Human Blood: An Introduction to Its Components and Types. Behavioral Sciences Department, Palomar College. Retrieved 2 December 2013.
- ^ "ABO Blood Group (Transferase A, Alpha 1-3-N-Acetylgalactosaminyltransferase;Transferase B, Alpha 1-3-Galactosyltransferase)". GeneCards: The Human Gene Compendium. Weizmann Institute of Science. Retrieved 2 December 2013.
- ^ Moran, Lawrence (2007-02-22). "Human ABO Gene". Retrieved 2 December 2013.
- ^ Kidd, Kenneth. "ABO blood group (transferase A, alpha 1-3-N-acetylgalactosaminyltransferase; transferase B, alpha 1-3-galactosyltransferase)". Retrieved 2 December 2013.
- ^ "Succinyl-CoA:3-ketoacid CoA transferase deficiency". Genetics Home Reference. National Institute of Health. Retrieved 4 November 2013.
- ^ a b c d "SUCCINYL-CoA:3-OXOACID CoA TRANSFERASE DEFICIENCY". OMIM. Retrieved 22 November 2013.
- ^ "SCOT deficiency". NIH. Retrieved 22 November 2013.
- ^ "Succinyl-CoA 3-Oxoacid Transferase Deficiency" (PDF). Climb National Information Centre. Retrieved 22 November 2013.
- ^ "Carnitine plamitoyltransferase I deficiency". Genetics Home Reference. National Institute of Health. Retrieved 4 November 2013.
- ^ a b c d e f g Weiser, Thomas (1993). "Carnitine Palmitoyltransferase II Deficiency". NIH. Retrieved 22 November 2013.
- ^ "Galactosemia". Genetics Home Reference. National Institute of Health. Retrieved 4 November 2013.
- ^ Dobrowolski SF, Banas RA, Suzow JG, Berkley M, Naylor EW (Feb 2003). "Analysis of common mutations in the galactose-1-phosphate uridyl transferase gene: new assays to increase the sensitivity and specificity of newborn screening for galactosemia". The Journal of Molecular Diagnostics. 5 (1): 42–7. doi:10.1016/S1525-1578(10)60450-3. PMC 1907369. PMID 12552079.
- ^ Murphy M, McHugh B, Tighe O, Mayne P, O'Neill C, Naughten E, Croke DT (Jul 1999). "Genetic basis of transferase-deficient galactosaemia in Ireland and the population history of the Irish Travellers". European Journal of Human Genetics. 7 (5): 549–54. doi:10.1038/sj.ejhg.5200327. PMID 10439960. S2CID 22402528.
- ^ Mahmood U, Imran M, Naik SI, Cheema HA, Saeed A, Arshad M, Mahmood S (Nov 2012). "Detection of common mutations in the GALT gene through ARMS". Gene. 509 (2): 291–4. doi:10.1016/j.gene.2012.08.010. PMID 22963887.
- ^ a b c "Galactosemia". NORD. Retrieved 22 November 2013.
- ^ Berry GT (2000). "Classic Galactosemia and Clinical Variant Galactosemia". GeneReviews [Internet]. PMID 20301691.
- ^ Bosch AM (Aug 2006). "Classical galactosaemia revisited". Journal of Inherited Metabolic Disease. 29 (4): 516–25. doi:10.1007/s10545-006-0382-0. PMID 16838075. S2CID 16382462.
- ^ Karadag N, Zenciroglu A, Eminoglu FT, Dilli D, Karagol BS, Kundak A, Dursun A, Hakan N, Okumus N (2013). "Literature review and outcome of classic galactosemia diagnosed in the neonatal period". Clinical Laboratory. 59 (9–10): 1139–46. doi:10.7754/clin.lab.2013.121235. PMID 24273939.
- ^ Strauss WL, Kemper RR, Jayakar P, Kong CF, Hersh LB, Hilt DC, Rabin M (Feb 1991). "Human choline acetyltransferase gene maps to region 10q11-q22.2 by in situ hybridization". Genomics. 9 (2): 396–8. doi:10.1016/0888-7543(91)90273-H. PMID 1840566.
- ^ Braida D, Ponzoni L, Martucci R, Sparatore F, Gotti C, Sala M (May 2014). "Role of neuronal nicotinic acetylcholine receptors (nAChRs) on learning and memory in zebrafish". Psychopharmacology. 231 (9): 1975–85. doi:10.1007/s00213-013-3340-1. PMID 24311357. S2CID 8707545.
- ^ Stone TW (Sep 1972). "Cholinergic mechanisms in the rat somatosensory cerebral cortex". The Journal of Physiology. 225 (2): 485–99. doi:10.1113/jphysiol.1972.sp009951. PMC 1331117. PMID 5074408.
- ^ Guzman MS, De Jaeger X, Drangova M, Prado MA, Gros R, Prado VF (Mar 2013). "Mice with selective elimination of striatal acetylcholine release are lean, show altered energy homeostasis and changed sleep/wake cycle". Journal of Neurochemistry. 124 (5): 658–69. doi:10.1111/jnc.12128. PMID 23240572. S2CID 22798872.
- ^ a b c d e f Oda Y (Nov 1999). "Choline acetyltransferase: the structure, distribution and pathologic changes in the central nervous system" (PDF). Pathology International. 49 (11): 921–37. doi:10.1046/j.1440-1827.1999.00977.x. PMID 10594838. S2CID 23621617.
- ^ "Choline O-Acetyltransferase". GeneCards: The Human Gene Compendium. Weizmann Institute of Science. Retrieved 5 December 2013.
- ^ Szigeti C, Bencsik N, Simonka AJ, Legradi A, Kasa P, Gulya K (May 2013). "Long-term effects of selective immunolesions of cholinergic neurons of the nucleus basalis magnocellularis on the ascending cholinergic pathways in the rat: a model for Alzheimer's disease" (PDF). Brain Research Bulletin. 94: 9–16. doi:10.1016/j.brainresbull.2013.01.007. PMID 23357177. S2CID 22103097.
- ^ González-Castañeda RE, Sánchez-González VJ, Flores-Soto M, Vázquez-Camacho G, Macías-Islas MA, Ortiz GG (Mar 2013). "Neural restrictive silencer factor and choline acetyltransferase expression in cerebral tissue of Alzheimer's Disease patients: A pilot study". Genetics and Molecular Biology. 36 (1): 28–36. doi:10.1590/S1415-47572013000100005. PMC 3615522. PMID 23569405.
- ^ Rowland LP, Shneider NA (May 2001). "Amyotrophic lateral sclerosis". The New England Journal of Medicine. 344 (22): 1688–700. doi:10.1056/NEJM200105313442207. PMID 11386269.
- ^ Casas C, Herrando-Grabulosa M, Manzano R, Mancuso R, Osta R, Navarro X (Mar 2013). "Early presymptomatic cholinergic dysfunction in a murine model of amyotrophic lateral sclerosis". Brain and Behavior. 3 (2): 145–58. doi:10.1002/brb3.104. PMC 3607155. PMID 23531559.
- ^ Smith R, Chung H, Rundquist S, Maat-Schieman ML, Colgan L, Englund E, Liu YJ, Roos RA, Faull RL, Brundin P, Li JY (Nov 2006). "Cholinergic neuronal defect without cell loss in Huntington's disease". Human Molecular Genetics. 15 (21): 3119–31. doi:10.1093/hmg/ddl252. PMID 16987871.
- ^ Karson CN, Casanova MF, Kleinman JE, Griffin WS (Mar 1993). "Choline acetyltransferase in schizophrenia". The American Journal of Psychiatry. 150 (3): 454–9. doi:10.1176/ajp.150.3.454. PMID 8434662.
- ^ Mancama D, Mata I, Kerwin RW, Arranz MJ (Oct 2007). "Choline acetyltransferase variants and their influence in schizophrenia and olanzapine response". American Journal of Medical Genetics Part B. 144B (7): 849–53. doi:10.1002/ajmg.b.30468. PMID 17503482. S2CID 6882521.
- ^ a b Mallard C, Tolcos M, Leditschke J, Campbell P, Rees S (Mar 1999). "Reduction in choline acetyltransferase immunoreactivity but not muscarinic-m2 receptor immunoreactivity in the brainstem of SIDS infants". Journal of Neuropathology and Experimental Neurology. 58 (3): 255–64. doi:10.1097/00005072-199903000-00005. PMID 10197817.
- ^ Engel AG, Shen XM, Selcen D, Sine S (Dec 2012). "New horizons for congenital myasthenic syndromes". Annals of the New York Academy of Sciences. 1275 (1): 54–62. Bibcode:2012NYASA1275...54E. doi:10.1111/j.1749-6632.2012.06803.x. PMC 3546605. PMID 23278578.
- ^ a b Maselli RA, Chen D, Mo D, Bowe C, Fenton G, Wollmann RL (Feb 2003). "Choline acetyltransferase mutations in myasthenic syndrome due to deficient acetylcholine resynthesis". Muscle & Nerve. 27 (2): 180–7. doi:10.1002/mus.10300. PMID 12548525. S2CID 10373463.
- ^ a b Bowen, R. "Terminal Transferase". Biotechnology and Genetic Engineering. Colorado State University. Retrieved 10 November 2013.
- ^ Kumar B, Singh-Pareek SL, Sopory SK (2008). "Chapter 23: Glutathione Homeostasis and Abiotic Stresses in Plants: Physiological, Biochemical and Molecular Approaches". In Kumar A, Sopory S (eds.). Recent advances in plant biotechnology and its applications : Prof. Dr. Karl-Hermann Neumann commemorative volume. New Delhi: I.K. International Pub. House. ISBN 9788189866099.
- ^ a b c Chronopoulou EG, Labrou NE (2009). "Glutathione transferases: emerging multidisciplinary tools in red and green biotechnology". Recent Patents on Biotechnology. 3 (3): 211–23. doi:10.2174/187220809789389135. PMID 19747150.
- ^ Sytykiewicz H (2011). "Expression patterns of glutathione transferase gene (GstI) in maize seedlings under juglone-induced oxidative stress". International Journal of Molecular Sciences. 12 (11): 7982–95. doi:10.3390/ijms12117982. PMC 3233451. PMID 22174645.
- ^ Shintani D. "What is Rubber?". Elastomics. University of Nevada, Reno. Retrieved 23 November 2013.
- ^ a b "Development of Domestic Natural Rubber-Producing Industrial Crops Through Biotechnology". USDA. Retrieved 23 November 2013.
- ^ 멤브롬 데이터베이스의 단일 패스 막전달효소 슈퍼패밀리
![Xgroup+Y{\xrightarrow[ {transferase}]{}}X+Ygroup](https://wikimedia.org/api/rest_v1/media/math/render/svg/d94a93496ced3931a4b7c646f418f4c9419d3f73)