선택적 안드로겐 수용체 변조기
Selective androgen receptor modulator| 선택적 안드로겐 수용체 변조기 | |
|---|---|
| 약품반 | |
 | |
| 클래스 식별자 | |
| 동의어 | 비스테로이드성 안드로겐(모든 SARM이 비스테로이드성은 아니지만)[1] |
| 사용하다 | 조사 |
| 생물학적 표적 | 안드로겐수용체 |
| 화학급 | 대부분 비스테로이드성 |
| 법적지위 | |
| 법적지위 | |
| 위키데이터에서 | |
선택적 안드로겐 수용체 조절제(SARMs, Selective Androgen receptor modulator)는 전립선 및 정액 소포와 같은 다른 조직보다 근육 및 뼈와 같은 특정 조직에서 안드로겐 수용체를 선택적으로 활성화하는 약물의 한 종류입니다.
비선택적 단백 동화 안드로겐 스테로이드(AAS)는 잠재적으로 다양한 질병에 유용하지만 부작용으로 인해 사용이 제한됩니다. 골격근과 뼈에서 단백 동화 효과가 있는 스테로이드를 찾으려는 시도는 실패했습니다. 즉, 골밀도와 제지방량을 증가시키고 다른 조직에서는 활동을 무시할 수 있었습니다. 1998년, 연구자들은 안드로겐 수용체에 선택적으로 결합하는 새로운 종류의 비스테로이드성 화합물(SARMs)을 발견하여 전립선과 정액 소포와 같은 생식 조직에서 훨씬 적은 효과로 근육과 뼈에서 강력한 작용을 하게 했습니다.
SARM은 골다공증, 악액질(낭비 증후군), 양성 전립선 비대증, 스트레스 요실금 및 유방암의 치료를 위한 인간 연구에서 조사되었습니다. 2020년[update] 현재 미국 식품의약국의 승인을 받은 SARM은 없습니다. 임상 연구에서 부작용은 드물고 경미하지만, SARM은 다른 부작용 중에서도 간 효소 상승, HDL 콜레스테롤 수치 감소 및 시상하부-뇌하수체-성선 축(HPG 축) 억제를 유발할 수 있습니다.
SARMs는 21세기 초부터 도핑에 사용되었으며, 2008년 세계반도핑기구에 의해 금지되었습니다. SARM은 인터넷 기반의 회색 시장에서 쉽게 구할 수 있으며 일반적으로 근육 성장을 자극하기 위해 레크리에이션으로 사용됩니다.
역사
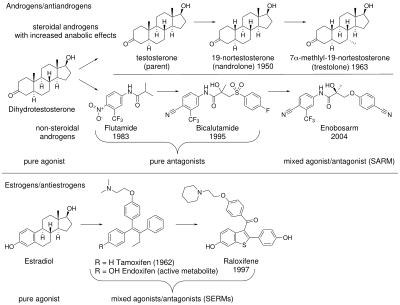
테스토스테론과 디하이드로테스토스테론(DHT)과 같이 내생적으로 생성되는 것을 포함한 단백 동화 안드로겐 스테로이드(AAS)는 안드로겐 수용체(AR)와 결합하여 활성화하여 그 효과를 생산합니다. AAS 효과는 안드로겐성(남성의 성적 특성 발달 및 유지)과 단백 동화성(골밀도, 근육량 및 근력 증가)으로 구분할 수 있습니다. AAS는 조혈, 응고, 대사 및 인지에도 영향을 미칩니다.[5][6] 1930년대에는 17α-알킬화 단백 동화 스테로이드가 발견되었는데, 이 스테로이드는 테스토스테론보다 조직 선택성이 커서 SARM으로 간주되기도 합니다.[7][8][9] 이러한 스테로이드는 테스토스테론 분자에 알킬기를 첨가하여 AR에 대한 결합 친화력을 변화시킴으로써 형성되었습니다.[10] 17α-알킬화된 단백 동화 스테로이드는 여전히 상당한 안드로겐 효과를 가지고 있으며, 또한 간독성도 있습니다.[8] 단백 동화작용을 하지만 안드로겐 효과가 최소화된 스테로이드를 개발하려는 노력은 성공적이지 못했습니다.[11]
비카루타미드, 플루타미드 및 닐루타미드와 같은 항안드로겐은 비스테로이드성 AR 길항제로서, AR과 결합하여 안드로겐 작용을 방지하며, 이러한 종류의 화학물질은 1970년대로 거슬러 올라갑니다.[5][12] 비스테로이드성 AR 작용제에 대한 관심은 선택적 에스트로겐 수용체 조절제(SERMs)의 치료적 사용이 명백해진 후 증가했습니다.[12] 비카루타미드 및 히드록시플루타미드와 구조적 유사성을 공유하는 아릴프로피오나미드의 발견은 AR에 부착되어 동화작용 및 항안드로겐 효과를 모두 생성하는 화합물을 만드는 방법을 제시했습니다.[5] 선택적 안드로겐 수용체 조절제(SARMs)는 전립선과 심혈관계와 같은 다른 조직에 대한 부작용을 피하면서 근육과 뼈에 대한 안드로겐의 동화 효과를 유지하려는 열망에서 개발되었습니다.[10]
비스테로이드성 SARM은 1998년에 Tennessee 대학에서 아릴프로피오나미드 SARM을 만든 연구 그룹과 퀴놀론으로 SARM을 만든 Ligand Pharmaceuticals의 두 연구 그룹에 의해 독립적으로 발명되었습니다. 그 이름은 SERMs와 유추하여 채택되었습니다.[12] 다른 SARMs는 테트라하이드로퀴놀린, 삼환식, 가교된 삼환식, 아닐린, 디아릴라닐린, 바이시클릭 히단토인, 벤즈이미다졸, 이미다졸로피라졸, 인돌 및 피라졸린 유도체를 포함합니다.[5] SARMs는 조직에 따라 AR의 작용제, 길항제 또는 부분 작용제가 될 수 있으며, 이는 부작용을 최소화하면서 특정 의학적 조건을 목표로 할 수 있습니다.[6] 인체 실험에 진출한 사람들은 뼈와 근육 조직에서 더 강한 효과를 보이고 전립선에서는 더 약한 효과를 보입니다.[7] SARM은 경구적으로 생물학적으로 이용 가능하며 간 대사를 통해 대부분 제거되며 아미드 가수분해 및 A-ring nitro 환원을 통해 대사됩니다.[10]
선택의 메커니즘
SARMs의 조직 특이적 효과의 작용 메커니즘은 2020년[update] 현재 계속 논의되고 있습니다.[5][13] 여러 가지 가설이 발전했습니다. 여기에는 5α-환원효소에 의한 SARM의 비활성화, 안드로겐 수용체 공동조절제의 조직 선택적 발현, SARM의 조직 선택적 흡수 및 비-유전체 신호전달이 포함됩니다.[5][14]
5α-환원효소
테스토스테론은 활성화되지 않은 비생식성 조직에서 활성화됩니다. 대조적으로, 5α-환원효소에 의한 조직 선택적 활성화는 생식 조직에서 중요한 활성화를 위해 더 활성화된 형태의 DHT로 필요합니다. 최종 결과는 테스토스테론과 그 대사 산물이 함께 조직 선택적이지 않다는 것입니다.[15] SARM은 5α-환원효소의 기질이 아니므로 전립선과 같은 조직에서 테스토스테론처럼 선택적으로 활성화되지 않습니다.[8] 이러한 활성화 부족은 SARMS에 효과적으로 어느 정도의 조직 선택성을 부여합니다.
안드로겐 수용체 코어조절제
SARMs의 선택성에 기여하는 또 다른 요인은 조직 선택적 전사 공동조절자 발현입니다.[16][14] 세포질에는 다른 I형 핵수용체와 마찬가지로 복잡하지 않은 안드로겐 수용체(AR)가 존재합니다. 리간드 결합 시, AR은 핵으로 옮겨져 DNA의 안드로겐 반응 요소와 결합하여 유전자 발현을 조절합니다.[17] 테스토스테론과 같은 AR 작용제는 유전자 발현의 상향 조절을 촉진하는 보조 활성제 단백질을 AR에 모집하는 반면, 길항제는 유전자 발현을 하향 조절하는 보조 억제제를 모집합니다. 또한 보조활성제 대 보조억제제의 비율은 조직 유형에 따라 차이가 있는 것으로 알려져 있습니다.[16][18] 구조적으로 순수한 AR 작용제는 H3 및 H4 근처에서 AR의 리간드 결합 도메인에서 나선-12(H12)의 위치를 안정화하여 보조 활성제에 포함된 FxxLF 모티프에 결합하는 표면 틈을 생성합니다.[17] 반대로, 길항제는 NCOR1 및 SMRT 보조억제제에서 발견되는 보조억제제 LXX(I/H)IXXX(I/L) 모티프의 결합을 촉진하면서 FXXLF 보조활성제 모티프의 결합을 차단하는 H12의 작용제 형태를 불안정하게 합니다.[17]
SERM과 유사하게, SARM은 뼈와 근육에서 작용제 안드로겐 수용체 활성을 나타내고 전립선과 같은 다른 조직에서 부분 작용제 또는 길항제 활성을 나타내는 혼합 작용제/길항제입니다.[14][6] 테스토스테론과 같은 비선택적 작용제는 AR에 결합되어 있지만 보조억제제는 아니므로 모든 조직에서 작용제입니다. 대조적으로, SARM은 H12의 작용제 형태를 부분적으로 불안정화시킴으로써 보조 활성화제와 보조 억제제를 모두 모집할 수 있습니다. 보조활성제가 과도하게 존재하는 조직(뼈와 근육)에서는 SARM이 작용제 역할을 합니다. 반대로, 보조억제제가 과도한 조직(예: 전립선)에서는, SARM이 부분작용제 또는 길항제로 작용합니다.[14]
SARMs enobosarm (osstarine)과 YK-11의 시험관 내 시험은 이들이 AR에 결합하는 것을 보여주었지만, 전체 AR 작용제와 달리 AR의 N-말단과 C-말단 사이의 상호작용을 차단하여 혼합 작용제/항제 작용 모드를 초래했습니다.[5][14]
조직분포
단백 동화 조직으로의 조직 선택적 흡수는 SARM 조직 선택성에 대한 또 다른 잠재적 메커니즘을 제시합니다. 그러나 방사선 라벨이 부착된 SARM을 사용한 자가방사선촬영 연구에서는 동화 조직에 우선적으로 분포하지 않는 것으로 나타났습니다.[8]
약물후보물질
| 이름. | 학급 | 개발자 | 에 대해 조사됨 | 최고 개발 단계 도달 | 구조. |
|---|---|---|---|---|---|
| Andarine (S-4, GTx-007) | 아릴프로피오나미드 | GTX, 온터널 테라퓨틱스[20] | 악액질[20] | 단계 I(중단)[20] |  |
| Arcarine (ORM-11984)[21] | 알[19] 수 없음 | 오리온스[21] | 양성 전립선 비대증, 저선량증, 골다공증[19] | 단계 I(중단)[21][19] | 구조미공개[19] |
| Enobosarm (ostarine, GTx-024, MK-2866, S-22) | 아릴프로피오나미드 | GTX, Veru Healthcare[22] | 유방암, 악액질, 근위축, 스트레스성 요실금[22] | 3단계[22] |  |
| DT-200 (GLPG-0492) | Imidazolidine-2,4-dione | 프로스켈리아, 아카시 테라퓨틱스, 갈라파고스 NV[23] | 근육이영양증, 악액질[23] | 1단계[19][23] |  |
| GSK-971086 | 알[24] 수 없음 | 글락소스미스클라인[24] | 근감소증[24] | 단계 I(중단)[24] | 구조미공개[24] |
| GSK-2849466 | 알[25] 수 없음 | 글락소스미스클라인[25] | 악액질, 심부전[25] | 단계 I(중단)[25] | 구조미공개[25] |
| GSK-2881078 | 인돌 | 글락소스미스클라인[26] | 악액질[26][27] | 2단계[26] |  |
| LGD-2941 (LGD-122941) | 퀴놀리논 | 리간드 제약[28] | 악액질, 성기능장애, 성선기능저하, 폐경, 골다공증[28] | 단계 I(중단)[28] |  |
| LGD-4033 (VK5211, ligandrol) | 피롤리딘벤조니트릴 | 리간드 제약[29] | 고관절 골절, 악액질, 저선량증, 골다공증으로[13][29] 인한 근육 소모 | 2단계[29] |  |
| LY305 | N-아릴하이드록시알킬 | 일라이 릴리[30] | 골다공증[30] | 1단계[30] |  |
| MK-0773 (PF-05314882) | 스테로이드 | GTX, 머크[31] | 근감소증, 골다공증[19][31] | 단계 II(중단)[19][31][32] |  |
| MK-3984 | 벤질프로피오나미드 | 머크 | 근감소증[19] | 1단계[19] |  |
| OPK-88004 (LY-2452473, TT-701) | 인돌 | 일라이 릴리, OPKO[33] | 양성 전립선 비대증, 전립선암의 삶의 질, 발기부전[33][34] | 2단계[33] |  |
| PF-06260414 | 이소퀴놀린 | 화이자[35] | 악액질[35] | 단계 I(중단)[35] |  |
| PS-178990 | 알[19] 수 없음 | 브리스톨-마이어스 스퀴브, 리간드 제약[36] | 그리고 일시정지, 악액질[36][19] | 단계 I(중단)[36][37][19] | 구조미공개[19] |
| Vosilasarm (RAD140, EP0062, testolone) | 페닐록사디아졸 | 엘립시스[38] | 유방암, 골다공증, 근감소증[39] | 단계 I/II[39] |  |
| YK-11 | 스테로이드 | 도호 대학 | 근육 소모[40] | 전임상 |  |
트레스톨론, 디메탄드로론 운데카노에이트 및 11β-메틸-19-노테스토스테론 도데실카보네이트와 같은 특정 동화 스테로이드는 때때로 SARM으로 분류됩니다.[19]
연구 및 치료적 활용 가능성
SARM은 조직 선택성으로 인해 쇠약성 질환을 포함한 다양한 질환을 치료할 수 있는 잠재력을 가지고 있습니다. 그들은 골다공증, 악액질, 양성 전립선 비대증, 스트레스 요실금, 전립선암, 유방암의 치료를 위한 인간 연구에서 조사되었으며 알츠하이머병, 듀첸 근위축증, 성선 기능 저하증 및 남성 피임약의 치료에도 고려되었습니다.[18][6] 2020년[update] 현재 미국 식품의약국에서 치료용으로 승인된 SARM은 없습니다.[18]
대부분의 SARM은 시험관 내 또는 설치류를 대상으로 테스트되었으며 사람을 대상으로 한 제한된 임상 시험이 수행되었습니다.[5][41] 초기 연구는 근육 소모에 초점을 맞췄습니다.[14] 에노보사르 (오스타린)은 가장 잘 연구된 SARM입니다. 제조업체인 GTX Incorporated에 따르면 2020년[update] 현재 1,700명 이상의 사람을 대상으로 매일 1mg에서 18mg의 용량을 포함한 25개의 연구가 수행되었습니다.[42][13] 2020년[update] 현재, 서로 다른 SARM을 구별하는 연구는 거의 없습니다.[5] SARM에 대한 연구의 대부분은 기업에서 수행되었으며 공개되지 않았습니다.[7]
성선기능저하증 및 호르몬대체요법
테스토스테론에 비해 잠재적으로 더 나은 SARM의 부작용 프로파일 때문에, SARM은 저선량증 치료 및 안드로겐 대체 요법에 사용하기 위해 제안되었습니다.[43][18] 1상과 2상 시험은 SARMs enobosarm과 GSK-2881078 (노인과 폐경 후 여성에서) 그리고 OPL-88004 (테스토스테론 수치가 낮은 전립선 암 생존자)가 전립선에 거의 영향을 주지 않으면서 마른 체형과 근육 크기를 증가시킨다는 예비 증거를 제공했습니다. 호르몬 대체 요법에 사용할 수 있는 SARM의 잠재력을 지원합니다.[10] 그러나 SARM은 5α-환원을 통한 안드로겐 강화 및 에스트로겐으로의 방향족화를 포함하여 테스토스테론의 전체 효과를 재현하지 않기 때문에 안드로겐 대체 요법에 사용하기에 이상적이지 않으며 이러한 맥락에서 테스토스테론을 대체할 수 없다고 주장되었습니다.[44][45] 특히 에스트로겐 신호전달은 뼈의 힘을 유지하는 등 정상적인 남성 생리와 건강을 위해 필수적입니다.[46][47]
양성 전립선 비대증
전립선암이 없을 때 전립선이 비대해지는 질환인 양성 전립선 비대증(BPH) 쥐 모델에서 SARMs는 전립선의 무게를 줄였습니다.[41] OPK-88004는 사람을 대상으로 한 2상 시험에 진출했지만, 시험의 1차 종점인 전립선 크기 측정이 어려워 종료됐습니다.[18]
암
SARMs는 유방암의 대부분을 차지하는 AR 및 에스트로겐 수용체(ER) 양성 유방암을 치료하는 데 도움이 될 수 있습니다.[6][48] AAS는 역사적으로 AR 양성 유방암 치료에 성공적으로 사용되었지만, 안드로겐 부작용과 에스트로겐으로의 방향족화(SARM에서는 발생하지 않음)에 대한 우려로 인해 항에스트로겐 치료제 개발 후 단계적으로 중단되었습니다.[48][14] AR 양성 삼중음성유방암(즉, ER-)에 대한 실험은 효능 부족으로 조기에 종료되었지만, enobosam은 2상 연구에서 일부 ER+, AR+ 유방암 환자에서 이점을 보여주었습니다. 면역조직화학에 의해 결정된 AR 양성이 40% 이상인 환자에서 임상적 이익률(CBR)은 80%, 객관적 반응률(ORR)은 48%로 환자들이 진행된 질병을 가지고 있고 많은 사전 치료를 받았다는 점에서 유망하다고 여겨졌습니다.[49][48] 2022년 FDA는 AR+, ER+, HER2- 전이성 유방암에 대해 에노보암에 패스트트랙 지정을 승인했습니다.[50] 보실라살과 같은 다른 SARM은 유방암 환자를 대상으로 한 임상시험에 도달했습니다.[38]
뼈와 근육 소모
2020년[update] 현재 만성 질환자의 근육 소모를 치료하기 위해 승인된 약물은 없으며, 따라서 부작용이 거의 없는 단백 동화 약물에 대한 충족되지 않은 필요성이 있습니다. 악액질과 근감소증(두 가지 유형의 근육 소모) 치료제에 대한 약물 승인을 방해하는 한 가지 측면은 약물의 효능을 입증할 수 있는 결과에 대한 불일치입니다. 여러 임상 실험에서 SARM이 사람의 제지방량을 개선한다는 사실이 밝혀졌지만, 힘과 신체 기능도 개선되는지는 확실하지 않습니다. II상 시험에서 결과를 약속한 후, enobosam의 III상 시험은 제지방량을 증가시키는 것으로 증명되었지만 기능에 있어서 유의미한 개선을 보이지는 않았습니다. 그것과 다른 약물들은 신체적 성능을 증가시킨다는 증거가 부족하여 규제 승인을 거부당했습니다. 기능 저하를 방지하는 것은 식품의약국에 의해 허용되는 최종 목표로 간주되지 않았습니다. 근육 소모가 있는 사람들의 식이 단백질 섭취 및 저항 훈련과 SARM이 어떻게 상호 작용하는지는 알려져 있지 않습니다.[13][18]
골반 바닥의 레베이터 애니 근육이 안드로겐 수용체 밀도가 높다는 점을 감안할 때 유망한 것으로 간주되는 스트레스 요실금에 대한 에노보암의 2상 시험은 최종 결과를 충족하지 못하고 포기되었습니다.[18][14]
뼈의 손실을 감소시킴으로써 작용하는 골다공증에 대한 다른 치료법들과는 달리, SARM은 뼈 조직의 성장을 촉진할 수 있는 가능성을 보여주었습니다. LY305는 인간을 대상으로 한 1상 시험에서 유망한 결과를 보였습니다.[18]
부작용
AAS와 테스토스테론 대체는 의료 사용을 줄이는 많은 부작용을 가지고 있는 반면, SARM은 잘 견디고 무작위 대조 시험에서 경미하고 드문 부작용을 가지고 있습니다.[41] SARM은 때때로 비바이러스성(non-birilizing)이라고 주장됩니다.[18][51] 그러나 실제로 SARM은 잠재적인 바이러스화 효과 측면에서 임상적으로 거의 특성화되지 않았습니다.[5] 어쨌든, SARM은 5α-환원효소의 기질이 아니며 피부, 모낭, 전립선과 같은 5α-환원효소 발현 조직에서 강화되지 않기 때문에 이론적인 수준에서 이들 조직에서 테스토스테론에 비해 안드로겐 강도가 감소할 것으로 예상할 수 있습니다.[52][53] SARM은 에스트로겐으로 방향족화될 수 없으므로 에스트로겐 부작용, 예를 들어 부인유방증을 유발하지 않습니다.[54][18][6] 대부분의 현재 형태의 테스토스테론 대체제와 달리 SARM은 경구 투여가 가능합니다.[6]
SARM 사용은 간 효소 상승과 HDL 콜레스테롤 감소를 유발할 수 있습니다.[54][18] 피부 패치를 통한 경피 투여는 이러한 영향을 줄일 수 있습니다.[18][30] 여러 증례 보고에서 SARM이 레크리에이션으로 사용될 때 간세포 약물 유발 간 손상과 관련이 [55]있지만 의료용으로 위험이 큰지는 알려져 있지 않습니다.[41][6] SARMs가 심혈관 사건의 위험을 증가시키는지 여부는 알려져 있지 않습니다.[41][6] SARM은 테스토스테론 대체보다 혈중 지질 프로필에 미치는 영향이 적으며, 안드로겐 유도 HDL 감소가 심혈관 위험을 증가시키는지는 알려져 있지 않으며, SARM은 인슐린 민감도를 증가시키고 중성지방을 낮춥니다.[6][13]
테스토스테론보다 시상하부-뇌하수체-고나달 축(HPG 축)의 억제를 덜 일으키지만, 연구에 따르면 성선 자극 호르몬, 유리 및 총 테스토스테론 및 SHBG는 SARM 사용으로 남성에서 화합물 및 용량 의존적 방식으로 감소될 수 있습니다.[5][13] 일반적으로 SHBG는 총 테스토스테론 및 총 콜레스테롤과 함께 감소되는 반면 헤마토크릿은 증가됩니다. 대부분의 연구에서 난포자극호르몬(FSH), 황체형성호르몬(LH), 전립선특이항원, 에스트라디올, DHT 수치가 변하지 않는다는 것을 발견했습니다.[41] 조사된 SARM 중 enobosarm은 임상 시험에서 사용된 것보다 훨씬 높은 용량에서도 성선 자극 호르몬을 가장 덜 억제하는 것 중 하나입니다. SARM을 사용하는 여성에서 HPG 축이 어떻게 영향을 받는지는 알려져 있지 않습니다.[5][13] SARM이 남성 피임약으로 잠재적으로 유용한 것은 성선 자극 호르몬 FSH와 LH를 억제하는 SARM의 효과 때문입니다.[56]
비의료용
의약품 연구 외에 SARMs는 소규모 실험실에서 생산되는 회색 시장 물질이며 종종 인간이 섭취하지 않는 것으로 추정되는 연구용 화학물질로 판매됩니다.[5][57][58] 사람이 소비할 수 있도록 SARM을 판매하는 것은 일부 국가에서 불법이며, 미국에서[59] 형사 유죄 판결을 받았으며 1989년 호주의 치료용품법에 따라 부과된 사상 최대의 벌금으로 이어졌습니다.[60] SARM은 인터넷에서 쉽게 구입할 수 있지만, 한 연구에 따르면 온라인에서 SARM으로 광고되는 제품의 대부분이 라벨이 잘못 부착되어 있는 것으로 나타났습니다. 사용에 대한 일화와 가이드는 온라인과 소셜 미디어에서도 확인할 수 있습니다.[61][54][6] 일부 화합물은 다른 작용 메커니즘을 가지고 있음에도 불구하고 일반적으로 SARM으로 레크리에이션용으로 판매됩니다. 성장호르몬 분비를 증가시키는 이부타모렌(MK-677); PPARβ/ δ의 작용제로 작용하는 운동 모방체 GW501516(카다린); 일주기 리듬에 작용하는 Rev-Erb의 작용제 SR9009(스테나볼릭) 등이 이들 물질입니다.
SARM은 특히 미국, 유럽 및 기타 서구 국가에서 [6]동화작용과 안드로겐 효과의 부족으로 인해 보디빌더 및 경쟁력 있는 운동선수들이 사용합니다.[54] SARMs의 조합에 대한 연구는 아직 없지만, SARMs를 사용하는 일부 사람들은 여러 개의 SARMs를 오락적으로 조합하거나 다른 화합물과 함께 SARM을 복용하기도 합니다. 그러나 사용된 용량은 임상시험의 용량을 초과하는 경우가 많습니다. SARMs에서 얻은 무지방 질량은 일반적으로 적당한 양의 테스토스테론 유도체로 얻은 질량보다 낮습니다.[5] SARM 사용자들을 대상으로 한 한 연구에 따르면, 90% 이상이 사용에 만족했고, 64%는 대다수가 부작용을 경험했음에도 불구하고 SARM을 다시 복용할 것이라고 합니다.[63]
SARMs는 2008년 세계반도핑기구에 의해 금지되었습니다.[5] SARMs는 섭취 후 소변과 모발에서 검출할 수 있습니다.[64] WADA는 2010년 SARMs에 대한 첫 번째 불리한 분석 결과를 보고했고 그 이후로 양성 반응의 수가 증가했습니다. 가장 일반적으로 검출되는 SARMs는 enobosarm(오스타린)과 LGD-4033(리간드롤)입니다.[65][66] NFL, NBA, UFC, NCAA, 그리고 올림픽에 출전하는 선수들이 양성 반응을 보였습니다.[55] SARM이 운동 경기력에 어떤 영향을 미치는지에 대한 증거는 제한적입니다.[67]
용어.
SARM은 때때로 "비스테로이드성 안드로겐"[1][68]이라고도 하지만, 모든 SARM이 비스테로이드성 구조인 것은 아니며 스테로이드성 SARM도 존재합니다.[19] 1998년에 발견된 최초의 SARM은 처음에는 비스테로이드성 안드로겐으로 불렸습니다.[69] 그러나 1999년에 이르러 이러한 비스테로이드성 안드로겐 수용체 작용제의 선택적 에스트로겐 수용체 조절제(SERM)-유사 혼합작용제-항제 및 조직 선택적 활성에 기초하여 "선택적 안드로겐 수용체 조절제" 또는 "SARM"이라는 용어가 도입되어 채택되기 시작했습니다.[70] 널리 사용되고 있음에도 불구하고, "선택적 안드로겐 수용체 조절제"라는 용어는 정확한 약리학적 설명보다는 오해의 소지가 있는 의약품 마케팅 용어라고 주장하는 데이비드 헨델스만과 같은 일부 저자들에 의해 비판을 받아 왔습니다.[44] 그는 또한 이전에 단백 동화 스테로이드의 경우에 주장된 바와 같이 SARM이 소위 안드로겐성 또는 바이러스화 효과로부터 단백 동화 효과를 분리한다는 개념을 비판했습니다.[44][71][72][73]
참고문헌
- ^ a b Tauchen J, Jurášek M, Huml L, Rimpelová S (February 2021). "Medicinal Use of Testosterone and Related Steroids Revisited". Molecules. 26 (4): 1032. doi:10.3390/molecules26041032. PMC 7919692. PMID 33672087.
SARMs are a novel group of compounds developed to selectively augment anabolic effects in muscles and bones, while avoiding undesirable androgenic effects in skin, larynx, and reproductive organs. The majority of these compounds lack the structural functionalities of the original anabolic steroids and are sometimes termed nonsteroidal androgens. It was hoped that these agents could be used in cases where conventional anabolic steroids produced undesirable side-effects, such as virilization in women and prostate hyperplasia in men [67]. Despite the enormous effort that has been expended in the development of selective anabolic agents, the androgenic effect is very hard to remove completely and many of the currently developed SARMs still do have some androgenic activity.
- ^ Koh B (22 March 2013). "Anti-doping agency warns cheats on the health risks of Endurobol". The Conversation. Retrieved 4 September 2023.
- ^ Mohler ML, Sikdar A, Ponnusamy S, Hwang DJ, He Y, Miller DD, Narayanan R (February 2021). "An Overview of Next-Generation Androgen Receptor-Targeted Therapeutics in Development for the Treatment of Prostate Cancer". International Journal of Molecular Sciences. 22 (4): 2124. doi:10.3390/ijms22042124. PMC 7924596. PMID 33672769.
- ^ de Vera IM, Waaninayake US, Burris TP (October 2018). "Structural Insights into Estrogen Receptors and Antiestrogen Therapies". In Zhang X (ed.). Estrogen Receptor and Breast Cancer: Celebrating the 60th Anniversary of the Discovery of ER. Springer International Publishing. ISBN 978-3-319-99350-8.
- ^ a b c d e f g h i j k l m n o p Machek SB, Cardaci TD, Wilburn DT, Willoughby DS (2020). "Considerations, possible contraindications, and potential mechanisms for deleterious effect in recreational and athletic use of selective androgen receptor modulators (SARMs) in lieu of anabolic androgenic steroids: A narrative review". Steroids. 164: 108753. doi:10.1016/j.steroids.2020.108753. ISSN 0039-128X. PMID 33148520. S2CID 225049089.
Sex-specific SARM effects on humans also remain considerably nebulous. SARMs may represent a more tempting option for female recreational use given potential previous tendencies towards less androgenic AAS (i.e. oxandrolone) [103]. Regardless, as the latter still imposes risk for permanent masculinization and hepatotoxicity, SARMs are largely uncharacterized for female-specific impacts.
- ^ a b c d e f g h i j k l Solomon ZJ, Mirabal JR, Mazur DJ, Kohn TP, Lipshultz LI, Pastuszak AW (2019). "Selective Androgen Receptor Modulators: Current Knowledge and Clinical Applications". Sexual Medicine Reviews. 7 (1): 84–94. doi:10.1016/j.sxmr.2018.09.006. PMC 6326857. PMID 30503797.
- ^ a b c Jasuja R, Zacharov MN, Bhasin S (2012). "The state-of-the-art in the development of selective androgen receptor modulators". Testosterone: Action, Deficiency, Substitution (4 ed.). Cambridge University Press. pp. 459–460. ISBN 978-1-107-01290-5.
- ^ a b c d Bhasin S, Jasuja R (2009). "Selective Androgen Receptor Modulators (SARMs) as Function Promoting Therapies". Current Opinion in Clinical Nutrition and Metabolic Care. 12 (3): 232–240. doi:10.1097/MCO.0b013e32832a3d79. ISSN 1363-1950. PMC 2907129. PMID 19357508.
- ^ Thevis M, Schänzer W (2010). "Synthetic anabolic agents: steroids and nonsteroidal selective androgen receptor modulators". Handb Exp Pharmacol. Handbook of Experimental Pharmacology. 195 (195): 99–126. doi:10.1007/978-3-540-79088-4_5. ISBN 978-3-540-79087-7. PMID 20020362.
One of the first synthetic analogs to testosterone prepared by the Noble laureate Ruzicka was 17α-methyltestosterone (Ruzicka et al. 1935).
- ^ a b c d Bhasin S, Krishnan V, Storer TW, Steiner M, Dobs AS (2023). "Androgens and Selective Androgen Receptor Modulators to Treat Functional Limitations Associated With Aging and Chronic Disease". The Journals of Gerontology: Series A. 78 (Supplement_1): 25–31. doi:10.1093/gerona/glad027. PMC 10272983. PMID 37325955.
- ^ Katzung BG (2017). Basic and Clinical Pharmacology 14th Edition. McGraw Hill Professional. p. 741. ISBN 978-1-259-64116-9.
- ^ a b c d Temerdashev AZ, Dmitrieva EV (2020). "Methods for the Determination of Selective Androgen Receptor Modulators". Journal of Analytical Chemistry. 75 (7): 835–850. doi:10.1134/S1061934820070187. S2CID 220398030.
- ^ a b c d e f g Fonseca GW, Dworatzek E, Ebner N, Von Haehling S (2020). "Selective androgen receptor modulators (SARMs) as pharmacological treatment for muscle wasting in ongoing clinical trials". Expert Opinion on Investigational Drugs. 29 (8): 881–891. doi:10.1080/13543784.2020.1777275. PMID 32476495. S2CID 219174372.
- ^ a b c d e f g h Narayanan R, Coss CC, Dalton JT (April 2018). "Development of selective androgen receptor modulators (SARMs)". Molecular and Cellular Endocrinology. 465: 134–142. doi:10.1016/j.mce.2017.06.013. PMC 5896569. PMID 28624515.
- ^ Kicman AT (June 2008). "Pharmacology of anabolic steroids". British Journal of Pharmacology. 154 (3): 502–521. doi:10.1038/bjp.2008.165. PMC 2439524. PMID 18500378.
- ^ a b Smith CL, O'Malley BW (February 2004). "Coregulator function: a key to understanding tissue specificity of selective receptor modulators". Endocrine Reviews. 25 (1): 45–71. doi:10.1210/er.2003-0023. PMID 14769827.
- ^ a b c Tan MH, Li J, Xu HE, Melcher K, Yong EL (January 2015). "Androgen receptor: structure, role in prostate cancer and drug discovery". Acta Pharmacologica Sinica. 36 (1): 3–23. doi:10.1038/aps.2014.18. PMC 4571323. PMID 24909511.
- ^ a b c d e f g h i j k l Christiansen AR, Lipshultz LI, Hotaling JM, Pastuszak AW (March 2020). "Selective androgen receptor modulators: the future of androgen therapy?". Translational Andrology and Urology. 9 (Suppl 2): S135–S148. doi:10.21037/tau.2019.11.02. ISSN 2223-4683. PMC 7108998. PMID 32257854.
- ^ a b c d e f g h i j k l m n o p Xie Y, Tian Y, Zhang Y, Zhang Z, Chen R, Li M, Tang J, Bian J, Li Z, Xu X (February 2022). "Overview of the development of selective androgen receptor modulators (SARMs) as pharmacological treatment for osteoporosis (1998-2021)". Eur J Med Chem. 230: 114119. doi:10.1016/j.ejmech.2022.114119. PMID 35063736. S2CID 245941791.
- ^ a b c "Andarine". AdisInsight. Springer Nature Switzerland AG.
- ^ a b c "Arcarine". Synapse. PatSnap.
- ^ a b c "Enobosarm - Veru Healthcare". AdisInsight. Springer Nature Switzerland AG.
- ^ a b c "DT 200". AdisInsight. Springer Nature Switzerland AG.
- ^ a b c d e "GSK 971086". AdisInsight. Springer Nature Switzerland AG.
- ^ a b c d e "GSK 2849466". AdisInsight. Springer Nature Switzerland AG.
- ^ a b c "GSK 2881078". AdisInsight. Springer Nature Switzerland AG.
- ^ Mohan D, Rossiter H, Watz H, Fogarty C, Evans RA, Man W, Tabberer M, Beerahee M, Kumar S, Millns H, Thomas S, Tal-Singer R, Russell AJ, Holland MC, Akinseye C, Neil D, Polkey MI (1 March 2023). "Selective androgen receptor modulation for muscle weakness in chronic obstructive pulmonary disease: a randomised control trial". Thorax. 78 (3): 258–266. doi:10.1136/thorax-2021-218360. ISSN 0040-6376. PMC 9985744. PMID 36283827.
- ^ a b c "LGD 2941". AdisInsight. Springer Nature Switzerland AG.
- ^ a b c "VK 5211". AdisInsight. Springer Nature Switzerland AG.
- ^ a b c d Krishnan V, Patel NJ, Mackrell JG, Sweetana SA, Bullock H, Ma YL, Waterhouse TH, Yaden BC, Henck J, Zeng QQ, Gavardinas K, Jadhav P, Saeed A, Garcia-Losada P, Robins DA, Benson CT (2018). "Development of a selective androgen receptor modulator for transdermal use in hypogonadal patients". Andrology. 6 (3): 455–464. doi:10.1111/andr.12479. PMID 29527831. S2CID 3858281.
- ^ a b c "MK 0773". AdisInsight. Springer Nature Switzerland AG.
- ^ Papanicolaou DA, Ather SN, Zhu H, Zhou Y, Lutkiewicz J, Scott BB, Chandler J (2013). "A phase IIA randomized, placebo-controlled clinical trial to study the efficacy and safety of the selective androgen receptor modulator (SARM), MK-0773 in female participants with sarcopenia". J Nutr Health Aging. 17 (6): 533–43. doi:10.1007/s12603-013-0335-x. PMID 23732550. S2CID 42439768.
- ^ a b c "OPK 88004". AdisInsight. Springer Nature Switzerland AG.
- ^ Pencina KM, Burnett AL, Storer TW, Guo W, Li Z, Kibel AS, Huang G, Blouin M, Berry DL, Basaria S, Bhasin S (2021). "A Selective Androgen Receptor Modulator (OPK-88004) in Prostate Cancer Survivors: A Randomized Trial". The Journal of Clinical Endocrinology & Metabolism. 106 (8): 2171–2186. doi:10.1210/clinem/dgab361. PMC 8277210. PMID 34019661.
- ^ a b c "PF 626414". AdisInsight. Springer Nature Switzerland AG.
- ^ a b c "PS 178990". AdisInsight. Springer Nature Switzerland AG.
- ^ "PS-178990". Synapse. PatSnap.
- ^ a b Lim E, Hamilton E, Palmieri C, Arkenau H, Brook S, Fisher G, Mazur A (1 March 2023). "Abstract OT1-02-02: A phase 1/2 study to evaluate the safety and efficacy of EP0062, an oral Selective Androgen Receptor Modulator (SARM), for the treatment of AR+/HER2-/ER+ advanced breast cancer". Cancer Research. 83 (5_Supplement): OT1–02–02-OT1-02-02. doi:10.1158/1538-7445.SABCS22-OT1-02-02. S2CID 257320030.
- ^ a b "Vosilasarm - Ellipses Pharma". AdisInsight. Springer Nature Switzerland AG.
- ^ Lee SJ, Gharbi A, Shin JE, Jung ID, Park YM (2021). "Myostatin inhibitor YK11 as a preventative health supplement for bacterial sepsis". Biochemical and Biophysical Research Communications. 543: 1–7. doi:10.1016/j.bbrc.2021.01.030. ISSN 0006-291X. PMID 33588136. S2CID 231938058.
- ^ a b c d e f Sigalos JT, Walker DT, Lipschultz LI (2023). "Selective Androgen Receptor Modulators in the Treatment of Hypogonadism and Men's Health". Men's Reproductive and Sexual Health Throughout the Lifespan: An Integrated Approach to Fertility, Sexual Function, and Vitality. Cambridge University Press. p. 266. doi:10.1017/9781009197533.034. ISBN 978-1-009-19755-7.
- ^ Zajac JD, Seeman E, Russell N, Ramchand SK, Bretherton I, Grossmann M, Davey RA (2020). "Testosterone". Encyclopedia of Bone Biology. Academic Press. p. 545. ISBN 978-0-12-814082-6.
- ^ Zaveri NT, Murphy BJ (2007). "Nuclear hormone receptors". In Taylor JB, Triggle DJ (eds.). Comprehensive Medicinal Chemistry II. Elsevier. pp. 993–1036. doi:10.1016/B0-08-045044-X/00063-8. ISBN 9780080450445.
A SARM for the treatment of hypogonadism or osteoporosis would be an AR agonist in the muscle and bone, with minimal hypertrophic agonist effects in the prostate.
- ^ a b c Handelsman DJ (July 2022). "History of androgens and androgen action". Best Pract Res Clin Endocrinol Metab. 36 (4): 101629. doi:10.1016/j.beem.2022.101629. PMID 35277356.
The next invention was that of the first non-steroidal androgen by Dalton et al. [111] in 1998, six decades after the first non-steroidal estrogen [112]. This creates a new class of non-steroidal synthetic androgen, often termed Specific Androgen Receptor Modulators (SARM), a misleading marketing term rather than an accurate pharmacological description [113,114], usurping a speculative but unsound analogy with Specific Estrogen Receptor Modulators (SERM). [...] none of the non-steroidal androgens under development [116,117] are marketed by 2021. Yet hope springs eternal for this new attempt to separate anabolic from androgenic properties of androgens to facilitate marketing for muscle wasting and other selective effects of testosterone.
- ^ Feingold KR, et al. (5 October 2020). "Androgen Physiology, Pharmacology, Use and Misuse". Endotext. PMID 25905231.
These features suggest that non-steroidal androgens have potential for development into pharmacologic androgen therapy regimens as tissue-selective mixed or partial androgen agonists ("selective androgen receptor modulators", SARM) (419, 718). Conversely, they are not ideal for androgen replacement therapy where the full spectrum of testosterone effects including aromatization is idealy required, especially for tissues such as the brain (148, 159) and bone (153) where aromatization is a prominent feature of testosterone action.
- ^ Russell N, Grossmann M (July 2019). "MECHANISMS IN ENDOCRINOLOGY: Estradiol as a male hormone". Eur J Endocrinol. 181 (1): R23–R43. doi:10.1530/EJE-18-1000. PMID 31096185.
- ^ Cooke PS, Nanjappa MK, Ko C, Prins GS, Hess RA (July 2017). "Estrogens in Male Physiology". Physiol Rev. 97 (3): 995–1043. doi:10.1152/physrev.00018.2016. PMC 6151497. PMID 28539434.
- ^ a b c Dai C, Ellisen LW (2023). "Revisiting Androgen Receptor Signaling in Breast Cancer". The Oncologist. 28 (5): 383–391. doi:10.1093/oncolo/oyad049. PMC 10166165. PMID 36972361.
- ^ Palmieri C, Linden HM, Birrell S, Lim E, Schwartzberg LS, Rugo HS, Cobb PW, Jain K, Vogel CL, O'Shaughnessy J, Johnston SR, Getzenberg RH, Barnette KG, Steiner MS, Brufsky A, Overmoyer B (2021). "Efficacy of enobosarm, a selective androgen receptor (AR) targeting agent, correlates with the degree of AR positivity in advanced AR+/estrogen receptor (ER)+ breast cancer in an international phase 2 clinical study". Journal of Clinical Oncology. 39 (15_suppl): 1020. doi:10.1200/JCO.2021.39.15_suppl.1020. ISSN 0732-183X. S2CID 236407030.
- ^ "FDA Grants Fast Track Designation to Enobosarm in AR+, ER+, HER2- Metastatic Breast Cancer". Cancer Network. 10 January 2022. Retrieved 27 August 2023.
- ^ Zhang X, Sui Z (February 2013). "Deciphering the selective androgen receptor modulators paradigm". Expert Opin Drug Discov. 8 (2): 191–218. doi:10.1517/17460441.2013.741582. PMID 23231475. S2CID 2584722.
- ^ Gao W, Dalton JT (February 2007). "Ockham's razor and selective androgen receptor modulators (SARMs): are we overlooking the role of 5α-reductase?". Mol Interv. 7 (1): 10–3. doi:10.1124/mi.7.1.3. PMC 2040232. PMID 17339601.
- ^ Yarrow JF, McCoy SC, Borst SE (May 2012). "Intracrine and myotrophic roles of 5α-reductase and androgens: a review". Med Sci Sports Exerc. 44 (5): 818–26. doi:10.1249/MSS.0b013e31823bfcbf. PMC 8382298. PMID 21988936.
- ^ a b c d Xie Y, Tian Y, Zhang Y, Zhang Z, Chen R, Li M, Tang J, Bian J, Li Z, Xu X (15 February 2022). "Overview of the development of selective androgen receptor modulators (SARMs) as pharmacological treatment for osteoporosis (1998–2021)". European Journal of Medicinal Chemistry. 230: 114119. doi:10.1016/j.ejmech.2022.114119. ISSN 0223-5234. PMID 35063736. S2CID 245941791.
- ^ a b Hahamyan H, Gould H, Gregory A, Dodson C, Gausden E, Voos J, Calcei J, Vasireddi N (2023). "Poster 390: Systematic Review of SARMs Abuse in Athletes". Orthopaedic Journal of Sports Medicine. 11 (7_suppl3): 2325967123S00352. doi:10.1177/2325967123S00352. ISSN 2325-9671. PMC 10392554. S2CID 260375399.
- ^ Bhasin S (2015). "Selective Androgen Receptor Modulators as Function Promoting Therapies". The Journal of Frailty & Aging. 4 (3): 121–122. doi:10.14283/jfa.2015.65. ISSN 2260-1341. PMC 6039107. PMID 27030938.
- ^ Sobolevsky T, Ahrens B (2021). "High-throughput liquid chromatography tandem mass spectrometry assay as initial testing procedure for analysis of total urinary fraction". Drug Testing and Analysis. 13 (2): 283–298. doi:10.1002/dta.2917. ISSN 1942-7603. PMID 32852861. S2CID 221347916.
- ^ Turnock DL, Gibbs DN (2023). "Click, click, buy: The market for novel synthetic peptide hormones on mainstream e-commerce platforms in the UK". Performance Enhancement & Health. 11 (2): 100251. doi:10.1016/j.peh.2023.100251. ISSN 2211-2669. S2CID 257706930.
- ^ Oberheiden N (26 June 2023). "The FDA Continues to Crack Down on SARM Manufacturing and Distribution". Federal Lawyer. Retrieved 13 October 2023.
- ^ Jacobson HL, Zhang A, Forrai Z (3 August 2021). "Failure to remove unlawful advertising attracts $12 million penalty". Lexology. Retrieved 13 October 2023.
- ^ Hahamyan HA, Vasireddi N, Voos JE, Calcei JG (2023). "Social media's impact on widespread SARMs abuse". The Physician and Sportsmedicine. 51 (4): 291–293. doi:10.1080/00913847.2022.2078679. ISSN 0091-3847. PMID 35574698. S2CID 248812455.
- ^ Handschin C (2016). "Caloric restriction and exercise "mimetics: Ready for prime time?". Pharmacological Research. 103: 158–166. doi:10.1016/j.phrs.2015.11.009. PMC 4970791. PMID 26658171.
- ^ Efimenko IV, Valancy D, Dubin JM, Ramasamy R (2022). "Adverse effects and potential benefits among selective androgen receptor modulators users: a cross-sectional survey". International Journal of Impotence Research. 34 (8): 757–761. doi:10.1038/s41443-021-00465-0. ISSN 1476-5489. PMID 34471228. S2CID 237378326.
- ^ Kintz P, Ameline A, Gheddar L, Raul J (2019). "LGD-4033, S-4 and MK-2866 – Testing for SARMs in hair: About 2 doping cases". Toxicologie Analytique et Clinique. 31 (1): 56–63. doi:10.1016/j.toxac.2018.12.001. ISSN 2352-0078.
- ^ "Selektive Androgenrezeptor-Modulatoren (SARMs)". Institut für Biochemie, Deutsche Sporthochschule Köln (in German). Retrieved 1 September 2023.
- ^ Kintz P (5 January 2022). "The forensic response after an adverse analytical finding (doping) involving a selective androgen receptor modulator (SARM) in human athlete". Journal of Pharmaceutical and Biomedical Analysis. 207: 114433. doi:10.1016/j.jpba.2021.114433. ISSN 1873-264X. PMID 34715583. S2CID 240229684.
- ^ Warrier AA, Azua EN, Kasson LB, Allahabadi S, Khan ZA, Mameri ES, Swindell HW, Tokish JM, Chahla J (2023). "Performance-Enhancing Drugs in Healthy Athletes: An Umbrella Review of Systematic Reviews and Meta-analyses". Sports Health: A Multidisciplinary Approach. doi:10.1177/19417381231197389. ISSN 1941-7381. PMID 37688400. S2CID 261620672.
- ^ Brown TR (December 2004). "Nonsteroidal selective androgen receptors modulators (SARMs): designer androgens with flexible structures provide clinical promise". Endocrinology. 145 (12): 5417–9. doi:10.1210/en.2004-1207. PMID 15545403.
- ^ Dalton JT, Mukherjee A, Zhu Z, Kirkovsky L, Miller DD (March 1998). "Discovery of nonsteroidal androgens". Biochem Biophys Res Commun. 244 (1): 1–4. doi:10.1006/bbrc.1998.8209. PMID 9514878.
- ^ Negro-Vilar A (October 1999). "Selective androgen receptor modulators (SARMs): a novel approach to androgen therapy for the new millennium". J Clin Endocrinol Metab. 84 (10): 3459–62. doi:10.1210/jcem.84.10.6122. PMID 10522980.
- ^ Handelsman DJ (May 2011). "Commentary: androgens and "anabolic steroids": the one-headed janus". Endocrinology. 152 (5): 1752–4. doi:10.1210/en.2010-1501. PMID 21511988.
Although development of the first nonsteroidal androgens (17, 18) as candidate selective AR modulators (19) raises hope of resurrecting this defunct term (20), prereceptor activation mechanisms cannot apply to nonsteroidal androgens, and the singular AR lacks a dual drive mechanism of the other paired sex steroid receptors. Consequently, it is not surprising that available knowledge (21) provides only slender hope that this failed, and probably false, dichotomy will now succeed through a renewed search guided by the same in vivo bioassay.
- ^ Handelsman DJ (July 2021). "Androgen Misuse and Abuse". Endocr Rev. 42 (4): 457–501. doi:10.1210/endrev/bnab001. PMID 33484556.
However, a third major quest, for the development of a nonvirilizing androgen ("anabolic steroid") suitable for use in women and children, based on dissociating the virilizing from the anabolic effects of androgens failed comprehensively (36). This failure is now understood as being due to the discovery of a singular androgen receptor (AR) together with the misinterpretation of nonspecific whole animal androgen bioassays employed to distinguish between anabolic and virilizing effects (37). The term "androgen" is used herein for both endogenous and synthetic androgens including references to chemicals named elsewhere as "anabolic steroids," "anabolic-androgenic steroids," or "specific AR modulators" (SARM), which continue to make an obsolete and oxymoronic distinction between virilizing and anabolic effects of androgens where there is no difference (36).
- ^ Handelsman DJ (2012-07-26). "Androgen therapy in non-gonadal disease". Testosterone. Cambridge University Press. pp. 372–407. doi:10.1017/cbo9781139003353.018. ISBN 978-1-139-00335-3.
The development of nonsteroidal androgens, marketed as "selective androgen receptor modulators" (SARMs), offers new possibilities for adjuvant pharmacological androgen therapy. In contrast to the full spectrum of androgen effects of testosterone, such SARMs would be pure androgens not subject to tissue-specific activation by aromatization to a corresponding estrogen or to amplification of androgenic potency by 5α-reduction. In this context the endogenous pure androgens nandrolone and DHT can be considered prototype SARMs. SARMs are not the modern embodiment of so-called "anabolic steroids," an outdated term referring to hypothetical but nonexistent non-virilizing androgens targeted exclusively to muscle, a failed concept lacking biological proof of principle (Handelsman 2011).


