시프로테론
Cyproterone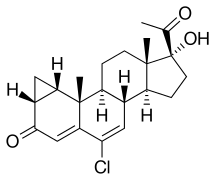 | |
| 임상 데이터 | |
|---|---|
| 기타 이름 | SH-80881; SH-881; NSC-758636; 1α, 2α-메틸렌-6-클로로-17α-히드록시-γ-프로게스테론6; 1α, 2α-메틸렌-6-클로로-17α-히드록시프레그나-4, 6-디엔-3, 20-디온 |
| 루트 행정부. | 입으로, 국소적으로 |
| 약물 클래스 | 스테로이드 항안드로겐 |
| ATC 코드 | |
| 식별자 | |
| |
| CAS 번호 | |
| PubChem CID | |
| 켐스파이더 | |
| 유니 | |
| 첸블 | |
| CompTox 대시보드 (EPA ) | |
| ECHA 정보 카드 | 100.218.313 |
| 화학 및 물리 데이터 | |
| 공식 | C22H27클론O3 |
| 몰 질량 | 374.91 g/g−1/sqm |
| 3D 모델(JSmol) | |
| |
| |
| (표준) | |
개발 코드명 SH-80881로도 알려진 사이프로테론은 스테로이드 항안드로겐으로 1960년대와 1970년대에 연구되었지만 의학용으로 [1][2][3]도입된 적이 없다.시프로테론 대신 도입된 시프로테론 아세테이트(CPA), 항안드로겐, 프로게스틴, 항나드로핀의 유사체이며 의약품으로 [1][2]널리 사용되고 있다.시프로테론과 CPA는 최초로 개발된 [4]항안드로겐 중 하나였다.
시프로테론이라는 용어는 종종 아세테이트 시프로테론의 동의어 및 줄임말로 사용되며, 이 용어가 발생할 때 거의 항상 혼동스럽게 언급되는 것은 CPA이며 실제로 시프로테론이 아님을 명확히 하는 것이 중요하다.CPA와 달리 시프로테론 자체는 의료용으로 도입된 적이 없기 때문에 의약품으로 사용할 수 없다.
약리학
약역학
항안드로겐 활성
시프로테론은 CPA와 유사하게 강력한 항안드로겐이다.[5][6]그러나 CPA에 [6]비해 안드로겐 수용체(AR)의 길항제로서의 효력은 약 3배 낮다.CPA와 마찬가지로, 시프로테론은 실제로 AR의 약한 부분 작용제이며, 따라서 일부 맥락에서 [7]항안드로겐 및 안드로겐 활성을 모두 가질 가능성이 있다.CPA와 달리, 시프로테론은 순수한[3] 항안드로겐이며 사실상 프로게스토겐 [8][9][10][11]활성이 없다.따라서 항원도트로핀이 아니며 실제로 남성에서 성나도트로핀을 발생시켜 시상하부-하수체-성선축에 [5][11][12]대한 AR 매개 음성 피드백의 저해에 의해 성나도트로핀과 테스토스테론 수치를 증가시킨다.
CPA와 달리 수컷 설치류에서 시프로테론은 수컷 설치류에서 고환 무게를 증가시키고, A형 정조세포의 총 수를 증가시키며, Sertoli [13]세포의 총 수를 증가시키고, Leydig 세포를 과자극하며, 정조세포 형성에 거의 영향을 미치지 않는 것으로 밝혀졌다.반대로,[12] 수컷 설치류의 경우 정자 형성이 억제되고 보조적인 성선 무게(예: 전립선, 정낭)와 생식력이 현저하게 감소하는 것으로 보고되었다. 그러나 치료 중단 후 변화에서 빠르게 회복되었다.어느 경우든 CPA는 효과적인 [14]항불균제가 아닌 것으로 알려져 있다.또한 CPA와 달리 시프로테론은 프로게스토겐 및 항나토픽 활성이 없기 때문에 여성의 [3][15]배란을 억제하지 않는다.
기타 액티비티
CPA와 시프로테론은 모두 약간의 약한 글루코콜티코이드 활성을 가지며 동물의 부신 및 비장의 무게를 억제하며 CPA는 생쥐의 [8][16]프레디손의 약 5분의 1의 효력을 가진다.CPA와 달리 시프로테론은 [6]시험관내 17β-히드록시스테로이드 탈수소효소 및 5α-환원효소의 억제를 보이는 것으로 보인다.CPA와 대조적으로, 시프로테론은 오피오이드 [17]수용체에 대한 친화력을 보이지 않는다.
화학
시프로테론은 1α,2α-메틸렌-6-클로로-17α-히드록시-γ-프로게스테론6 또는 1α,2α-메틸렌-6-클로로-17α-히드록시프레그나-4,6-디엔-3,20-디온으로도 알려져 있으며, [1][2]프로게스테론의 유도체이다.이는 CPA의 [1][2]유리 알코올 또는 17α-탈아세틸화 유사체입니다.
역사
시프로테론은 CPA와 함께 [18]1962년에 처음 특허를 받았으며 1963년과 1965년에 [1]후속 특허를 받았다.1967년에서 [19][20]1972년 사이에 임상적으로 연구되었다.CPA와 달리, 의약품은 의료용으로 [1][2]판매된 적이 없었다.시프로테론은 최초로 [21]개발된 순수 항안드로겐이었으며 스테로이드성 항안드로겐 벤로테론, BOMT 및 비스테로이드성 항안드로겐 플루타미드를 [4]포함한 이 등급의 예를 밀접하게 따랐다.
사회와 문화
일반명
시프로테론은 그 [1][2]약과 그것의 총칭이다.개발 코드명 SH-80881 [1][2]및 SH-881로도 알려져 있습니다.
조사.
임상 연구에서 시프로테론은 CPA보다 훨씬 덜 강력하고 항안드로겐으로서 효과가 있는 것으로 확인되었으며, 이는 수반성 항안드로겐 [3]작용의 결여로 인해 상당한 부분일 가능성이 있다.시프로테론은 비에리히(1970, 1971)에 의해 성조숙증 치료제로 연구되었지만 유의미한 개선은 [22]관찰되지 않았다.남성의 경우, 100mg/일 시프로테론은 여드름 치료에 다소 비효율적인 것으로 입증되었으며, 이는 남성에서 시프로테론의 프로고나트로픽 효과 및 항안드로겐 [3][23]활성의 반작용과 관련이 있는 것으로 가정되었다.그러나 테스토스테론 수치가 훨씬 낮고 약물이 프로고나도트로픽 활성이 없는 여성의 경우 치료 [3]시작 후 2-4주 이내에 모든 환자의 피지 생성을 감소시키는 데 하루 100~200mg/200mg의 경구 시프로테론이 효과적이었다.반면 국소 시프로테론은 훨씬 덜 효과적이었고 [3]위약을 거의 능가하지 않았다.
또 다른 연구는 안드로겐증이 [3]있는 여성의 피지 생성을 감소시키는 시프로테론 100mg/일 실망스러운 결과를 보여주었다.마찬가지로, 이 약물은 여성의 다모증 치료에서 실망스러운 결과를 보였으며, 일부 사례에서만 뚜렷한 [3]탈모가 발생했다.같은 연구에서 여드름 감소는 더 좋았지만 CPA에 의해 생성된 여드름 감소에 비해 현저히 떨어졌으며 지루 개선만이 [3]만족스러운 것으로 간주되었다.시프로테론에 경구 피임약을 첨가한 결과 여드름과 지루증이 시프로테론에만 [3]비해 다소 개선되었다.제이콥스(1979)에 따르면, "사이프로테론은 여기서 [24]논할 수 없는 이유로 임상적 가치가 없는 것으로 입증되었다.어떤 경우든, 시프로테론은 하루에 [3]최대 300mg의 용량으로 환자에 의해 잘 내성이 있다.
레퍼런스
- ^ a b c d e f g h J. Elks (14 November 2014). The Dictionary of Drugs: Chemical Data: Chemical Data, Structures and Bibliographies. Springer. pp. 339–. ISBN 978-1-4757-2085-3.
- ^ a b c d e f g Index Nominum 2000: International Drug Directory. Taylor & Francis US. 2000. p. 289. ISBN 978-3-88763-075-1. Retrieved 29 May 2012.
- ^ a b c d e f g h i j k l Constantin E. Orfanos; Rudolf Happle (1990). Hair and Hair Diseases. Springer Science & Business Media. pp. 1197–. ISBN 978-3-642-74612-3.
- ^ a b Schröder, Fritz H.; Radlmaier, Albert (2009). "Steroidal Antiandrogens". In V. Craig Jordan; Barrington J. A. Furr (eds.). Hormone Therapy in Breast and Prostate Cancer. Humana Press. pp. 325–346. doi:10.1007/978-1-59259-152-7_15. ISBN 978-1-60761-471-5.
The progestational effect [of CPA] is linked to the presence of the acetyl group at position C17 of the steroid. Consequently, the free alcohol of CPA, cyproterone, which lacks the acetyl group, is devoid of progestational properties. However, it still exerts antiandrogenic activity, although less pronounced than CPA. Consequently, cyproterone was the first compound falling into the nowadays well-known class of pure antiandrogens.
- ^ a b Moltz, L.; Römmler, A.; Schwartz, U.; Hammerstein, J. (1978). "Effects of Cyproterone Acetate (CPA) on Pituitary Gonadotrophin Release and on Androgen Secretion Before and After LH-RH Double Stimulation Tests in Men". International Journal of Andrology. 1 (s2b): 713–719. doi:10.1111/j.1365-2605.1978.tb00518.x. ISSN 0105-6263.
[...] Hammerstein 1977). This consideration is based on the fact that free cyproterone is a potent anti- androgen without antigonadotrophic activity and causes, therefore, an in- crease in gonadotrophins and in androgens (Graf et al. 1974). In [...]
- ^ a b c Giorgi EP, Shirley IM, Grant JK, Stewart JC (1973). "Androgen dynamics in vitro in the human prostate gland. Effect of cyproterone and cyproterone acetate". Biochem. J. 132 (3): 465–74. doi:10.1042/bj1320465. PMC 1177610. PMID 4125095.
Cyproterone (6-chloro-17-hydroxy-1,2α-methylenepregna-4,6-diene-3,20-dione) and cyproterone acetate (17-acetoxy-6-chloro-1,2α-methylene-pregna-4,6-diene-3,20-dione) are powerful anti-androgens, which exert multiple actions in many species. Cyproterone acetate has three times the anti-androgenic potency of cyproterone, and also has some progestational properties (for review, see Neumann et al., 1970). [...] Cyproterone seemed to decrease the activity of 17α-hydroxysteroid dehydrogenase and of 5α-steroid reductase in human prostate in vitro, as it does in testes and liver of rats (Breuer & Hoffmann, 1967; Hoffmann & Breuer, 1968; Denef et al., 1968). Cyproterone acetate did not seem to have any direct effect on the activity of these two enzymes.
- ^ Charles H. Sawyer; Roger A. Gorski (1971). Steroid Hormones and Brain Function. University of California Press. pp. 366–. ISBN 978-0-520-01887-7.
- ^ a b A. Hughes; S. H. Hasan; G. W. Oertel; H. E. Voss; F. Bahner; F. Neumann; H. Steinbeck; K.-J. Gräf; J. Brotherton; H. J. Horn; R. K. Wagner (27 November 2013). Androgens II and Antiandrogens / Androgene II und Antiandrogene. Springer Science & Business Media. pp. 279–. ISBN 978-3-642-80859-3.
The only chemical difference between cyproterone and cyproterone acetate consists of a free or esterified hydroxyl group at C17 but this difference accounts for profound differences in the mechanism of action and possibilities for use in the intact organism. Both steroids are highly active antiandrogens at any route of administration, the acetate has a greater antiandrogenic potency than the free alcohol. With the exception of a slight depressive effect on the adrenals, cyproterone does not have other side-activities unrelated to antiandrogenicity. It has, therefore, been termed "pure antiandrogen". Cyproterone acetate has one major additional activity: it is one of the strongest gestagens that have ever been synthesized [23, 70, 32, 77], [...]
- ^ Hammerstein, J. (1981). "Antiandrogens — Basic Concepts for Treatment". Hair Research. pp. 330–335. doi:10.1007/978-3-642-81650-5_49. ISBN 978-3-642-81652-9.
Contrary to benorterone, free cyproterone, and flutamide, CPA is not a pure anti- androgen. In fact, it is one of the most potent progestogens known and, in comparison to that potency, it is a relatively weak antiandrogen and a still weaker anti- gonadotropin.
- ^ Spona, J.; Schneider, W. H. F.; Bieglmayer, Ch.; Schroeder, R.; Pirker, R. (1979). "Ovulation Inhibition with Different Doses of Levonorgestrel and Other Progestogens: Clinical and Experimental Investigations". Acta Obstetricia et Gynecologica Scandinavica. 58 (s88): 7–15. doi:10.3109/00016347909157223. ISSN 0001-6349. PMID 393050. S2CID 30486799.
Cyproterone which has a very weak biological progestogen potency exhibited low affinity for the progestogen-receptor (Table I).
- ^ a b A. Labhart (6 December 2012). Clinical Endocrinology: Theory and Practice. Springer Science & Business Media. pp. 473–. ISBN 978-3-642-96158-8.
Cyproterone acetate is 250 and 3330 times as potent a progestational agent as progesterone and cyproterone alcohol (10< respectively (Clauberg assay). [...] The pure anti-androgens, such as cyproteron, block the receptors of the negative feedback system. An uninhibited secretion of the releasing factors and an increased production of gonadotropins results, so that the inhibitory effect on the endorgans may finally be overcome by overpoduction of testosterone (Neumann, 1971). Cyproterone acetate, however, with its marked progestational effect, inhibits the release of LH and FSH at the same time and thus has a lasting anti-androgenic effect (Neumann, 1970). Thus, cyproteron leads to an increase in LH, whereas cyproteron acetate inhibits both LH and FSH.
- ^ a b Steinbeck H, Mehring M, Neumann F (1971). "Comparison of the effects of cyproterone, cyproterone acetate and oestradiol on testicular function, accessory sexual glands and fertility in a long-term study on rats". J. Reprod. Fertil. 26 (1): 65–76. doi:10.1530/jrf.0.0260065. PMID 5091295.
- ^ Viguier-Martinez M.C.; Hochereau De Reviers M.T. (1977). "Comparative action of cyproterone and cyproterone acetate on pituitary and plasma gonadotropin levels, the male genital tract and spermatogenesis in the growing rat" (PDF). Annales de Biologie Animale, Biochimie, Biophysique. 17 (6): 1069–1076. doi:10.1051/rnd:19770814.
- ^ Ewing, L L; Robaire, B (1978). "Endogenous Antispermatogenic Agents: Prospects for Male Contraception". Annual Review of Pharmacology and Toxicology. 18 (1): 167–187. doi:10.1146/annurev.pa.18.040178.001123. ISSN 0362-1642. PMID 206192.
Cyproterone (6-chloro-17a-hydroxy-1a,2a-methylene-pregna-4,6-diene-3,20-dione) and cyproterone acetate have received considerable attention as antispermatogenic substances. Cyproterone, which has·only weak antigonadotropic properties, was found to be a poor antispermatogenic agent (42). In contrast, cyproterone acetate, which inhibits gonadotropin secretion, was found to be an antispermatogenic agent (142).
- ^ Stewart, Mary Ellen; Pochi, Peter E. (1978). "Antiandrogens and the Skin". International Journal of Dermatology. 17 (3): 167–179. doi:10.1111/j.1365-4362.1978.tb06057.x. ISSN 0011-9059. PMID 148431. S2CID 43649686.
While CPA alone probably suppresses ovulation, cyproterone, which possesses no progestational activity, does not!8,72
- ^ Broulik PD, Starka L (1975). "Corticosteroid-like effect of cyproterone and cyproterone acetate in mice". Experientia. 31 (11): 1364–5. doi:10.1007/bf01945829. PMID 1204803. S2CID 11452300.
- ^ Gutiérrez M, Menéndez L, Brieva R, Hidalgo A, Baamonde A (1998). "Different types of steroids inhibit [3H]diprenorphine binding in mouse brain membranes". Gen. Pharmacol. 31 (5): 747–51. doi:10.1016/s0306-3623(98)00110-4. PMID 9809473.
- ^ 미국 특허 3,234,093
- ^ Apostolakis, M.; Tamm, J.; Voigt, K.-D. (1967). "Biochemical and Clinical Studies with Cyproterone". European Journal of Endocrinology. 56 (1 Suppl): S56. doi:10.1530/acta.0.056S056. ISSN 0804-4643.
- ^ Walsh PC, Swerdloff RS, Odell WD (1972). "Cyproterone: effect on serum gonadotropins in the male". Endocrinology. 90 (6): 1655–9. doi:10.1210/endo-90-6-1655. PMID 5020316.
- ^ Craig, Jordan V.; Furr, B.J.A. (5 February 2010). Hormone Therapy in Breast and Prostate Cancer. Springer Science & Business Media. pp. 326–. ISBN 978-1-59259-152-7.
- ^ Rager K, Huenges R, Gupta D, Bierich JR (1973). "The treatment of precocious puberty with cyproterone acetate". Acta Endocrinol. 74 (2): 399–408. doi:10.1530/acta.0.0740399. PMID 4270254.
Free cyproterone was first tried as a therapy for precocious puberty by Bierich (1970, 1971). The results, however, did not show any significant improvement.
- ^ Gerhard Raspé (1969). Schering Workshop on Steroid Metabolism: "in vitro versus in vivo.". Pergamon Press. ISBN 9780080175447.
[...] In this investigation a number of normal male volunteers were treated for three weeks with 100 mg free cyproterone per day. Sebum production was measured by the Straufi-Pochi method before treatment and on the 7th, 10th, 11th, 15th, 18th, [...]
- ^ Howard S. Jacobs; Royal College of Obstetricians and Gynaecologists (Great Britain) (1979). Advances in gynaecological endocrinology: proceedings of the Sixth Study Group of the Royal College of Obstetricians and Gynaecologists, 18th and 19th October, 1978. The College. p. 367. ISBN 978-0-87489-225-3.
Limited clinical experience also exists with benorterone, the first anti-androgen tried in man, and with free cyproterone. In the late sixties benorterone was reported to give promising results in 93 androgenized women but was soon withdrawn from clinical trial, mainly because of the development of gynaecomastia in the male. As a big advantage compared with CPA, it was found to be effective not only orally but also topically. Free cyproterone, on the other hand, proved to be without clinical value for reasons that cannot be discussed here. Thus we are left with CPA as the only anti-androgen that is already on the market in several countries.
추가 정보
- A. Hughes; S. H. Hasan; G. W. Oertel; H. E. Voss; F. Bahner; F. Neumann; H. Steinbeck; K.-J. Gräf; J. Brotherton; H. J. Horn; R. K. Wagner (27 November 2013). Androgens II and Antiandrogens / Androgene II und Antiandrogene. Springer Science & Business Media. pp. 241–545. ISBN 978-3-642-80859-3.


