우라늄
Uranium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 우라늄 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 발음 | /j ʊˈ레 ɪ니 əm/ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 외모 | 은회색 금속성; 공기 중에 흩날리는 검은 산화물 코트로 부식됨 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 표준 원자량 Ar°(U) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 주기율표의 우라늄 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자번호 (Z) | 92 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 그룹. | f-블록 그룹(숫자 없음) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 기간 | 7교시 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 블록 | f-block | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전자구성 | [Rn] 5f3 6d1 7s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 쉘당 전자수 | 2, 8, 18, 32, 21, 9, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 물성 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 단계 STP에서 | 단단한 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 융점 | 1405.3 K (1132.2 °C, 2070 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 끓는점 | 4404 K (4131 °C, 7468 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 밀도 (rt 근처) | 19.1g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 액체 상태일 때(m.p.) | 17.3g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 핵융합열 | 9.14kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 기화열 | 417.1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 몰 열용량 | 27.665 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
증기압
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자의 성질 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 산화상태 | -1,[3] +1, +2, +3,[4] +4, +5, +6(암포테릭 산화물) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전기음성도 | 폴링 척도: 1.38 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 이온화 에너지 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자 반지름 | 경험: 오후 156시 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 공유 반지름 | 196±7pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 반데르발스 반지름 | 186pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 기타속성 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 자연발생 | 원시의 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 결정구조 | orthorhombic | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 열팽창 | 13.9 µm/(m⋅K) (at 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 열전도율 | 27.5W(m⋅K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전기저항 | 0.280 µΩ⋅m (at 0 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 자기순서 | 상자성의 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 영률 | 208GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전단탄성률 | 111 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 벌크 모듈러스 | 100GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 음속 가느다란 막대 | 3155 m/s (at 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 포아송비 | 0.23 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 비커스 경도 | 1960-2500 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 브리넬 경도 | 2350–3850 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS 번호 | 7440-61-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 역사 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 명명 | 그리스 하늘의 신 천왕성의 이름을 딴 천왕성 행성의 이름을 따서 만든 것입니다. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 디스커버리 | 마르틴 하인리히 클라프로트 (1789) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1차 격리 | 외젠 멜치오르 펠리고트 (1841) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 우라늄 동위 원소 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
우라늄은 화학 원소로 기호 U와 원자 번호 92를 가지고 있습니다. 주기율표의 악티나이드 계열에 속하는 은회색 금속입니다. 우라늄 원자는 92개의 양성자와 92개의 전자를 가지고 있는데, 그 중 6개가 원자가 전자입니다. 우라늄은 보통 알파입자를 방출함으로써 방사성 붕괴를 합니다. 이 붕괴의 반감기는 서로 다른 동위원소에 따라 159,200년에서 45억년으로 다양하여 지구의 나이를 측정하는 데 유용합니다. 천연 우라늄에서 가장 일반적인 동위 원소는 우라늄-238(중성자 146개)과 우라늄-235(중성자 143개)입니다. 우라늄은 가장 높은 원자량을 가지고 있습니다. 밀도는 납보다 약 70% 높고 금이나 텅스텐보다 약간 낮습니다. 토양, 암석 및 물에서 수 백만 분의 1 이하의 저농도로 자연적으로 발생하며, 우라늄 함유 광물인 우라니나이트에서 상업적으로 추출됩니다.[7]
우라늄의 많은 현대적인 사용은 독특한 핵 특성을 이용합니다. 우라늄-235는 자연적으로 발생하는 유일한 핵분열성 동위원소로 원자력 발전소와 핵무기에 널리 사용됩니다. 그러나 천연 우라늄에 우라늄-235가 적게 존재하기 때문에 (대부분 우라늄-238) 우라늄은 충분한 우라늄-235가 존재하도록 농축을 해야 합니다. 우라늄-238은 빠른 중성자에 의해 핵분열이 가능하고 가임성이 있어 원자로에서 핵분열성 플루토늄-239로 변환될 수 있습니다. 또 다른 핵분열성 동위원소인 우라늄-233은 천연 토륨에서 생산될 수 있으며, 향후 원자력 기술에서 산업적 용도로 사용될 수 있도록 연구됩니다. 우라늄-238은 빠른 중성자로 자발적인 핵분열이나 심지어 유도된 핵분열이 일어날 확률이 작으며, 우라늄-235와 우라늄-233은 느린 중성자의 핵분열 단면적이 훨씬 높습니다. 이러한 동위원소는 충분한 농도에서 지속적인 핵 연쇄 반응을 유지합니다. 이것은 원자로에서 열을 발생시키고 핵무기용 핵분열 물질을 생성합니다. 고갈 우라늄(238U)은 운동 에너지 침투기 및 갑옷 도금에 사용됩니다.[8]
1789년 이 광물 피치블렌드에서 우라늄이 발견된 것은 마틴 하인리히 클라프로트의 공으로, 그는 최근 발견된 이 행성의 이름을 따서 이 새로운 원소의 이름을 천왕성이라고 지었습니다. 외젠-멜치오르 펠리고는 이 금속을 처음으로 분리한 사람이며, 1896년 앙리 베크렐에 의해 이 금속의 방사성 특성이 발견되었습니다. 1934년에 시작된 오토 한, 리세 마이스너, 엔리코 페르미 등의 연구는 원자력 산업과 전쟁에 사용된 최초의 핵무기인 리틀 보이에서 원자력 발전 산업에서 연료로 사용되도록 이끌었습니다. 미국과 소련 간의 냉전 기간 동안 이어진 군비 경쟁은 우라늄 금속과 우라늄에서 추출한 플루토늄-239를 사용한 수만 개의 핵무기를 생산했습니다. 이러한 무기 및 관련 핵 시설의 해체는 다양한 핵 군축 프로그램 내에서 수행되며 수십억 달러의 비용이 듭니다. 핵무기에서 얻은 무기급 우라늄을 우라늄-238로 희석해 원자로 연료로 사용합니다. 이러한 원자로의 개발과 배치는 CO가2 없는 강력한 에너지원이기 때문에 전 세계적으로 계속되고 있습니다. 사용 후 핵연료는 방사성 폐기물을 형성하는데, 대부분 우라늄-238로 구성되어 있으며 건강과 환경에 중대한 영향을 미칩니다.
특성.

우라늄은 은백색의 약한 방사성 금속입니다. 모스 경도는 6으로 유리를 긁기에 충분하며 티타늄, 로듐, 망간 및 니오븀과 거의 동일합니다. 가단성, 연성, 약간 상자성, 강한 전기 양극성 및 불량한 전기 도체입니다.[9][10] 우라늄 금속은 밀도가 19.1g/cm로3 [11]납(11.3g/cm3)[12]보다 밀도가 매우 높지만 텅스텐, 금(19.3g/cm3)보다는 밀도가 약간 낮습니다.[13][14]
우라늄 금속은 온도에 따라 반응성이 증가하면서 거의 모든 비금속 원소와 그 화합물과 반응합니다.[15] 염산과 질산은 우라늄을 녹이지만 염산 이외의 비산화산은 원소를 매우 느리게 공격합니다.[9] 미세하게 나누면 차가운 물과 반응할 수 있고, 공기 중에서는 우라늄 금속에 어두운 산화 우라늄 층이 코팅됩니다.[10] 우라늄 광석은 화학적으로 추출되어 이산화우라늄 또는 산업에서 사용할 수 있는 다른 화학적 형태로 변환됩니다.
우라늄-235는 핵분열이 가능한 것으로 밝혀진 최초의 동위원소였습니다. 자연적으로 발생하는 다른 동위원소들은 핵분열이 가능하지만 핵분열은 불가능합니다. 우라늄-235는 느린 중성자 충격을 받으면 대부분의 경우 두 개의 작은 핵으로 분열하여 핵 결합 에너지와 더 많은 중성자를 방출합니다. 이 중성자들 중 너무 많은 수가 다른 우라늄-235 핵에 흡수되면 핵 연쇄 반응이 일어나 열이 터지거나 (어떤 상황에서는) 폭발합니다. 원자로에서는 이러한 연쇄 반응이 느려지고 중성자 독에 의해 제어되어 자유 중성자의 일부를 흡수합니다. 이러한 중성자 흡수 물질은 종종 원자로 제어 로드의 일부입니다(원자로 제어 프로세스에 대한 설명은 원자로 물리학 참조).
우라늄-235는 원자폭탄을 만드는 데 15파운드(6.8kg) 정도만 사용할 수 있습니다.[16] 리틀 보이라고 불리는 히로시마 상공에서 폭발한 핵무기는 우라늄 핵분열에 의존했습니다. 그러나 첫 번째 핵폭탄(트리니티에서 사용된 가젯)과 나가사키 상공에서 폭발한 폭탄(팻 맨)은 모두 플루토늄 폭탄이었습니다.
우라늄 금속은 다음과 같은 세 가지 동소성 형태를 갖습니다.[17]
- α(정통형)는 최대 668°C(1,234°F)까지 안정적입니다. 사방정계, 공간군 63번, Cmcm, 격자 매개변수 a = 285.4 pm, b = 587 pm, c = 495.5 pm
- 668~775 °C(1,234~1,427 °F)에서 안정적인 β(4각형). 정방정계, 공간군 P4/mn, P4nm 또는 P4n2, 격자 파라미터 a = 565.6 pm, b = c = 1075.9 pm.
- 775 °C(1,427 °F)에서 녹는점까지의 γ(체 중심 입방체)—이 상태는 가장 가단성이 있고 연성이 강한 상태입니다. 체 중심 입방체, 격자 매개변수 a = 352.4 pm.
적용들
군사의

우라늄의 주요 용도는 고밀도 침투기입니다. 이 탄약은 티타늄 또는 몰리브덴과 같은 1~2%의 다른 원소와 합금된 고갈된 우라늄(DU)으로 구성됩니다.[19] 높은 충돌 속도에서 발사체의 밀도, 경도 및 피로호성으로 인해 중무장된 표적을 파괴할 수 있습니다. 탱크 갑옷 및 기타 탈착식 차량 갑옷은 고갈된 우라늄 플레이트로 경화할 수도 있습니다. 고갈된 우라늄의 사용은 페르시아만과 발칸 반도 전쟁 중에 미국, 영국 및 다른 국가들이 이러한 군수품을 사용하여 토양에 남아있는 우라늄 화합물에 대한 의문이 제기된 후 정치적, 환경적으로 논쟁의 여지가 있게 되었습니다(걸프 전쟁 증후군 참조).[16]
고갈된 우라늄은 방사성 물질을 저장하고 운반하는 데 사용되는 일부 용기의 차폐 물질로도 사용됩니다. 금속 자체는 방사성이지만 밀도가 높기 때문에 라듐과 같은 강력한 공급원의 방사선을 차단하는 데 납보다 더 효과적입니다.[9] 고갈된 우라늄의 다른 용도로는 항공기 제어 표면을 위한 평형추, 미사일 재진입 차량을 위한 밸러스트 및 차폐 재료가 있습니다.[10] 이 물질은 밀도가 높기 때문에 관성 유도 시스템과 자이로스코프 나침반에서 발견됩니다.[10] 고갈된 우라늄은 기계 가공과 주조가 용이할 뿐만 아니라 상대적으로 저렴한 비용으로 인해 유사한 밀도의 금속보다 선호됩니다.[20] 고갈된 우라늄에 노출되는 주요 위험은 방사능이 아닌 산화우라늄에 의한 화학적 중독입니다(우라늄은 약한 알파 방출기에 불과함).
제2차 세계대전의 후기, 냉전, 그리고 그 이후에는 우라늄-235가 핵분열성 폭발 물질로 사용되어 핵무기를 생산했습니다. 처음에는 우라늄-235를 사용하는 비교적 간단한 장치와 우라늄-238에서 유래한 플루토늄-239를 사용하는 더 복잡한 메커니즘의 두 가지 주요 유형의 핵분열 폭탄이 제작되었습니다. 나중에 훨씬 더 복잡하고 훨씬 더 강력한 유형의 핵분열/융합 폭탄(열핵무기)이 만들어졌는데, 플루토늄 기반 장치를 사용하여 삼중수소와 중수소의 혼합물이 핵융합을 겪도록 합니다. 그러한 폭탄들은 핵융합 과정에서 나오는 빠른 중성자들에 의해 이 물질의 핵분열로부터 그 힘의 절반 이상을 얻어내는, 핵융합이 일어나지 않는 우라늄 케이스에 잠깁니다.[21]
민간인
민간 부문에서 우라늄의 주요 사용은 원자력 발전소에 연료를 공급하는 것입니다. 우라늄-235 1kg은 이론적으로 완전한 핵분열을 가정할 때 약 20테라줄(2×10줄13)의 에너지를 생산할 수 있습니다. 150만 킬로그램(1,500톤)의 석탄만큼의 에너지를 생산할 수 있습니다.[8]
상업용 원자력 발전소는 일반적으로 약 3% 우라늄-235까지 농축된 연료를 사용합니다.[8] CANDU 및 Magnox 설계는 농축되지 않은 우라늄 연료를 사용할 수 있는 유일한 상업용 원자로입니다. 미국 해군 원자로에 사용되는 연료는 일반적으로 우라늄-235가 고농축되어 있습니다(정확한 값은 분류됩니다). 브리더 원자로에서 우라늄-238은 다음과 같은 반응을 통해 플루토늄-239로 변환될 수 있습니다.[10]

방사능이 발견되기 이전(그리고 때때로 이후)에 우라늄은 주로 노란색 유리와 도자기 유리에 소량 사용되었으며, 예를 들어 우라늄 유리와 피에스타웨어에 사용되었습니다.[22]
마리 퀴리(Marie Curie)가 우라늄 광석(pitchblende)에서 라듐을 발견하고 분리하면서 라듐을 추출하기 위한 우라늄 채굴이 시작되었고, 이는 시계와 항공기 다이얼의 야광 페인트를 만드는 데 사용되었습니다.[23][24] 이것은 1그램의 라듐을 추출하는 데 3톤의 우라늄이 필요하기 때문에 엄청난 양의 우라늄을 폐기물로 남겼습니다. 이 폐기물은 유리 산업으로 전용되어 우라늄 유리를 매우 저렴하고 풍부하게 만들었습니다. 도자기 유리 외에도 우라늄 타일 유리는 녹색, 노란색, 연모색, 검은색, 파란색, 빨간색 및 기타 색상으로 생산할 수 있는 일반 욕실 및 주방 타일을 포함하여 대부분의 용도를 차지했습니다.


우라늄은 또한 사진 화학 물질(특히 토너로서 질산우라늄),[10] 무대 조명 전구용 램프 필라멘트,[25] 의치의 외관 개선,[26] 얼룩 및 염료용 가죽 및 목재 산업에 사용되었습니다. 우라늄 염은 비단이나 양모의 매염입니다. 아세트산우라닐과 포름산우라닐은 투과전자현미경에서 전자 밀도가 높은 "염색체"로 사용되어 초박형 섹션에서 생물학적 표본의 대조도를 높이고 바이러스, 분리된 세포 소기관 및 거대분자의 음성 염색에 사용됩니다.
우라늄의 방사능이 발견되면서 우라늄의 추가적인 과학적, 실용적인 용도가 생겨났습니다. 우라늄-238의9 반감기가 길기 때문에 초기 화성암의 연대를 추정하는 데 사용하고 우라늄-토륨 연대 측정, 우라늄-납 연대 측정, 우라늄-우라늄 연대 측정 등 다른 유형의 방사선 연대 측정에 사용하기에 적합합니다. 고에너지 X선을 만드는 데 있어 우라늄 금속은 X선 표적에 사용됩니다.[10]
역사
발견 전 사용
우라늄이 천연 산화물 형태로 사용된 것은 적어도 서기 79년으로 거슬러 올라가는데, 그 때는 로마 제국에서 세라믹 유리에 노란색을 추가하기 위해 사용되었습니다.[10] 이탈리아 나폴리만 포실리포 곶의 로마 별장에서 산화우라늄이 1% 함유된 노란색 유리가 R에 의해 발견되었습니다. 1912년 옥스퍼드 대학교의 T. 군터.[27] 피치블렌데는 중세 후기부터 보헤미아 요아힘스탈(현재 체코의 야치모프)의 합스부르크 은광에서 추출되어 지역 유리 제조 산업에서 착색제로 사용되었습니다.[28] 19세기 초, 세계에서 유일하게 알려진 우라늄 광석의 원천은 이 광산들이었습니다. 냉전이 종식되고 SDAG 비스무트가 해체된 후 독일 측에서는 오레 산맥의 우라늄 채굴이 중단되었습니다. 체코 쪽에서는 2007년 우라늄 가격 거품이 일 때 채굴을 재개하려는 시도가 있었지만 우라늄 가격이 하락하면서 이를 곧 포기했습니다.[29][30]
디스커버리

이 원소의 발견은 독일의 화학자 마르틴 하인리히 클라프로트 덕분입니다. 1789년 그가 베를린의 실험실에서 일하는 동안, 클라프로트는 피치블렌드를 질산에 녹이고 용액을 수산화나트륨으로 중화함으로써 노란색 화합물(이우라네이트 나트륨일 가능성이 있음)을 침전시킬 수 있었습니다.[28] 클라프로트는 노란색 물질이 아직 발견되지 않은 원소의 산화물이라고 가정하고 숯으로 가열하여 검은 가루를 얻었는데, 이것이 바로 새로 발견된 금속 그 자체라고 생각했습니다(사실 그 가루는 우라늄의 산화물이었습니다).[28][31] 그는 새로 발견된 원소의 이름을 윌리엄 허셜에 의해 8년 전에 발견된 천왕성(그리스의 하늘의 원시 신의 이름을 따서 명명됨)이라고 지었습니다.[32]
1841년 파리 국립예술학교(Central School of Arts and Manufactures)의 분석화학 교수 외젠-멜치오르 펠리고는 사염화우라늄을 칼륨과 함께 가열하여 우라늄 금속의 첫 번째 샘플을 분리했습니다.[28][33]
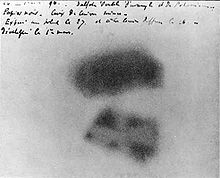
앙리 베크렐은 1896년 우라늄을 이용하여 방사능을 발견했습니다.[15] 베크렐은 파리에서 노출되지 않은 사진판 위에 우라늄 염인 KUO22(SO4)(2우라닐 황산칼륨)의 샘플을 서랍에 남기고 이 판이 "안개"가 되었다고 언급함으로써 발견했습니다.[34] 그는 우라늄에 의해 방출되는 보이지 않는 빛이나 광선의 형태가 판을 노출시켰다고 판단했습니다.
제1차 세계대전 당시 중부열강은 포병총통과 고속공구강을 만들기 위해 몰리브덴이 부족할 때 페로우라늄 합금을 대체재로 일상적으로 사용했는데, 이는 몰리브덴과 동일한 물리적 특성을 많이 나타내기 때문입니다. 1916년 이 관행이 알려지자 미국 정부는 몇몇 저명한 대학에 우라늄을 제조 및 금속 가공에 사용하는 연구를 요청했습니다. 이러한 공식들로 만들어진 도구들은 맨하탄 프로젝트와 냉전이 핵분열 연구와 무기 개발을 위해 우라늄에 많은 수요를 두기 전까지 [35][36]수십 년 동안 사용되었습니다.
핵분열 연구

1934년 엔리코 페르미가 이끄는 연구팀은 우라늄에 중성자를 충돌시키면 베타선이 생성된다는 사실을 발견했습니다.[37] 이 핵분열 생성물은 처음에 원자번호 93과 94를 가진 새로운 원소로 오인되었는데, 로마 사피엔자 대학 학장인 오르소 마리오 코르비노는 이 원소를 각각 아우세늄과 헤스페리움이라고 이름 지었습니다.[38][39][40][41] 우라늄이 더 가벼운 원소로 핵분열(분열)하고 결합 에너지를 방출하는 능력을 발견하도록 이끈 실험은 베를린에 있는 한의 실험실에서 오토 한과 프리츠 슈트라스만에[37] 의해 수행되었습니다. 리세 마이트너와 그녀의 조카인 물리학자 오토 로버트 프리쉬는 1939년 2월 물리학적 설명을 발표하고 이 과정을 "핵분열"이라고 이름 붙였습니다.[42] 얼마 지나지 않아 페르미는 우라늄의 핵분열이 핵분열 반응을 유지할 수 있을 만큼의 중성자를 방출할 수도 있다는 가설을 세웠습니다. 이 가설의 확인은 1939년에 이루어졌고, 이후 연구 결과 우라늄-235의 핵분열마다 평균 약 2.5개의 중성자가 방출된다는 사실이 밝혀졌습니다.[37] 페르미는 알프레드 O. C. 니어에게 핵분열 성분을 측정하기 위해 우라늄 동위원소를 분리할 것을 촉구했고, 1940년 2월 29일 니어는 미네소타 대학교에서 만든 기구를 사용하여 테이트 연구소에서 세계 최초의 우라늄-235 샘플을 분리했습니다. 컬럼비아 대학의 사이클로트론을 사용하여 존 더닝은 3월 1일 이 샘플이 분리된 핵분열성 물질임을 확인했습니다.[43] 추가적인 연구는 훨씬 더 일반적인 우라늄-238 동위원소가 우라늄-235와 마찬가지로 열 중성자에 의해 핵분열을 일으키는 플루토늄으로 변환될 수 있다는 것을 발견했습니다. 이러한 발견으로 인해 수많은 국가들이 핵무기와 원자력 개발에 착수하게 되었습니다. 독일에서 핵분열이 발견되었음에도 불구하고, Uranverein (우라늄 클럽) 독일의 전시 핵전력 및/또는 무기 연구 프로젝트는 제한된 자원과 내분으로 인해 방해를 받았습니다. 이 분야의 몇몇 저명한 과학자들의 망명 또는 involve과 사용 가능한 흑연 샘플의 불순물을 설명하지 못하는 것과 같은 몇 가지 중대한 실수로 인해 실제보다 중성자 감속제로 적합하지 않은 것으로 보입니다. 독일이 천연 우라늄/중수 원자로를 건설하려는 시도는 미국인들이 독일의 마지막 전시 원자로 실험 장소인 하이게를로흐에 도달했을 때 임계점에 근접하지 못했습니다.[44]
1942년 12월 2일, 맨하탄 프로젝트의 일환으로 엔리코 페르미가 이끄는 다른 팀은 최초의 인공적인 자생 핵 연쇄 반응인 시카고 파일-1을 시작할 수 있었습니다. 농축 우라늄-235를 사용한 초기 계획은 아직 충분한 양이 공급되지 않아 폐기되었습니다.[45] 시카고 대학의 스태그필드 가판대 아래에 있는 연구소에서 일하던 이 연구팀은 360톤의 흑연, 53톤의 산화우라늄, 5.5톤의 금속 우라늄을 한데 모아 그러한 반응에 필요한 조건을 만들어 냈는데, 대부분은 웨스팅하우스 램프 공장에서 임시 생산 과정으로 공급했습니다.[37][46]
핵무기

핵분열성 물질이 고농축 우라늄인 우라늄 기반 장치(코드명 "리틀 보이")와 플루토늄 기반 장치(트리니티 테스트 및 "팻 맨" 참조)의 두 가지 유형이 제2차 세계 대전 중 미국에 의해 개발되었습니다. 리틀 보이는 1945년 8월 6일 일본 히로시마 상공에서 폭발했을 때 전쟁에 사용된 최초의 핵무기가 되었습니다. 12,500톤의 TNT에 해당하는 생산량으로 폭발한 폭탄의 폭발과 열파는 거의 50,000개의 건물을 파괴하고 약 75,000명의 사망자를 냈습니다(히로시마와 나가사키 원자폭탄 참조).[34] 처음에는 우라늄이 상대적으로 드물었고, 알려진 우라늄 재고를 모두 사들이는 것만으로도 핵 확산을 피할 수 있을 것으로 여겨졌지만, 10년 안에 전 세계 여러 곳에서 우라늄의 대량 매장이 발견되었습니다.[47]
원자로

테네시주 오크리지에 있는 오크리지 국립 연구소(ORNL)의 X-10 흑연 원자로는 이전에는 클린턴 파일과 X-10 파일로 알려져 있었지만, (엔리코 페르미의 시카고 파일에 이어) 세계에서 두 번째로 만들어진 인공 원자로이며, 연속 운전을 위해 설계되고 건설된 최초의 원자로였습니다. 1951년 12월 20일 아이다호주 아르코 인근 원자력위원회 국립원자로시험장에 위치한 아르곤 국립연구소의 실험용 브리더 원자로 I호는 최초로 전기를 생산한 원자로가 되었습니다.[48] 처음에는 원자로에 의해 150와트 전구 4개가 켜졌지만, 개선으로 결국 전체 시설에 전력을 공급할 수 있게 되었습니다(나중에 아르코 마을은 아르곤 국립 연구소가 설계하고 운영하는 또 다른 원자로인 BORAX-III가 생산한 원자력으로 모든 전기를 생산하는 세계 최초가 되었습니다).[49][50] 세계 최초의 상업적 규모의 원자력 발전소인 소련의 오브닌스크는 1954년 6월 27일 원자로 AM-1로 발전을 시작했습니다. 그 밖의 초기 원자력 발전소는 1956년 10월 17일에 발전을 시작한 영국의 칼더 홀과 [51]1958년 5월 26일에 시작한 펜실베니아의 쉬핑포트 원자력 발전소입니다. 원자력은 1954년 잠수함인 USS 노틸러스의 추진에 처음으로 사용되었습니다.[37][52]
선사시대 자연발생 핵분열
1972년, 프랑스의 물리학자 프란시스 페린은 아프리카 가봉의 오클로 광산에 있는 세 개의 광상에서 오래되고 더 이상 활동하지 않는 15개의 천연 핵분열 원자로를 발견했습니다. 이것은 총칭 오클로 화석 원자로로 알려져 있습니다. 광석 매장량은 17억년 전으로, 우라늄-235는 지구상 우라늄의 약 3%를 차지하고 있습니다.[53] 이는 다른 지원 조건이 존재하는 경우 지속적인 연쇄 반응을 허용하기에 충분히 높습니다. 건강을 위협하는 핵폐기물을 포함하는 주변 퇴적물의 용량은 유카산 핵폐기물 저장소에 사용 후 핵연료를 저장할 수 있는 가능성을 뒷받침하는 증거로 미국 연방정부에 의해 인용되었습니다.[53]
오염과 냉전의 유산
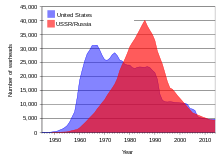
1950년대와 1960년대 초 소련과 미국, 1970년대와 1980년대[20] 프랑스의 지상 핵실험은 우라늄 딸 동위원소에서 상당한 양의 낙진을 전 세계에 퍼뜨렸습니다.[54] 여러 원전 사고로 인해 추가 낙진과 오염이 발생했습니다.[55]
우라늄 광부들은 암 발병률이 더 높습니다. 예를 들어, 나바호 우라늄 채굴자들 사이에서 폐암의 초과 위험은 문서화되어 있고 그들의 직업과 관련이 있습니다.[56] 미국의 1990년 법인 방사선 피폭 보상법은 암이나 기타 호흡기 질환 진단을 받은 우라늄 채굴자들에게 10만 달러의 '자비 지급'을 요구했습니다.[57]
소련과 미국의 냉전 시기에 막대한 우라늄 비축량이 쌓였고 우라늄으로 만든 농축우라늄과 플루토늄을 이용해 수만 개의 핵무기를 만들었습니다. 1991년 소련이 해체된 후, 약 600톤(540미터톤)의 고농축 무기 등급 우라늄(핵탄두 40,000개를 만들 수 있는 양)이 러시아 연방과 다른 여러 구소련 국가들의 부적절한 경비 시설에 보관되었습니다.[16] 1993년부터 2005년까지 최소 16차례에 걸쳐 아시아, 유럽 및 남미 경찰이 밀수된 폭탄급 우라늄 또는 플루토늄의 선적을 감청했으며, 대부분은 구소련 소식통으로부터 온 것입니다.[16] 1993년부터 2005년까지 미국 연방정부가 운영하는 물질보호·통제·회계 프로그램은 러시아의 우라늄과 플루토늄 비축량을 보호하기 위해 약 5억 5천만 달러를 지출했습니다. 이 돈은 연구 및 저장 시설의 개선 및 보안 강화에 사용되었습니다.[16]
1990년대 초 정치·경제적 혼란이 안정화된 이후 러시아 핵시설의 안전성이 크게 향상되었습니다. 예를 들어, 1993년에 국제 원자력 사건 척도에서 1등급 이상을 차지한 사건은 29건이었고, 1995-2003년에는 연간 4건 미만으로 감소했습니다. 한 번의 전신 CT 촬영에 해당하는 20mSv 이상의 연간 방사선량을 받는 직원 수는 2000년을 전후로 크게 감소했습니다.[58] 2015년 11월, 러시아 정부는 5620억 루블(약 80억 달러)의 예산으로 2016년부터 2030년까지의 핵 및 방사선 안전을 위한 연방 프로그램을 승인했습니다. 그것의 핵심 쟁점은 "원자력 산업의 70년 동안, 특히 소련 시절에 축적된 이연 부채"입니다. 예산의 약 73%는 노후화되고 노후화된 원자로와 원자력 시설, 특히 국가 방위 프로그램과 관련된 시설의 폐로에 사용될 것이고, 20%는 핵 연료와 방사성 폐기물의 처리 및 처리에, 5%는 원자력과 방사선 안전의 감시 및 보장에 사용될 것입니다.[59]
발생
기원.
철보다 원자량이 많은 모든 원소와 마찬가지로 우라늄도 초신성과 중성자별 병합에서 r-과정(급속 중성자 포획)에 의해 자연적으로 형성될 뿐입니다.[60] 원시 토륨과 우라늄은 r-공정에서만 생성되는데, s-공정(느린 중성자 포획)이 너무 느리고 비스무트 이후 불안정의 틈을 통과할 수 없기 때문입니다.[61][62] 현존하는 두 개의 원시 우라늄 동위원소인 U와 U 외에도, r-공정은 또한 상당한 양의 U를 생성했는데, U는 반감기가 더 짧고 소멸된 방사성 핵종이기도 하며, Th로 완전히 붕괴된 지 오래되었습니다. 추가 우라늄-236은 Pu의 붕괴에 의해 생성되었으며, 이는 관측된 토륨의 풍부함과 우라늄의 풍부함을 설명합니다.[63] 우라늄의 자연적인 풍부함은 멸종된 Pu(반생 375,000년)와 Cm(반생 1,600만년)의 붕괴로 보충되어 각각 U와 U를 생성했지만, 이러한 현상은 부모의 반감기가 U와 Pu보다 짧고 생산량이 적기 때문에 거의 무시할 수 있을 정도로 발생했습니다. 토륨의 모체: 태양계가 형성될 때의 Cm/235U 비는 (7.0±1.6)×10이었습니다−5.[64]
비생물적, 비생물적


우라늄은 모든 암석, 토양, 물에서 낮은 수준으로 발견되는 자연적으로 발생하는 원소입니다. 우라늄은 지각에서 51번째로 풍부한 원소입니다. 우라늄은 지구상에서 자연적으로 대량으로 발견되는 가장 높은 원소이며, 거의 항상 다른 원소들과 결합되어 발견됩니다.[10] 지구 맨틀의 우라늄, 토륨, 칼륨-40의 붕괴는 지구의 외핵을 액체 상태로 유지하고 맨틀 대류를 유도하여 판구조론을 유도하는 주요 열원으로[65][66] 여겨지고 있습니다.
우라늄의 지각 평균 농도는 (기준에 따라) 100만분의 2~4ppm,[9][20] 즉 은의 약 40배에 달합니다.[15] 지표에서 25km(15mi) 아래까지의 지각은 10kg17(2×10lb17)의 우라늄을 포함하는 것으로 계산되며, 바다는 10kg13(2×10lb13)을 포함할 수 있습니다.[9] 토양 중 우라늄 농도는 100만분의 0.7~11부(인산비료 사용으로 농지 토양 중 최대 15부)이며,[67] 해수 중 농도는 10억분의 3입니다.[20]
우라늄은 안티몬, 주석, 카드뮴, 수은, 은보다 많고 비소나 몰리브덴 정도로 풍부합니다.[10][20] 우라늄은 우라니나이트(가장 흔한 우라늄 광석), 카르노나이트, 아우투나이트, 우라노판, 토버나이트, 코비나이트를 포함한 수백 가지 광물에서 발견됩니다.[10] 상당한 농도의 우라늄은 인산염 암석 퇴적물과 같은 일부 물질에서 발생하며, 갈탄과 같은 광물과 우라늄이 풍부한 광석의[10] 모나자이트 모래(0.1% 미만의[15] 우라늄으로 상업적으로 회수됨)에서 발생합니다.
Shewanella putrefaciens, Geobacter metallireducens 및 Burkholderia fungorum의 일부 균주와 같은 일부 박테리아는 성장을 위해 우라늄을 사용하고 U(VI)를 U(IV)로 전환합니다.[68][69] 최근 연구에 따르면 이 경로에는 중간 U(V) 5가 상태를 통한 가용성 U(VI)의 환원이 포함됩니다.[70][71] 이끼벌레와 같은 다른 유기체나 박테리아 시트로박터와 같은 미생물은 환경의 최대 300배 수준의 우라늄 농도를 흡수할 수 있습니다.[72] 시트로박터 종은 글리세롤 인산염(또는 다른 유사한 유기 인산염)이 주어지면 우라닐 이온을 흡수합니다. 하루가 지나면 1g의 박테리아가 9g의 인산우라닐 결정으로 둘러싸여 있을 수 있습니다. 이것은 이 유기체들이 우라늄으로 오염된 물을 오염 제거하기 위해 생물 정화에 사용될 수 있는 가능성을 만듭니다.[28][73] 프로테오박테리움 지오박터는 지하수에서 우라늄을 생물매개하는 것으로 나타났습니다.[74] 진균류 Glomus intraradice는 공생 식물의 뿌리에 우라늄 함량을 증가시킵니다.[75]
자연에서 우라늄(VI)은 알칼리성 pH에서 고용해성 탄산염 복합체를 형성합니다. 이는 핵폐기물에서 나오는 지하수와 토양에 대한 우라늄의 이동성과 가용성을 증가시켜 건강상의 위험을 초래합니다. 그러나 알칼리성 pH에서 과량의 탄산염이 존재할 경우 인산염으로서 우라늄을 침전시키기가 어렵습니다. 스핑고모나스 종 균주 BSAR-1은 알칼리 용액으로부터 우라닐 인산염 종으로서 우라늄의 생물침전을 위해 적용된 고활성 알칼리성 포스파타제(PhoK)를 발현하는 것으로 밝혀졌습니다. 대장균에서 PhoK 단백질을 과발현하여 침전 능력을 높였습니다.[76]
식물은 토양에서 약간의 우라늄을 흡수합니다. 식물에서 우라늄의 건조 중량 농도는 10억분의 5에서 60분의 1이며, 연소된 나무에서 나오는 재는 100만분의 4까지 농도를 가질 수 있습니다.[28] 식품 공장의 우라늄 건조 중량 농도는 일반적으로 사람들이 먹는 음식을 통해 하루에 1~2마이크로그램을 섭취하면 더 낮습니다.[28]
생산 및 광업
2021년 전 세계 우라늄 생산량은 48,332톤이며, 이 중 21,819톤(45%)이 카자흐스탄에서 채굴되었습니다. 다른 중요한 우라늄 채굴 국가는 나미비아(5,753t), 캐나다(4,693t), 호주(4,192t), 우즈베키스탄(3,500t), 러시아(2,635t)입니다.[77]
우라늄 광석은 오픈 피트, 지하, 현장 침출, 시추공 채굴 등 여러 방식으로 채굴됩니다.[8] 저등급 우라늄 광석은 일반적으로 0.01~0.25%의 우라늄 산화물을 함유하고 있습니다. 광석에서 금속을 추출하려면 광범위한 조치를 취해야 합니다.[78] 캐나다 서스캐처원의 아타바스카 분지 퇴적물에서 발견되는 고급 광석은 평균 23%의 우라늄 산화물을 함유할 수 있습니다.[79] 우라늄 광석을 분쇄하여 고운 가루로 만든 다음 산 또는 알칼리로 침출시킵니다. 침출수는 침전, 용매 추출 및 이온 교환의 여러 시퀀스 중 하나를 거칩니다. 옐로케이크라고 불리는 이 혼합물은 적어도 75%의 우라늄 산화물 UO를38 함유하고 있습니다. 그런 다음 옐로케이크를 소성하여 정제 및 전환 전에 제분 공정에서 불순물을 제거합니다.[80]
상업용 등급의 우라늄은 알칼리 또는 알칼리 토금속과 함께 우라늄 할로겐화물을 환원시켜 생산할 수 있습니다.[10] 용융 염화칼슘(CaCl
2)과 염화나트륨(NaCl) 용액에 녹인 KUF
5 또는 UF의
4 전기분해를 통해 우라늄 금속을 제조할 수도 있습니다.[10] 매우 순수한 우라늄은 뜨거운 필라멘트 위에서 우라늄 할로겐화물의 열분해를 통해 생산됩니다.[10]
자원 및 매장량

우라늄 kg당 미화 130달러로 경제성이 있는 광석에는 610만 톤의 우라늄이 존재하는 것으로 추정되며,[82] 3500만 톤은 광물자원(최종적인 경제적 추출에 대한 합리적인 전망)으로 분류됩니다.[83]
호주는 세계적으로 알려진 우라늄 광석 매장량의[82] 28%를 보유하고 있으며, 세계에서 가장 큰 단일 우라늄 매장량을 보유하고 있는 곳은 남호주의 올림픽 댐 광산입니다.[84] 중앙아프리카공화국 음보모우 현의 바쿠마에는 상당한 우라늄 매장량이 있습니다.[85]
일부 우라늄은 또한 해체된 핵무기에서 유래합니다.[86] 예를 들어, 1993-2013년 러시아는 메가톤스 프로그램 내에서 15,000톤의 저농축 우라늄을 미국에 공급했습니다.[87]
바닷물에는 46억 톤의 우라늄이 추가로 녹아 있을 것으로 추정됩니다(1980년대 일본 과학자들은 이온 교환기를 이용해 바닷물에서 우라늄을 추출하는 것이 기술적으로 가능하다는 것을 보여주었습니다).[88][89] 바닷물에서 우라늄을 추출하는 실험이 있었지만 [90]물에 존재하는 탄산염 때문에 수율이 낮았습니다. 태평양 노스웨스트 국립 연구소의 연구원들이 검증한 결과에 따르면, 2012년 ORNL 연구원들은 고체 또는 가스 분자, 원자 또는 이온의 표면 유지를 수행하고 물에서 독성 금속을 효과적으로 제거하는 HiCap이라는 새로운 흡수 물질의 성공적인 개발을 발표했습니다.[91][92]
저장품
2005년에는 10개국이 세계 농축 우라늄 산화물의 대부분을 차지했습니다. 캐나다(27.9%), 호주(22.8%), 카자흐스탄(10.5%), 러시아(8.0%), 나미비아(7.5%), 니제르(7.4%), 우즈베키스탄(5.5%), 미국(2.5%), 아르헨티나(2.1%), 우크라이나(1.9%)[94] 순으로 나타났습니다. 2008년 카자흐스탄은 2009년까지 생산량을 늘려 세계 최대 우라늄 공급국이 될 것으로 전망되었고,[95][96] 카자흐스탄은 2010년부터 세계 우라늄 시장을 장악하고 있습니다. 2021년 점유율은 45.1%로 나미비아(11.9%), 캐나다(9.7%), 호주(8.7%), 우즈베키스탄(7.2%), 니제르(4.7%), 러시아(5.5%), 중국(3.9%), 인도(1.3%), 우크라이나(0.9%), 남아프리카공화국(0.8%) 등이 뒤를 이었습니다.[77] 대부분의 우라늄은 기존의 광석 지하 채굴(생산량의 29%)이 아니라 현장 침출(66%)[77][97]에 의해 생산되었습니다.
1960년대 후반, 유엔 지질학자들은 소말리아에서 주요 우라늄 매장량과 다른 희귀 광물 매장량을 발견했습니다. 이번 발견은 업계 전문가들이 당시 알려진 전 세계 우라늄 매장량 80만 톤의 25% 이상을 매장량으로 추정한 가운데 가장 큰 규모였습니다.[98]
궁극적인 가용 공급은 적어도 향후 85년 동안 충분할 것으로 여겨지지만,[83] 일부 연구에서는 20세기 후반의 과소 투자가 21세기에 공급 문제를 일으킬 수 있다고 지적합니다.[99] 우라늄 퇴적물은 로그 정규 분포를 따르는 것으로 보입니다. 광석 등급이 10배 감소할 때마다 회수 가능한 우라늄 양이 300배 증가합니다.[100] 즉, 높은 등급의 광석은 거의 없고 그에 비례하여 낮은 등급의 광석은 훨씬 더 많이 이용할 수 있습니다.
화합물
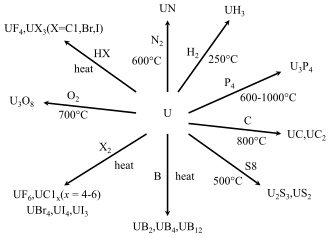
산화상태 및 산화물
산화물
많은 대형 공장에서 생산되는 하소 우라늄 옐로우케이크에는 가장 산화된 우라늄부터 가장 산화되지 않은 우라늄 산화종이 다양한 형태로 분포되어 있습니다. 칼시너에서 체류 시간이 짧은 입자는 일반적으로 체류 시간이 긴 입자 또는 스택 스크러버에서 회수된 입자보다 덜 산화됩니다. 우라늄 함량은 일반적으로 UO를
3
8 참조하며, 이는 UO가
3
8 분석 화학 보고 표준으로 사용된 맨해튼 프로젝트 시절로 거슬러 올라갑니다.[101]
우라늄-산소 시스템의 상 관계는 복잡합니다. 우라늄의 가장 중요한 산화 상태는 우라늄입니다.Ⅳ)과 우라늄(VI) 그리고 그에 해당하는 두 산화물은 각각 이산화우라늄(UO
2)과 삼산화우라늄(UO
3)입니다.[102] 일산화우라늄(UO), 오산화이우라늄(UO
2
5), 과산화우라늄(UO
4·2HO
2)과 같은 다른 우라늄 산화물도 존재합니다.
산화우라늄의 가장 일반적인 형태는 산화삼우라늄(UO
3
8)과 산화우라늄(UO
2)입니다.[103] 두 산화물 형태 모두 물에 대한 용해도가 낮고 광범위한 환경 조건에서 비교적 안정적인 고체입니다. 산화트리우라늄은 (조건에 따라) 우라늄의 가장 안정적인 화합물이며 자연에서 가장 흔하게 발견되는 형태입니다. 이산화우라늄은 우라늄이 원자로 연료로 가장 많이 사용되는 형태입니다.[103] 주변 온도에서 UO는
2 점차 UO로
3
8 전환됩니다. 우라늄 산화물은 안정성 때문에 일반적으로 저장 또는 폐기에 선호되는 화학적 형태로 간주됩니다.[103]
수성화학

우라늄의 많은 산화 상태의 염은 수용성이며 수용액에서 연구될 수 있습니다. 가장 일반적인 이온 형태는 U3+
(갈색-적색), U(녹색4+
), UO+
2(불안정) 및 UO2+
2(황색)이며, 각각 U(III), U(IV), U(V) 및 U(VI)입니다.[104] UO 및 US와 같은 고체 및 반금속 화합물은 공식 산화 상태 우라늄에 대해 존재합니다.II), 그러나 그 상태에 대한 용액에는 단순 이온이 존재하지 않는 것으로 알려져 있습니다. U의3+
이온은 물에서 수소를 방출하기 때문에 매우 불안정한 것으로 간주됩니다. UO2+
2 이온은 우라늄(VI) 상태를 나타내며, 탄산우라닐, 염화우라닐, 황산우라닐과 같은 화합물을 형성하는 것으로 알려져 있습니다. UO는2+
2 또한 다양한 유기 킬레이트제와 복합체를 형성하며, 그 중 가장 일반적으로 접하는 것은 아세트산 우라닐입니다.[104]
우라늄의 우라닐 염과 다원자 이온 우라늄-옥사이드 양이온 형태와는 달리, 다원자 우라늄-옥사이드 음이온을 포함하는 염인 우라네이트는 일반적으로 수용성이 아닙니다.
탄산염
탄산염 음이온과 우라늄(VI)의 상호작용은 매질이 물에서 탄산염을 포함하는 용액으로 바뀔 때 푸어바익스 다이어그램을 크게 변화시킵니다. 탄산염의 대부분은 물에 불용성이지만(학생들은 알칼리 금속 이외의 모든 탄산염은 물에 불용성이라는 것을 종종 배웁니다), 탄산 우라늄은 종종 물에 녹습니다. U(VI) 양이온은 2개의 말단 산화물과 3개 이상의 탄산염을 결합하여 음이온 복합체를 형성할 수 있기 때문입니다.
 | 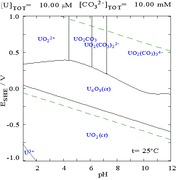 |
| 비복잡성 수성 매질 중의 우라늄 (예: 과염소산/수산화sodium). | 탄산염 중의 우라늄 |
 | 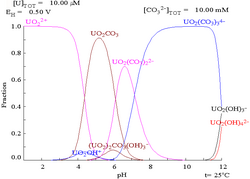 |
| 비복잡성 수성 매질에서 우라늄의 다양한 화학적 형태의 상대적 농도 (예: 과염소산/수산화sodium). | 탄산수 수용액 중 우라늄의 다른 화학적 형태의 상대적 농도.[105] |
pH의 영향
탄산염이 있는 상태의 우라늄 분획 다이어그램은 이것을 더 잘 보여줍니다: 우라늄(VI) 용액의 pH가 증가하면 우라늄은 수화된 산화 우라늄으로 전환되고 높은 pH에서는 음이온성 수산화물 복합체가 됩니다.
탄산염이 첨가되면 pH가 높아지면 우라늄은 일련의 탄산염 복합체로 전환됩니다. 이러한 반응의 한 가지 효과는 pH 6~8 범위에서 우라늄의 용해도가 증가한다는 것인데, 이는 사용 후 이산화우라늄 핵연료의 장기적인 안정성과 직접적인 관련이 있습니다.
수소화물, 탄화물 및 질화물
250~300°C(482~572°F)로 가열된 우라늄 금속은 수소와 반응하여 우라늄 하이드라이드를 형성합니다. 더 높은 온도는 수소를 가역적으로 제거합니다. 이 성질은 우라늄 수소화물이 다양한 탄화우라늄, 질화물 및 할로겐화물 화합물과 함께 반응성 우라늄 분말을 생성하는 데 편리한 출발 물질이 되도록 합니다.[106] 우라늄 하이드라이드는 낮은 온도에서 얻어지는 α 형태와 형성 온도가 250 ℃ 이상일 때 생성되는 β 형태의 두 가지 결정 변형이 존재합니다.[106]
탄화우라늄과 질화우라늄은 둘 다 산에 최소로 용해되고 물과 반응하며 공기 중에서 점화되어 UO를
3
8 형성할 수 있는 비교적 불활성인 반금속 화합물입니다.[106] 우라늄의 탄화물에는 단탄화우라늄, 디카본화우라늄
2, 트리카본화이우라늄 등이
2
3 있습니다. UC와 UC는
2 모두 용융 우라늄에 탄소를 첨가하거나 금속을 고온에서 일산화탄소에 노출시켜 형성됩니다. 1800 °C 이하에서 안정적인 UC는
2
3 UC와 UC의
2 가열된 혼합물에 기계적 응력을 가하여 준비됩니다.[107] 금속을 질소에 직접 노출시켜 얻은 질화 우라늄에는 우라늄 모노나이트라이드(UN), 우라늄 디나이트라이드(UN
2), 디우라늄 트리나이트라이드(UN
2
3) 등이 있습니다.[107]
할라이드

모든 불화우라늄은 사불화우라늄(UF
4)을 사용하여 제조되며, UF
4 자체는 이산화우라늄의 수소불화에 의해 제조됩니다.[106] Reduction of UF
4 with hydrogen at 1000 °C produces uranium trifluoride (UF
3). Under the right conditions of temperature and pressure, the reaction of solid UF
4 with gaseous uranium hexafluoride (UF
6) can form the intermediate fluorides of U
2F
9, U
4F
17, and UF
5.[106]
상온에서 UF는
6 증기압이 높아 일반 우라늄-238 동위원소에서 희유우라늄-235를 분리하는 기체 확산 과정에서 유용합니다. 이 화합물은 다음과 같은 과정을 통해 이산화우라늄과 수소화우라늄으로부터 제조될 수 있습니다.[106]
- UO + 4 HF → UF + 2 HO (500 °C, 흡열)
- UF + F → UF (350 °C, 흡열)
생성된 백색 고체인 UF는
6 반응성이 높고(플루오르화에 의해), 쉽게 서브라임(거의 이상적인 기체로 행동하는 증기를 방출)되며, 현재 존재하는 것으로 알려진 가장 휘발성이 높은 우라늄 화합물입니다.[106]
사염화우라늄(UCL
4)을 제조하는 한 가지 방법은 염소와 우라늄 금속 또는 수소화우라늄을 직접 결합하는 것입니다. 수소에 의한 UCl의
4 환원은 삼염화우라늄(UCl
3)을 생성하고 우라늄의 더 높은 염화물은 추가 염소와의 반응에 의해 제조됩니다.[106] 모든 염화우라늄은 물과 공기와 반응합니다.
우라늄의 브로마이드와 요오드는 각각 브롬과 요오드가 우라늄과 직접 반응하거나 그 원소의 산에 UH를
3 첨가하여 형성됩니다.[106] 알려진 예로는 UBr
3, UBr
4, UI
3, UI
4 등이 있습니다. UI가
5 준비된 적이 없습니다. 옥시할라이드 우라늄은 수용성이며, UOF
2
2, UOCl
2, UOBr
2
2
2
2 등이 있습니다. 옥시할라이드의 안정성은 할로겐화 성분의 원자량이 증가함에 따라 감소합니다.[106]
동위 원소
우라늄도 원자번호 82보다 큰 모든 원소와 마찬가지로 안정한 동위원소가 없습니다. 82개 이상의 양성자를 포함하는 핵종에서는 강한 핵력이 전자기적 반발력을 능가하지 못하기 때문에 우라늄의 모든 동위원소는 방사성을 띠고 있습니다.[108] 그럼에도 불구하고 가장 안정적인 두 동위원소인 U와 U는 원시 방사성 핵종으로 자연에서 발생할 수 있을 만큼 충분히 긴 반감기를 가지고 있으며, 측정 가능한 양은 지구가 형성된 이래로 생존해 왔습니다.[109] 이 두 핵종은 토륨-232와 함께 거의 안정된 비스무트-209보다 무거운 유일한 원시 핵종으로 확인되었습니다.[5][110]
천연 우라늄은 우라늄-238(자연적 풍부도 99.28%), 우라늄-235(0.71%), 우라늄-234(0.0054%)의 세 가지 주요 동위 원소로 구성됩니다. 플루토늄-244의 붕괴 생성물인 우라늄-240;[110] U가 자발적인 핵분열을 겪을 때 생성되어 다른 U 원자에 포획된 중성자를 방출하는 우라늄-239; U가 중성자를 포획할 때 생성되어 두 개를 더 방출하고 그 후 넵투늄-237로 붕괴되는 우라늄-236. U에서 중성자 포획으로 인해 미량으로 발생하고 플루토늄-244의 붕괴 생성물로 발생하며,[110] 마지막으로 우라늄-233은 넵투늄-237의 붕괴 사슬에서 형성됩니다. 또한 우라늄-232는 천연 토륨-232의 이중 베타 붕괴에 의해 생성될 것이지만, 이 에너지적으로 가능한 과정은 관찰된 적이 없습니다.[113]
우라늄-238은 우라늄의 가장 안정한 동위원소로 반감기는 약 4.463×10년으로9 [5]대략 지구 나이와 같습니다. 우라늄-238은 주로 알파 방출체이며, 토륨-234로 붕괴됩니다. 최종적으로 18개의 구성원으로 구성된 우라늄 계열을 통해 206개의 납으로 붕괴됩니다.[15] 우라늄-238은 핵분열성은 아니지만, 중성자 활성화 후에 또 다른 핵분열성 동위원소인 플루토늄-239로 전환될 수 있기 때문에 비옥한 동위원소입니다. 실제로 U핵은 하나의 중성자를 흡수하여 방사성 동위원소 우라늄-239를 생성할 수 있습니다. 239U는 베타 방출에 의해 넵투늄-239로 붕괴하고, 이 베타 방출체는 며칠 안에 차례로 붕괴하여 플루토늄-239로 붕괴합니다. 239푸는 1945년 7월 16일 뉴멕시코주에서 있었던 '트리니티 실험'에서 처음으로 폭발한 원자폭탄에서 핵분열성 물질로 사용되었습니다.[37]
우라늄-235의 반감기는 약 7.04×10년이며8, U 다음으로 안정한 우라늄 동위원소이며, 또한 주로 알파 방출체이며, 토륨-231로 붕괴됩니다.[5] 우라늄-235는 원자로와 핵무기 모두에 중요한데, 지구상의 자연에 존재하는 우라늄 동위원소 중 핵분열성이 있는 유일한 동위원소이기 때문입니다. 열중성자에 의해 두세 개의 파편(핵분열 생성물)으로 쪼개질 수 있다는 뜻입니다.[15] 악티늄 계열이라고 불리는 U의 붕괴 사슬은 15개의 구성원을 가지고 있으며 결국에는 납-207로 붕괴됩니다.[15] 이러한 붕괴 시리즈의 일정한 붕괴 속도는 방사선 측정 연대 측정에서 모 원소 대 딸 원소의 비율을 비교하는 데 유용합니다.
우라늄-236의 반감기는 2.342×10년으로7[5] 자연계에서는 상당한 양이 발견되지 않습니다. 우라늄-236의 반감기는 너무 짧아서 원시적인 것이 아닙니다. 하지만 우라늄-236은 알파 붕괴의 딸 토륨-232의 멸종된 조상으로 밝혀졌습니다.[63] 우라늄-236은 U에서 중성자 포획이 핵분열을 유발하지 않을 때 또는 플루토늄-240의 붕괴 생성물로서 사용된 핵연료에서 발생합니다. 우라늄-236은 핵분열성 Pu를 생성하기 위해 세 번의 중성자 포획이 더 필요하기 때문에 비옥하지 않으며, 핵분열성 자체가 아니기 때문에 장수하는 방사성 폐기물로 간주됩니다.[114]
우라늄-234는 우라늄 계열의 구성원이며, 그 조상인 U와 평형 상태에서 발생하며, 반감기가 245,500년인[5] 알파 붕괴를 거쳐 상대적으로 수명이 짧은 일련의 동위원소를 통해 납-206으로 붕괴합니다.
우라늄-233은 반감기가 16만 년으로 알파 붕괴를 겪으며, U와 마찬가지로 핵분열성입니다.[10] 토륨은 중성자 충격을 통해 토륨-232에서 번식할 수 있으며, 일반적으로 원자로에서 이 과정을 토륨 연료 주기라고 합니다. U의 핵분열성과 토륨의 자연적 풍부함([115]우라늄의 3배) 때문에 U는 2022년[update] 현재 널리 사용되지는 않지만 U와 Pu의 가능한 대안으로 핵 연료로 사용되는 것으로 조사되었습니다.[116][115] 우라늄-233의 붕괴 사슬은 넵투늄 계열의 일부를 형성하며 거의 안정한 비스무트-209(반수명 2.01×10년19)[5]와 안정한 탈륨-205에서 끝납니다.
우라늄-232는 반감기가 68.9년인 알파 방출체입니다.[5] 이 동위원소는 U 생성의 부산물로 생성되며, Tl과 같은 짧은 수명의 알파 및 감마 방출체를 통해 핵분열되지 않고 붕괴되기 때문에 성가신 것으로 간주됩니다.[116] 또한 토륨-232가 이중 베타 붕괴를 겪을 수 있어야 우라늄-232를 생성할 수 있을 것으로 예상되지만, 이는 아직 실험적으로 관찰되지 않았습니다.[5]
U에서 U를 포함한 모든 동위원소는 작은 클러스터 붕괴 가지(10−10% 미만)를 가지고 있으며, U 외에 모든 bar U도 작은 자발 핵분열 가지를 가지고 있습니다.[5] 즉, 자발 핵분열의 가장 큰 가지 비율은 U의 경우 약 5×10−5% 또는 약 200만 분의 1입니다.[117] 더 짧은 수명의 미량 동위원소 U와 U는 각각 6.752일과 23.45분의 반감기로 베타 붕괴를 겪습니다.[5]
우라늄 동위원소는 총 28개로 질량수가 214[118]~242개로 220개를 제외하고 확인되었습니다.[5][119] 천연 시료나 핵연료에서 발견되지 않는 우라늄 동위원소 중 가장 수명이 긴 것은 반감기가 20.23일인 알파 방출체 U입니다.[5] 이 동위원소는 표적 알파 입자 치료(TAT)에 사용되는 것으로 간주되었습니다.[120] 다른 모든 동위원소는 반감기가 1시간보다 짧지만, U(반수명 4.2일)와 U(반수명 14.1시간)는 제외됩니다.[5] 가장 짧은 수명을 가진 동위원소는 U로 반감기는 660나노초로 지금까지 알려지지 않은 U의 반감기는 더욱 짧을 것으로 예상됩니다.[121] 양성자가 풍부한 동위원소는 주로 알파 붕괴를 거치지만, U와 U는 각각 양전자 방출과 전자 포획을 통해 프로탁티늄 동위원소로 붕괴하고, 중성자가 풍부한 U, U, U는 베타 붕괴를 거쳐 넵투늄 동위원소를 형성합니다.[5][119]
농축

자연에서 우라늄은 우라늄-238(99.2742%)과 우라늄-235(0.7204%)로 발견됩니다. 동위원소 분리는 기체 냉각 원자로와 가압 중수로를 제외한 핵무기 및 대부분의 원자력 발전소에 사용되는 핵분열성 우라늄-235를 농축(농축)합니다. 우라늄-235의 핵분열 원자에 의해 방출되는 대부분의 중성자는 핵 연쇄 반응을 지속하기 위해 다른 우라늄-235 원자에 충돌해야 합니다. 이를 달성하기 위해 필요한 우라늄-235의 농도와 양을 '임계질량'이라고 합니다.
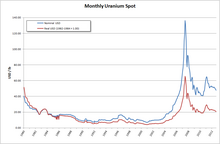
우라늄-235 분율이 3%에서 5%[122] 사이여야 '농축'으로 간주됩니다. 이 과정은 우라늄-235가 고갈되고 그에 상응하는 우라늄-238의 분율이 증가하는 엄청난 양의 우라늄을 생산하며, 이를 고갈된 우라늄 또는 'DU'라고 합니다. ' 고갈'로 간주되기 위해서는 U 농도가 0.3%[123]를 넘지 않아야 합니다. 2001년 이후 우라늄 가격이 상승했기 때문에 우라늄-235가 0.35% 이상 함유된 농축 광미는 재농축을 위해 고려되고 있으며, 고갈된 육불화우라늄 가격은 2001년 5달러에서 2007년 7월 1kg당 130달러를 넘어섰습니다.[123]
기체 상태의 육불화우라늄(UF
6)을 고속원심분리기를 이용해 UF와6 UF의6 분자량 차이로 분리하는 가스원심분리기 공정이 가장 저렴하고 선도적인 농축 공정입니다.[34] 기체 확산 공정은 농축을 위한 선도적인 방법이었고 맨해튼 프로젝트에 사용되었습니다. 이 과정에서 육불화우라늄은 은-아연막을 통해 반복적으로 확산되고, 우라늄의 다른 동위원소들은 확산 속도에 의해 분리됩니다(우라늄-238은 더 무겁기 때문에 우라늄-235보다 약간 느리게 확산됩니다).[34] 분자 레이저 동위원소 분리법은 우라늄-235와 불소의 결합을 차단하기 위해 정밀한 에너지의 레이저 빔을 사용합니다. 이렇게 하면 우라늄-238이 불소와 결합된 채로 남아 우라늄-235 금속이 용액에서 침전될 수 있습니다.[8] 농축의 대안적인 레이저 방법은 원자 증기 레이저 동위원소 분리(AVLIS)로 알려져 있으며 염료 레이저와 같은 가시광선 가변 레이저를 사용합니다.[124] 사용되는 또 다른 방법은 액체 열 확산입니다.[9]
알려진 자연 샘플에서 U 대 U 비율의 유일한 유의한 편차는 가봉의 오클로에서 발생합니다. 약 20억년 전에 천연 핵분열 원자로가 U 대 U의 비율이 저농축 우라늄의 비율과 더 비슷했을 때, 인간이 만든 경수로의 과정과 유사한 중성자 감속제 역할을 하도록 허용한 것입니다. 프랑스에서 우라늄 농축 과정에서 예상치에서 약간의 U 농도 편차가 발견되면서 이론적으로 미리 예측됐던 이런 자연 핵분열 원자로의 존재가 입증됐습니다. U를 훔치는 것과 같은 악의적인 인간 행동을 배제하기 위한 후속 조사는 일반적인 핵분열 생성물(또는 그들의 안정한 딸 핵종)의 동위원소 비율을 핵분열에 대해 예상되는 값과 일치하지만 그러한 원소의 비 핵분열에서 파생된 샘플에 대해 예상되는 값에서 벗어남으로써 이론을 확인했습니다.
인체노출
사람은 공기 중의 먼지를 흡입하거나 오염된 물과 음식을 섭취함으로써 우라늄(또는 라돈과 같은 방사성 딸)에 노출될 수 있습니다. 공기 중에 있는 우라늄의 양은 보통 매우 적지만, 인산염 비료를 가공하는 공장에서 일하거나, 핵무기를 만들거나 실험한 정부 시설 근처에 살거나, 고갈된 우라늄 무기가 사용된 현대 전장 근처에서 일하거나, 석탄 화력 발전소 근처에서 살거나 일하는 사람들, 우라늄 광석을 채굴하거나 처리하거나 원자로 연료로 사용하기 위해 우라늄을 농축하는 시설은 우라늄에 대한 노출이 증가했을 수 있습니다.[125][126] 우라늄 퇴적물(천연 또는 인공 슬래그 퇴적물) 위에 있는 주택 또는 구조물은 라돈 가스에 노출될 확률이 높아질 수 있습니다. 산업안전보건국(OSHA)은 작업장 내 우라늄 노출 허용 한도를 8시간 근무에 걸쳐 0.25mg/m로3 설정했습니다. 국립산업안전보건연구원(NIOSH)은 8시간 근무에 대한 권장 노출 한도(REL)를 0.2mg/m로3 설정하고, 단기 노출 한도는 0.6mg/m로3 설정했습니다. 10mg/m에서는3 우라늄이 즉시 생명과 건강에 위험합니다.[127]
대부분의 섭취된 우라늄은 소화 과정에서 배설됩니다. 산화물과 같은 불용성 형태의 우라늄을 섭취하면 0.5%만 흡수되는 반면, 용해성이 더 높은 우라닐 이온의 흡수는 최대 5%[28]까지 가능합니다. 그러나 용해성 우라늄 화합물은 체내를 빠르게 통과하는 경향이 있는 반면, 불용성 우라늄 화합물은 특히 먼지를 통해 폐로 흡입될 경우 더 심각한 노출 위험을 초래합니다. 흡수된 우라늄은 혈류로 들어간 후에 인산염에 대한 우라늄의 친화성 때문에 생체 축적되어 뼈 조직에 수년간 머무르는 경향이 있습니다.[28] 통합 우라늄은 뼈, 간, 신장 및 생식 조직에 축적되는 우라닐 이온이 됩니다.[128]
우라늄과 같이 원자번호 Z가 높은 원소는 자연 배경 감마선과 X선의 흡수 및 광전자의 재방출을 통해 팬텀 또는 2차 방사선독성을 나타낸다는 점에서 우라늄의 방사선 및 화학적 독성이 복합적으로 작용하고, DNA의 인산 부분에 대한 우라늄의 높은 친화성과 결합하여 단일 가닥 및 이중 가닥 DNA 파괴를 증가시킵니다.[129]
우라늄은 피부를 통해 흡수되지 않고, 우라늄이 방출하는 알파입자는 피부를 투과하지 못합니다.[25]
우라늄은 강철 표면과[130] 대수층에서 오염을 제거할 수 있습니다.[131][132]
효과 및 주의사항
우라늄은 약한 방사능 외에도 독성 금속이기 때문에 신장, 뇌, 간, 심장 및 기타 시스템의 정상적인 기능은 우라늄 노출에 의해 영향을 받을 수 있습니다.[28][133][134] 우라늄은 생식 독성 물질이기도 합니다.[135][136] U 붕괴의 주요 형태인 알파 방사선은 범위가 매우 짧고 피부를 투과하지 않기 때문에 방사선 효과는 일반적으로 국소적입니다. 흡입된 우라늄에서 나오는 알파 방사선은 피폭된 원자력 노동자들에게 폐암을 유발하는 것으로 입증되었습니다.[137] CDC는 천연 우라늄이나 고갈된 우라늄에 노출되어 인간 암이 발생하지 않았다는 연구 결과를 발표했지만,[138] 우라늄과 그 붕괴 생성물, 특히 라돈에 노출되는 것은 건강에 중대한 위협입니다.[139] 스트론튬-90, 요오드-131 및 기타 핵분열 생성물에 대한 노출은 우라늄 노출과 관련이 없지만 의료 절차 또는 사용 후 원자로 연료에 대한 노출 또는 핵무기의 낙진으로 인해 발생할 수 있습니다.[140]
고농도의 육불화우라늄에 우연히 노출되어 인명 피해가 발생했지만, 그 사망은 우라늄 자체보다는 독성이 강한 불산과 불화우라닐의 발생과 관련이 있었습니다.[141] 미세하게 나누어진 우라늄 금속은 우라늄이 열을 잘 흡수하기 때문에 화재 위험을 나타냅니다. 작은 알갱이들은 실온의 공기에서 자발적으로 점화됩니다.[10]
우라늄 금속은 일반적으로 충분한 예방책으로 장갑과 함께 취급됩니다.[142] 우라늄 농축액은 사람들이 그것을 흡입하거나 섭취하지 않도록 취급되고 함유됩니다.[142]
참고 항목
- K-65 잔기
- 우라늄 생산량에 따른 나라 목록
- 우라늄 매장량에 따른 나라 목록
- 우라늄 계획 목록
- 원자력 재해 및 방사능 사고 목록
- 원자력 및 방사선 사고 및 사고
- 원자력공학
- 핵연료주기
- 핵물리학
- 분자 U2 내의 5중 결합(이전에는 파이 결합으로 생각됨)
- 토륨 연료 사이클
- 세계 우라늄 청문회
메모들
- ^ "Standard Atomic Weights: Uranium". CIAAW. 1999.
- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. (4 May 2022). "Standard atomic weights of the elements 2021 (IUPAC Technical Report)". Pure and Applied Chemistry. doi:10.1515/pac-2019-0603. ISSN 1365-3075.
- ^ 가스상에서 th(-I) 및 U(-I)가 옥타카르보닐 이온으로 검출되었습니다.
- ^ Morss, L.R.; Edelstein, N.M.; Fuger, J., eds. (2006). The Chemistry of the Actinide and Transactinide Elements (3rd ed.). Netherlands: Springer. ISBN 978-9048131464.
- ^ a b c d e f g h i j k l m n o Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). "The NUBASE2020 evaluation of nuclear properties" (PDF). Chinese Physics C. 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- ^ Magurno, B.A.; Pearlstein, S, eds. (1981). Proceedings of the conference on nuclear data evaluation methods and procedures. BNL-NCS 51363, vol. II (PDF). Upton, NY (USA): Brookhaven National Lab. pp. 835 ff. Retrieved 6 August 2014.
- ^ "Uranium". Encyclopaedia Britannica. Retrieved 22 April 2017.
- ^ a b c d e 엠슬리 2001, 페이지 479.
- ^ a b c d e f "Uranium". The McGraw-Hill Science and Technology Encyclopedia (5th ed.). The McGraw-Hill Companies, Inc. 2005. ISBN 978-0-07-142957-3.
- ^ a b c d e f g h i j k l m n o p q Hammond, C. R. (2000). The Elements, in Handbook of Chemistry and Physics (PDF) (81st ed.). CRC press. ISBN 978-0-8493-0481-1.
- ^ "Uranium". Royal Society of Chemistry.
- ^ "Lead". Royal Society of Chemistry.
- ^ "Tungsten". Royal Society of Chemistry.
- ^ "Gold". Royal Society of Chemistry.
- ^ a b c d e f g "uranium". Columbia Electronic Encyclopedia (6th ed.). Columbia University Press. Archived from the original on 27 July 2011. Retrieved 27 September 2008.
- ^ a b c d e "uranium". Encyclopedia of Espionage, Intelligence, and Security. The Gale Group, Inc. Archived from the original on 27 July 2011. Retrieved 27 September 2008.
- ^ Rollett, A. D. (2008). Applications of Texture Analysis. John Wiley and Sons. p. 108. ISBN 978-0-470-40835-3.
- ^ a b c Grenthe, Ingmar; Drożdżyński, Janusz; Fujino, Takeo; Buck, Edgar C.; Albrecht-Schmitt, Thomas E.; Wolf, Stephen F. (2006). "Uranium". In Morss, Lester R.; Edelstein, Norman M.; Fuger, Jean (eds.). The Chemistry of the Actinide and Transactinide Elements (PDF). Vol. 5 (3rd ed.). Dordrecht, the Netherlands: Springer. pp. 52–160. doi:10.1007/1-4020-3598-5_5. ISBN 978-1-4020-3555-5. Archived from the original (PDF) on 7 March 2016.
- ^ "Development of DU Munitions". Depleted Uranium in the Gulf (II). Gulflink, official website of Force Health Protection & Readiness. 2000.
- ^ a b c d e 엠슬리 2001, 페이지 480.
- ^ "Nuclear Weapon Design". Federation of American Scientists. 1998. Archived from the original on 26 December 2008. Retrieved 19 February 2007.
- ^ 호머 러플린 차이나 주식회사 "굿모닝 아메리카 방송 관련 성명" 2012년 4월 1일 Wayback Machine에서 아카이브, 2011년 3월 16일 2012년 3월 25일 액세스.
- ^ "Dial R for radioactive – 12 July 1997 – New Scientist". Newscientist.com. Retrieved 12 September 2008.
- ^ "Uranium Mining". Atomic Heritage Foundation. Retrieved 23 December 2020.
- ^ a b "EPA Facts about Uranium" (PDF). U.S. Environmental Protection Agency. Archived from the original (PDF) on 29 November 2014. Retrieved 20 September 2014.
- ^ "Uranium Containing Dentures (ca. 1960s, 1970s)". ORAU Museum of Radiation and Radioactivity. Oak Ridge Associated Universities. 1999. Retrieved 11 October 2021.
- ^ 엠슬리 2001, 페이지 482.
- ^ a b c d e f g h i j 엠슬리 2001, 477쪽.
- ^ Velek, Victor (7 May 2008). "Uran stumbles in wooing towns". Prague Post. Retrieved 7 July 2022.
- ^ "The History of Ore & Uranium Mining in Czechia". November 2017.
- ^ Klaproth, M. H. (1789). "Chemische Untersuchung des Uranits, einer neuentdeckten metallischen Substanz". Chemische Annalen. 2: 387–403.
- ^ "Uranium". The American Heritage Dictionary of the English Language (4th ed.). Houghton Mifflin Company. Archived from the original on 27 July 2011. Retrieved 15 January 2007.
- ^ Péligot, E.-M. (1842). "Recherches Sur L'Uranium". Annales de chimie et de physique. 5 (5): 5–47.
- ^ a b c d 엠슬리 2001, 478쪽.
- ^ "The Electric Journal". Westinghouse Club. 10 April 1920 – via Google Books.
- ^ Gillett, Horace Wadsworth; Mack, Edward Lawrence (10 April 1917). Preparation of ferro-uranium. Technical Paper 177 – U.S. Bureau of Mines. U.S. Govt. print. off. – via Google Books.
- ^ a b c d e f Seaborg 1968, 페이지 773.
- ^ Fermi, Enrico (12 December 1938). "Artificial radioactivity produced by neutron bombardment: Nobel Lecture" (PDF). Royal Swedish Academy of Sciences. Archived from the original (PDF) on 9 August 2018. Retrieved 14 June 2017.
- ^ De Gregorio, A. (2003). "A Historical Note About How the Property was Discovered that Hydrogenated Substances Increase the Radioactivity Induced by Neutrons". Nuovo Saggiatore. 19: 41–47. arXiv:physics/0309046. Bibcode:2003physics...9046D.
- ^ Nigro, M. (2004). "Hahn, Meitner e la teoria della fissione" (PDF). Archived from the original (PDF) on 25 March 2009. Retrieved 5 May 2009.
- ^ van der Krogt, Peter. "Elementymology & Elements Multidict". Retrieved 5 May 2009.
- ^ Meitner, L.; Frisch, O. (1939). "Disintegration of Uranium by Neutrons: a New Type of Nuclear Reaction". Nature. 143 (5218): 239–240. Bibcode:1969Natur.224..466M. doi:10.1038/224466a0. S2CID 4188874.
- ^ "Alfred O. C. Nier". www.aps.org. Retrieved 4 December 2016.
- ^ Manfred Popp (21 September 2016). "Wissenschaftsgeschichte: Hitlers Atombombe – warum es sie nicht gab – Spektrum der Wissenschaft". Spektrum.de. Retrieved 25 February 2022.
- ^ "Chicago Pile One". large.stanford.edu. Retrieved 4 December 2016.
- ^ Walsh, John (19 June 1981). "A Manhattan Project Postscript" (PDF). Science. 212 (4501). AAAS: 1369–1371. Bibcode:1981Sci...212.1369W. doi:10.1126/science.212.4501.1369. PMID 17746246. Retrieved 23 March 2013.
- ^ 헬름라이히, J.E. 희귀한 광석을 모으는 것: 우라늄 획득의 외교, 1943-1954, Princeton UP, 1986: ch. 10 ISBN 0-7837-9349-9
- ^ "Reactors Designed by Argonne National Laboratory: Fast Reactor Technology". U.S. Department of Energy, Argonne National Laboratory. 2012. Retrieved 25 July 2012.
- ^ "History and Success of Argonne National Laboratory: Part 1". U.S. Department of Energy, Argonne National Laboratory. 1998. Archived from the original on 26 September 2006. Retrieved 28 January 2007.
- ^ "Reactors Designed by Argonne National Laboratory: Light Water Reactor Technology Development". U.S. Department of Energy, Argonne National Laboratory. 2012. Retrieved 25 July 2012.
- ^ "1956: Queen switches on nuclear power". BBC News. 17 October 1956. Retrieved 28 June 2006.
- ^ "STR (Submarine Thermal Reactor) in "Reactors Designed by Argonne National Laboratory: Light Water Reactor Technology Development"". U.S. Department of Energy, Argonne National Laboratory. 2012. Retrieved 25 July 2012.
- ^ a b "Oklo: Natural Nuclear Reactors". Office of Civilian Radioactive Waste Management. Archived from the original on 3 June 2004. Retrieved 28 June 2006.
- ^ Warneke, T.; Croudace, I. W.; Warwick, P. E. & Taylor, R. N. (2002). "A new ground-level fallout record of uranium and plutonium isotopes for northern temperate latitudes". Earth and Planetary Science Letters. 203 (3–4): 1047–1057. Bibcode:2002E&PSL.203.1047W. doi:10.1016/S0012-821X(02)00930-5.
- ^ "The Worst Nuclear Disasters". Time. 25 March 2009. Archived from the original on 28 March 2009. Retrieved 24 May 2010.
- ^ Gilliland, Frank D.; Hunt, William C.; Pardilla, Marla; Key, Charles R. (March 2000). "Uranium Mining and Lung Cancer Among Navajo Men in New Mexico and Arizona, 1969 to 1993". Journal of Occupational and Environmental Medicine. 42 (3): 278–283. doi:10.1097/00043764-200003000-00008. PMID 10738707.
- ^ Brugge, Doug; Goble, Rob (2002). "The History of Uranium Mining and the Navajo People". American Journal of Public Health. 92 (9). Ajph.org: 1410–1419. doi:10.2105/AJPH.92.9.1410. PMC 3222290. PMID 12197966.
- ^ Van Unnik, J. G.; Broerse, J. J.; Geleijns, J.; Jansen, J. T.; Zoetelief, J.; Zweers, D. (1997). "Survey of CT techniques and absorbed dose in various Dutch hospitals". The British Journal of Radiology. 70 (832): 367–371. doi:10.1259/bjr.70.832.9166072. PMID 9166072. (18개 병원 3000건 검사)
- ^ 러시아의 핵연료 주기 세계 원자력 협회. 2021년 12월 업데이트.
- ^ "History/Origin of Chemicals". NASA. Retrieved 1 January 2013.
- ^ Burbidge, E. M.; Burbidge, G. R.; Fowler, W. A.; Hoyle, F. (1957). "Synthesis of the Elements in Stars". Reviews of Modern Physics. 29 (4): 547. Bibcode:1957RvMP...29..547B. doi:10.1103/RevModPhys.29.547.
- ^ Clayton, Donald D. (1968). Principles of Stellar Evolution and Nucleosynthesis. New York: Mc-Graw-Hill. pp. 577–91. ISBN 978-0226109534.
- ^ a b Trenn, Thaddeus J. (1978). "Thoruranium (U-236) as the extinct natural parent of thorium: The premature falsification of an essentially correct theory". Annals of Science. 35 (6): 581–97. doi:10.1080/00033797800200441.
- ^ Tissot, François L. H.; Dauphas, Nicolas; Grossmann, Lawrence (4 March 2016). "Origin of uranium isotope variations in early solar nebula condensates". Science Advances. 2 (3): e1501400. arXiv:1603.01780. Bibcode:2016SciA....2E1400T. doi:10.1126/sciadv.1501400. PMC 4783122. PMID 26973874.
- ^ Biever, Celeste (27 July 2005). "First measurements of Earth's core radioactivity". New Scientist. Retrieved 7 July 2022.
- ^ "Potassium-40 heats up Earth's core". physicsworld.com. 7 May 2003. Retrieved 14 January 2007.
- ^ Schnug, E., Sun, Y., Zhang, L., Windmann, H., Lottermoser, B.G., Ulrich, A.E., Bol, R., Makeawa, M. 및 Haneklaus, S.H. (2023) "인산염 비료가 포함된 기본 부하 – 토양 생산성에 대한 제약?" In: Bolan, N.S. and Kirkham, M.B. (eds.) 생산성 유지를 위한 토양 제약 관리 CRC Press.
- ^ Min, M.; Xu, H.; Chen, J.; Fayek, M. (2005). "Evidence of uranium biomineralization in sandstone-hosted roll-front uranium deposits, northwestern China". Ore Geology Reviews. 26 (3–4): 198. Bibcode:2005OGRv...26..198M. doi:10.1016/j.oregeorev.2004.10.003.
- ^ Koribanics, N. M.; Tuorto, S. J.; Lopez-Chiaffarelli, N.; McGuinness, L. R.; Häggblom, M. M.; Williams, K. H.; Long, P. E.; Kerkhof, L. J. (2015). "Spatial Distribution of an Uranium-Respiring Betaproteobacterium at the Rifle, CO Field Research Site". PLOS ONE. 10 (4): e0123378. Bibcode:2015PLoSO..1023378K. doi:10.1371/journal.pone.0123378. PMC 4395306. PMID 25874721.
- ^ Renshaw, J. C.; Butchins, L. J. C.; Livens, F. R.; et al. (June 2005). "Bioreduction of uranium: environmental implications of a pentavalent intermediate". Environmental Science & Technology. 39 (15): 5657–5660. Bibcode:2005EnST...39.5657R. doi:10.1021/es048232b. PMID 16124300.
- ^ Vitesse, GF; Morris, K; Natrajan, LS; Shaw, S (January 2020). "Multiple Lines of Evidence Identify U(V) as a Key Intermediate during U(VI) Reduction by Shewanella oneidensis MR1". Environmental Science & Technology. 54 (4): 2268–2276. Bibcode:2020EnST...54.2268V. doi:10.1021/acs.est.9b05285. PMID 31934763.
- ^ 엠슬리 2001, 페이지 476 및 482.
- ^ Macaskie, L. E.; Empson, R. M.; Cheetham, A. K.; Grey, C. P. & Skarnulis, A. J. (1992). "Uranium bioaccumulation by a Citrobacter sp. as a result of enzymically mediated growth of polycrystalline HUO
2PO
4". Science. 257 (5071): 782–784. Bibcode:1992Sci...257..782M. doi:10.1126/science.1496397. PMID 1496397. - ^ Anderson, R. T.; Vrionis, H. A.; Ortiz-Bernad, I.; Resch, C. T.; Long, P. E.; Dayvault, R.; Karp, K.; Marutzky, S.; Metzler, D. R.; Peacock, A.; White, D. C.; Lowe, M.; Lovley, D. R. (2003). "Stimulating the in situ activity of Geobacter species to remove uranium from the groundwater of a uranium-contaminated aquifer". Applied and Environmental Microbiology. 69 (10): 5884–5891. Bibcode:2003ApEnM..69.5884A. doi:10.1128/AEM.69.10.5884-5891.2003. PMC 201226. PMID 14532040.
- ^ Gadd, G. M. (March 2010). "Metals, minerals and microbes: geomicrobiology and bioremediation". Microbiology. 156 (Pt 3): 609–643. doi:10.1099/mic.0.037143-0. PMID 20019082.
- ^ Nilgiriwala, K.S.; Alahari, A.; Rao, A. S. & Apte, S.K. (2008). "Cloning and Overexpression of Alkaline Phosphatase PhoK from Sphingomonas sp. Strain BSAR-1 for Bioprecipitation of Uranium from Alkaline Solutions". Applied and Environmental Microbiology. 74 (17): 5516–5523. Bibcode:2008ApEnM..74.5516N. doi:10.1128/AEM.00107-08. PMC 2546639. PMID 18641147.
- ^ a b c d "World Uranium Mining". World Nuclear Association. Retrieved 31 January 2023.
- ^ Seaborg 1968, 페이지 774.
- ^ "Athabasca Basin, Saskatchewan". Retrieved 4 September 2009.
- ^ Gupta, C. K. & Mukherjee, T. K. (1990). Hydrometallurgy in extraction processes. Vol. 1. CRC Press. pp. 74–75. ISBN 978-0-8493-6804-2.
- ^ "Uranium production". Our World in Data. Retrieved 6 March 2020.
- ^ a b "Uranium Supplies: Supply of Uranium – World Nuclear Association". www.world-nuclear.org.
- ^ a b "Global Uranium Resources to Meet Projected Demand". International Atomic Energy Agency. 2006. Retrieved 29 March 2007.
- ^ "Uranium Mining and Processing in South Australia". South Australian Chamber of Mines and Energy. 2002. Archived from the original on 6 January 2012. Retrieved 14 January 2007.
- ^ Ngoupana, P.-M.; Felix, B. (2011). Barker, A. (ed.). "Areva suspends CAR uranium mine project". Central African Republic News. Retrieved 7 March 2020.
- ^ "Military Warheads as a Source of Nuclear Fuel". World-nuclear.org. Retrieved 24 May 2010.
- ^ "Megatons to Megawatts". U.S. Enrichment Corp. Archived from the original on 16 July 2008.
- ^ "Uranium recovery from Seawater". Japan Atomic Energy Research Institute. 23 August 1999. Archived from the original on 17 October 2009. Retrieved 3 September 2008.
- ^ "How long will nuclear energy last?". 12 February 1996. Archived from the original on 10 April 2007. Retrieved 29 March 2007.
- ^ Tsezos, M.; Noh, S. H. (1984). "Extraction of uranium from sea water using biological origin adsorbents". The Canadian Journal of Chemical Engineering. 62 (4): 559–561. doi:10.1002/cjce.5450620416.
- ^ "ORNL technology moves scientists closer to extracting uranium from seawater". Oak Ridge National Laboratory, United States. 21 August 2012. Archived from the original on 25 August 2012. Retrieved 22 February 2013.
- ^ "Fueling nuclear power with seawater". Pnnl.gov. 21 August 2012. Retrieved 22 February 2013.
- ^ "NUEXCO Exchange Value (Monthly Uranium Spot)". Archived from the original on 12 December 2007.
- ^ "World Uranium Production". UxC Consulting Company, LLC. Archived from the original on 27 February 2007. Retrieved 11 February 2007.
- ^ Mithridates (24 July 2008). "Page F30: Kazakhstan to surpass Canada as the world's largest producer of uranium by last year (2009)". Mithridates.blogspot.com. Retrieved 12 September 2008.
- ^ "Kazakistan uranyum üretimini artıracak". Zaman.com.tr (in Turkish). Zaman Gazetesi. 28 July 2008. Archived from the original on 13 January 2009. Retrieved 12 September 2008.
- ^ "In Situ Leach Mining (ISL) of Uranium – World Nuclear Association". www.world-nuclear.org. Retrieved 6 May 2021.
- ^ "Big Uranium Find Announced in Somalia". The New York Times. 16 March 1968. Retrieved 16 May 2014.
- ^ "Lack of fuel may limit U.S. nuclear power expansion". Massachusetts Institute of Technology. 21 March 2007. Retrieved 29 March 2007.
- ^ Deffeyes, Kenneth S. & MacGregor, Ian D. (January 1980). "World Uranium Resources". Scientific American. 242 (1): 66. Bibcode:1980SciAm.242a..66D. doi:10.1038/scientificamerican0180-66. OSTI 6665051.
- ^ Kloprogge, J. Theo; Ponce, Concepcion P.; Loomis, Tom A. (2021). The periodic table : nature's building blocks : an introduction to the naturally occurring elements, their origins and their uses. Amsterdam: Elsevier. pp. 861–862. ISBN 978-0-12-821538-8. OCLC 1223058470.
- ^ Seaborg 1968, 페이지 779.
- ^ a b c "Chemical Forms of Uranium". Argonne National Laboratory. Archived from the original on 22 September 2006. Retrieved 18 February 2007.
- ^ a b Seaborg 1968, 페이지 778.
- ^ a b c d 푸이그도메네크, Ignasi (2004) Hydra/Medusa Chemical Equilibrium Database 및 Ploting Software. KTH 왕립 공과대학교
- ^ a b c d e f g h i j Seaborg 1968, 페이지 782.
- ^ a b Seaborg 1968, 페이지 780.
- ^ Beiser, A. (2003). "Nuclear Transformations" (PDF). Concepts of Modern Physics (6th ed.). McGraw-Hill Education. pp. 432–434. ISBN 978-0-07-244848-1. Archived from the original (PDF) on 4 October 2016. Retrieved 4 July 2016.
- ^ Roederer, I. U.; Kratz, K.; Frebel, A.; Christlieb, N.; Pfeiffer, B.; Cowan, J. J.; Sneden, C. (2009). "The end of nucleosynthesis: Production of lead and thorium in the early galaxy". The Astrophysical Journal. 698 (2): 1963–1980. arXiv:0904.3105. Bibcode:2009ApJ...698.1963R. doi:10.1088/0004-637X/698/2/1963. hdl:2152/35050. S2CID 14814446.
- ^ a b c 플루토늄-244가 원시 핵종으로 발생한 것은 논란의 여지가 있지만, 일부 검출 보고는 성간 매질에서 떨어지는 것으로 보고되었습니다.[111][112]
- ^ Lachner, J.; et al. (2012). "Attempt to detect primordial 244Pu on Earth". Physical Review C. 85 (1): 015801. Bibcode:2012PhRvC..85a5801L. doi:10.1103/PhysRevC.85.015801.
- ^ Wallner, A.; Faestermann, T.; Feige, J.; Feldstein, C.; Knie, K.; Korschinek, G.; Kutschera, W.; Ofan, A.; Paul, M.; Quinto, F.; Rugel, G.; Steier, P. (2015). "Abundance of live 244Pu in deep-sea reservoirs on Earth points to rarity of actinide nucleosynthesis". Nature Communications. 6: 5956. arXiv:1509.08054. Bibcode:2015NatCo...6.5956W. doi:10.1038/ncomms6956. ISSN 2041-1723. PMC 4309418. PMID 25601158.
- ^ Tretyak, V.I.; Zdesenko, Yu.G. (2002). "Tables of Double Beta Decay Data — An Update". At. Data Nucl. Data Tables. 80 (1): 83–116. Bibcode:2002ADNDT..80...83T. doi:10.1006/adnd.2001.0873.
- ^ Marouli, M.; Pommé, S.; Jobbágy, V.; Van Ammel, R.; Paepen, J.; Stroh, H.; Benedik, L. (2014). "Alpha-particle emission probabilities of 236U obtained by alpha spectrometry". Applied Radiation and Isotopes. 87: 292–296. doi:10.1016/j.apradiso.2013.11.020. ISSN 0969-8043. PMID 24309010.
- ^ a b Near Term and Promising Long Term Options for the Deployment of Thorium Based Nuclear Energy (PDF) (Report). Vienna: International Atomic Energy Agency. 2022.
- ^ a b Forsburg, C. W.; Lewis, L. C. (24 September 1999). "Uses For Uranium-233: What Should Be Kept for Future Needs?" (PDF). Ornl-6952. Oak Ridge National Laboratory.
- ^ Goffer, Zvi (2006). Archaeological Chemistry (2nd ed.). Wiley. p. 106. ISBN 978-0-471-91515-7.
- ^ Zhang, Z. Y.; et al. (2021). "New α -Emitting Isotope 214 U and Abnormal Enhancement of α -Particle Clustering in Lightest Uranium Isotopes". Physical Review Letters. 126 (15): 152502. arXiv:2101.06023. Bibcode:2021PhRvL.126o2502Z. doi:10.1103/PhysRevLett.126.152502. PMID 33929212. S2CID 231627674. Retrieved 15 May 2021.
- ^ a b Niwase, T.; Watanabe, Y. X.; Hirayama, Y.; et al. (2023). "Discovery of New Isotope 241U and Systematic High-Precision Atomic Mass Measurements of Neutron-Rich Pa-Pu Nuclei Produced via Multinucleon Transfer Reactions" (PDF). Physical Review Letters. 130 (13): 132502-1–132502-6. Bibcode:2023PhRvL.130m2502N. doi:10.1103/PhysRevLett.130.132502. PMID 37067317. S2CID 257976576.
- ^ Mastren, T.; Stein, B. W.; Parker, T. G.; Radchenko, V.; Copping, R.; Owens, A.; Wyant, L. E.; Brugh, M.; Kozimor, S. A.; Noriter, F. M.; Birnbaum, E. R.; John, K. D.; Fassbender, M. E. (2018). "Separation of protactinium employing sulfur-based extraction chromatographic resins". Analytical Chemistry. 90 (11): 7012–7017. doi:10.1021/acs.analchem.8b01380. ISSN 0003-2700. OSTI 1440455. PMID 29757620.
- ^ Khuyagbaatar, J.; et al. (11 December 2015). "New Short-Lived Isotope 221U and the Mass Surface Near N = 126". Physical Review Letters. 115 (24): 242502. Bibcode:2015PhRvL.115x2502K. doi:10.1103/PhysRevLett.115.242502. PMID 26705628. S2CID 12184696.
- ^ "Uranium Enrichment". Argonne National Laboratory. Archived from the original on 24 January 2007. Retrieved 11 February 2007.
- ^ a b Diehl, Peter. "Depleted Uranium: a by-product of the Nuclear Chain". Laka Foundation. Archived from the original on 13 January 2013. Retrieved 31 July 2009.
- ^ Duarte, F. J.; Hillman, L. W., eds. (1990). Dye Laser Principles. Academic. p. 413. ISBN 978-0-12-222700-4. Archived from the original on 17 September 2010.
- ^ "Radionuclide Basics: Uranium". U.S. Environmental Protection Agency. 16 February 2023. Retrieved 19 April 2023.
- ^ "ToxFAQ for Uranium". Agency for Toxic Substances and Disease Registry. 18 March 2014. Retrieved 19 April 2023.
- ^ "CDC – NIOSH Pocket Guide to Chemical Hazards – Uranium (insoluble compounds, as U)". National Institute for Occupational Safety and Health. 30 October 2019. Retrieved 19 April 2023.
- ^ Permyakov, Eugene (2009). Metalloproteomics. Hoboken: John Wiley & Sons. p. 564. ISBN 978-0-470-44774-1. OCLC 609844907.
- ^ 버스비, C. and Schnug, E. (2008). "우라늄 오염의 고도화된 생화학적, 생물물리학적 측면" In: De Kok, L.J. and Schnug, E. (Eds) 비료 유래 우라늄의 하중과 운명. 백후이스 출판사, 레이든, 네덜란드. ISBN 978-90-5782-193-6
- ^ Francis, A. J.; Dodge, C. J.; McDonald, J. A.; Halada, G. P. (2005). "Decontamination of uranium-contaminated steel surfaces by hydroxycarboxylic acid with uranium recovery". Environmental Science & Technology. 39 (13): 5015–21. Bibcode:2005EnST...39.5015F. doi:10.1021/es048887c. PMID 16053105.
- ^ Gandhi, T. Pushparaj; Sampath, Prasanna Venkatesh; Maliyekkal, Shihabudheen M. (15 June 2022). "A critical review of uranium contamination in groundwater: Treatment and sludge disposal". The Science of the Total Environment. 825: 153947. Bibcode:2022ScTEn.825o3947G. doi:10.1016/j.scitotenv.2022.153947. ISSN 1879-1026. PMID 35189244. S2CID 246988421.
- ^ Prusty, Sourav; Somu, Prathap; Sahoo, Jitendra Kumar; Panda, Debasish; Sahoo, Sunil Kumar; Sahoo, Shraban Kumar; Lee, Yong Rok; Jarin, T.; Sundar, L. Syam; Rao, Koppula Srinivas (December 2022). "Adsorptive sequestration of noxious uranium (VI) from water resources: A comprehensive review". Chemosphere. 308 (Pt 1): 136278. Bibcode:2022Chmsp.308m6278P. doi:10.1016/j.chemosphere.2022.136278. ISSN 1879-1298. PMID 36057349. S2CID 251999162.
- ^ Craft, E. S.; Abu-Qare, A. W.; Flaherty, M. M.; Garofolo, M. C.; Rincavage, H. L. & Abou-Donia, M. B. (2004). "Depleted and natural uranium: chemistry and toxicological effects" (PDF). Journal of Toxicology and Environmental Health Part B: Critical Reviews. 7 (4): 297–317. Bibcode:2004JTEHB...7..297C. CiteSeerX 10.1.1.535.5247. doi:10.1080/10937400490452714. PMID 15205046. S2CID 9357795.
- ^ Agency for Toxic Substances and Disease Registry (ATSDR) (February 2013). "2. Relevance to Public Health" (PDF). Toxicological Profile for Uranium (Report). Atlanta, GA: U.S. Department of Health and Human Services, Public Health Service. pp. 11–38. CAS# 7440-61-1.
- ^ Hindin, Rita; Brugge, D.; Panikkar, B. (2005). "Teratogenicity of depleted uranium aerosols: A review from an epidemiological perspective". Environ Health. 4 (1): 17. Bibcode:2005EnvHe...4...17H. doi:10.1186/1476-069X-4-17. PMC 1242351. PMID 16124873.
- ^ Arfsten, D. P.; Still, K. R.; Ritchie, G. D. (2001). "A review of the effects of uranium and depleted uranium exposure on reproduction and fetal development". Toxicology and Industrial Health. 17 (5–10): 180–91. Bibcode:2001ToxIH..17..180A. doi:10.1191/0748233701th111oa. PMID 12539863. S2CID 25310165.
- ^ Grellier, James; Atkinson, Will; Bérard, Philippe; Bingham, Derek; Birchall, Alan; Blanchardon, Eric; Bull, Richard; Guseva Canu, Irina; Challeton-de Vathaire, Cécile; Cockerill, Rupert; Do, Minh T; Engels, Hilde; Figuerola, Jordi; Foster, Adrian; Holmstock, Luc; Hurtgen, Christian; Laurier, Dominique; Puncher, Matthew; Riddell, Tony; Samson, Eric; Thierry-Chef, Isabelle; Tirmarche, Margot; Vrijheid, Martine; Cardis, Elisabeth (2017). "Risk of lung cancer mortality in nuclear workers from internal exposure to alpha particle-emitting radionuclides". Epidemiology. 28 (5): 675–684. doi:10.1097/EDE.0000000000000684. PMC 5540354. PMID 28520643.
- ^ "Public Health Statement for Uranium" (PDF). CDC. Retrieved 5 May 2023.
- ^ 페르날드 사료 원료 생산 센터 근로자에 대한 라돈 노출 페이지 검토: 2020년 4월 8일. 미국 국립 산업 안전 보건 연구소(NIOSH)
- ^ 1968년 미국 원자력 위원회 핵종 도표
- ^ Dart, Richard C. (2004). Medical Toxicology. Lippincott Williams & Wilkins. p. 1468. ISBN 978-0-7817-2845-4.
- ^ a b "Radiation Fact Sheets #27, Uranium (U)". Washington State Department of Health, Office of Radiation Protection. 2010. Archived from the original on 28 September 2011. Retrieved 23 August 2011.
참고문헌
- Emsley, John (2001). "Uranium". Nature's Building Blocks: An A to Z Guide to the Elements. Oxford: Oxford University Press. pp. 476–482. ISBN 978-0-19-850340-8.
- Seaborg, Glenn T. (1968). "Uranium". The Encyclopedia of the Chemical Elements. Skokie, Illinois: Reinhold Book Corporation. pp. 773–786. LCCN 68029938.
외부 링크
- 미국 에너지정보청의 핵연료 데이터 및 분석
- 우라늄의 현시세
- 세계 우라늄 매장량 지도
- Dittmar, William (1888). . Encyclopædia Britannica. Vol. XXIV (9th ed.). p. 7.
- 알소스 디지털 도서관의 우라늄에 대한 주석이 달린 서지학
- NLM 유해물질 데이터베이스 – 우라늄, 방사능
- CDC – NIOSH 포켓 화학적 위험 가이드
- 나미비아 랑거 하인리히 광산에서 우라늄 채굴
- 월드 핵뉴스
- 환경 의학 분야의 ATSDR 사례 연구: 우라늄 독성 미국 보건복지부
- 비디오 주기율표 우라늄 (노팅엄 대학교)


![World uranium production (mines) and demand[77]](http://upload.wikimedia.org/wikipedia/commons/thumb/7/75/U_production-demand.png/431px-U_production-demand.png)

![Uranium production 2015, in tonnes[81]](http://upload.wikimedia.org/wikipedia/commons/thumb/9/9a/Uranium_production%2C_OWID.svg/425px-Uranium_production%2C_OWID.svg.png)




