MTA3
MTA3| MTA3 | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||
| 식별자 | |||||||||||||||||||||||||||||||
| 에일리어스 | MTA3, 전이 관련 1 패밀리 멤버 3 | ||||||||||||||||||||||||||||||
| 외부 ID | OMIM: 609050 MGI: 2151172 HomoloGene: 14282 GeneCard: MTA3 | ||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| 위키데이터 | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
전이관련단백질 MTA3는 사람에게서 [5][6][7][8]MTA3유전자에 의해 암호화되는 단백질이다.MTA3 단백질은 핵뿐만 아니라[9] 다른 세포 구획에 위치하는 MTA3는 뉴클레오좀 리모델링 및 탈아세틸레이트(NuRD) 복합체의 구성요소이며 유전자 [10][11][12]발현에 관여한다.MTA3의 발현 패턴은 유선 종양 [13][14]발생 시 MTA1, MTA2의 발현 패턴과 반대입니다.그러나, MTA3는 또한 다양한 인간 [15][16][17]암에서 과다하게 발현된다.
검출
마우스 Mta3는 My G. Mahoney 연구팀에 [5]의해 인간 MTA1 부분 단편과 함께 마우스 각질세포 cDNA 라이브러리를 스크리닝하는 과정에서 개방된 판독 프레임을 가진 부분 cDNA로 처음 확인되었다.전장 Mta3 cDNA는 C57B1/6J 마우스피부의 [5]RNA를 이용하여 5'-RACE 방법론을 통해 복제되었다.추출된 아미노산과 GeneBank의 배열과의 비교는 MTA3를 세 번째 MTA 패밀리 멤버로 설정했다.
유전자 및 스플라이스 변종
Mta3는 생쥐의 경우 염색체 12p, 사람의 경우 2p21의 경우 MTA3에 국소화된다.인간의 MTA3 유전자는 20개의 엑손과 19개의 대체 스플라이스된 트랜스크립트를 포함한다.이들 중 9개의 MTA3 전사체는 392, 514, 515, 537, 590 및 594개의 아미노산 6개의 단백질, 2개의 MTA3 전사체 코드 18 아미노산 및 91개의 아미노산 폴리펩타이드를 [18]코드화할 것으로 예측된다.나머지 10개의 트랜스크립트는 비코딩 RNA입니다.뮤린 Mta3 유전자는 9개의 트랜스크립트를 포함하고 있으며, 그 중 6개는 251개의 아미노산부터 591개의 아미노산까지의 단백질을 코드하는 반면, 1개의 트랜스크립트는 40개의 아미노산 폴리펩타이드를 코드하는 것으로 예측된다.뮤린 Mta3 유전자는 두 개의 예측된 비암호화 RNA를 포함하고 있다.
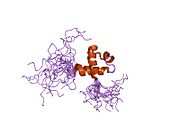
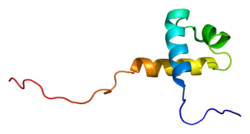
구조.
MTA3 단백질 도메인의 전체 구성은 BAH(Broomo-Adjacent Homology), ELM2(egl-27 및 MTA1 호몰로지), SANT(SWI, ADA2, N-CoR, TFIIB-BATA)를 가진 다른 두 패밀리 멤버와 유사하다.Mta3의 SH3 모티브는 [5]신호 단백질을 포함하는 SH3인 Fyn 및 Grb2와 상호작용할 수 있도록 합니다.
기능.
MTA3의 기능은 암 유형의 맥락에서 차등 조절되는 것으로 여겨진다.예를 들어 유방암과[13][14] 자궁내막선암에서 [17]MTA3 발현이 하향 조절된다.MTA3는 비소세포 폐암[15], 사람의 태반 및 융모막암 [16]세포에서 과압된다.유방암에서 MTA3의 상실은 달팽이를 상향 조절하여 E-카드헤린 접착 [19]분자를 억제함으로써 EMT와 유방암 세포의 침투를 촉진한다.유방상피와 유방암 세포에서 MTA3는 에스트로겐 조절 유전자이며 호르몬 반응의 모든 수식어인 MTA1과 MTA를 포함하는 더 큰 조절 네트워크의 일부이며 성장과 [19][20][21][22]분화에 관련된 과정에 참여한다.따라서 MTA3-NuRD 복합체는 유선상피세포 및 마우스에서의 Wnt4의 발현을 조절하고 Wnt4의존성 [23]덕트형성을 제어한다.
억제 작용과는 대조적으로, MTA3는 영양아세포의 저산소 조건 하에서 HIF1α와 그 표적 유전자의 발현을 자극하며 임신 [24]중 분화에 관여하는 것으로 생각된다.MTA3-NuRD 복합체 및 하류 표적은 제브라피쉬 모델[11][25] 시스템에서 원시 조혈 및 혈관신생에 참여하는 것으로 나타났다. BCL6 코어프레셔 복합체의 일부로서 MTA3는 PRDM1을 포함한 표적 유전자의 BCL6 의존적 억제를 조절하고 B세포의 [26][27]분화를 조절한다.
규정
에스트로겐 수용체는 유방암 [19][20][21]세포에서 MTA3의 발현을 자극한다.SP1 전사인자는 MTA3의 [21]전사를 자극합니다.MicroRNA-495는 비소세포 폐암 세포의 성장과 [28]이동뿐만 아니라 MTA3 mRNA의 수치를 억제한다.한의학인 β-elemene은 유방암[29] 세포에서 MTA3의 발현을 상향 조정한다.
대상
MTA3-NuRD 복합체는 상피에서 [23]간엽 전이(EMT),[19] 유선 상피 세포에서 Wnt4 발현의 마스터 조절기인 스네일을 억제하고 BCL6-코어 프레셔 복합체는[26][27] GTA3와 상호작용하여 GATA3의 발현을 조절한다.또한 MTA3는 저산소 조건에서 [24]HIF1과 그 활성화 활성을 상향 조절한다.
메모들
이 기사의 2016년 버전은 외부 전문가에 의해 이중 출판 모델로 업데이트되었습니다.대응하는 학술 동료 리뷰 기사는 Gene에 게재되었으며 다음과 같이 인용할 수 있다. Rakesh Kumar; Rui-An Wang (15 May 2016). "Structure, expression and functions of MTA genes". Gene. Gene Wiki Review Series. 582 (2): 112–21. doi:10.1016/J.GENE.2016.02.012. ISSN 0378-1119. PMC 4785049. PMID 26869315. Wikidata Q28273245. |
레퍼런스
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG000057935 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG000055817 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b c d e Simpson A, Uitto J, Rodeck U, Mahoney MG (Jul 2001). "Differential expression and subcellular distribution of the mouse metastasis-associated proteins Mta1 and Mta3". Gene. 273 (1): 29–39. doi:10.1016/s0378-1119(01)00563-7. PMID 11483358.
- ^ Fujita N, Jaye DL, Kajita M, Geigerman C, Moreno CS, Wade PA (Apr 2003). "MTA3, a Mi-2/NuRD complex subunit, regulates an invasive growth pathway in breast cancer". Cell. 113 (2): 207–19. doi:10.1016/S0092-8674(03)00234-4. PMID 12705869. S2CID 5773916.
- ^ Kumar R, Wang RA, Bagheri-Yarmand R (Oct 2003). "Emerging roles of MTA family members in human cancers". Seminars in Oncology. 30 (5 Suppl 16): 30–7. doi:10.1053/j.seminoncol.2003.08.005. PMID 14613024.
- ^ "Entrez Gene: MTA3 metastasis associated 1 family, member 3".
- ^ Liu J, Wang H, Huang C, Qian H (Dec 2014). "Subcellular localization of MTA proteins in normal and cancer cells". Cancer and Metastasis Reviews. 33 (4): 843–56. doi:10.1007/s10555-014-9511-7. PMID 25398252. S2CID 7959609.
- ^ a b Li DQ, Kumar R (2015). Unravelling the Complexity and Functions of MTA Coregulators in Human Cancer. Advances in Cancer Research. Vol. 127. pp. 1–47. doi:10.1016/bs.acr.2015.04.005. ISBN 9780128029206. PMID 26093897.
- ^ a b Sen N, Gui B, Kumar R (Dec 2014). "Physiological functions of MTA family of proteins". Cancer and Metastasis Reviews. 33 (4): 869–77. doi:10.1007/s10555-014-9514-4. PMC 4245464. PMID 25344801.
- ^ Kumar R (Dec 2014). "Functions and clinical relevance of MTA proteins in human cancer. Preface". Cancer and Metastasis Reviews. 33 (4): 835. doi:10.1007/s10555-014-9509-1. PMC 4245326. PMID 25348751.
- ^ a b Zhang H, Stephens LC, Kumar R (Mar 2006). "Metastasis tumor antigen family proteins during breast cancer progression and metastasis in a reliable mouse model for human breast cancer". Clinical Cancer Research. 12 (5): 1479–86. doi:10.1158/1078-0432.CCR-05-1519. PMID 16533771.
- ^ a b c Si W, Huang W, Zheng Y, Yang Y, Liu X, Shan L, Zhou X, Wang Y, Su D, Gao J, Yan R, Han X, Li W, He L, Shi L, Xuan C, Liang J, Sun L, Wang Y, Shang Y (Jun 2015). "Dysfunction of the Reciprocal Feedback Loop between GATA3- and ZEB2-Nucleated Repression Programs Contributes to Breast Cancer Metastasis". Cancer Cell. 27 (6): 822–36. doi:10.1016/j.ccell.2015.04.011. PMID 26028330.
- ^ a b Li H, Sun L, Xu Y, Li Z, Luo W, Tang Z, Qiu X, Wang E (2013). "Overexpression of MTA3 Correlates with Tumor Progression in Non-Small Cell Lung Cancer". PLOS ONE. 8 (6): e66679. Bibcode:2013PLoSO...866679L. doi:10.1371/journal.pone.0066679. PMC 3686714. PMID 23840517.
- ^ a b Brüning A, Makovitzky J, Gingelmaier A, Friese K, Mylonas I (Jul 2009). "The metastasis-associated genes MTA1 and MTA3 are abundantly expressed in human placenta and chorionic carcinoma cells". Histochemistry and Cell Biology. 132 (1): 33–8. doi:10.1007/s00418-009-0595-z. PMID 19363681. S2CID 35576465.
- ^ a b c Brüning A, Blankenstein T, Jückstock J, Mylonas I (Dec 2014). "Function and regulation of MTA1 and MTA3 in malignancies of the female reproductive system". Cancer and Metastasis Reviews. 33 (4): 943–51. doi:10.1007/s10555-014-9520-6. PMID 25319202. S2CID 17544666.
- ^ Kumar R, Wang RA (May 2016). "Structure, expression and functions of MTA genes". Gene. 582 (2): 112–21. doi:10.1016/j.gene.2016.02.012. PMC 4785049. PMID 26869315.
- ^ a b c d Fujita N, Jaye DL, Kajita M, Geigerman C, Moreno CS, Wade PA (Apr 2003). "MTA3, a Mi-2/NuRD complex subunit, regulates an invasive growth pathway in breast cancer". Cell. 113 (2): 207–19. doi:10.1016/S0092-8674(03)00234-4. PMID 12705869. S2CID 5773916.
- ^ a b Mishra SK, Talukder AH, Gururaj AE, Yang Z, Singh RR, Mahoney MG, Francí C, Vadlamudi RK, Kumar R (Jul 2004). "Upstream determinants of estrogen receptor-alpha regulation of metastatic tumor antigen 3 pathway". The Journal of Biological Chemistry. 279 (31): 32709–15. doi:10.1074/jbc.M402942200. PMC 1262658. PMID 15169784.
- ^ a b c Fujita N, Kajita M, Taysavang P, Wade PA (Dec 2004). "Hormonal regulation of metastasis-associated protein 3 transcription in breast cancer cells". Molecular Endocrinology. 18 (12): 2937–49. doi:10.1210/me.2004-0258. PMID 15358836.
- ^ Kumar R (Apr 2003). "Another tie that binds the MTA family to breast cancer". Cell. 113 (2): 142–3. doi:10.1016/s0092-8674(03)00274-5. PMID 12705862. S2CID 2627972.
- ^ a b Zhang H, Singh RR, Talukder AH, Kumar R (Nov 2006). "Metastatic tumor antigen 3 is a direct corepressor of the Wnt4 pathway". Genes & Development. 20 (21): 2943–8. doi:10.1101/gad.1461706. PMC 1620027. PMID 17050676.
- ^ a b Wang K, Chen Y, Ferguson SD, Leach RE (Dec 2013). "MTA1 and MTA3 Regulate HIF1a Expression in Hypoxia-Treated Human Trophoblast Cell Line HTR8/Svneo". Medical Journal of Obstetrics and Gynecology. 1 (3). PMC 4332396. PMID 25705708.
- ^ Li X, Jia S, Wang S, Wang Y, Meng A (Dec 2009). "Mta3-NuRD complex is a master regulator for initiation of primitive hematopoiesis in vertebrate embryos". Blood. 114 (27): 5464–72. doi:10.1182/blood-2009-06-227777. PMID 19864643.
- ^ a b Fujita N, Jaye DL, Geigerman C, Akyildiz A, Mooney MR, Boss JM, Wade PA (Oct 2004). "MTA3 and the Mi-2/NuRD complex regulate cell fate during B lymphocyte differentiation". Cell. 119 (1): 75–86. doi:10.1016/j.cell.2004.09.014. PMID 15454082. S2CID 17391732.
- ^ a b Parekh S, Polo JM, Shaknovich R, Juszczynski P, Lev P, Ranuncolo SM, Yin Y, Klein U, Cattoretti G, Dalla Favera R, Shipp MA, Melnick A (Sep 2007). "BCL6 programs lymphoma cells for survival and differentiation through distinct biochemical mechanisms". Blood. 110 (6): 2067–74. doi:10.1182/blood-2007-01-069575. PMC 1976344. PMID 17545502.
- ^ Chu H, Chen X, Wang H, Du Y, Wang Y, Zang W, Li P, Li J, Chang J, Zhao G, Zhang G (Apr 2014). "MiR-495 regulates proliferation and migration in NSCLC by targeting MTA3". Tumour Biology. 35 (4): 3487–94. doi:10.1007/s13277-013-1460-1. PMID 24293376. S2CID 15816727.
- ^ Zhang X, Zhang Y, Li Y (Aug 2013). "β-elemene decreases cell invasion by upregulating E-cadherin expression in MCF-7 human breast cancer cells". Oncology Reports. 30 (2): 745–50. doi:10.3892/or.2013.2519. PMID 23732279.
외부 링크
- MTA3+단백질+미국 국립의학도서관의 의학 주제 제목(MeSH)
- PDB의 UniProt: Q924K8(마우스 전이 관련 단백질 MTA3)에서 PDBe-KB에 제공되는 모든 구조 정보의 개요.